临床医学检验常用质量控制指标参数学习
临床医学检验中血液细胞检验质量控制要点分析

临床医学检验中血液细胞检验质量控制要点分析1. 背景介绍血液细胞检验是临床医学检验中的核心内容之一,通过对血液中的各种细胞类型进行定量和定性的检测,可以为医生提供重要的诊断和治疗依据。
血液细胞检验的质量控制对于确保检验结果的准确性和可靠性具有重要意义,因此需要严格遵守相关的质控要点和方法。
2. 质量控制要点分析(1)实验室内部校准和质控实验室内部校准和质控是确保血液细胞检验质量的基础。
在进行血液细胞检验之前,实验室需要对仪器进行校准,确保仪器的准确度和稳定性。
实验室还需要建立内部质控程序,定期对检验结果进行质控,及时发现和纠正偏差,保证检验结果的准确性和可靠性。
(2)质控品使用在血液细胞检验中,质控品的使用对于确保检验结果的准确性和可靠性至关重要。
实验室需要选择符合国家标准的质控品,并严格按照生产厂家的说明书进行使用和操作。
定期对质控品进行检验,评估其稳定性和可靠性,及时更换和调整质控品,保证检验结果的准确性和可靠性。
(3)操作规程和标准化规范的操作规程和标准化是保证血液细胞检验质量的重要保障。
实验室需要建立完善的操作规程和标准化的操作程序,确保所有的检验人员都按照规范操作。
实验室还需要对检验人员进行定期培训和考核,提高其操作技能和质量意识,保证检验结果的准确性和可靠性。
(4)质量管理体系建立健全的质量管理体系对于确保血液细胞检验质量至关重要。
实验室需要建立质量管理部门和质量管理责任人,负责监督和管理实验室的质量管理工作。
实验室还需要建立质量管理文件和记录,对实验室的各项质量控制活动进行记录和归档,为质量管理工作提供可靠的数据支持。
(5)外部质量评价参加外部质量评价是验证实验室检验质量的重要手段。
实验室需要选择符合国家标准的外部质量评价机构,定期参加外部质量评价活动,评估实验室的检验结果与外部质量评价中心的结果是否一致。
实验室还需要对评价结果进行分析和处理,及时发现和纠正问题,提高检验结果的准确性和可靠性。
临床生化检验分析质量指标

临床生化检验分析质量指标临床生化检验是一种重要的医学检验方法,通过对患者的体液样本进行分析,可以获得关于患者体内生物化学代谢状态的信息,为临床诊断和治疗提供了重要的参考依据。
而临床生化检验分析质量指标则是评价检验结果的准确性和可靠性的重要标准。
首先,作为临床生化检验的重要指标,精确度是评价分析质量的关键因素之一。
精确度是指检验结果与真值之间的接近程度,包括系统误差和随机误差两个方面。
系统误差是由于实验条件、试剂、仪器等因素引起的固定的偏差,而随机误差则是由于实验操作过程中的不确定性引起的波动。
为了提高精确度,需要严格控制实验条件,确保试剂的质量和稳定性,采用准确的仪器和方法,同时加强人员培训,从而减小误差对结果的影响。
其次,在临床生化检验中,灵敏度和特异度也是评价分析质量的重要指标。
灵敏度是指检验方法能够对阳性样本准确地识别出来的能力,特异度是指检验方法能够对阴性样本准确地识别出来的能力。
提高灵敏度可以减少假阴性结果的发生,提高特异度可以减少假阳性结果的发生。
为了提高灵敏度和特异度,需要选择合适的检验方法和标准,确保方法的准确性和稳定性,在临床应用中根据实际需要进行合理调整,从而提高检验结果的可靠性。
此外,稳定性也是评价临床生化检验分析质量的重要指标之一。
稳定性是指检验结果在不同存储条件和时间的变化情况。
对于生化指标来说,可能受到温度、光照、PH值等因素的影响,因此需要在适当的条件下进行样本的采集、保存和运输,以保证结果的准确性和可靠性。
同时,还需要建立合理的质控体系,定期进行内部和外部质量控制,及时发现和纠正可能存在的问题,确保检验结果的稳定性和可靠性。
最后,参考范围的确定和标准化也是评价临床生化检验分析质量的重要内容。
参考范围是指正常人群中某一指标的变异范围,通常以百分位数表示。
在临床应用中,参考范围的确定对于判断患者是否健康或是否存在某种疾病非常重要。
因此,需要根据不同人群的特点和检验方法的特性,进行科学、准确的参考范围确定,同时加强标准化管理,确保不同实验室之间的结果可以相互比较和参考。
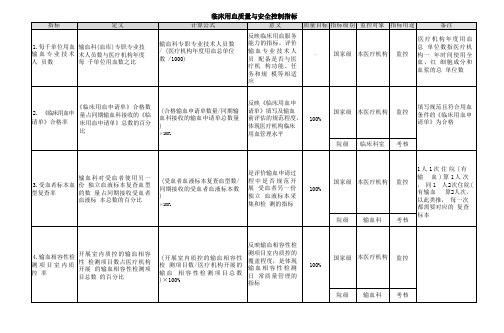
临床用血质量与安全控制指标
国家级
本医疗机构
监控
填写规范且符合用血条件的《临床用血申请单》为合格
院级
临床科室
考核
3.受血者标本血型复查率
输血科对受血者使用另一份独立血液标本复查血型的数量占同期接收受血者血液标本总数的百分比
(受血者血液标本复查血型数/同期接收的受血者血液标本数)
×100%
是评价输血申请过程中是否规范开展受血者另一份独立血液标本采集和检测的指标
—
国家级
本医疗机构
监控
医疗机构年度用血总单位数指医疗机构一年时间使用全血、红细胞成分和血浆的总单位数
2.《临床用血申
请单》合格率
《临床用血申请单》合格数量占同期输血科接收的《临床用血申请单》总数的百分比
(合格输血申请单数量/同期输血科接收的输血申请单总数量)
×100%
反映《临床用血申请单》填写及输血前评估的规范程度,体现医疗机构临床用血管理水平
血风险的监控能力
0
院级
各临床科室
考核
1.输血标本:用于输
血相容性检测(血型鉴定、交叉配血)试验的血液标本;
2.标本错误:指试管内的血液不是来自试管标签上所标注姓名的患者的血液标本
16.红细胞急诊输血申请率
单位时间红细胞急诊输血申请单数量占红细胞输血申请单总数量的百分比
(急诊输血申请单数量/输血申请单总数量)×100%
反映一二级手术患者血液使用情况
一
国家级
本医疗机构
监控
仅统计红细胞成分及全血用量
8.三、四级手术台均用血量
单位时间三级和四级手术台均用血量
三级和四级手术用血总单位数/同期三级和四级手术总台次
反映三四级手术患者血液使用情况
临床检验医疗质量控制指标

附件二2018年临床检验医疗质量控制指标室间质量评价上报表一、医院和实验室基本信息1.实验室所在机构性质?A 公立(继续第2题,跳过第3题)B 私立(跳过第2题,继续第3题)2.若选公立,则您实验室所在机构等级及类型?A 三甲综合B三甲专科 C 三乙综合 D 三乙专科 E 二甲综合 F 二甲专科G 二乙综合H 二乙专科I 二级以下医院J 其他3.若选私立,则您实验室所在机构等级及类型?A民营医院B独立实验室C体检中心D门诊部E其他4.实验室所在医院床位数?A 0-500B 501-1000C 1001-1500D 1501-2000E 2000以上5.实验室所在医院是否有LIS(实验室信息系统)和HIS(医院信息系统)?A有LIS和HIS B有LIS,无HIS C无LIS,有HIS D无LIS和HISLIS系统厂商为:,该厂商联系人,联系电话HIS系统厂商为:6.实验室所在医院日均门诊量?()人次7.实验室建筑面积?m28.实验室所有仪器设备总值?万元9.医院年业务额?万元/年;实验室年业务额?万元/年10.本实验室目前为止已开展检验项目总数(不包括外送)项其中:自动化仪器检测项目数?项手工检测项目数?项各专业检验项目数:临检项,占总业务额百分比%生化项,占总业务额百分比%免疫项,占总业务额百分比%微生物项,占总业务额百分比%基因扩增项,占总业务额百分比%其他项,占总业务额百分比%本实验室外送项目项11.科室人员组成实验室负责人:性别年龄学位学历职称已任职时间年实验室总人数二、检验全过程质量指标您实验室LIS是否纳入质量指标相关数据采集与统计:□是□否注意事项:如您实验室无某条目项目数据,请填写“未统计”,如数据为0,请填写数字“0”1. 月度指标2.年度指标(仅用于第1次调查)(六)本年度因分析设备故障导致检验报告延迟的次数:次三、2018年新增检验全过程质量指标(选填项)1. 月度指标2. 年度指标(仅用于第1次调查)。
临床检验质量控制-ppt课件

*
12
质量控制需要理清的概念
质量特性
控制方法
• 正确度
(溯源)校准
• 精密度
室内质控
• 内部结果一致性
检测系统比对
• 准确性、地区可比性
室间质评
(能力验证和室间比对)
*
13
分析质量指标
(真实度)
取均值不考 虑随机误差
(离散性)
BiasxT10% 0 T
TEB1.6C5( VS) D
2* 021/7偏 /28 差 XT T10% 0
19 2.80%
项目
WBC RBC Hb HCT MCV MCH MCHC PLT PT APTT INR FIB
*
CLIA’88 (TEa)
15% 6% 7% 6% 6% 6% 6% 25% 15% 15% 15% 25%
1/3×TEa 3σ规则 5% 2% 2.3% 2% 2% 2% 2% 8.3% 5% 5% 5% 8.3%
注:常规工作中将质控品就放在校准品后面,得到的质控结果是对分析 不精密度的不真实的估计,对批量标本检测时出现的偏倚或漂移无法作出 估计。
*
31
质控方法
质控方法应具既能灵敏地检出分析误差(即具有较高的误差检出概 率),又能特异地识别误差(即具有较低的假失控概率)。使用多规 则方法可改善误差检出,同时具有低概率的假失控。
单值质控
经典的 多值质控
灵活的 多值质控
*
• Levey-Jennings质控方法
– 质控品:1个。 – 质控规则:12s或13s;图形变化。 – 质控图: Levey-Jennings质控图。
• 特点
– 最常用的方法。 – 它方便易行,但却相对简单粗糙,往往不能
临床生化检验质量控制总结

大于2.0要复查,如果怀疑携带污染问题处理办法:X-X-A-X-B-X-C-X-D-----,标本针污染可造成低值偏高,尿蛋白建议连续测两次. • 5、酸碱试剂相互影响白蛋白对肌酐有携带污染. • 6、CK-MB比CK高,方法学影响,主要CK-BB增高影响,主要是儿科及消化 道肿瘤病人. • 7、HDL-C+LDL-C大于TCHO,胆固醇偏低或高低密偏高,找原因. • 8、标本混浊增加吸光度引起总蛋白偏高. • 9、胆汁酸负数因空白吸光度偏高,试剂针污染有关,血脂类试剂加有大 量胆酸钠,可降低胆汁酸结果.
生化实验干扰因素
• 10、AMY含高浓度钙离子. • 11、CHE\GLU\UR\UA\LDH等含磷. • 12、ALT\AST含LDH干扰 • 13、CK\CK-MB含GLU • 14、钒酸盐法直胆影响ALT • 15、真假胆酶分离:如果反向发展,病情严重,重度肝细胞坏死.特别注
意仪器提示观察反应曲线,是否底物耗尽. • 16、反复离心可使钾升高. • 17、标本采集顺序:血培养-血凝-无填写试管-其他有填写剂试管,EDTA
维生素C是临床最常用的药物之一,它对疾病的治疗作用是不容置疑的.但是,对于临床检验,它却是多种物质测定的干扰者, 这是因为它的化学结构和化学性质特殊缘故.
抗坏血酸干扰临床机检验的机制: 主要是因为其本身具有三个特性,其一是强还原性,它可干扰与氧化还原反应有关的许多反应.如:使班氏尿糖定性试验 呈假阳性,使酶法测定葡萄糖、甘油三酯、总胆固醇的结果下降,对血尿酸的酶法测定呈负干扰,而对血尿酸的磷钨酸法测定呈 正干扰.其二是具有弱酸性可竞争尿胆原的排泄,使尿胆原下降.其三是其药理特性,如:可以降低血清总胆固醇水平.抗坏血酸对 临床检验的影响见附表. 总之,抗坏血酸对检验的干扰是广泛的,其中对有的检验项目只须治疗浓度就可干扰,如胆红素、尿糖等.因此,临床检验时 应特别注意其影响,这是实验室全面质量管理中应非常重视的问题. 抗坏血酸对临床检验的影响 检验项目 影响性质 影响机制 血清胆红素 升高 干扰反应程序 血清胆固醇 下降 药理特性并干扰试验 血清肌酐 升高 干扰试验 血清葡萄糖 下降 干扰试验 尿葡萄糖 升高或下降 班氏法升高 氧化酶法下降 血清乳酸脱氢酶 下降 干扰试验 粪潜血 假阴性 干扰试验 血浆凝血酶原时间 减少 可缩短抗凝剂作用 血清甘油三酯 下降 对动脉粥样硬化病人有降低作用 血清尿酸 升高或下降 磷钨酸法升高 酶法下降 尿血红蛋白 下降 抑制愈创木酚法 尿胆原 下降 低PH值时减少排泄 尿17-酮类固醇 升高 影响间二硝基苯法 尿17-羟类固醇 升高 干扰试验
医学临床检验知识点总结

医学临床检验知识点总结一、临床检验的概念及意义1. 临床检验的概念临床检验是指利用医学分析仪器和设备对人体组织、器官、血液、尿液、排泄物、分泌物等进行检测和分析的一种医学检验方法,以帮助临床医生做出诊断、评估疾病的严重程度和预后,并指导治疗方案。
2. 临床检验的意义临床检验在临床医学中起着极为重要的作用,它能够为医生提供客观的实验数据,帮助医生判断患者是否患有某种疾病,评估疾病的严重程度,监测疾病的病程和治疗效果,进行疾病的预后评估,指导临床治疗和康复。
二、临床检验的常用指标及其意义1. 血常规血常规是临床上最常用的检测项目之一,包括白细胞计数、红细胞计数、血红蛋白浓度、血小板计数、红细胞压积和平均红细胞体积等指标。
它可以帮助医生诊断和监测贫血、白细胞减少或增多、出血、骨髓增生功能异常等疾病。
2. 生化指标生化指标包括血清蛋白、肝功能、肾功能、血脂、血糖、电解质等指标。
它可以帮助医生评估患者的肝脏功能状态、肾脏功能状态、血液脂质代谢状态、糖代谢状态和电解质平衡状态,为诊断和治疗疾病以及监测治疗效果提供重要参考。
3. 免疫学指标免疫学指标包括白细胞计数、淋巴细胞计数、CD4+T细胞计数等指标。
它可以帮助医生评估患者的免疫功能状态,指导治疗和预后评估。
4. 尿常规尿常规是通过对尿液中的蛋白质、糖、白细胞、红细胞等指标的检测来评估患者的肾脏功能状态和泌尿系统的疾病情况的一种检查方法。
5. 生物化学指标生物化学指标包括血浆内分泌激素、肿瘤标志物等指标。
它可以帮助医生评估患者的内分泌功能状态、肿瘤的发生情况和预后。
6. 微生物学指标微生物学指标包括细菌培养、真菌培养、病毒检测等指标。
它可以帮助医生确定感染的病原体,指导抗感染治疗。
7. 其他指标其他指标包括凝血功能、心肌酶、肿瘤标志物等。
它们在协助临床医生诊断心血管疾病、肿瘤和其他疾病方面具有重要作用。
三、临床检验技术及方法1. 常规检验技术常规检验技术包括显微镜检查、光度法、色谱法、质谱法、流式细胞术等。
临床医学检验重要环节的质量控制

临床医学检验重要环节的质量控制临床医学检验是医学临床诊断和治疗过程中不可或缺的一个环节,准确的检验结果对疾病的早期发现、治疗和预防都有着至关重要的意义。
然而,检验结果的准确性不仅取决于仪器设备、试剂和技术的精度,也离不开质量控制这一重要环节。
质量控制是指应用于加工生产、检验、服务等工作中,为保证生产和服务质量而采取的有组织的控制活动,从而达到不断改进产品和服务的目的。
临床医学检验的质量控制主要分为三个方面:内部质量控制、外部质量评估和不良事件的监测与管理。
内部质量控制内部质量控制是指在实验室内部开展的、严格按照规定流程、参数和标准进行的质量控制活动。
内部质量控制是确保检验结果准确可靠的重要手段,主要包括标准曲线、试剂质量、仪器校准、日常质量控制及纠错等。
(1)标准曲线标准曲线是临床化验中常用的一种标准化控制方法,通常采用制备、检测和使用同一批次的标准品,根据不同样本浓度设置不同的标准曲线,用来评估样本中的化学浓度。
在此过程中,需要严格按照各项参数和标准进行操作,以确保标准曲线的准确性和可重复性。
(2)试剂质量试剂质量也是影响检验结果准确性的重要因素之一。
在使用试剂时,需要仔细确认其有效期、保存条件、正确性和耐受性,以及有无污染。
同时,在选择试剂时也需要注意相关批次的一致性和稳定性,(3)仪器校准临床化验仪器是保证检验结果准确性的重要保障。
因此,在使用仪器前需要对其进行严格的校准和维护,确保仪器的精度和稳定性。
在校准仪器时,需要仔细检查相关参数和标准值,并进行测量和比对,以确保仪器性能和准确性。
(4)日常质量控制日常质量控制是指在分析样本前,对仪器、试剂和标准曲线等进行的标准化测试。
通过不断监测和比对测试结果,可以及时发现不符合标准的情况,并采取纠正措施。
这样可以有效提高测试结果的准确性和可靠性,保证检验质量。
(5)纠错纠错是内部质量控制中一个非常重要的环节。
当发现检测结果异常时,需要及时确认问题所在,纠正错误,以保证结果的精度和可靠性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
临床医学检验常用质量控制指标参数学习临床医学检验常用质量控制指标参数学习灵敏度vs检出限1.灵敏度:又称分析灵敏度(analytical sensitivity)。
国际纯粹和应用化学联合会(International Union of Pure andApplied Chemistry,IUPAC)将方法的灵敏度定义为被测组分浓度或含量改变1个单位时所引起的分析信号的变化[1]。
通过定义,我们可以发现灵敏度就是分析校准曲线的斜率。
曲线斜率越大,表示方法的灵敏度越高。
这点很好理解,假设在称量范围内我们用电子秤和天平同时称量100克淀粉,如果在被测物里再增加0.1克淀粉,天平可以很容易称量出来精确差异,而电子称却不发生变化。
我们就说天平比电子秤灵敏度高。
除此之外,在分析实践中还有针对某一类方法灵敏度的特定表达方式,如对于紫外-可见分光光度法,则用摩尔吸光系数表示。
摩尔吸光系数越大,在一定条件下校准曲线的斜率也越大,表示灵敏度越高。
2.检出限:IUPAC将检出限(limit of detection,LoD)定义为给定分析程序具有适当的确定检出分析物的最小浓度或量[1]。
若LoD 处的分析信号为Xd,则Xd=xB+k·sB。
其中k为可靠性系数,IUPAC建议取k=3,xB和sB分别为有限次测量的空白均值和空白标准差。
若用校准曲线斜率(m)表示灵敏度,用浓度(Cd)表示检出限,根据校准曲线可知:Xd=xB+m·Cd。
又因Xd=xB+k·sB,故Cd=(Xd-xB)/m=k·sB/m。
由此可见,当k确定后,若空白的标准差一定,m与Cd 呈反比。
因此,人们习惯于把具有较低LoD的分析方法说成该方法具有较高的灵敏度(注意:这是一种推论,而不是等价说明)。
恰巧是这个现象经常出现在我们的日常生活与工作中,让我们产生一点混淆:低LoD一定伴随高灵敏度甚至有些人认为“低LoD=高灵敏度”。
然而,LoD不仅与灵敏度有关,还与空白信号的标准差有关,空白信号波动范围大,样品中含有较低的分析物浓度时产生的分析信号不易与空白区别,致使检出限增高。
因此,减小空白的标准差可使LoD降低,而对方法的灵敏度没有影响,由此可见灵敏度和LoD是完全不同的两个概念。
实际上,很多方法本身的灵敏度很高,但由于受空白标准差的影响,LoD很难达到理想的程度。
理想的方法应具有高的分析灵敏度和低的LoD。
IUPAC定义的LoD实际上就是检出低限双侧99.7%分布范围的上限。
空白限vs检出低限1.空白限(limitof blank,LoB):LoB是美国临床和实验室标准化协会(CLSI)EP17-A文件中使用的术语,它是指在规定的可能性条件下,空白样品被观察到的最大检测结果[1]。
最理想的情况是我们检测每一份空白样品的结果都应该为0,但是由于随机误差的存在,空白样品检测值会分布在一个较低水平的区间之内。
EP17-A规定,空白样品单侧95%分布的上限就是LoB。
此时会有5%的空白样品被误认为有分析物的存在,这就是假阳性,我们犯这种错误(Ⅰ类错误或α错误)的概率就是5%。
当某份样品的观察值超过LoB,则表明样品中的分析物浓度超过了0。
同理,由于随机误差的存在,低浓度分析物样品的检测值如果低于了LoB,我们就会误认为样品中不存在可检出的分析物,得出假阴性的结果,这就是Ⅱ类错误或β错误。
因此,LoB的存在决定了我们犯错误的几率大小,如何确定低浓度样品和空白检测的界值至关重要。
ISO推荐在α=β=5%条件下,确定LoB。
若空白值呈正态分布,LoB为单侧95%分布的上限,即LoB=μB+1.645σB,式中μB和σB分别为空白样品检测的均值和标准差。
如果空白值呈非正态分布怎么办?此时实验室必须用非参数方法进行评估。
原理:假定空白样品重复测量结果数为NB,将数据由小到大排列,估计第95百分位数所在位置为[NB(95/100)+0.5]的值,即LoB=PctB(100-α)=PctB(95)。
建立LoB:通常需对1个或数个空白样品进行重复检测,共获得60个空白结果(NB=60)估计LoB。
验证LoB:厂商声明了LoB时,实验室应对空白样品进行至少20次重复检测,若没有3个重复测量值超出声明的LoB,则验证通过,可直接使用厂商声明的LoB。
但目前绝大多数厂商尚未按EP17-A文件提供LoB,因此,实验室应按照上述方法建立自己实验室的LoB。
2.检出低限(lowerlimit of detection,LLD):LLD是指样品单次检测可以达到的非空白检测响应量对应的分析物含量[2-4]。
也就是说分析物最低要达到多少浓度,才能不被检测为0,不会产生假阴性。
以样品响应量与样品内分析物含量呈正比例关系为例,通常的做法是对空白样品进行至少10次重复测量,假定空白样品多次重复测量的检测信号值服从正态分布,以空白样品检测信号±2s(双侧95%分布范围的上限)或±3s(双侧99.7%分布范围的上限)所对应的分析物含量即为LLD。
值得注意的是,若直接读出浓度单位的检测系统对低于0的检测将报告为0,其分布不呈正态,此时应使用初始值来计算均值和标准差,然后再转换成浓度单位。
从LoB和LLD的定义讲,二者本质是一样的,细微区别在于:(1)LoB是通过空白样品来描述,LLD是通过低浓度分析物来描述;(2)测量次数和统计方法略有不同;(3)LoB是空白样品重复测定结果单侧95%分布范围的上限,LLD是双侧95%或99.7%分布范围的上限;(4)LoB适用于正态分布和非正态分布,而LLD只适用于正态分布。
检出限vs生物检出限1.检出限:以前我们讲过IUPAC定义的检出限(limit of detection,LoD),但是EP17-A文件中定义的LoD和IUPAC定义的LoD明显不同。
在EP17-A文件中它是指样本中可被检测到的最低分析物浓度,可以在规定的可能性条件下予以检出,但还不能量化为一个确切的值[1]。
当实际样品浓度等于LoB时,50%的样本检测结果低于LoB,其余50%的样本检测结果高于LoB,即含有分析物可以检测的量,所以β=50%。
当实际样品浓度检测结果的第5百分位数的值等于LoB时,检测结果的95%超出了LoB,可以肯定含有分析物的量与空白明显不同,但有5%的结果低于LoB,即与空白没有差异,所以β=5%,LoD是这个样品的实际浓度,它是可靠检测到的最低实际浓度。
若低浓度样品检测结果呈正态分布,其单侧5%分布的上限相当于LoB,此时的均值即为LoD,μs=LoD=LoB+1.645σs。
如果样品的检测结果不呈正态分布,或不能转化为正态分布,可以按非参数方法估计LoD。
此时,LoD=LoB+DSβ。
DSβ即中位数和第5百分数的间距。
建立LoD:制备1~4倍LoB浓度的系列实验样品,批间或日间重复测定若干次共获得至少60个低浓度样品的检测结果,根据低浓度样检测结果的分布规律,按照参数检验或非参数检验的方法计算LoD。
验证LoD:在验证厂商声明的LoD时,建议对相当于厂商给定的LoD浓度的样品进行至少20次重复检测,估计结果数超过LoB的比例。
若85%的数据高于LoB,则说明实验数据支持厂商声明的LoD。
否则实验室应联系厂商,或建立自己的LoD。
2.生物检出限:生物检出限(biologic limit of detection,BLD)定义为某样品单次检测可能具有的最小响应量刚大于检出低限(LLD)响应量时,该样品内含有的分析物浓度[2-4]。
这与EP17-A文件定义的LoD基本相同,只是实验要求的样本数和所用的统计方法不同。
建立BLD:以样品响应量随样品内分析物量呈正比例关系为例,通常的做法是制备几个浓度略高于LLD的低浓度样品日间至少重复测定10次,低浓度样品检测信号-2s(双侧95%分布范围的下限)或-3s (双侧99.7%分布范围的下限)刚大于LLD时,样品中所具有的分析物含量即为BLD。
定量检出限vs功能灵敏度1.定量检出限:定量检出限(limit of quantitation,LoQ)是EP17-A文件中使用的术语,它是指在声明的实验条件下能够得到可靠结果的样本中分析物的最低浓度,并在该浓度下的总误差符合准确度要求(临床应用可接受)[1-2]。
总误差目标可以来源于实验室的需求、室间质评结果和厂商的声明。
通常情况下,低浓度样品很难获得具有溯源性的参考值,因此偏移未知,此时没有必要进行LoQ试验。
EP17-A文件并未要求为每个检验方法确定LoQ。
建立LoQ:在缺乏足够低水平参考物质的情况下,可以用已知浓度或活性的样品适当稀释制备成低浓度实验样品,但样品中的分析物浓度应高于分析测量范围的下限。
实验方法类似于LoD,对多个低浓度实验样品进行重复检测,每个浓度推荐最少40个重复测量,计算每个浓度重复测量的标准差和已知值的偏倚,即可获得该水平下总误差的估计值:总误差=偏倚+2s,如果这个估计值刚小于设定的总误差目标,此时样品中所具有的分析物含量即为LoQ。
2.功能灵敏度:功能灵敏度(functional sensitivity,FS)是指以日间变异系数(CV)为20 %时对应LoD样品具有的平均浓度,这是检测系统或方法可定量报告分析物的最低浓度[3-6]。
FS用于确定检测系统可报告的最低限值。
日间CV为20%大致上是诊断实验要求的最大不精密度。
近年来发表的有关FS评价实验如心肌肌钙蛋白、B型利钠肽原和NT-proBNP 测定来看,几乎都是评估在满足相关国际或国家指南对精密度要求的条件下进行评估。
如心力衰竭标志物指南对NT-proBNP 测定的不精密度质量要求为CV≤10%,Yeo等[5]曾对罗氏Elecsys1010、2010和E170电化学发光免疫检测系统的功能灵敏度进行评价,在CV=10%条件下的功能灵敏度为30 ng/L;张秀明等[4,6]曾对最新一代的罗氏Cobas E601电化学发光免疫系统检测NT-proBNP 的功能灵敏度进行评价,FS=8.82 ng/L。
因此,我们可以将功能灵敏度的定义理解为:在满足精密度质量要求的条件下,对应LoD样品具有的平均浓度。
FS的建立:通常制备一系列的低浓度样品,日间重复测定至少10次以上,计算每个低浓度样品检测信号的均值、标准差和CV,从中选择CV最接近10%或20%(满足精密度质量标)的低浓度样品均值对应的分析物浓度为FS。
检出限使用的注意事项在ISO15189中要求对检测系统的分析性能进行验证,证实其能够满足预期的质量要求方可用于临床检测。
美国临床实验室修正法规(Clinical Laboratory Improvement Amendments,CLIA)仅要求实验室对更改的非简易方法以及未经食品药品监督管理局(Food and Drug Administration,FDA)批准的检测系统如实验室自行建立的方法建立检出限(limit of detection,LoD)。
