物理化学试卷第9章可逆电池选择
09 第九章 可逆电池的电动势及其应用

(一)可逆电池与不可逆电池
2. 可逆电极
⑴第一类电极
金属与其阳离子组成的电极 氢电极 氧电极 气体电极 卤素电极 汞齐电极
⑵第二类电极
金属-难溶盐及其阴离子组成的电极 金属-氧化物电极
⑶第三类电极
氧化-还原电极
第一类电极及其反应
电极
Mz+(a+)|M(s) H+ (a+)|H2(p),Pt
电极反应
Pt, H2 ( p ) | H2 SO4 (aq) | Au2O3 (s) Au(s)
又知H2O(g)的
D f Gm 228.6kJ mol
1
,该温度下,水的饱和蒸气压为3167Pa,求在298K时氧 气的逸度等于多少,才能使Au2O3与Au呈平衡?
考研真题
根据25℃时下列反应的标准电极电势: (1)Fe2+ + 2e- → Fe(s),ϕ1θ = -0.439 V (2)Fe3+ + e- → Fe2+,ϕ2θ = 0.770 V 可得Fe3+ + 3e- → Fe(s)所对应的标准电极电势 ϕ3θ = (A)0.331V; (B)-0.036V; (C)0.036V; (D)-0.331V。
二、 计算题
例1 25℃及1Pθ下,将一可逆电池短路,使有96500库 仑的电量通过电池,此时放出的热量恰为该电池可逆 操作时所吸入的热量的 43 倍。在 25℃及 1Pθ 下,该电
池的电动势的温度系数是 0.00014V·K-1 ,试求此电池
在25℃及1Pθ下的Qr、 DH 、D S 、 D G 、E ?
E Dr H m d dT 2 T zFT
物化课件第九章_可逆电池的电动势及其应用

可逆电池必须同时满足上述两个条件。
上一内容 下一内容 回主目录
返回
2014-3-8
电池Ⅰ
放电:E>V
V
A
充电:加外加电压V>E
V
A
盐桥
Cu
CuSO4
Zn
ZnSO4
Cu
CuSO4
Zn
ZnSO4
Cu极电势高为正 Cu极 Cu2++2e- Cu Zn极 Zn 2e- Zn2+ Cu2++Zn Cu +Zn2+
电池表示式和电池反应的“互译”
由电池反应写电池表示式(设计电池): 先写出电极反应,确定电极——确定电解质溶液——复核 (1)氧化还原反应
Zn(s)+H2SO4(aq)→H2(p)+ZnSO4(aq) 电池:Zn(s)|ZnSO4(a)||H2SO4 (a)|H2(p),Pt 验证: (-) Zn(s) →Zn2++2e(+) 2H++2e-→H2(p)
返回
2014-3-8
(3)氧化还原反应(没有离子参加): H2(p)+1/2O2(p)→H2O(l)
H2 (p) -2e- 2H+ (aH+)
1/2O2 (p) +2H+ (aH+) +2e- H2O
Pt |H2 (p) | H+ (aH+) | O2 (p) |Pt H2 (p) +2OH- (aOH-) -2e- 2H2O 1/2O2 (p) +H2O+2e- 2OH- (aOH-)
上一内容 下一内容 回主目录
09- 可逆电池的电动势及其应用(课程习题解)

第九章 可逆电池的电动势及其应用习题及解答(2012.3)【1】写出下列电池中各电极的反应和电池反应。
(1)2222|()|()|()|H Cl Pt H p HCl a Cl p Pt ; (2)22|()|()||()|()H H Ag Pt H p H a Ag a Ag s ++++; (3)()|()|()||()|()|()I Cl Ag s AgI s I a Cl a AgCl s Ag s ----;(4)2242244()|()|()||()|()SO Cu Pb s PbSO s SO a Cu a Cu s -+-+;(5)22|()|()|()|()H Pt H p NaOH a HgO s Hg l ; (6)2223|()|()|()|()H Pt H p H aq Sb O s Sb s +; (7)3212|(),()||()|()Ag Pt Fe a Fe a Ag a Ag s ++++;(8)()()|()||()|()|()am Na OH Na Hg a Na a OH a HgO s Hg l +-+-. 【解】 (1)负极:22()22()H H H p e H a +-+-→ 正极:22()22()Cl Cl Cl p e Cl a ---+→电池反应:2222()()2()H Cl H p Cl p HCl a += (2)负极:22()22()H H H p e H a +-+-→正极:2()22()Ag Ag a e Ag s ++-+→电池反应:22()2()2()2()H Ag H H p Ag a Ag s H a +++++=+ (3)负极:()()()I Ag s I a e AgI s ---+-→正极:()()()Cl AgI s e Ag s Cl a ---+→+电池反应:()()()()I Cl AgCl s I a AgI s Cl a ----+=+(4)负极:24244()()2()SO Pb s SO a e PbSO s ---+-→正极:22()2()Cu Cu a e Cu s ++-+→电池反应:2242244()()()()()Cu SO Pb s Cu a SO a PbSO s Cu s +-+-++=+(5)负极:222()2()22()H OH H p OH a e H O l ---+-→正极:2()()22()()OH HgO s H O l e OH a Hg l ---++→+电池反应:222()()()()H H p HgO s Hg l H O l +=+ (6)负极:223()66()H H p e H aq -+-→正极:232()6()62()3()Sb O s H aq e Sb s H O l +-++→+电池反应:222323()()2()3()H H p Sb O s Sb s H O l +=+ (7)负极:2321()()Fe a e Fe a +-+-→正极:()()Ag Ag a e Ag s ++-+→电池反应:2321()()()()Ag Fe a Ag a Fe a Ag s +++++=+ (8)负极:2()()22()2()am Na Na Hg a e Na a Hg l +-+-→+正极:2()()22()()OH HgO s H O l e OH a Hg l ---++→+电池反应:22()()()()2()2()3()am Na OH Na Hg a HgO s H O l Na a OH a Hg l +-+-++=++ 【3】(1)Weston 标准电池为42424()8/3()()Cd Hg CdSO H O s CdSO aq Hg SO s Hg ⋅饱和()写出电极反应和电池反应;(2)从饱和Weston 标准电池的电动势与温度的关系式:572/ 1.01845 4.0510(/293.15)9.510(/293.15)E V T K T K --=-⨯--⨯-试求在298.15K ,当电池可逆地产生2mol 电子的电荷量时,电池反应的r m G ∆,r m H ∆和r m S ∆。
物化9(可逆电池)

原电池
电解池
原电池
负极: Z n (s) Z n 2 2 e 正极: C u 2 + (s) 2 e C u (s)
Zn(s) C u
2+
放电反应:
Zn
2+
C u(s)
电解池
阴极:
Zn
2
2 e Z n (s )
2
阳极:
充电反应:
Zn
2+
C u (s ) C u
§ 9.2
电池电动势的测定
电池电动势:可逆电池无电流通过时,两电极
间电势差。 电动势的测量:对消法或补偿法,而不用伏特计 (为什么)。 所用仪器称为电势差计,其原理线路图如下。
设E为电池电动势,U为两极间电势差,R0为导线电 阻(外阻),Ri为电池内阻,I为电流。 根据Ohm定律
E ( R0 Ri ) I
$
左边负极(氧化反应)
A g (s) C l ( a C l ) A g C l(s) e
右边正极(还原反应)
H (aH ) e
1 2
H2( p ) 1 2
$
$
电池净反应
A g (s) H C l( a 1 ) A g C l(s)
H 2( p )
微溶氧化物电极常见的有银-氧化银电极、汞-氧化 汞电极 银-氧化银电极: 符号 : OH-(a-) | Ag2O(s) | Ag(s) 或 H+(a+) | Ag2O(s) | Ag(s) 电极反应分别为: Ag2O(s) + H2O + 2e- → 2Ag(s) + 2OH-(a-) Ag2O(s) + 2H+(a+) + 2e- → 2Ag(s) + H2O
【通用】《物理化学(第五版)》第九章复习题答案.ppt
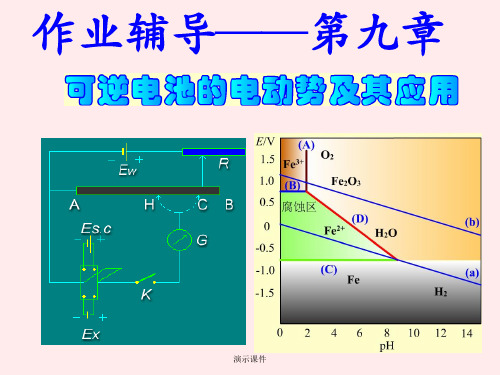
演示课件
复习题
7.在公式ΔrGmΘ=-zEΘF中,ΔrGmΘ是否表示 该电池各物都处于标准态时,电池反应的 Gibbs自由能变化值?
答:在公式ΔrGmΘ=-zEΘF中,ΔrGmΘ表示该 电池各物都处于标准态时,在T,p保持不变 的条件下,按电池反应进行1mol的反应时 系统的Gibbs自由能变化值。
ln
m m'
高价型:Mz+Az-(m1)|Mz+Az-(m2)
E
j=
t z
- t- z 演示课-件
RT F
ln
m1 m2
基本公式
用可逆电池的测定值计算热力学函数变化
值
rGm zFE , rGm zFE
E
RT zF
ln
K
a
r Sm
( r Gm T
)p
E zF (T ) p
E
QR
T rSm
答:可逆电极有三种类型: (1)金属气体电极 如Zn(s)|Zn2+ (m) Zn2+(m) +2e- = Zn(s) (2)金属难溶盐和金属难溶氧化物电极 如:
Ag(s)|AgCl(s)|Cl-(m) AgCl(s)+ e- = Ag(s)+Cl-(m) (3)氧化还原电极 如: Pt|Fe3+(m1),Fe2+(m2) Fe3+(m1) +e- = Fe2+(m2) 对于气体电极和氧化还原电极,在书写时要标明电极
反应所依附的惰性金属。
演示课件
复习题
2.什么叫电池的电动势?用伏特表侧得的电 池的端电压与电池的电动势是否相同?为何 在测电动势时要用对消法?
物理化学——第9章-可逆电池

3
2
4
2
§ 9.2 电动势的测定
Cell
Cell
V 不可逆电池的端电压
电位 差计 可逆电池的电动势
§ 9.2 电动势的测定
对消法测定可逆 电池电动势 (P65)
§ 9.3 可逆电池的书写方法
规定: 负极|电解质溶液|正极 负极|负极溶液| |正极溶液|正极
1. “|” 表示相界面,有电势差存在。 2.“||”表示盐桥,使液接电势降到可以忽略不计。 3. 要注明温度,不注明就是298.15 K; 要注明物态;气体要注明压力;溶液要注明浓度。
p77
1/2H2 (p ) H (aH =1) e
规定:
θ
H / H2 g
=0
氢电极
用途
测其它电极的相对电势 方法:
标准氢电极 || 任意电极x ( =?)
p78
标准氢电极做负极 待测电极做正极
θ E电池 = +– - = +– H
/ H2 g
= +
2、可逆电极
第二类电极(the second-class electrode)
金属表面覆盖一层该金属的难溶盐,然 后再浸入含有该盐的相同阴离子溶液中组成 的电极。
甘汞电极(calomel electrode) 电极符号: Hg, Hg2Cl 2 (s) KCl (a)
电极反应: Hg2Cl2 2e 2Hg Cl
1和3可消除或忽略,E只与2和4有关
即: E只和2个电极电势有关 E电池 = 2 + 4
§ 9.6 电极电势和电池的电动势
(1) 标准氢电极
傅献彩《物理化学》(第5版)(下册)课后习题-可逆电池的电动势及其应用(圣才出品)
可逆的热效应为
十万种考研考证电子书、题库视频学习平台
。
(3)若在相同温度压力下,热化学方程式的热效应为
。
7.一个可逆电动势为 1.70 V 的原电池,在恒温槽中恒温至 293 K。当此电池短路时
(即直接发生化学反应,不作电功),相当于有 1000℃的电荷量通过。假定电池中发生的反
T
T
T
所以 S (总) = S (槽) + S (电池) = − Qp + Qp +Wf = Wf = 10001.70 = 5.8J gK−1。
TT
T
293
如果分别求算恒温槽和电池的熵变,还需要知道电池反应的焓变值,或者与电池反应相
同的化学反应的等压热效应。
8.分别写出下列电池的电极反应、电池反应,列出电动势 E 的计算公式,并计算电池 的标准电动势 设活度因子均为 1,气体为理想气体。所需的标准电极电势从电极电势表中 查阅。
(9) Pb(s)| PbO(s)|OH − (aq)| HgO(s)| Hg (l )
( ) ( ) ( ) ( ) (10) Pt | Sn4+ aSn4+ ,Sn2+ aSn2+ ||Tl3+ aTl3+ ,Tl+ aTl+ | Pt
3.从饱和 Weston 电池的电动势与温度的关系式,试求在 298.15 K,当电池可逆地产 生 2 mol 电子的电荷量时,电池反应的△rGm,△rHm 和△rSm。已知该关系式为
应与可逆放电时的反应相同,试求以此电池和恒温槽都看作系统时总的熵变。如果要分别求
算恒温槽和电池的熵变,还,则热效应 Q=
,恒温槽热量得失为-Qp,
故有
物理化学第9章可逆电池
第九章 可逆电池本章用化学热力学的观点讨论电极反应的可逆行为。
原电池是将化学能转变为电能的装置,两个电极和电解质溶液是电池最重要的组成部分。
电极电势是本章主要概念之一,它是相对于标准氢电极而言的电势,是一种相对值,即把一个电极与标准氢电极组成一个已消除了液接电势的原电池,其电动势就是给定电极的标准电极电势。
对于一个可逆化学电池,电极两极间的电势差称电池的电动势,可用电池反应的能斯特方程计算。
因为电池电动势与热力学量之间密切相关,所以本章内容是围绕电动势而展开。
一、基本内容(一) m r G ∆=-zFE式中m r G ∆为电池反应的摩尔吉布斯自由能变;z 是电池反应的电子的物质的量;E 为电池的电动势。
此式运用于等温等压的可逆过程,所以E 为可逆电池的电动势。
此式表明,在可逆电池中,化学反应的化学能(m r G ∆)全部转变成了电能z FE 。
该式将化学反应的性质与电池的性质联系起来,是电化学的基本公式之一。
若参与电池反应的所有物质均处于各自的标准态,则上式成为θm r G ∆=-zFE $其中E $称为电池的标准电动势,对于指定的电池,E $只是温度的函数。
(二) 电池反应的能斯特公式若电池反应为 aA+bB =gG+hHE=E $-zF RT ㏑b Ba A h Hg G a a a a ⋅⋅ 此式表明,电池的电动势取决于参加反应的各物质的状态,它对如何改变电池电动势具有指导的意义,计算时首先要正确写出电池反应式。
(三) 电极反应的能斯特公式p m r TzFT zFE H )E(∂∂+-=∆若电极反应为 aA+bB+ze -=gG+hHE=E $-zF RT ㏑b Ba A hHg G a a a a ⋅⋅ 式中E 和E $分别为该电极的电极电势和标准电极电势。
此式表明,一个电极的电势取决于参与电极还原的各物质的状态。
计算的关键是要正确写出电极上的还原反应。
(四) E =负正E E -,E $=θθ负正E E -式中E 和E $分别为可逆电池的电动势和标准电动势;正E (θ正E )和负E (θ负E )分别为正极和负极的电极电势(标准电极电势)。
物理化学第九章可逆电池
RT
8.314 298.15
QR=T△S=298.15×(-88.77)=-26.47KJ
2004年8月13日
§9-3 可逆电池的热力学—可逆电池的Nernst方程
2. 可逆电池的Nernst方程(Nernst equation of reversible cell) 1889年,Nernst提出著名的经验方程。 对于一个一般的电池反应: aA+bB+···=gG+hH+··· Nernst方程为:
放电时∶ Zn + CuSO4 =Cu + ZnSO4 充电时: Cu + Cu2+ =Cu2+ + Cu 电池反应不可逆,电池不是可逆电池 使用盐桥的双液电池可近似地认为是 可逆电池,但并非是严格的热力学可逆电 池,因为盐桥与电解质溶液界面存在因离 子扩散而引起的相间电势差,扩散过程不 是热力学可逆过程。
当K与Ex接通时,
Ex = AC' Ew AB
则
Ex AC' Es AC
(9-2-4) (9-2-5) (9-2-6)
2004年8月13日
§9-2 可逆电池的表示方法和电池电动势的测定
— 电池电动势的测定和标准电池
3.2 标准电池(standard cell)
标准电池的结构如下图所示,
2004年8月13日
§9-2 可逆电池的表示方法和电池电动势的测定
— 电池电动势的测定和标准电池
标准电池的电池符号为:
10%Cd
(Hg)
CdSO4
•
8 3
H2O(s)饱和溶液
Hg2
SO(4 s),Hg
美国的Wolff提出计算不同温度时Weston标准 电池的电动势公式:
物理化学全程导学及习题全解175-206 第九章可逆电池的电动势及其应用
第九章 可逆电池的电动势及其应用1. 原电池是使化学能能为电能的装置,其主要组成是两个电极和电解液,在等温等压条件下,体系发生变化时,系统吉氏自由能的减少等于对外所做的最大膨胀功.此时转变过程以热力学可逆方式进行,电池为可逆电池.()f ,max r T,pG W =V若非膨胀功只有电功,则(),r T p G nEF =-V如果可逆电动势为E 的电池按电池反应进行进度ξ=1mol 时吉氏自由能的变化值可以写成: ()r T,p G zEF =-V2. 该式是联系热力学和电化学扩要桥梁.可逆电池必须满足的两个条件:1. 电极上的化学反应可向正、反两个方向进行。
可逆电池工作时,电池是在接近平衡养状态下工作的。
可逆电极有以下三种类型:第一类电极:由金属浸在含有该金属离子的溶液构成。
第二类电极:由金属表面覆盖一该金属难溶盐薄层,然后浸入含有该难溶盐负离子的溶液构成。
第三类电极:由惰性金属插入含有某种离子的不同氧化态的溶液中构成电极。
电池的电动势不能直接用伏特计测量。
一般使用对消法。
需要一个电动势已知并且稳定的辅助电池,即标准电池。
常用的标准电池是韦斯顿标准电池。
电极中还包括标准氢电极。
人为规定其电极电势为0电池的书面表示采用的规则是,负极写在在方,进行氧化反应,正极写在右方,进行还原反应用单垂线表示不同物相的界面,用双垂线表示盐桥。
不觉 应注意气体应注明压力,电解质溶液应注明活度。
在书面电极和电池反应时应遵守物量和电荷量守衡。
电动势产生机理:(1)电极与电解质溶液界面间形成的电势差。
(2)接触电势。
(3)液体接界电势。
液接电势可以通过盐桥来减小。
3.可逆电池的热力学及电动势测定的应用。
Nerst 方程 g hGHc dC DIn a a RT E E zF a a =- In RTE K zF=r m T p E S zF ∂⎛⎫= ⎪∂⎝⎭V ,m T r pE H zEF zFT ∂⎛⎫=-+ ⎪∂⎝⎭Vr m R pE Q T S zFT T ∂⎛⎫=⋅= ⎪∂⎝⎭V还原电极电势:Ina RT zF a ϕϕ=--还原态氧化态应用:求电解质溶液的平均活度因子; 求难溶盐的溶度积; pH 值的测定:()s r x s pH pH In10E EF RT -==典型例题讲解例1 以M 代表某金属,MCl 2是其氧化物,是强电解质,设下列电池:()12M|MCl 1mol kg |AgCl|Ag -⋅在0~60℃间的电动势E 与温度之间的关系为: 57 =1.200V+4.0010V+9.0010V E --⨯⨯,25℃时,()()2M |M 0.9636,Ag |Ag |Cl 0.2223V E E ++-==-==(1)写出电极反应及电池反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
题目部分,(卷面共有25题,47.0分,各大题标有题量和总分) 一、选择(25小题,共47.0分)
1.(2分)电极 Tl3+,Tl+/Pt 的电势为?1$=1.250 V,电极 Tl+/Tl 的电势 ?2$=-0.336 V则电极
Tl3+/Tl 的电势 ?3$为: ( ) A、 0.305 V B、 0.721 V C、 0.914 V D、 1.568 V 2.(2分)以下关于玻璃电极的说法正确的是: ( ) A、 玻璃电极是一种不可逆电极 B、 玻璃电极的工作原理是根据膜内外溶液中被测离子的交换 C、 玻璃电极易受溶液中存在的氧化剂、还原剂的干扰 D、 玻璃电极是离子选择性电极的一种 3.(2分)反应 Cu2+(a1)─→Cu2+(a2), 已知 a1>a2, 可构成两种电池 (1) Cu(s)│Cu2+(a2)‖Cu2+(a1)│Cu(s) (2) Pt│Cu2+(a2),Cu+(a')‖Cu2+(a1),Cu+(a')│Pt 这两个电池电动势 E1与E2的关系为: ( ) A、 E1=E2 B、 E1=2 E2
C、 E1=12E2 D、 无法比较 4.(2分)298 K 时,在下列电池的右边溶液中加入 0.01 mol·kg-1的 Na2S 溶液, 则电池的电动势将: ( ) Pt│H2(p?)│H+(a=1)‖CuSO4(0.01 mol·kg-1)│Cu(s) A、 升高 B、 下降 C、 不变 D、 无法判断 5.(1分)已知 ?? (Zn2+,Zn)=-0.763 V, 则下列电池反应的电动势为:Zn(s)+2 H+(a=1)=Zn2+(a=1)+H2(p?) ( ) A、 -0.763 V B、 0.763 V C、 0 V D、 无法确定 6.(2分)已知 ?? (Cl2/Cl-)=1.36 V, ?? (Br2/Br-)=1.07 V, ?? (I2/I-)=0.54 V, ?? (Fe3+/Fe2+)=0.77 V。请判断在相同温度和标准态下说法正确的是: ( ) A、 只有 I- 能被 Fe3+ 所氧化 B、 Br- 和Cl- 都能被 Fe3+ 所氧化 C、 卤离子都能被 Fe3+ 所氧化 D、 卤离子都不能被 Fe3+ 所氧化 7.(2分)298 K 时,已知 ?? (Fe3+,Fe2+)=0.77 V, ?? (Sn4+,Sn2+)=0.15 V, 当这两个电极组成自发电池时, E?为: ( ) A、 1.39 V B、 0.62 V C、 0.92 V D、 1.07 V 8.(2分)在 298 K 时,浓度为 0.1 mol·kg-1和 0.01 mol·kg-1 HCl 溶液的液接电势为EJ(1),浓度为 0.1 mol·kg-1和 0.01 mol·kg-1 KCl 溶液的液接电势 EJ(2) 则: ( ) A、 EJ(1) = EJ(2) B、 EJ(1) > EJ(2) C、 EJ(1) < EJ(2) D、 EJ(1) << EJ(2) 9.(1分)某电池的电池反应可写成:
(1) H2(g) + 12O2(g) ─→ H2O(l) (2) 2H2(g) + O2(g) ─→ 2H2O(l) 用 E1,E2表示相应反应的电动势,K1,K2 表示相应反应的平衡常数,下列各组 关系正确的是: ( ) A、 E1= E2 K1= K2 B、 E1≠ E2 K1= K2 C、 E1= E2 K1≠ K2 D、 E1≠ E2 K1≠ K2 10.(2分)有电池反应:
(1) 12Cu(s) +12Cl2(p?) ─→ 12Cu2+(a=1) + Cl-(a=1) E1 (2) Cu(s) + Cl2(p?) ─→Cu2+(a=1) + 2Cl-(a=1) E2 则电动势 E1/E2的关系是: A、E1/E2= 1/2 B、 E1/E2= 1 C、 E1/E2= 2 D、 E1/E2= 1/4 11.(2分)下列电池中,电动势与氯离子活度无关的电池是: A、 Zn│ZnCl2(aq)‖KCl(aq)│AgCl│Ag B、 Pt│H2│HCl(aq)│Cl2│Pt C、 Ag│AgCl(s)│KCl(aq)│Cl2│Pt D、 Hg│Hg2Cl2(s)│KCl(aq)‖AgNO3(aq)│Ag 12.(2分)电池 Cu│Cu+‖Cu+,Cu2+│Pt 和 Cu│Cu2+‖Cu+,Cu2+│Pt 的反应均可 简写作 Cu + Cu2+ = 2Cu+, 此两电池的: ( )
A、?rGm$,E? 均相同
B、 ?rGm$ 相同, E? 不相同 C、 ?rGm$ 不相同,E? 相同 D、 ?rGm$、E? 均不相同 13.(2分)电池反应中,当各反应物及产物达到平衡时,电池电动势为: ( ) A、 等于零 B、 E? C、 (RT/zF)lnKa D、 不一定 14.(2分)关于液体接界电势 EJ, 正确的说法是: ( ) A、 只有电流通过时才有 EJ存在 B、 只有无电流通过电池时才有 EJ C、 只有种类不同的电解质溶液接界时才有 EJ D、 无论电池中有无电流通过, 只要有液体接界存在, EJ总是存在 15.(2分) 电池中使用盐桥的作用是: ( ) A、使电池变成无液体接界的可逆电池 B、基本消除电池中的液体接界电势 C、消除电池中存在的扩散现象 D、使液体接界电势为零 16.(2分)使用盐桥,将反应Fe2++Ag+ = Fe3++Ag设计成的自发电池是: ( ) A、Ag(s)|Ag+||Fe3+,Fe2+|Pt B、Ag(s)|AgCl(s)|Cl -||Fe3+,Fe2+|Pt C、Pt|Fe3+,Fe2+||Ag+|Ag(s) D、Pt|Fe3+,Fe2+||Cl -|AgCl(s)|Ag(s) 17.(2分)在用对消法测定可逆电池电动势时,通常必须用到: ( ) A、 标准氢电极 B、 甘汞电极 C、 标准电池 D、 活度为 1 的电解质溶液 18.(2分)下列电池中哪个的电动势与 Cl- 离子的活度无关? ( ) A、Zn│ZnCl2(aq)│Cl2(g)│Pt B、 Ag│AgCl(s)│KCl(aq)│Cl2(g)│Pt C、 Hg│Hg2Cl2(s)│KCl(aq)‖AgNO3(aq)│Ag D、 Pt│H2(g)│HCl(aq)│Cl2(g)│Pt 19.(2分)对应电池Ag(s)|AgCl(s)|KCl(aq)|Hg2Cl2(s)|Hg(l)的化学反应是: ( ) A、2Ag(s)+Hg22+(aq) = 2Hg(l) +2Ag+ B、2Hg+2Ag+ = 2Ag +Hg22+ C、2AgCl+2Hg = 2Ag +Hg2Cl2 D、2Ag+Hg2Cl2 = 2AgCl +2Hg 20.(2分)满足电池能量可逆条件的要求是: ( ) A、电池内通过较大电流 B、没有电流通过电池 C、有限电流通过电池 D、有一无限小的电流通过电池 21.(2分)电池可逆对外作电功时, 热效应QR的表示式为: ( )
A、 QR=?rHm B、 QR=zFTpTE)(
C、 QR=zEFpTE)( D、 QR=?rHm+?rGm 22.(2分)把插在AgNO3(1.0 mol·kg-1)溶液中的Ag(s)与插在Cu(NO3)2(1.0 mol·kg-1)溶液中的Cu(s) 利用盐桥连接成电池,这时测出的电动势为: ( ) [设活度系数均为1,E?(Ag+|Ag) = 0.80 V,E?(Cu2+|Cu) = 0.34V ] A、 1.14 V B、 0.46 V C、 - 1.14 V D、 - 0.46 V 23.(1分)恒温、恒压下,可逆电池放电过程的: ( ) A、 ?H = Q B、 ?H < Q C、 ?H > Q D、 ?H与Q的 关系不定 24.(2分)有大小尺寸不同的两个锌锰干电池同时出厂,两者体积比是 5:1,假定两个电池工作环境、工作电流和最后耗尽时的终止电压相同,若小电池初始开路电压为 1.5 V,可以对外输出电能为 W ,则大电池的初始电压和可以对外输出的电能,理论上应该为: ( ) A、 1.5 V W kJ B、7.5 V W kJ C、 1.5 V 5W kJ D、 7.5 V 5W kJ
25.(2分)已知 ?? (Cl2,Cl-) = 1.3595 V, 下列反应12Cl2(p?) + 12H2(p?) = H+ (pH=0, ? (H+)=1) + Cl-(? (Cl-)=1)的 ?rGm值为: ( ) A、 -131.2 kJ·mol-1 B、131.2 kJ·mol-1 C、 -12.60 kJ·mol-1 D、 -262.4 kJ·mol-1
====================答案==================== 答案部分,(卷面共有25题,47.0分,各大题标有题量和总分) 一、选择(25小题,共47.0分) 1.(2分)[答案] B 2.(2分)[答案] D 3.(2分)[答案] C 4.(2分)[答案] B 5.(1分)[答案] B 6.(2分)[答案] A 7.(2分)[答案] B 8.(2分)[答案] B 9.(1分)[答案] C 10.(2分)[答案] B 11.(2分)[答案] C 12.(2分)[答案]
