2012年秋季期 生化理论授课课件-6 酵母核糖酸的分离及组分鉴定
实验4 酵母RNA的分离及组分鉴定

实验4 酵母RNA的分离及组分鉴定酵母RNA是由酵母细胞合成的核糖核酸,包含了酵母细胞的遗传信息,并参与了细胞的生理代谢过程。
本实验旨在通过离心分离和酸性酚/氯仿法提取,纯化酵母RNA,并通过紫外吸收光谱和琼脂糖凝胶电泳等方法对酵母RNA进行组分鉴定。
一、材料与方法1.材料酵母细胞、DTT、Tris、EDTA、NaCl、硝酸、醋酸等。
2.方法1)制备样品a.在液氮中将酵母细胞粉磨成细粉;b.称取10mg酵母细胞粉末加入1ml去离子水中,振荡混匀,制成1mg/ml的酵母细胞悬液。
2)离心分离a.取1ml稀释后的酵母细胞悬液,离心10000rpm/10min,弃去上清液;b.用10μl无菌去离子水重悬沉淀,制成1mg/ml的RNA悬液。
3)RNA的提取和纯化a.取1ml离心沉淀物加入700μl去离子水,混合均匀,加入100μl10%SDS和100μl 酸性酚(pH4.5)混合,振荡15min;b.加入300μl氯仿,振荡混合,离心12,000g/10min;c.取上层水相(约600μl),加入等量异丙醇混合,振荡;d.离心12,000g/5min,弃去上清液,将胶状RNA沉淀用70%酒精重悬,制成1mg/ml的RNA溶液。
4)鉴定RNAa.测定RNA含量和纯度b.通过琼脂糖凝胶电泳检测RNA条带。
c.用紫外吸收光谱测定RNA吸收光谱曲线。
5)结果分析a.通过鉴定RNA的吸收峰和电泳图谱来分析RNA组分。
二、实验结果1.酵母RNA提取和纯化效果良好,制得1mg/ml的RNA溶液。
2.根据紫外吸收光谱结果,可以看到RNA在260nm的吸收峰高于280nm,证明纯化后的RNA具有良好的纯度。
3.琼脂糖凝胶电泳显示,RNA溶液中有一个清晰的28S条带和一个模糊的18S条带,证明RNA转录水平较高。
三、讨论和结论通过离心分离和酸性酚/氯仿法提取纯化酵母RNA,可以得到高质量和高纯度的RNA样品。
此外,琼脂糖凝胶电泳和紫外吸收光谱可以对RNA组分和质量进行鉴定,为后续的RNA研究提供了有价值的基础数据。
实验三酵母核酸的制备及成份鉴定

3.戊糖 根据核糖经浓盐酸或浓硫酸作用则生成糠醛, 后者能与3,5二羟甲苯缩合而形成绿色化合物而鉴定。
• 脱氧核糖在浓酸中生成ω-羟基-γ-酮基戊醛,它和二 苯胺作用生成蓝色化合物。
三、器材
锥形瓶 大研钵 电子天平 离心机 恒温水浴锅
注意仪器使用方法 离心管平衡!!
四、试剂和材料
用95%乙醇洗涤沉淀,离心3min(4000rpm)弃去 上清液,共进行两次。 沉淀可在空气中干燥,即为 酵母RNA的粗制品。
五、操作
2、RNA水解液的制备: 取中2加0热0m1g0分提钟取后的制核成酸水,解加液入并1.进5 M行组H2分SO的4 鉴10定ml。,在沸水浴
3、RNA组分的鉴定:
按顺序以A:B:C:蒸馏水=1:1:1:2(V/V)混匀,现配。 AB馏、、水21中.75%%。(H2NSOH44:)6M将o71O72m4:l浓2.硫5g酸(缓NH缓4)加4入M8o32Om7l溶水于中1。00ml蒸 C、10%Vc:10g Vc溶于100ml蒸馏水中,用棕色瓶贮存。颜 色呈淡黄色时可以使用,如呈深黄或棕色则失效。
实验三 酵母核糖核酸的提取及组分鉴定
(先打开水浴锅,温度设置成100摄氏度) 一、目的 二、原理 三、器材 四、试剂和材料 五、操作 六、注意事项
一、目的
了解核酸的组分,并掌握鉴定核酸组分 的方法以
了解苔黑酚定量测定RNA的方法。
二、原理
酵母核糖核酸中RNA含量较多,RNA可溶 于碱性溶液,在碱提取液中加入酸性乙 醇溶液可以使解聚的核糖核酸沉淀,即 得到RNA的粗制品。
五、操作
1、酵母RNA的提取(2-3人一份) 将4g酵母溶于20ml0.04 M NaOH溶液中(先以少量 NaOH溶液湿润酵母,并充分研磨), 将悬浮液转移 到250ml锥形瓶中,在沸水浴30分钟,不时搅拌,冷 却后转入离心管进行离心 . ----(蛋白质变性沉淀,RNA溶于
实验三 酵母核糖核酸的提取及测定

实验三酵母核糖核酸的提取及测定—预习报告一、研究背景生物大分子物质通常是指动物植物微生物进行新陈代谢时所产生的蛋白质和核酸等有机化合物。
它不仅是生物科学工作者研究者的重要对象,且与化学、医学和食品等工业部门有密切关系。
在科研和医学方面,探讨结构与功能、防治某些疾病时常需要较纯的生物大分子物质。
然而这类物质往往与自然界存在的各种不同的化合物结合在一起或自身之间相互结合在一起,离体后稳定性较差,含量偏低,且提取的材料复杂,因此纯化的方法也很多。
微生物是工业上大量生产核酸的原料,其中酵母最为理想。
本次实验以干酵母粉为实验材料,提取RNA,并测定其含量。
二、研究目标掌握核酸分离纯化的基本设计思想及主要操作细节和生物制品开发的基本思路。
三、研究策略酵母细胞中RNA通常与蛋白质结合。
要提取RNA就要破细胞壁,让它释放出来。
浓盐法通过改变细胞膜的通透性释放出胞内物质,然后沸水浴使RNA水解酶失活。
再通过调节pH将RNA充分沉淀,洗涤,干燥,测量。
四、研究方案及可行性分析浓盐法是在加热条件下,利用高浓度的盐改变细胞膜的通透性,使RNA释放出来。
提取RNA时需注意掌握温度,直接在90~100℃浸提,避免在20~70℃之间的时间过长,磷酸二酯酶和磷酸单酯酶作用活跃的温度范围,会使RNA因降解而降低提取率。
洗涤沉淀时要反复抽提,离心以纯化RNA。
测定提取的核酸含量,只需测定组成核苷酸的任意一种组分即可。
碱基在260nm有光吸收,采用紫外吸收法可测定核酸含量。
五、具体实验设计1、所需主要材料:食品用干酵母粉;试剂:10%NaCl, 6MHCl , 95%乙醇,2%氨水,RNA沉淀剂(0.5g钼酸铵+193ml水+7ml70%过氯酸);仪器设备:烘箱,离心机,天平,紫外分光光度计,移液器,恒温水浴锅,玻璃匀浆器,pH计。
主要器皿:研钵,离心管,容量瓶25ml 50ml;具塞试管;三角瓶;小烧杯。
2、具体操作步骤1.提取:称取7g酵母粉,于研钵中小心研磨成面粉状粉末,转移至三角瓶。
实验三 酵母核糖核酸的提取及测定
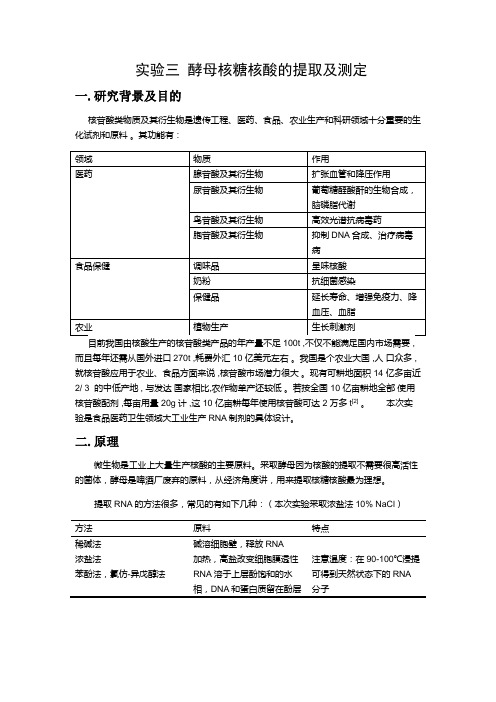
实验三酵母核糖核酸的提取及测定一.研究背景及目的核苷酸类物质及其衍生物是遗传工程、医药、食品、农业生产和科研领域十分重要的生化试剂和原料。
其功能有:二.原理微生物是工业上大量生产核酸的主要原料。
采取酵母因为核酸的提取不需要很高活性的菌体,酵母是啤酒厂废弃的原料,从经济角度讲,用来提取核糖核酸最为理想。
提取RNA的方法很多,常见的有如下几种:(本次实验采取浓盐法10%NaCl)核酸是由糖、碱基、磷酸以一定比例构成的,理论上定量核酸只需测定其中一种即可。
定磷法准确、微量、快速,是最好的方法。
紫外吸收法简单快速,但是当体系内有蛋白质及其他含共轭双键物质存在时干扰较大。
本次实验采用紫外吸收法。
基本的提取策略为:我们可以通过使用化学因素破坏细胞膜,使其中的核酸流出来,接着纯化、测定含量即可。
其中影响我们纯度和定量的主要因素就是蛋白质及有共轭双键物质的干扰,所以,我们的主要目标就是排除蛋白质和有共轭双键物质对含量测定的影响。
尽量保持RNA的完整性有利于提取率。
对于RNA酶的干扰,工业生产的流水化作业,使得人员参与较少,而且工业生产并不像实验室对RNA的完整性要求那么高,所以工业生产中RNA酶的存在不是主要矛盾。
三.仪器与试剂试剂:10%NaCl;6MHCl;95%乙醇(分析纯);2%氨水;RNA沉淀剂仪器:722-分光光度计(上海分析仪器总厂);微量可调手动移液器(大龙牌);具塞试管(15ml);漏斗(25ml一只,50ml两只);研钵;匀浆器;低速离心机(飞鸽牌,TDL-40B,上海安亭科学仪器厂);药物天平(HCTP12B1,北京宣武天平厂制);硫酸纸;烘箱()四.实验步骤按下表进行操作:五.数据整理与结果计算I.干燥RNA 样品含量:260260280一般RNA 的OD 260/ OD 280>2;DNAOD 260/ OD 280约为1.9;样品中有蛋白质含量较高时比值下降。
因此,可推断,该体系为RNA 且较纯。
酵母核糖核酸的提取及测定

酵母核糖核酸的提取及测定酵母核糖核酸的提取及测定⼀、实验背景及⽬的核糖核酸(RNA)和它的降解物核苷酸、核苷及其衍⽣物在⽣物化学、医药、⾷品添加剂、农业等领域有着⼴泛的应⽤。
⽐如能够促进作物的⽣长,在⽔稻、⼩麦、柑橘及多种蔬菜⽣产中应⽤,取得了明显的增产效果。
像鸟苷酸(GMP)和肌苷酸(IMP)还是强⼒助鲜剂,胞苷酸(CMP)和尿苷酸(UMP)可作为⽣产治疗癌症、肝炎及冠⼼病等药物的原料。
⽽利⽤微⽣物资源提取氨基酸、核苷酸等⽣物⼩分⼦,具有成本低、⾮化学合成、⽆毒、⽆害的特点。
[1] 随着啤酒等发酵⾏业的快速发展,产⽣了相应的⼤量发酵副产物,如何利⽤这些副产物,既做到不污染环境,还能产⽣良好的经济效益,⼀直是研究的热点。
⽽啤酒废酵母中RNA 含量达6%~8%,是⽣产RNA的较好原料,此外,抽提后的菌体蛋⽩质(占⼲菌体的50%)还具有很⾼的利⽤价值。
所以利⽤啤酒废酵母⽣产RNA形成了⾮常有益的产业链。
[2] 本实验⽬的就是学习从酵母中提取RNA的⽅法并掌握其测定⼿段。
⼆、实验原理微⽣物是⼯.业上⼤量⽣产核酸的原料,其中以酵母最为理想,酵母核酸中主要是RMA (2.67~10.0%),DNA很少(0.03~0.516%),菌体容易收集,RMA也易于分离。
RMA提制过程是先使RNA从细胞中释放,并使它和蛋⽩质分离,然后将菌体除去,再根据RNA等电点在pH2. 0~2.5的特点,将体系pH调⾄其等电点,使之沉淀,进⾏离⼼收集。
提取RNA的⽅法很多,在⼯业⽣产上常⽤的是稀碱法和浓盐法。
稀碱法利⽤碱使细菌细胞壁⽔解,使RNA释放出来,浓盐法是在加热条件下,利⽤⾼浓度的盐改变细胞膜的通透性,使RNA释放出来,RNA 钠盐易溶于⽔,在含盐的菌体溶液中,RVA 有较⾼的溶解度。
⼆者均通过控制温度使蛋⽩质变性沉淀,通过离⼼将RNA及蛋⽩质和酵母菌体分离,进⽽在等电点沉淀RNA,从⽽达到提取⽬的。
本实验采⽤浓盐法(10% NaCl),是⾷品医药卫⽣领域制备RNA 制剂的经典⽅案。
酵母RNA分离和定量测定(“鉴定”相关文档)共10张

➢ 量取上清,缓缓加入2倍体积的95%乙醇,边倒边搅,待沉淀完全 (静置片刻),再离心,3000r,3min,弃上清。向沉淀中加适量95% 乙醇(10mL)搅散转移到布氏漏斗抽干,重复一次。用乙醚洗沉淀2次。 干滤渣即RNA粗制品,称量并记录总量(M)。
➢ 准确称量50mg干滤渣(M2)用于苔黑酚法测RNA含量,其余的干 滤渣用于以下鉴定
五、实验操作
2. 鉴定
将用于鉴定的干滤渣转移到锥形瓶中,加入10%H2SO4 5mL,煮沸 ( ((用用1232))试)试mi核嘌磷 管管n后糖呤酸取取鉴1碱1mm定LL水水组解解分液液。,,加加入入2m1Lm氨L定水磷,试再剂加,沸入水1m浴L ,Ag观NO察,观察 p嘌干利掌干磷核用核6向稀准嘌R分学称 p布嘌嘌分布R掌 R稀62%H7H7NNN呤滤用握滤酸糖试糖沉碱确呤光会8氏呤呤光氏握碱--试 试AAAN11g与 渣 等 R渣 与 在 管 在 淀 法 称 与 光 用 漏 与 与 光 漏 R法00水干 水水a纸纸%%NNO硝即电即钼浓取浓中提量硝度苔斗硝硝度斗提解酵 解解((AA))H酸R点R酸盐1盐加取5酸计黑及酸酸计及取提 产 母产 提产55,,4m0NN--银控铵酸酸适的银(酚抽银银(抽的0取生于 生取 生m77LAARRm))g水共制试中中量共法滤共共滤R66R的的的的 的粗粗2NNL干775NNAA解热剂,,热测装热热装R9沸原核核原 核制制000AA滤5可可nnN液产作与与产定置产产置水m理糖糖理 糖为为品品%mmA渣溶溶L,生用苔苔生生生R乙浴))及、、及 、析 变 变,,锥(于于N加嘌产黑黑嘌嘌嘌醇3比比方嘌嘌方 嘌出性性称称A形M0碱碱入呤生酚酚呤呤呤(色色法呤呤法 呤R含Rm时量量2瓶性性NN)i2盐磷((盐盐盐1皿皿。碱碱。 碱量,并并n,mAA溶溶0,用基钼基基基3344和和和。应记记m,,L加,,液液00常55于氨L银酸银银银磷磷磷严录录个个可可--入),,搅二二苔水化,化化化酸酸酸格总总用用0搅再再拌羟羟黑,合后合合合.可可可控量量于于散用用。甲甲酚再物者物物物用用用制((RR转乙乙苯苯法加NN的在的的的下下下MpM移醇醇AAH))测入))白还白白白述述述组组。到沉沉及及R1。。色原色色色方方方分分m布淀淀N高高絮剂絮絮絮法法法L鉴鉴A氏得得铁铁状抗状状状A含鉴鉴鉴定定漏到到g盐盐沉坏沉沉沉量定定定N及及斗RR酸酸O淀血淀淀淀,:::NN单单抽3试试。酸。。。AA其,核核干粗粗剂剂(余观苷苷,制制共共或的察酸酸重品品热热硫干制制复。。产产酸滤备备一生生亚渣,,次特特铁用不不。殊殊)于能能的的的以作作绿绿作下为为色色用鉴RR((下定NN66AA形77生生00成nn物物mm蓝活活定定色性性量量的实实))钼验验。。蓝材材(料料6。。603nm定量)。
实验三 酵母核糖核酸的提取及测定
实验三酵母核糖核酸的提取及测定生物111 杨明轩1102040128一、研究背景及目的生物大分子通常指的是动物、植物和微生物进行新陈代谢是所产生的蛋白质、核酸等有机化合物。
它们不仅是生物科学工作者研究的重要对象,而且与化学、医学和食品等工业部门有着密切的关系。
核酸作为生命体常见而重要的大分子物质,它通过酶解或化学法水解可得到4个核苷酸,再经脱磷酸可得4种相应的核苷。
核酸构成遗传物质、传递遗传信息、构成核糖体和酶等大分子、合成多糖,与正常的生命活动密不可分。
医学家、诺贝尔奖得主富兰克研究认为,人体的老化是因其体内的核酸变质减少所致,可见核酸在生物正常发育中的重要性。
由于核酸在生命体中的物质构成、功能方面的作用,近100年来核糖核酸(RNA)被广泛应用与食品工业、医药工业和农业生产上。
在食品工业方面,RNA是开发新型食品调味品、保健品必不可少的原料;在医药工业上,RNA是生产治疗冠心病、肿瘤、心肌梗塞等疾病药物的原料;在农业上,RNA及其衍生物广泛用作农作物的生长促进物质。
而在这些领域,所需要的是并不是结构完整的RNA,而是其单体核苷酸。
因此,我们需要获得能够在食品医药卫生领域应用的核苷酸。
而核酸制品无非是利用其核苷酸或衍生物,因而工业上生产核酸的目的在于获得纯品核苷酸,以作为生产各种药物或测序分析等的原料。
在工业生产中,还常常考虑到利润和成本的问题。
因而实验室里提取核酸和将其放到工业大生产中是不同的。
工业生产对核酸制品的完整性要求不高,而注重其产率和成本。
考虑核苷酸分子的复杂结构,直接化学合成是十分困难的。
所以目前人们主要采取从生物体系中分离纯化RNA,将其水解并通过其他分离手段获得小分子核苷酸的方法。
本实验在于模拟工业生产的流程,探究提取酵母核糖核酸的工艺,掌握提取和测定酵母核糖核酸的方法,明确从生物体中提取RNA的思路和具体操作方法,了解产业开发的思路,体会工业化生产与实验室科研之间的不同。
二、实验原理1、材料的选择由于工业生产上要求的是产品的纯度和产率,对完整性要求不高,我们本次实验的整个设计思路和所用方法都将围绕这一点进行。
实验三酵母核糖核酸(RNA)的提取
精选ppt课件
12
2.磷酸的鉴定:取试管两只,分别标明测 定管与对照管,然后依次加入下列各试剂:
管号
RNA水解 5%H2SO4 钼酸铵试剂 液
测定管 0.2ml
不加
5滴
VC 5滴
对照管 不加
0.2ml
5滴
5滴
放置数分钟,观察两管颜色有何不同。 磷酸+钼酸铵——磷钼酸+Vc——钼蓝
精选ppt课件
13
实验三 酵母菌RNA的提取、鉴定及
定量测定
精选ppt课件
1
一、实验目的
• 掌握稀碱(NaOH)法分离酵母RNA的原理 与方法
• 了解RNA的组分并掌握定性鉴定的具体方法。
精选ppt课件
2
二、实验原理
• (一)目前常用的RNA的制备方法 • 浓盐法:是用高浓度盐溶液处理,同时加热,以改变细胞壁
的通透性,使核酸从细胞内释放出来。成本低、适于大规模 操作。
3.核糖的鉴定:取试管两只,分别标明测定管与 对照管,然后依次加入下列各试剂。
管 号 RNA水解液 5%H2SO4 3,5-二羟甲苯
测定管 4滴
不加
6滴
对照管 不加
4滴
6滴
将两试管放入沸水浴内加热10分钟,比较两管之颜色。
精选ppt课件
14
4.脱氧核糖的鉴定:取两试管分别标明测定管与 对照管,然后依次加入下列各试剂。
管 号 RNA水解液 5%H2SO4 二苯胺
测定管 4滴
不加
6滴
对照管 不加
4滴
6滴
将两试管同时放入沸水浴内,加热10分钟后,比较两 管之颜色。
精选ppt课件
15
思考题
生化实验(四)
至离心管 3000rpm, 离心10分钟
至离心管, 静置5min
3000rpm,
弃去上清液
收集沉淀
沉淀为RNA
离心10分钟
2.RNA的水解
10%硫酸3mL 沸水浴中5min
沉淀
RNA水解
液滴管搅匀
水解液
水解液是否为磷酸、嘌呤碱和核糖?
3.RNA的组分鉴定
(1)磷酸的鉴定
10滴水解液 4滴钼酸铵试剂 4%维生素C 6滴 摇匀 沸水中加热 3-5min
观察有何颜 色变化?
(2)嘌呤碱的鉴定
0.1mol/L 逐滴加
l mol/L氨水
硝酸银5滴
先有沉淀,滴 加到消失后
水解液10滴
观察有无白 色沉淀?
(3)核糖的鉴定
苔黑酚1mL 10滴水解液 混匀 沸水中加热
观察有何颜 色变化?
5-10min
离心机
离心机
五、注意事项
1. RNA提取时,加入10%NaCl搅匀后置 沸水浴10min,加热过程中应至少搅动 两次。 离心时,必须先使用天平对所离心样本 (包括离心套筒)称量配平。离心结束 后,待仪器完全停止转动后方可打开盖 子取出离心管,套管放回原位。 第一次离心结束后,应将上清液一次性 倒入另一试管,避免沉淀漂浮,混入上 清液。 嘌呤碱鉴定时, l mol/L氨水要逐滴加 入。
实验器材
公用试剂
小组试剂
三、实验原理
1、核酸的分类与分布
DNA:主要存在于细胞核的染色体中, 线粒体、叶绿体、质粒有少量 RNA:存在于,其中以RNA含量较多(占干重的 3%-10%)而DNA较少(约占,干重0.5%以下)。
3、浓盐法提取RNA
10%NaCl使RNA核蛋白中的RNA解聚,并溶 于盐溶液中,离心除去菌体残渣及变性蛋白质后, 调节溶液的pH至RNA的等电点(pH2.0~2.5), RNA即可沉淀析出。
生物化学实验报告-酵母RNA的提取与鉴定
实验五酵母RNA的提取与鉴定一、实验目的1.掌握稀碱法分离酵母RNA的原理与操作过程。
2.了解RNA的组分并掌握定性鉴定的具体方法。
二、实验原理1.酵母核酸中RNA含量较多,DNA含量则少于2%。
2.RNA可溶于碱性溶液,当碱被中和后,可加乙醇使其沉淀,有此可得粗RNA制品。
3.用碱液提取的RNA有不同程度的降解三、实验仪器1.离心机2.水浴锅3.电炉4.烧杯5.量筒四、实验试剂1.干酵母粉2.0.2%氢氧化钠溶液:2g氢氧化钠溶于蒸馏水并稀释至1000ml。
3.乙酸4.95%乙醇5.无水乙醚6.10%硫酸7.氨水9.5%硝酸银溶液:5g硝酸银溶于蒸馏水并稀释至100ml,贮于棕色瓶中。
1.苔黑酚-三氯化铁溶液:将100mg苔黑酚溶于100ml浓盐酸中,再加入100mgFeCl3.6H2O。
临用时配制。
五、实验步骤1.RNA的提取:(1)称取2g干酵母粉于100ml烧杯中,加入0.2%氢氧化钠溶液10ml,沸水浴加热30分钟,经常搅拌(如沸水浴过程中溶液蒸干可再加5~10ml氢氧化钠)。
然后加入乙酸数滴,使提取液呈酸性(pH 试纸检验),离心10-15分钟(4000r.p.m)。
(2)取上清液,加入2倍体积的95%乙醇,边加边搅,加毕,静止,待完全沉淀,过滤。
(3)滤渣先用95%乙醇洗2次,每次约5毫升,再用无水乙醚洗2次,每次也约5ml。
(4)洗涤时可小心地用玻璃棒搅动沉淀。
乙醚滤干后,滤渣即为粗RNA,可鉴定。
2.鉴定:(1)取上述RNA约0.5g,加10%硫酸5ml,加热至沸1—2分钟,将RNA水解。
(2)取水解液0.5ml,加入苔黑酚-三氯化铁溶液1ml,加热至沸1分钟,观察颜色变化。
(3)水解液2ml,加入氨水2ml和5%硝酸银溶液1ml,观察是否产生絮状嘌呤银化合物。
六、实验结果加热至沸1分钟后,溶液变成绿色;产生絮状嘌呤银化合物沉淀七、实验分析实验注意事项1.过滤时,洗涤不能带水,否则沉淀粘在滤纸上取不下来。
