标准空气洁净度分级ISO14644-1标准与GMP标准对照表
ISO14644-1_洁净室及相关控制环境国际标准

.洁净室及相关控制环境国际标准ISO14644前言ISO为全球各国标准化团体(ISO 会员团体)的联合会。
其国际标准工作一般是由IS O各技术委员会执行。
每个会员团体若对技术委员会的某一课题感兴趣,均有权作为此技术委员会的代表。
任何与ISO保持联系的国际组织,无论是政府的还是非政府的组织,同样可参加此项工作。
ISO与国际电气技术委员会(IEC)在电气技术标准化方面进行紧密合作。
国际标准草案由其技术委员会认可后送各会员团体进行传阅,以待表决。
草案作为国际标准颁布至少需要75%的会员团体投赞成票。
国际标准ISO 14644-1由ISO/TC209洁净室及相关受控环境技术委员会提出。
ISO 14644在洁净室及相关受控环境的总标题下,由下述各部分组成:第1部分:空气洁净度等级划分第2部分:为认证与ISO 14644-1 连续的相符性的测试和监测技术要求第3部分:计量和测试方法第4部分:设计、施工和启动第5部分:运行第6部分:术语和定义第7部分:增强的洁净装置用户应注意,第2至第7部分的标题为第1部分发行时的工作标题。
如果从工作计划中删除了一部分或几部分,剩余部分可以重新编写。
附录B和C为ISO 14644的组成部分,附录A、D、E和F仅作资料用。
.引言洁净室及相关受控环境保证空气中悬浮粒子被控制在合适的级别,以确保完成对污染敏感的有关活动。
以下行业的产品和工艺均得益于空气中悬浮污染物的控制:航天、微电子、医药、医疗器械、食品和保健品。
ISO 14644的本部分指定ISO分级的各级别,以此作为洁净室及相关受控环境内空气洁净度的技术要求。
本部分不仅确定了空气中悬浮粒子测试的程序,而且确定了测试的标准方法。
为划分等级,ISO 14644的本部分仅限于确定粒子浓度限值用的指定的粒径范围。
本部分还提供了标准协议,以依据大于或小于指定分级用粒径范围的悬浮粒子浓度等级标识。
ISO 14644的本部分为洁净室和污染控制系列标准中的一个标准。
无尘车间等级划分标准

无尘车间等级划分标准无尘车间是一种对环境要求非常高的生产场所,它的等级划分标准对于保障生产过程的洁净度至关重要。
无尘车间等级的划分标准主要是根据车间内空气中悬浮颗粒物的数量和大小来确定的。
根据国际标准,无尘车间的等级划分主要包括ISO 14644-1和GMP两种标准。
ISO 14644-1标准是国际上对无尘车间等级划分的基本标准,它将无尘车间的洁净度等级划分为ISO 1至ISO 9共10个等级。
ISO 1级是洁净度最高的等级,允许的最大颗粒物数量为每立方米不超过10个;而ISO 9级则是洁净度最低的等级,允许的最大颗粒物数量为每立方米超过35,200个。
ISO 14644-1标准的等级划分主要是根据车间内空气中的颗粒物数量来确定的,这些颗粒物的大小范围从0.1微米到5微米不等。
GMP是药品生产领域常用的无尘车间等级划分标准,它将无尘车间的洁净度等级划分为A、B、C、D四个等级。
其中A级是洁净度最高的等级,适用于对洁净度要求非常高的生产环境,比如药品生产;而D级则是洁净度最低的等级,适用于对洁净度要求较低的生产环境,比如普通物流仓储。
在无尘车间的等级划分标准中,除了空气中悬浮颗粒物的数量和大小外,还包括了空气流速、温度、湿度、静电等因素。
这些因素的控制对于保障无尘车间的洁净度至关重要,它们直接影响着生产过程的质量和效率。
在实际生产中,无尘车间的等级划分标准需要根据具体的生产环境和产品要求来确定。
不同行业、不同产品对于无尘车间的洁净度要求是不同的,因此在设计和运行无尘车间时,需要根据实际情况来确定适合的洁净度等级划分标准。
总的来说,无尘车间的等级划分标准是保障生产过程洁净度的重要依据,它直接影响着产品质量和生产效率。
在实际应用中,需要根据国际标准和行业标准来确定适合的洁净度等级划分标准,同时结合实际情况进行调整,以确保无尘车间的洁净度达到要求,满足生产的需要。
GMP对洁净度的等级要求

GMP洁净车间空气洁净度等级,“药品生产质量管理规范”(GMP)中规定:药品生产的洁净厂房内的生产环境参数如:温度和相对湿度以及压差等均是由生产工艺决定的,一般温度为18℃~24℃,相对湿度为45%~65%。
在“药品生产质量管理规范”(GMP)的实施指南中规定的比较具体。
即药品生产洁净厂房中的温度和相对湿度是以穿洁净工作服的操作人员不产生不舒服、不舒适为基准的。
无菌药品的生产所需的洁净区可以分为四个级别A 级:高风险操作区,如灌装区、放置胶塞桶和与无菌制剂直接接触的敞口包装容器的区域及无菌装配或连接操作的区域,应当用单向流操作台(罩)维持该区的环境状态。
单向流系统在其工作区域必须均匀送风,风速为0.36-0.54m/s(指导值)。
应当有数据证明单向流的状态并经过验证。
在密闭的隔离操作器或手套箱内,可使用较低的风速。
B 级:指无菌配制和灌装等高风险操作A 级洁净区所处的背景区域。
C 级和D 级:指无菌药品生产过程中重要程度较低操作步骤的洁净区。
以上各级别空气悬浮粒子的标准与ISO14644-1中洁净度等级(以≥0.5μm和≥5μm的悬浮粒子为限度标准)的关系.注:此表摘自《药品生产质量管理规范2010版》洁净度A级用于高风险作业区,如:灌装区、放胶塞区、敞口包装容器区和无菌装配区等区域。
其单向流区工作区必须均匀送风,其风速为0.36 m/s ~0.54 m/s。
确认A级,每个测点的采样量不得少于1 m3;洁净度为ISO 4.8级,并以≥5.0 µm悬浮粒子的浓度为限度标准。
采样管的长度要短,以勉≥5.0 µm的粒子沉降,影响测试结果。
单向流应采用等动力采样。
洁净度B级用于洁净度A级区域的背景区域。
静态洁净度为ISO 5级。
C级和D级用于无菌药品生产过程中工艺要求洁净较低的区域。
C级静态和动态分别为ISO 7级和ISO 8级。
D级静态为ISO 8级。
动态可采用培养基模拟灌装过程以证明达到动态洁净度级别。
洁净室(无菌室)分级

洁净室(无菌室)洁净室(无菌室)是微生物检测的重要场所和最基本的设施,是微生物检测质量的重要保证。
按洁净厂房设计规范要求设计,并按JGJ71—1990 《洁净室的施工及验收规范》(原JGJ7190废止,更新GB50591-2010 (2011。
2.1实施)的方法和标准方法执行.分级要求见表我国GMP实施指南提出的级别。
实验室总体布局和各部位的安排应有利于减少潜在的对样本的污染和对人员的危害,实验室应有效控制进入无菌或洁净等特定区域的人员。
应按定期消毒洁净室(无菌室),按洁净室标准监测。
空气洁净级别不同的相邻区间的静压差大于5Pa,洁净室与室外大气的静压差大于10 Pa。
洁净厂房设计规范 GB50073—2001 (部分章节)第一章总则第二章空气洁净度等级第2.0.1条空气洁净度应按表2。
0.1规定划分为四个等级。
注:对于空气洁净度为100级的洁净室内大于等于5微米尘粒的计算应进行多次采样。
当其多次出现时,方可认为该测试数值是可信的。
2.0。
2条洁净室空气洁净度等级的检验,应以动态条件下测试的尘粒数为依据。
洁净室空气洁净度的测试,应符合附录二规定。
医药工业洁净室(区)悬浮粒子浮游菌和沉降菌的测试方法GB/T16292~16294—1996,已更新为2010版保健食品良好生产规范GB17405—1998网上资料洁净室是一个超级洁净的环境,它不但要控制通风、过滤、温度、湿度、气压以及离子化等,还要同时对环境内的材料和其他参数进行控制.洁净室的洁净度决定于空气中的悬浮微粒数量,微粒的首要计量单位是微米,即10-6米,大致相当于0.000039英寸。
洁净室级别划分最为通行使用的方法来自ISO14644标准。
该标准以每立方米空气中0。
1微米的微粒来划分洁净室级别,它取代了过去的美国国家标准209—1992(详见表1),而后者是以每立方英尺空气中0。
5微米的微粒数来划分洁净级别的。
按照这两个标准规定,209标准中的100级洁净室中每立方英尺空气中大于等于的0。
净化级别划分和规定
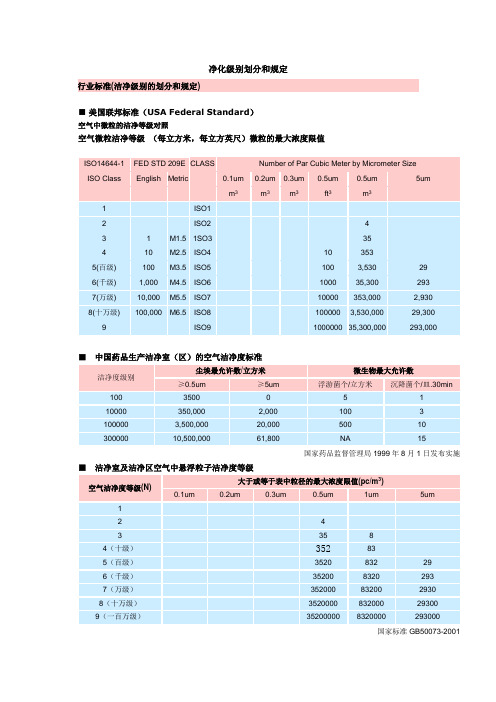
ISO9
1000000
35,300,000
293,000
■中国药品生产洁净室(区)的空气洁净度标准
洁净度级别
尘埃最允许数/立方米
微生物最大允许数
≥0.5um
≥5um
浮游菌个/立方米
沉降菌个/皿.30min
100
3500
0
5
1
10000
350,000
2,000
100
3
100000
3,500,000
20,000
ISO14644-1
FED STD 209E
CLASS
Number of Par Cubic Meter by Micrometer Size
ISO Class
English
Metric
0.1um
0.2um
0.3um
0.5um
0.5um
5um
m3
m3
m3
ft3
m3
1
ISO1
2
ISO2
4
3
1
M1.5
1SO3
35
4
10
M2.5
ISO4
10
353
5(百级)
100
M3.5
ISO5
100
3,530
29
6(千级)
1,000
M4.5
ISO6
1000
35,300
293
7(万级)
10,000
M5.5
ISO7
10000
353,000
2,930
8(十万级)
100,000
M6.5
ISO8
100000
ISO_ 14644-1_2015 中文

国际标准ISO 14644-1第二版2015年12月15日洁净室和相关受控环境第一部分:根据粒子浓度划分空气洁净度等级内容:前言简介1 范围2参考标准3术语和定义3.1 通则3.2 尘埃粒子3.3 占用状态3.4 测试仪器(见附件F)3.5 仪器标准4 分级4.1占用状态4.2 粒子粒径4.3 ISO等级序数4.4 命名4.5 十进制的洁净度中间等级和粒径阈值5 相符性认证5.1 原则5.2 测试5.3 尘埃粒子浓度评估5.4 测试报告附件A(标准)根据粒子浓度对空气洁净度进行分级的基准方法附件B(资料)分级计算举例附件C(资料)尘埃粒子计数和粒径附件D(资料)顺序采样法附件E(资料)十进制的洁净度中间等级和粒径阈值的标准附件F(资料)测试仪器参考文献ISO 为全球各国标准化团体(ISO 会员团体)的联合会。
其国际标准工作一般是由ISO 各技术委员会执行。
每个会员团体若对技术委员会的某一课题感兴趣,均有权作为此技术委员会的代表。
任何与ISO 保持联系的国际组织,无论是政府的还是非政府的组织,同样可参加此项工作。
ISO与国际电气技术委员会(IEC)在电气技术标准化方面进行紧密合作。
ISO/IEC法令第1部分描述了用来制订此文件的规程和后期修订。
特别应注意的是不同类型ISO文件需要不同经批准的标准。
此文件的修订与ISO/IEC法令第2部分的编辑规则一致。
(见/directives)需注意的是此文件的一些内容可能受专利权保护。
ISO不对其中单个或所有专利权的辨别负责。
在制订文件过程中,任何专利权细节的辨别将会在简介和/或ISO专利声明清单里出现。
(见/patents)此文件中出现的任何商标名仅仅是为了便于用户,并不构成要约。
有关一致性评估的ISO特定术语和表达的意义解释,以及ISO在贸易技术性壁垒中坚持接近WTO原则的信息,见以下链接:Foreword - Supplementary information负责此文件的是ISO/TC 209洁净室和相关受控环境技术委员会。
空气洁净度等级
空气洁净度等级air clea nli ness class洁净空间单位体积空气中,以大于或等于被考虑粒径的粒子最大浓度限值进行划分的等级标准。
空气净化等级的划分:一般在洁净室内有登记的,采用多种工序操作时,应根据各工序不同的要求,采用不同的空气洁净度等级,依据工序要求确定等级。
医药工业药生产工序的洁净级别和洁净区的划分,应参照《药品生产质量管理规范中制剂和原料药工艺内容及环境区域划分而定。
药品生产洁净室的空气洁净度划分为四个等级。
在满足生产工艺要求的前提下,首先应采用低洁净等级的洁净湿或局部空气净化;其次可采用局部工作区域空气净化和第等级全市空气净化相结合或采用全面空气净化。
也有的地方按空气过滤的等级一般通风用过滤器分类一大气尘记数法GB12218-89 分级I II 川IV V粒径(卩m > 5.0 > 1.0粒径(卩m)> 5.0 > 1.0欧洲现行分类比重法(%) Arrestance比色法或计数法(%) Dust-spot 最易穿透粒径法(%)美国效率规格计数法(%)Particle Efficiency 计重法(%)Arrestanee•药品生产洁净室(区)的空气洁净度划分为四个级别:结净室(区)空气洁净级别表洁净度级别尘粒最大允许数/立方米微生物最大允许数> 0.5 卩m >5m 浮游困/立方米沉降菌/皿100级3,500 0 5 110,000 级350, 0002,000 1003100,000级3, 500, 00020, 000 50010300,000级10,500, 00060, 000 1000 15> 0.5> 0.5Or Particle Efficie ncy。
最全洁净室等级标准
最全洁净室等级标准【洁净室等级标准】空气洁净度:洁净空气中含尘量多少的程度(即含尘浓度)。
含尘浓度高则洁净度低,含尘浓度低则洁净度高。
1、美国空军技术条令世界上第一个洁净度标准。
1961年3月问世。
美国联邦标准的基石。
2、美国联邦标准2091963年12月问世。
洁净室等级标准可以分为以下几个:洁净室(洁净室)需要将一定范围内空气中的微粒子、有害空气、细菌等之污染物排除,并将无尘室内温度、洁净度、室内压力、气流速度与气流分布、噪音振动及照明、静电控制在某一需求范围内,为了达到这些效果而专门设计的无尘室不论外部空气如何变化,其室内均能有效维持原先所设定要求的洁净度、温湿度及压力等性能之特性。
洁净室可以分为以下几个级别:也就是说值越小,净化级别就越高。
洁净度越高造价就越高。
无尘洁净室洁净度级别:一级>十级>百级>千级>万级>十万级>三十万级1级这个级别的洁净室主要用于制造集成电路的微电子工业,对集成电路的精确要求为亚微米。
10级这个级别的洁净室主要用于带宽小于2微米的半导体工业。
100级很多人认为,这一级洁净室是最常用因而是最重要的洁净室,人们常常错误地将100级洁净室称为无菌室,以说明“无菌”的或“无尘”的环境要求,100级无尘室可用于医药工业的无菌制造工艺等,这一洁净室大量应用于,植如体内物品的制造,外科手术,包括移植手术,集成器的制造,那些对细菌感染特别敏感的病人的隔离治疗,比如像骨髓移植病人术后的隔离治疗。
1000级(即千级洁净室)这个级别的洁净室主要用于高质量光学产品的生产,还用于测试,装配飞机蛇螺仪,装配高质微型轴承等。
10000级万级洁净室用于液压设备或气压设备的装配,某些情况下也用于食品饮料工业,此外,万级洁净室在医工业中也很常用。
100000级十万级洁净室用于很多的工业部门,比如光学产品的制造,用于较小的元器件制造大型的电子系统,液压或气压系统的制造,食品饮料的生产,医、药工业也常常使用这一级洁净室。
ISO14644-1_洁净室及相关控制环境国际标准要点
洁净室及相关控制环境国际标准ISO14644前言ISO 为全球各国标准化团体(ISO 会员团体)的联合会。
其国际标准工作一般是由IS O 各技术委员会执行。
每个会员团体若对技术委员会的某一课题感兴趣,均有权作为此技术委员会的代表。
任何与ISO 保持联系的国际组织,无论是政府的还是非政府的组织,同样可参加此项工作。
ISO 与国际电气技术委员会(IEC )在电气技术标准化方面进行紧密合作。
国际标准草案由其技术委员会认可后送各会员团体进行传阅,以待表决。
草案作为国际标准颁布至少需要75%的会员团体投赞成票。
国际标准ISO 14644-1 由ISO/TC209 洁净室及相关受控环境技术委员会提出。
ISO 14644 在洁净室及相关受控环境的总标题下,由下述各部分组成:第1 部分:空气洁净度等级划分第2 部分:为认证与ISO 14644-1 连续的相符性的测试和监测技术要求第3 部分:计量和测试方法第4 部分:设计、施工和启动第5 部分:运行第6 部分:术语和定义第7 部分:增强的洁净装置用户应注意,第2 至第7 部分的标题为第1 部分发行时的工作标题。
如果从工作计划中删除了一部分或几部分,剩余部分可以重新编写。
附录B和C为ISO 14644 的组成部分,附录A、D、E和F仅作资料用。
引言洁净室及相关受控环境保证空气中悬浮粒子被控制在合适的级别,以确保完成对污染敏感的有关活动。
以下行业的产品和工艺均得益于空气中悬浮污染物的控制:航天、微电子、医药、医疗器械、食品和保健品。
ISO 14644 的本部分指定ISO 分级的各级别,以此作为洁净室及相关受控环境内空气洁净度的技术要求。
本部分不仅确定了空气中悬浮粒子测试的程序,而且确定了测试的标准方法。
为划分等级,ISO 14644 的本部分仅限于确定粒子浓度限值用的指定的粒径范围。
本部分还提供了标准协议,以依据大于或小于指定分级用粒径范围的悬浮粒子浓度等级标识。
ISO 14644 的本部分为洁净室和污染控制系列标准中的一个标准。
中国新版GMP洁净度级别-2010新版GMP洁净区等级划分
中国新版GMP洁净度级别-2010新版GMP洁净区等级划分《药品生产质量管理规范(2010年修订)》(新版GMP)于2011年3月1日起施行,本文主要介绍新版GMP中关于洁净度等级中的A、B、C、D四个级别,以及新版GMP与98版中关于洁净度等级的区别。
GMP中A、B、C、D级控制上有动静态之分,而百级、万级、十万级则基本无动静态之分,两者之间有着明显的差异。
新版GMP参照ISO14644中规定具体标准如下:新版GMP采用了欧盟和最新WHO的A、B、C、D分级标准,并对无菌药品生产的洁净度级别提出了非常具体的要求。
静态测量:是指所有设备均已安装就绪,但未运行且没有操作人员在现场的状态。
动态测量:是指生成设备均按预定的工艺模式运行且有规定数量的操作人员在现场操作的状态。
无菌药品的生产所需的洁净区可以分为4个级别: 2010新版GMP洁净区等级划分A级:高风险操作区,如灌装区、放置胶塞桶和与无菌制剂直接接触的敞口包装容器的区域及无菌装配或连接操作的区域,应当用单向流操作台(罩)维持该区的环境状态。
单向流系统在其工作区域必须均匀送风,风速为0.36-0.54m/s(指导值)。
应当有数据证明单向流的状态并经过验证。
在密闭的隔离操作器或手套箱内,可使用较低的风速。
?B级:指无菌配制和灌装等高风险操作A级洁净区所处的背景区域。
C级和D级:指无菌药品生产过程中重要程度较低操作步骤的洁净区中国 GMP(2010修订)2010年版GMP附录1 无菌药品,第三章,第九条……洁净区各级别空气悬浮粒子的标准规定如下表:新版GMP洁净度等级A、B、C、D?A级洁净区??洁净操作区的空气温度应为?20-24℃??洁净操作区的空气相对湿度应为?45%-60%?操作区的风速:水平风速≥0.54m/s????????垂直风速≥0.36m/s?高效过滤器的检漏大于99.97%?照度:>300lx-600lx??噪音:≤75db(动态测试)??B级洁净区???洁净操作区的空气温度应为?20-24℃???洁净操作区的空气相对湿度应为?45%-60%?房间换气次数:≥25次/h?压差:??B级区相对室外≥10Pa,同一级别的不同区域按气流流向应保持一定的压差。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
标准空气洁净度分级ISO14644-1标准与xxGMP标准、与xx手术室标准对照表空气洁净度等级(N) 大于或等于表中粒径的最大浓度限值(pc/m3) (个/每立方米空气粒子)
xxGMP规定;
1)洁净区的设计必须符合相应的“静态”标准,以达到“动态”的洁净要求。
“静态”是指安装已经完成并已运行,但没有操作人员在场的状态。
而“动态”是指生产设施按预定工艺模式运行并有规定数量的操作人员现场操作的状态.
2)生产操作全部结束,操作人员撤离生产现场并经15~20 min(指导值)自净后,洁净区应达到表中的“静态”标准。
药品或敞开容器直接暴露环境微粒动态测试结果应达到表中A级的标准。
3)无菌操作的隔离操作器所处环境的级别至少应为D级。
4)为了确定A级区的级别,每个采样点的采样量不得少于。
A级区空气尘埃粒子的级别为ISO 4.8,以≥0.5μm 的尘粒为限度标准。
B级区(静态)的空气尘埃粒子的级别为ISO 5,同时包括表中两种粒径的尘粒。
对于C级区(静态和动态)而言,空气尘埃粒子的级别分别为ISO 7和ISO 8。
对于D级区(静态)空气尘埃粒子的级别为ISO 8。
测试方法可参照ISO14644-1。
5)在确认级别时,应使用采样管较短的便携式尘埃粒子计数器,以避免在远程采样系统长的采样xx≥5.0μm 尘粒的沉降。
在单向流系统中,应采用等动力学的取样头。
6)可在常规操作、培养基模拟灌装过程中进行测试,证明达到了动态的级别,但培养基模拟试验要求在“最差状况”下进行动态测试。
附表;洁净区微生物监测的动态标准(1)。
