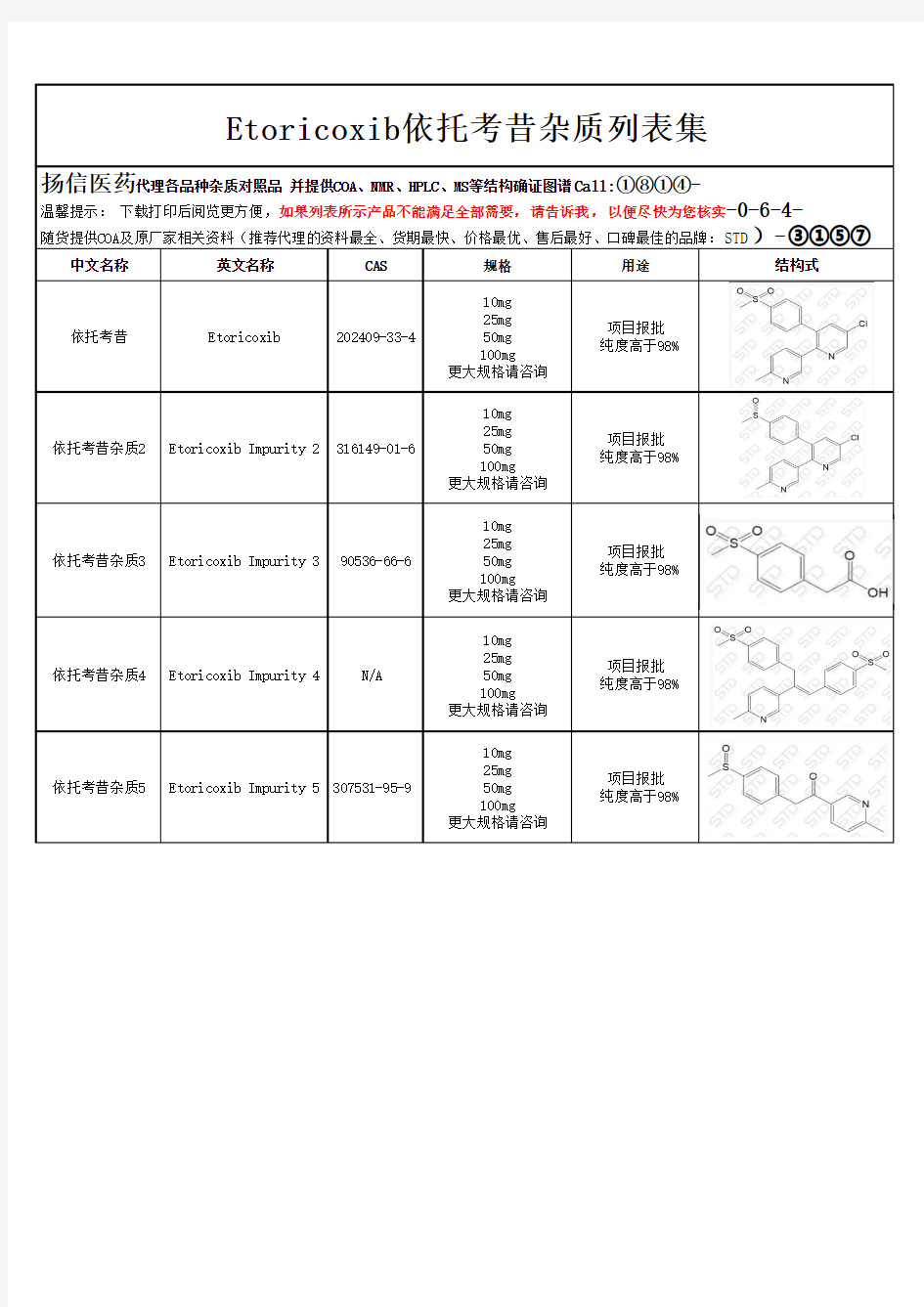
Etoricoxib依托考昔杂质列表集
塞来昔布(西乐葆)说明书
药品名称: 通用名称:塞来昔布胶囊 英文名称:Celebrex (Celecoxib Capsules) 商品名称:西乐葆 成份: 塞来昔布 适应症: 在决定使用本品前,应仔细考虑本品和其他治疗选择的潜在利益和风险。根据每例患者 的治疗目标,在最短治疗时间内使用最低有效剂量(见【注意事项】-警告)。 1)用于缓解骨关节炎的症状和体征。 2)用于缓解成人类风湿关节炎的症状和体征。 3)用于治疗成人急性疼痛。(见【临床试验】) 4)作为常规疗法(如:内镜监测,手术)的一项辅助治疗,可减少家族性腺瘤息肉(FAP) 患者的腺瘤性结直肠息肉的数目。目前尚不清楚FAP患者腺瘤性结直肠息肉数目减少的 临床益处。停用本品后其治疗效果是否能维持还不明确。尚无本品治疗FAP患者超过6 个月的疗效和安全性的研究(见【临床试验】、【注意事项】-警告和注意事项)。 规格: (1)0.1g (2) 0.2g 用法用量: 在决定使用本品前,应仔细考虑本品和其他治疗选择的潜在利益和风险。根据每例患者 的治疗目标,在最短治疗时间内使用最低有效剂量(见【注意事项】-警告)。 骨关节炎和类风湿关节炎,根据个体情况决定本品治疗的最低剂量。进食的时间对此使 用剂量没有影响。 骨关节炎:本品缓解骨关节炎的症状和体征推荐剂量为200mg,每日一次口服或1OOmg 每日两次口服。 类风湿关节炎:本品缓解类风湿关节炎的症状和体征推荐剂量为1OOmg至200mg,每日
两次。急性疼痛:推荐剂量为第1天首剂400mg,必要时,可再服200mg;随后根据需要, 每日两次,每次200mg。 家族性腺瘤息肉(FAP): FAP患者在接受本品治疗时,应继续其常规的治疗。用于FAP 患者减少腺瘤性结直肠息肉数目治疗时,推荐剂量为口服400mg (200mg胶囊两粒)每 日两次,与食物同服。特殊人群 肝功能受损患者:中度肝功能损害患者(Child-Pugh II级)本品的每日推荐剂量应减 少大约50%。不建议严重肝功能受损患者使用本品(见[药代动力学]-特殊人群)。 不良反应: 在临床对照研究中,已有大约4250例骨关节炎(OA)患者,2100例类风湿关节炎(RA) 患者和1050例术后疼痛患者接受本品治疗。其中超过8500例患者接受的每日总剂量达 200mg(1OOmg每日两次或200mg每日一次)或更高,包括400多例患者接受每日总剂量 达800mg(400mg每日两次)。约有3900例患者接受上述剂量6个月或6个月以上,其 中约2300例患者达一年或一年以上,124例达2年或2年以上。 关节炎上市前的临床对照研究中的不良事件: 在有安慰剂或阳性药物对照的12项临床研究中,不良事件导致的停药率在塞来昔布胶囊 组是7.1%,在安慰剂组为6.1%。本品组最常见的因不良事件而停药的原因是消化不良和 腹痛(在接受本品治疗的患者中分别为0.8%和0.7%)。安慰剂组0.6%的患者因消化不 良而退出研究,因腹痛退出的患者也为0.6%。 关节炎对照研究中塞来昔布胶囊治疗组发生率大于2%的不良事件 表3显示了在骨关节炎(OA)或类风湿关节炎(RA)患者中进行的12个含安慰剂和/或 阳性药物组的临床对照研究中所有塞来昔布胶囊治疗组发生率大于2%的不良事件(不论 是否与治疗有无因果关系),由于这12项试验的研究期限不同,这些试验中的患者使用 药物的时间不同,所以从这些百分数中不能得到累积发生率。 以下为不论是否与治疗有因果关系,发生率小于2%(0.1-1.9%)的不良事件(患者服用 塞来昔布胶囊100-200mg每日两次或200mg每日一次) 胃肠道系统:便秘、憩室炎、吞咽困难、打嗝、食道炎、胃炎、胃肠炎、胃食管反流、 痔疮、裂孔疝、黑粪症、口干、口腔炎、里急后重、牙齿不适、呕吐 心血管系统:高血压加重、心绞痛、冠状动脉病变、心肌梗塞 全身性:敏感症加重、过敏反应、衰弱、胸痛、非特定囊肿、全身水肿、面部水肿、疲 劳、发热、面部潮红、感冒样症状、疼痛、周围疼痛 免疫系统疾病:单纯性疱疹、带状疱疹、细菌感染、真菌感染、软组织感染、病毒感染、 念珠菌病、生殖系统念珠菌病、中耳炎 中枢周围神经系统:腿抽筋、张力亢进、感觉迟钝、偏头痛、神经痛、神经病、感觉异 常、眩晕 女性生殖系统:乳腺纤维腺瘤、乳腺肿瘤、乳房痛、痛经、月经失调、阴道流血、阴道 炎 男性生殖系统:前列腺疾病
【CN109810060A】一种塞来昔布基因毒性杂质及其制备方法与应用【专利】
(19)中华人民共和国国家知识产权局 (12)发明专利申请 (10)申请公布号 (43)申请公布日 (21)申请号 201910220811.5 (22)申请日 2019.03.22 (71)申请人 天地恒一制药股份有限公司 地址 410331 湖南省长沙市长沙国家生物 产业基地康天路109号 (72)发明人 贺境杰 曾伟强 高玉贺 程雪清 王衡新 (51)Int.Cl. C07D 231/12(2006.01) (54)发明名称 一种塞来昔布基因毒性杂质及其制备方法 与应用 (57)摘要 本发明公开了一种塞来昔布基因毒性杂质 及其制备方法与应用,所述杂质化学名称为4- (2-氧-5-对甲苯基-3-三氟甲基-吡唑-1-基)-苯磺酰胺,结构如下: 式Ⅰ。制备过程是将塞来昔布和氧化剂在有机溶剂中搅拌反应,经HPLC监控反应完成后,经萃取、分液、浓缩后得到粗品,再经过柱层析纯化后得到。该方法操作简单,反应条件温和,产物纯度 高,可用于塞来昔布基因毒性杂质研究及检测用 对照品,有利于塞来昔布的杂质控制和质量研究,从而提高塞来昔布的质量控制水平,降低塞 来昔布的毒副作用。权利要求书2页 说明书4页 附图2页CN 109810060 A 2019.05.28 C N 109810060 A
权 利 要 求 书1/2页CN 109810060 A 1.一种塞来昔布基因毒性杂质,其特征在于,所述杂质化学名称为4-(2-氧-5-对甲苯基-3-三氟甲基-吡唑-1-基)-苯磺酰胺,具有式Ⅰ所示的结构: 式Ⅰ。 2.根据权利要求1所述的一种塞来昔布基因毒性杂质,其特征在于,所述杂质具有如下的核磁数据: 1HNMR(DMSO-d6 400MHz) :7.96 (d,2H),7.69(d,2H),7.59(s,2H), 7.18(s,1H),7.15(s,4H),2.26(s,3H);其中各峰位移±0.2ppm。 3.一种塞来昔布基因毒性杂质的制备方法,其特征在于,所述方法为基于式Ⅱ在溶剂 中与氧化剂反应生成权利要求1中式Ⅰ 的过程: 式Ⅱ 式Ⅰ。 4.根据权利要求3所述的一种塞来昔布基因毒性杂质的制备方法,其特征在于,所述氧化剂为双氧水、过氧乙酸或间氯过氧苯甲酸的任一种或其组合。 5.根据权利要求3所述的一种塞来昔布基因毒性杂质的制备方法,其特征在于,所述溶剂为三氟乙酸、乙酸或水的任一种或其组合。 6.根据权利要求3所述的一种塞来昔布基因毒性杂质的制备方法,其特征在于,所述方法具体包括以下步骤: 步骤一、将塞来昔布和有机溶剂按重量比1:8-20加入至反应瓶中,搅拌,控制温度﹣5-25℃,再加入1-3倍的氧化剂,继续搅拌,保温4-30h完成反应; 步骤二、将步骤一制备的反应物进行萃取、分液、浓缩后得到粗产品; 步骤三、将步骤二得到的粗产品经过柱层析纯化后得到式I化合物。 7.根据权利要求6所述的一种塞来昔布基因毒性杂质的制备方法,其特征在于,所述步骤一中加入氧化剂后反应在HPLC监控下完成;所述步骤二中采用二氯甲烷作为萃取剂。 8.根据权利要求7所述的一种塞来昔布基因毒性杂质的制备方法,其特征在于,所述步骤三中过柱层析的洗脱剂为二氯甲烷和甲醇,比例为1:0-40:1。 2
西药执业药师药学专业知识(一)模拟题280含答案
西药执业药师药学专业知识(一)模拟题280 一、最佳选择题 每题的备选答案中只有1个最佳答案 1. 宜选用塞来昔布治疗的疾病是 A.肾绞痛 B.痛风 C.胃溃疡 D.支气管哮喘 E.骨关节炎 答案:E [解答] 本题考查塞来昔布的临床作用。塞来昔布为COX-2抑制药,主要用于治疗风湿性关节炎或骨关节炎。故答案为E。 2. 下述说法正确的是 A.男性一般较女性对药物敏感 B.患者心理状态会影响药物作用 C.中年人一般较老年人对药物敏感 D.成人一般较儿童对药物敏感 E.在正常状态和疾病状态药物作用是一样的 答案:B [解答] 本题考查机体方面对药物的影响。女性对药物比男性更敏感,因男性比女性摄入更多脂肪及胆固醇,通常高脂肪食物会减少药物吸收;此外,皮下脂肪含量也有性别差异,女性较男性丰富,这可能影响到经皮吸收药物疗效。一般老年人比中年人对药物敏感,因为老年人的生理功能逐渐减退,对药物的耐受性相应也较差。儿童比成人对药物敏感。正常状态和疾病状态药物作用是不一样的。
故答案为B。 3. 心脏骤停时,心肺复苏的首选药物是 A.间羟胺 B.去甲肾上腺素 C.肾上腺素 D.多巴胺 E.异丙肾上腺素 答案:C [解答] 本题考查药物的临床作用。肾上腺素能激动心脏的β1受体,使心肌收缩加强,收缩时间缩短,心率加快,传导加速,心输出量增加,并舒张冠状血管,增加心肌血液供应,且作用迅速,是一种强效的心脏兴奋药,在心脏骤停时,作为心肺复苏的首选抢救药。故答案为C。 4. 硝酸甘油抗心绞痛的药理学基础是 A.增强心肌收缩力 B.改善心肌供血 C.松弛血管平滑肌 D.降低心肌耗氧量 E.以上说法均不对 答案:E [解答] 本题考查硝酸甘油的作用机制。硝酸甘油防治心绞痛的药理学基础是改变心肌血流分布,增加缺血区血流灌注。故答案为E。 5. 在治疗量时,主要兴奋大脑皮质的药物是 A.尼可刹米 B.咖啡因
西乐葆(塞来昔布胶囊)
西乐葆(塞来昔布胶囊) 【药品名称】 商品名称:西乐葆 通用名称:塞来昔布胶囊 英文名称:Celecoxib Capsules 【成份】 本品主要成分及其化学名称为:塞来昔布,4-[5-(4-甲苯基)-3-(三氟甲基)-1氢-1-吡唑-1-基]苯磺酰胺 【适应症】 用于治疗急性期或慢性期骨关节炎和类风湿关节炎的症状和体征。 【用法用量】 成人骨关节炎:推荐剂量为200mg,每日1次或分2次口服。临床研究中也曾用至每日400mg的剂量。 关节炎类风湿关节炎:推荐剂量为100mg或200mg,每日2次。临床研究中的剂量曾用至每日800mg。 老年人:不必调整剂量。 肝功能损伤患者:轻至中度肝功能损害患者无需调整剂量,对于重度肝功能损害患者无临床使用经验。 肾功能损伤患者:轻至中度肾功能损害患者无需调整剂量,对于重度肾功能损害患者无临床使用经验。 儿童:塞来昔布没有在18岁以下人群中进行过临床研究。 【不良反应】
在对照临床试验中报告的不良反应按发生率分类为:>1%,但等于或少于安慰剂组:中枢神经系统:头痛。胃肠道:便秘、恶心。其他:关节痛、腰背痛、失眠、肌痛、外周痛、瘙痒。>1%,发生率高于安慰剂组(括号内%为高于安慰剂组的百分数):中枢神经系统:眩晕(0.4%)。胃肠道:腹痛(1.8%)、腹泻(2.3%)、消化不良(2.2%)、胀气(1.2%)、牙齿疾病(0.1%)、呕吐(0.6%)。呼吸道:支气管炎(0.2%)、咳嗽(0.7%)、咽炎(1.2%)、鼻炎(0.6%)、鼻窦炎(0.1%)、上呼吸道感染(0.2%)。其他:意外受伤(0.4%)、过敏加重(0.2%)、流感样症状(0.4%)、外周水肿(0.4%)、皮疹(0.1%)、尿道感染(0.2%)。在超过3000病人年的临床研究中,未证实本品与致命的、严重的或罕见的不良反应有因果关系。 【禁忌】 对本产品中任何成份过敏者。已知对磺胺过敏者。 【注意事项】 塞来昔布含有磺胺基团。临床研究中,哮喘患者服用本品后未发生支气管痉挛,但由于未在阿司匹林或其他非甾类抗炎药诱发哮喘、荨麻疹或急性鼻炎的患者中评估本品,因此,尚未有研究资料以前,此类患者应避免服用本品。对驾驶和操作机器能力的影响:没有研究过本品对驾驶汽车和操作能力的影响,但基于其药效学及总体安全性特征来看,应不会影响这类能力。 【特殊人群用药】 儿童注意事项: 塞来昔布没有在18岁以下人群中进行过临床研究。 妊娠与哺乳期注意事项: 没有关于妊娠期应用本品的资料,只有潜在益处大于对胎儿的危害时,妊娠妇女才可以考虑用本品治疗。动物试验中观察到的对早期胚胎的影响主要与COX-2的抑制有关,如胚胎着
孟鲁司特钠杂质-(最新结构)列表
名称结构cas及其他 Montelukast R, R-Isomer CAS No. N/A C41H46ClNO5S2 M.W. 732.41 Montelukast R, S-Isomer CAS No. N/A C41H46ClNO5S2 M.W. 732.41 cis-Montelukast CAS No. 774538-96-4 C35H36ClNO3S M.W. 586.20 Montelukast Impurity I C35H36ClNO4S M.W. 602.20 Montelukast Keto Carbinol Impurity CAS No. N/A C34H32ClNO4S M.W. 586.16 Montelukast Impurity H CAS No. 851755-56-1 C34H32ClNO4S M.W. 586.16 Montelukast S-Enantiomer Sodium Salt C35H35ClNO3S.Na M.W. 585.19 22.99
Montelukast Sulfone C35H36ClNO5S M.W. 618.20 Montelukast Dihydro Impurity CAS No. 142147-98-6 C35H38ClNO3S M.W. 588.22 Montelukast Cyclopropacetaneamide Impurity CAS No. 866923-63-9 C35H37ClN2O2S M.W. 585.21 Montelukast 1, 2-Diol CAS No. 186352-97-6 C35H36ClNO4S M.W. 602.20 Montelukast CN Impurity CAS No. N/A C35H35ClN2OS M.W. 567.20 Montelukust Keto Impurity CAS No. N/A C28H24ClNO2 M.W. 441.96 Montelukast Related Impurity 1 CAS No. 1258428-71-5 C29H26ClNO2 M.W. 455.99 Montelukast Related Impurity 2 CAS No. 149968-11-6 C28H22ClNO3 M.W. 455.95
塞来昔布说明书
. 塞来昔布 【药物名称】 中文通用名称:塞来昔布Celecoxib 英文通用名称:其他名称:塞来考昔、西乐葆、Celebrex。 【临床应用】 1.用于缓解骨性关节炎的症状和体征。 2.用于缓解成人类风湿关节炎的症状和体征。 3.用于幼年型类风湿关节炎(国外资料)。 4.作为常规疗法(内镜监测、手术等)的辅助治疗,可减少家族性腺瘤息肉(FAP)患者腺瘤性结直肠息肉量。 5.用于强直性脊柱炎、原发性痛经、急性疼痛。 【药理】 1.药效学本药是昔布类非甾体类抗炎药(NSAIDs),能特异性抑制环氧酶-2(COX-2)。炎性因子可诱导COX-2生成,导致炎性前列腺素类物质的合成和聚集,尤其是前列腺素E,从而引起局部炎症、2水肿和疼痛。而本药可通过抑制COX-2阻止炎性前列腺素类物质的产生,达到抗炎、镇痛及解热作用。 1 / 48 . 体外及体内试验表明,本药与基础表达的环氧酶-1(COX-1)的亲和力极弱,治疗剂量下不影响由COX-1激活的前列腺素类物质的合成,因此不干扰组织中与COX-1相关的正常生理过程,尤其是在胃、肠
和肾等组织中。 2.药动学本药口服吸收迅速而完全,相对生物利用度约为99%(相对于口服混悬液),口服后约3小时达血药峰浓度。食物可延缓其吸收。药物吸收后广泛分布于全身各组织。稳态分布容积约为400L,血浆蛋白结合率约为97%。本药主要在肝脏经细胞色素P 2C9(CYP 2C9)代谢,已证实血浆中有3种代谢产物(醇、相应的450羧基酸和其葡糖苷酸结合物),代谢产物对COX-1、COX-2无抑制活性。服用单剂放射性核素标记的药物后,57%从粪便排出,27%随尿液排泄,粪便及尿液中的绝大多数代谢产物为羧基酸(给药剂量的73%)。少量葡糖苷酸从尿液排泄,仅有少于3%给药量的药物以原形从粪便及尿液中排泄。多次给药无蓄积作用。血液透析不能有效清除药物。 【注意事项】 1.禁忌症(1)对本药过敏者。(2)对阿司匹林或其他NSAIDs过敏者(可诱发哮喘、荨麻疹或过敏反应,有严重甚至致死的过敏反应报道)。 (3)对磺胺类药过敏者。(4)冠状动脉搭桥手术(CABG)围手术期疼痛患者。(5)重度肝功能不全者。(6)进行性肾脏疾病患者。 2 / 48 . 2.慎用(1)有支气管哮喘、过敏性鼻炎、荨麻疹史者。(2)肾功能不全者。(3)高血压或心脏疾病患者(可能因体液潴留或水肿而加重)(国外资料)。(4)有胃肠道溃疡、出血、穿孔史者(国外资料)。(5)有肝功能不全史者(国外资料)。 3.药物对儿童的影响国内尚无18岁以下患者用药的安全性及有效
塞来昔布胶囊
塞来昔布胶囊 【药品名称】 通用名称:塞来昔布胶囊 英文名称:Celecoxib Capsules 【成份】 本品主要成分及其化学名称为:塞来昔布,4-[5-(4-甲苯基)-3-(三氟甲基)-1氢-1-吡唑-1-基]苯磺酰胺 【适应症】 用于治疗急性期或慢性期骨关节炎和类风湿关节炎的症状和体征。 【用法用量】 成人骨关节炎:推荐剂量为200mg,每日1次或分2次口服。临床研究中也曾用至每日400mg的剂量。 关节炎类风湿关节炎:推荐剂量为100mg或200mg,每日2次。临床研究中的剂量曾用至每日800mg。 老年人:不必调整剂量。 肝功能损伤患者:轻至中度肝功能损害患者无需调整剂量,对于重度肝功能损害患者无临床使用经验。 肾功能损伤患者:轻至中度肾功能损害患者无需调整剂量,对于重度肾功能损害患者无临床使用经验。 儿童:塞来昔布没有在18岁以下人群中进行过临床研究。 【不良反应】 在对照临床试验中报告的不良反应按发生率分类为:>1%,但等于或少于安慰剂组:中枢
神经系统:头痛。胃肠道:便秘、恶心。其他:关节痛、腰背痛、失眠、肌痛、外周痛、瘙痒。>1%,发生率高于安慰剂组(括号内%为高于安慰剂组的百分数):中枢神经系统:眩晕(0.4%)。胃肠道:腹痛(1.8%)、腹泻(2.3%)、消化不良(2.2%)、胀气(1.2%)、牙齿疾病(0.1%)、呕吐(0.6%)。呼吸道:支气管炎(0.2%)、咳嗽(0.7%)、咽炎(1.2%)、鼻炎(0.6%)、鼻窦炎(0.1%)、上呼吸道感染(0.2%)。其他:意外受伤(0.4%)、过敏加重(0.2%)、流感样症状(0.4%)、外周水肿(0.4%)、皮疹(0.1%)、尿道感染(0.2%)。在超过3000病人年的临床研究中,未证实本品与致命的、严重的或罕见的不良反应有因果关系。 【禁忌】 对本产品中任何成份过敏者。已知对磺胺过敏者。 【注意事项】 塞来昔布含有磺胺基团。临床研究中,哮喘患者服用本品后未发生支气管痉挛,但由于未在阿司匹林或其他非甾类抗炎药诱发哮喘、荨麻疹或急性鼻炎的患者中评估本品,因此,尚未有研究资料以前,此类患者应避免服用本品。对驾驶和操作机器能力的影响:没有研究过本品对驾驶汽车和操作能力的影响,但基于其药效学及总体安全性特征来看,应不会影响这类能力。 【特殊人群用药】 儿童注意事项: 塞来昔布没有在18岁以下人群中进行过临床研究。 妊娠与哺乳期注意事项: 没有关于妊娠期应用本品的资料,只有潜在益处大于对胎儿的危害时,妊娠妇女才可以考虑用本品治疗。动物试验中观察到的对早期胚胎的影响主要与COX-2的抑制有关,如胚胎着床前后流产,但对长期的生殖功能无影响。致畸研究发现,塞来昔布对家兔无致畸作用。在
塞来昔布治疗类风湿性关节炎疗效观察
塞来昔布治疗类风湿性关节炎疗效观察 作者单位:201822 上海市嘉定区中心医院通讯作者:谭利民 目的探讨塞来昔布治疗类风湿性关节炎的疗效。方法将本院2009年12月~2010年6月收治的60例类风湿关节炎分为观察组和对照组。对照组采用常规治疗,观察组采用塞来昔布治疗。比较两组患者的临床疗效、关节疼痛指数、肿胀指数、握力、晨僵、血沉的变化及不良反应。结果观察组显效12例,有效9 例,总有效率为700%显著高于对照组的500%,差异有统计学意义(P<005)。且观察组的关节疼痛指数、肿胀指数、握力、晨僵和血沉的改善显著优于对照组,差异有统计学意义(P<005)。观察组的不良反应显著少于对照组,差异有统计学意义(P<005)。结论塞来昔布治疗类风湿性关节炎疗效较好, 且不良反应较少,值得临床推广。标签:塞来昔布;类风湿性关节炎;疗效;不良反应doi:10.3969/j.issn.1674-4985.2012.01.020类风湿性关节炎(RA)是一种以关节和关节周围组织的非感染性炎症为主的全身性自身免疫性疾病,其病因至今尚未完全明了。该病发作时关节肿胀明显,疼痛剧烈,致残率高,是造成人群丧失劳动力和致残的主要原因之一[1]。非甾体类抗炎药是治疗类风湿性关节炎的主要药物,主要是通过抑制还氧化酶1和还氧化酶2来发挥镇痛和消炎的作用,但该类药物的胃肠道的不良反应较大。塞来昔布是一种特异性COX2抑制剂,既能消炎镇痛,又无胃肠道反应。本院2009年12月~2010年6月采用塞来昔布治疗RA患者30例,疗效满意,现报告如下。1资料与方法 11一般资料60例均为本院收治的类风湿性关节炎患者,所有病例均符合1987年美国风湿病协会(ARA)类风湿关节炎分类诊断标准。所有入选患者均经医生详细询问病史,仔细体格检查,入选标准为:(1)病程在>6个月;(2)3个或3个以上的关节肿胀,肿胀>6周;(3)关节触痛≥6个;(4)晨僵持续时间≥45 min至少超过6周;(5)红细胞沉降率(ESR)≥28 mm/h;(6)C反应蛋白(CRP)≥正常上限的15倍;(7)至少2周未服用任何抗类风湿性关节炎药物。排除银屑病性关节炎、红斑狼疮、骨性关节炎、强直性脊柱炎。其中男18例,女42例,年龄38~75岁,平均(525±112)岁,病程1~12年。X线均提示有胸、 腰椎钙化并呈竹节样改变。将该组患者按照治疗方法的不同分为观察组和对照组,每组30例。两组患者在年龄、性别、病程、临床表现、关节压痛、肿胀等 方面差异具有统计学意义(P>005),具有可比性。 12治疗方法(1)对照组采用常规方法治疗,按照药物的每日推荐推荐用
玻璃酸钠联合塞来昔布治疗膝关节骨性关节炎的临床疗效观察
第37卷2013年第10期 黑龙江医学 H E I L O N G J I A N G,M ED I C A L J O U R N A L V01.37.N o.10 0cL2013943 玻璃酸钠联合塞来昔布治疗膝关节骨性关节炎的临床疗效观察 刘世海,郑海萍,何藻鹏,黄继辉 (佛山市顺德区乐从医院,广东佛山528315) 摘要:目的观察玻璃酸钠联合塞来昔布治疗膝关节骨性关节炎的临床疗效。方法将本院收治的108例膝关节骨性关节炎患者随机分为3组,即联合治疗组(A组,40膝)、玻璃酸钠治疗组(B组,40膝)及塞来昔布治疗组(C组,40膝)。结果3组患者经用药治疗l周后,评价其疗效,差异无统计学意义(P>0.05);经6周用药治疗后,再评价其疗效,发现A组疗效优于B、C组,总有效率差异有统计学意义(P<0.05);在不良反应观察中发现A组不良反应率与B、C组相比较,差异有统计学意义(P<0.05)。结论短期内各组用药疗效未见明显差别,但中长期治疗效果经观察发现,玻璃酸钠联合塞来昔布治疗膝关节骨性关节炎,能明显改善症状,且疗效持久、不良反应少,值得临床推广。 关键词:玻璃酸钠;塞来昔布;膝关节;骨性关节炎 doi:10.3969/j.i s s n.1004—5775.2013.10.016 学科分类代码:320.2745中图分类号:R684.3文献标识码:A St udy蛐Ⅱ地T r姻衄ent of KⅡ∞ost eoar t ht i t融w i伍Som哪H yal um眦t e锄d C el e∞】db/LI U SK—hai,Z I瑶N G H ai—pi ng,衄Zao—p蚰g,“甜.//(“cD醒目唧妇f o,鼬口砌P历曲勃f,Fos加n528315,C H矾A) A bS恤眦:O bj删靶To obs er ve t he em cac y of s odi um hya l urona t e com bi ned w i t h ce l e coxi b i n t11e t re a t m ent of ost e oaI t hr i t i s of knee j oi nt.M em ods B y se l ec t i ng a ho spi t a l cl i ni c al l y pat i en t s di a gnos ed w i t h ost eoar t hr i t i s of t he knee,108ca se s w a s di vi de d i nt o A,B and C group s i n accor d粕ce w i tl I t lle pr i nc i pl e of r al l dom aU0cati on,舳d each group has40kne es.R姻l l l t s A f t e r on e w ee k of t he r apy,t l l e em c a—cy of dm e pa t i ent s t est ed by t he Lyshol m r at i ngs粕d t Il eir di&rence w∞not s t at i s ti cal l y s i gIl i fi cal l t(P>0.05).A ft er si x w eeks of t her a-py,t l l e em cac y of t l l ree pa t i ent s t e st e d by t he L ys hol m枷ngs and t hei r di雎rence w船s诅t i st i c al l y si印i6c锄t(P>0.05).T hat i U ust r at e s t l l e疆i cacy of gm up A w a s ben er t l l粕B柚d C gr oup.T I l m ugh com p撕ng a dver se r e ac t i on r a t es of gm up A w i t h t he ot he r gm ups,t he d证er ence w鹊st at i st i c al l y si脚c柚t(P<0.05).C∞d吣i蛐r I.1le s h on—t er n l em cac y of仃eat m en t i n each group s how ed n o dim r ence,but tl le l ong—t e瑚t陀atm ent dfe ct of s odi um hyal u m nat e com bi ned w i t h ce l e coxi b t I℃at m e nt of kn ee os t eoanhr i t i s c an s i gni6cand y i m pr ove s ym pt om s,l as t i ng e岱e ct,a dve I s e r e act i oI l s,and f ew er a dver se r eact i ons.T he co m bi n at i o n t he ra py s houl d be pI.0m o t ed.K ey w or ds:S0di um hyal u啪砒e;Cel eco灿;K nee;0st eo柚ri t i s 随着年龄增长,骨性关节炎(0s t eoanIl矗t i s,0A)发病率不断增高。研究发现,60岁以上人群表现出O A患者达50%以上,而膝关节骨性关节炎是常见的O A类疾病…。膝关节骨性关节炎主要病理过程是关节损伤、软骨软化、关节退行性病变等,继发肌肉、滑膜和关节囊炎症的病变心J。研究报道表明,高分子多糖类物质在临床上治疗骨性关节炎取得较理想的疗效,尤其是玻璃酸钠临床应用广泛,但其疗效不能持久且容易复发。因此,本研究主要观察玻璃酸钠与抗炎药塞来昔布联合治疗膝关节骨性关节炎的临床疗效及其不良反应,确定膝关节骨性关节炎较好的治疗方式,现报告如下。 1资料与方法 1.1临床资料 选取2012—04—2013—04间医院收治的108例确诊为膝关节骨性关节炎患者,按照随机分配原则及就诊时间的先后顺序将患者分为玻璃酸钠联合塞来昔布治疗组(A组),玻璃酸钠治疗组(B组)及塞来昔布治疗组(C组)。其中A组36例,男性21例,女性15例,年龄37—69岁,平均年龄60.18岁,病程5个月~8年,40膝;B组35例,男性19例,女性16例,年龄38—76岁,平均年龄62.59岁,病程3个月~10年,40膝;c组37例,男性21例,女性14例,年龄38~71岁,平均年龄63.14岁,病程4个月~9年,40膝。3组患者性别、年龄、病程时间等方面经统计学分析,差异无统计学意义(P>O.05)。1.2临床诊断标准 依照1995年美国风湿病学会(A m er i can col l ege of R heum at ol ogy,A C R)推荐的膝关节骨性关节炎诊断标准p1:(1)近1月大多数有膝疼痛感;(2)有骨摩擦声响; (3)晨僵30I I l i n以上;(4)年龄为35岁以上患者;(5)患者有骨性膨大;(6)x射线照片显示有骨赘。其中同时达到(1)、(2)、(3)、(4)描述症状患者,或(1)、(2)、(5)描述症状患者,或(1)、(4)、(5)描述症状患者,或(1)、(6)描述症状患者,均可被诊断为膝关节骨性关节炎。1.3病例入选标准 (1)符合上述诊断标准;(2)长期服用药物者,需停用药物2周后可纳入观察;(3)年龄35~80岁;(4)站
塞来昔布胶囊
商品名:西乐葆 通用名:塞来昔布胶囊 【药理学作用】 塞来昔布是非甾体类抗炎药,动物模型中观察到其有抗炎、镇痛和退热的作用。塞来昔布胶囊的作用机理是通过抑制环氧化酶-2(COX-2)从而抑制前列腺素的生成。在人体治疗浓度下,本品对同工酶—环氧化酶-1 (COX-1)无抑制作用。在动物结肠肿瘤模型中,塞来昔布减缓了肿瘤的发生和进展。 【适应症】 1. 缓解骨关节炎的症状和体征 2. 缓解成人类风湿关节炎的症状和体征 3. 辅助治疗家族性腺瘤息肉(FAP) 【剂量与用法】 骨关节炎:本品用于缓解骨关节炎的症状和体征的推荐剂量为200mg,每日一次口服,或100mg,每日两次口服。 类风湿关节炎:本品用于缓解类风湿关节炎的症状和体征的推荐剂量为100mg至200 mg, 每日两次。 家族性腺瘤息肉(FAP):FAP患者在接受本品治疗时,应继续其常规治疗。用于FAP患者减少腺瘤性结直肠息肉数目治疗时,推荐剂量为口服400mg(200mg胶囊两粒)每日两次,与食物同服。 肝功能损伤患者:中度肝功能损害患者(Child-Pugh II级) 的推荐剂量是常规剂量的约50%。儿童用药:目前尚无关于18岁以下儿童应用本品的疗效和安全性的资料。 老年患者用药:在以肾小球滤过率、尿素氮和肌酐检测肾功能,出血时间和血小板聚集检测血小板功能的临床研究中,发现在老年和年轻的志愿者中无差异。 【禁忌】 本品禁用于对塞来昔布过敏者。本品不可用于已知对磺胺过敏者。本品不可用于服用阿司匹林或其他非甾体类抗炎药后会诱发哮喘、荨麻疹或过敏反应的患者。 【警告】 胃肠道(GI) 疗效—GI溃疡、出血和穿孔的危险性接受非甾体类抗炎药治疗的患者,可在任何时候伴或不伴预先症状出现严重的胃肠道毒性如:胃、小肠或大肠的出血、溃疡和穿孔。较轻的上消化道反应(如消化不良) 较常见且可见于非甾体抗炎药(NSAIDs)治疗过程的任何时候。 过敏反应 上市后用药经验表明,使用本品的患者极少发生过敏反应和血管性水肿。与普通NSAIDs 相同,在未服用过本品的患者中也可以发生过敏反应。本品不应用于有阿司匹林三联征的患者。 进展期肾脏疾病 尚无在进展期肾脏疾病的患者中应用本品的报道。如必须使用,应密切监测患者的肾功能。妊娠期 在妊娠晚期应避免使用本品。
塞来昔布说明书
塞来昔布 【药物名称】 中文通用名称:塞来昔布 英文通用名称:Celecoxib 其他名称:塞来考昔、西乐葆、Celebrex。 【临床应用】 1.用于缓解骨性关节炎的症状和体征。 2.用于缓解成人类风湿关节炎的症状和体征。 3.用于幼年型类风湿关节炎(国外资料)。 4.作为常规疗法(内镜监测、手术等)的辅助治疗,可减少家族性腺瘤息肉(FAP)患者腺瘤性结直肠息肉量。 5.用于强直性脊柱炎、原发性痛经、急性疼痛。 【药理】 1.药效学本药是昔布类非甾体类抗炎药(NSAIDs),能特异性抑制环氧酶-2(COX-2)。炎性因子可诱导COX-2生成,导致炎性前列腺素类物质的合成和聚集,尤其是前列腺素E2,从而引起局部炎症、水肿和疼痛。而本药可通过抑制COX-2阻止炎性前列腺素类物质的产生,达到抗炎、镇痛及解热作用。
体外及体内试验表明,本药与基础表达的环氧酶-1(COX-1)的亲和力极弱,治疗剂量下不影响由COX-1激活的前列腺素类物质的合成,因此不干扰组织中与COX-1相关的正常生理过程,尤其是在胃、肠和肾等组织中。 2.药动学本药口服吸收迅速而完全,相对生物利用度约为99%(相对于口服混悬液),口服后约3小时达血药峰浓度。食物可延缓其吸收。药物吸收后广泛分布于全身各组织。稳态分布容积约为400L,血浆蛋白结合率约为97%。本药主要在肝脏经细胞色素 P450 2C9(CYP 2C9)代谢,已证实血浆中有3种代谢产物(醇、相应的羧基酸和其葡糖苷酸结合物),代谢产物对COX-1、COX-2无抑制活性。服用单剂放射性核素标记的药物后,57%从粪便排出,27%随尿液排泄,粪便及尿液中的绝大多数代谢产物为羧基酸(给药剂量的73%)。少量葡糖苷酸从尿液排泄,仅有少于3%给药量的药物以原形从粪便及尿液中排泄。多次给药无蓄积作用。血液透析不能有效清除药物。 【注意事项】 1.禁忌症 (1)对本药过敏者。(2)对阿司匹林或其他NSAIDs过敏者(可诱发哮喘、荨麻疹或过敏反应,有严重甚至致死的过敏反应报道)。(3)对磺胺类药过敏者。(4)冠状动脉搭桥手术(CABG)围手术期疼痛患者。(5)重度肝功能不全者。(6)进行性肾脏疾病患者。
塞来昔布对伴有关节炎的缓解期溃疡性结肠炎患者的安全性评价
塞来昔布对伴有关节炎的缓解期溃疡性结肠炎患者的安全性评价 摘要目的观察塞来昔布对伴有关节炎的缓解期溃疡性结肠炎(UC)患者的影响,为指导临床安全、合理用药提供临床依据。方法61例伴有关节炎且处于缓解期UC患者,使用前瞻性研究方法随机分成治疗组(32例)和对照组(29例)。治疗组在综合治疗基础上口服塞来昔布治疗,对照组在综合治疗基础上加用安慰剂治疗,疗程均为1个月,治疗前后分别对患者进行Mayo评分及病理组织学分级,评估两组患者的肠道炎症情况。结果两组治疗前后组内、组间Mayo评分中排便次数、便血量、结肠镜下肠黏膜损害、医生总体评价比较差异均无统计学意义(P>0.05)。病例分级:对照组治疗前后比较差异无统计学意义(P=0.489>0.05);治疗组治疗前后比较差异无统计学意义(P=0.794>0.05);两组治疗前比较差异无统计学意义(P=0.931>0.05);两组治疗后比较差异无统计学意义(P=0.531>0.05)。结论口服塞来昔布1个月不增加伴有关节炎的缓解期UC患者肠道损害,疗效安全有效。 关键词塞来昔布;溃疡性结肠炎;关节炎;Mayo评分 溃疡性结肠炎(ulcerative colitis,UC)是一种病因尚不十分清楚的直肠和结肠慢性非特异性炎症性疾病。临床表现为腹泻、粘液脓血便、腹痛、里急后重,病情轻重不等,可以有皮肤、黏膜、关节、眼、肝胆等损害的肠外表现[1]。其中关节损害最为常见,发生率可达35%[1]。临床上对伴有关节炎的UC患者往往需要口服非甾体类消炎药(NSAIDs)。NSAIDs共同的作用机制是抑制体内环氧合酶(cyclooxygenas,COX)活性。非选择性COX抑制剂,因其抑制COX-1,减少胃肠道及肾脏等部位生理性前列腺素的产生,从而表现出各种毒副作用。塞来昔布属于COX-2抑制剂,在抑制炎症组织前列腺素的产生从而发挥抗炎、消肿和镇痛的同时,减少胃肠道损伤等副作用。为更好评估选择性NSAIDs对伴有关节炎UC患者的安全性,指导临床合理用药,本文选取不同患者口服塞来昔布和安慰剂,通過各种指标了解其对UC患者的影响。现报告如下。 1 资料与方法 1. 1 一般资料选取2014年6月~2016年8月在枣庄市立医院消化内科住院并符合入选标准的61例伴有关节炎的缓解期UC患者。入选标准:①所有患者均符合UC诊断标准,经过积极药物治疗后UC患者处于缓解期。②伴有关节损害:外周关节炎或脊柱关节炎。③需长期口服NSAIDs维持治疗。将患者随机分成治疗组(32例)和对照组(29例)。治疗组:男18例,女14例,年龄18~65岁,中位年龄36岁。对照组:男16例,女13例,年龄20~59岁,中位年龄33岁。两组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。 1. 2 方法所有患者治疗前后均行血常规、尿常规、大便常规、肝肾功、离子、肿瘤标记物检查,同时了解排便次数、血便次数,治疗前后均行电子结肠镜检查,同时取组织送病理。两组处于缓解期UC患者继续给予5-氨基水杨酸
