有机试剂在分析中的应用_习题解析
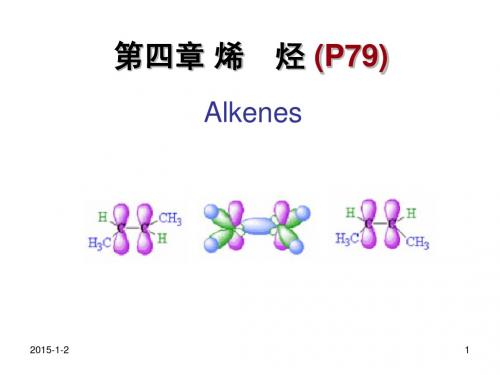
第4章 烯烃
CH CH2 CH3CH2CHCHCH3 CH3
CH3
H CH3 C C H CH2CH3
4-甲基-3-乙基-1-戊烯
(E)-3,5-二甲基-3-庚烯
2015-1-2
23
§4.2 烯烃的制法(P103)
一、烯烃的工业来源和制法 低级烯烃主要是通过石油的各种馏分裂解和原油直接裂 解得到。
原料不 同或裂解 条件不同 得到各种 烯烃的比 例也不同
价原子数目,Z为氮等三价原子数,氧为0. 三键看作两个双键.
2015-1-2
6
一、烯烃的命名
普通命名法(见书上4.1.1) IUPAC命名法 1)选主链:选择含双键最长的碳链为主链,命”某烯”. 2)编号码:近双键端开始编号,将双键位号写在母体名称前. 3)名支链:支链基团作为取代基.
3-乙基-1-己烯
Csp2 变为Csp3 ,平面结构变为四面体结构。
加 成
2015-1-2
31
烯烃加成的三种主要类型
C C + A B C A C B
加 成
重点
亲电加成
A A A
B B B H2
A A
+ +
B B
(异裂)
自由基加成
催化加氢
(均裂)
2015-1-2
32
(一)烯烃的亲电加成反应
H C H C H H
2015-1-2 7
例:命名下列化合物:
1)选主链:含双键最长的碳链 8 8
CH3C CCH2CH2CH2CH2CH2 CH2 CH2 CH2CH2CH3
11
• 含双键的,最
2)编号码:起始编号,双键的标号 • 靠近双键端起编号,命名时标明双键位次
苯胺二苯胺磷酸显色剂原理_概述说明以及解释

苯胺二苯胺磷酸显色剂原理概述说明以及解释1. 引言1.1 概述苯胺二苯胺磷酸显色剂是一种常用的有机试剂,常用于生物化学分析、化学传感器开发以及工业检测与监控等领域。
它具有较强的显色能力和选择性,能够在特定的反应条件下与目标物质发生化学反应并形成可见的色谱,从而实现对目标物质的检测和分析。
本文将详细介绍苯胺二苯胺磷酸显色剂的原理、应用领域以及实验方法和步骤,并对其未来的研究方向和重点进行展望。
1.2 文章结构本文主要分为五个部分。
引言部分介绍了文章的背景和目的,并概括描述了苯胺二苯胺磷酸显色剂的概述和应用领域。
接下来的部分将详细探讨该显色剂的原理、化学反应过程以及显色机制。
然后,文章将阐述该显色剂在生物化学分析、化学传感器开发以及工业检测与监控等领域中的具体应用情况。
接着,文章将对使用苯胺二苯胺磷酸显色剂的实验方法和步骤进行详解,并对实验结果进行分析和讨论。
最后,本文将总结已有的研究成果并探讨未来进一步研究的方向和重点。
1.3 目的本文旨在全面介绍苯胺二苯胺磷酸显色剂的原理、应用领域和实验方法,为读者提供一个清晰的概述说明。
通过深入了解该显色剂的化学反应过程和显色机制,读者可以更好地理解其在不同领域中的应用场景和优势。
此外,本文还将对该显色剂未来的研究方向和重点进行展望,以期为相关研究人员提供一定的参考和启示。
2. 苯胺二苯胺磷酸显色剂原理:2.1 理论基础:苯胺二苯胺磷酸显色剂是一种常用的有机显色剂,其原理主要基于化学反应和显色机制。
该显色剂由两个苯环通过一个二苯胺磷酸分子相连组成,具有稳定的结构和特殊的性质。
2.2 化学反应过程:在分析过程中,苯胺二苯胺磷酸与待测物发生化学反应,形成可见光吸收或发射的产物,引起溶液颜色的变化。
2.3 显色机制:一般情况下,苯胺二苯胺磷酸显色剂在原始状态时呈无色溶液。
当与指定物质相互作用后,发生化学反应生成特定的产物时,这些产物能够吸收特定波长范围内的可见光,并将其转换为显著的颜色。
有机汞试剂在有机合成中的应用

有机汞试剂在有机合成中的应用
有机汞试剂是有机合成中应用最广泛的试剂,其特性使它在药物、特种材料、精细化工等领域的合成取得了显著的进步。
有机汞试剂的催化配体以多种形式存在,可以用于不同的有机反应,其中适用于各种催化活性体系的有机汞试剂也被广泛应用。
它具有触发反应速度快、反应条件温和、反应条件容易控制等优点。
由于有机汞试剂具有可控性和可继续性,使其用于催化有机氨基延迟偶联反应,有它的存在,反应速率大大提高,反应产物能够高收率高纯度产生。
有机汞试剂在有机合成反应中的应用,不仅可以促进反应的速度,同时还可以对反应产物的纯度产生较大的影响。
与其它试剂相比,有机汞试剂的环境安全性更高,代替传统的溶剂的使用,也减少了有机反应中溶剂的使用量。
有机汞试剂在药物合成中的应用较为广泛,它能有效促进药物试剂形成反应体系,提高药物合成反应的可控性,为有机合成反应提供较高的物性稳定性,有效控制环境污染。
总之,有机汞试剂作为一种重要的合成试剂,具有良好的催化剂和环境安全性,因此在有机合成中被广泛应用。
它可以有效提高反应的速率,改善反应的可控性,同时还可以减少污染的源头。
高中生物常用试剂及其作用

高中生物常用试剂及其作用高中生物实验中常用的试剂有很多种,根据实验的不同目的和需要,选择的试剂也有所不同。
以下是一些常见的高中生物实验试剂及其作用的介绍:1. 蒸馏水(Distilled water):用于制备其他试剂的溶液,去除水中的杂质和离子。
2. 水合铜硫酸(Copper sulfate pentahydrate):用于检测蛋白质的存在。
蛋白质与水合铜硫酸反应生成紫色沉淀,称为比色法。
3. Lugol碘试液(Lugol's iodine solution):用于检测淀粉的存在。
淀粉与Lugol碘试液反应生成蓝黑色复合物。
4. 苏丹红(Sudan red):用于检测有机物质中的脂肪。
脂肪与苏丹红结合生成红色颜料。
5. FeCl3 溶液(Ferric chloride solution):用于检测酚类和酮类化合物的存在。
酚类和酮类与FeCl3反应生成蓝色溶液。
6. 硫酸铜(Copper sulfate):用于测定蓝藻中叶绿素含量的溶液。
7. 氯化铁溶液(Ferric chloride solution):用于检测植物叶片中的鞣料和类黄酮。
鞣料和类黄酮与氯化铁反应生成蓝、黑色或紫红色溶液。
8. Coomassie亮蓝R-250(Coomassie brilliant blue R-250):用于染色蛋白质,可定量测定蛋白质的浓度。
9. 活性炭(Activated charcoal):用于吸附有机物质,净化溶液和去除气体中的有害物质。
10. 氢氧化钠溶液(Sodium hydroxide solution):用于调节溶液的pH值,调控酶活性。
11. 盐酸(Hydrochloric acid):用于调节溶液的酸碱度,促进酶的反应。
12. 硫酸(Sulfuric acid):用于消化样品、蛋白质的分解和酶的去活化。
13. 氯化钠溶液(Sodium chloride solution):用于调节细胞培养基的渗透压。
格式试剂的名词解释

格式试剂的名词解释在化学领域中,格式试剂是一种常用的实验室试剂,其主要功能是用于对化合物进行分析和检测。
它们具有特定的组成和特性,可以在实验过程中发挥重要作用。
一、格式试剂的定义和分类格式试剂是指具有一定纯度和特殊用途的化学试剂,用于在实验中确定物质的性质、测定物质的含量或进行化学反应。
根据其用途和特性,格式试剂可以分为不同的类别。
1. 无机格式试剂:无机格式试剂主要由金属盐和无机酸、碱等组成。
例如,硫酸、盐酸、氢氧化钠等常见的无机格式试剂,它们常用于酸碱中和反应、无机盐的合成和浓度测定等实验。
2. 有机格式试剂:有机格式试剂主要由有机化合物组成,例如,乙醇、甲苯、醚类化合物等。
它们常用于有机合成反应、有机物性质的测定、鉴定和分离等实验。
3. 分析格式试剂:分析格式试剂主要用于分析化学实验中,用于检测和分析物质的成分和性质。
例如,石墨烯、硫酸铜、硫酸铁等分析格式试剂,在化学分析中常用于定性分析、定量分析和质量分析等实验。
二、常见格式试剂及其应用1. 酸碱类格式试剂:酸碱类格式试剂是进行酸碱反应和中和反应时常用的试剂。
例如,盐酸、硫酸、氢氧化钠等常用的酸碱类格式试剂,在中学化学实验中常用于气体制备、酸碱溶液的中和及滴定实验等。
2. 氧化还原类格式试剂:氧化还原反应是化学实验中常见的一类反应。
而氧化还原类格式试剂则用于促使这一类反应的进行。
例如,硫酸铜、硫酸亚铁等常用的氧化还原类格式试剂,在实验中常用于酸化还原滴定、氧化反应的观察和分析等。
3. 水质检测类格式试剂:水质检测是环境科学和水文学中的重要内容。
而水质检测类格式试剂常用于对水中各种化学指标的检测和分析。
例如,溴酸盐试剂、氨氮试剂等常用的水质检测类格式试剂,用于对水中物质的浓度和成分进行测定。
4. 有机合成类格式试剂:有机合成是有机化学中的重要领域。
而有机合成类格式试剂用于有机合成反应的进行和有机物质的分离和纯化。
例如,溴化钠、氢氧化钾等常用的有机合成类格式试剂,在实验室中常用于有机合成反应的催化剂和试剂。
有机化合物的官能团鉴定反应与分析实验

有机化合物的官能团鉴定反应与分析实验有机化合物的官能团鉴定反应与分析实验是一种常用的方法,它可以通过一系列不同的化学反应来确认有机化合物中存在的官能团。
本实验将介绍几种典型的官能团鉴定反应,并通过实验数据进行分析。
实验仪器和试剂:1. 仪器:反应瓶、加热装置、试管、集气瓶、显色管等。
2. 试剂:甲醇、甲酸、苯酚、酒精、叔丁醇、醛类试剂、碘水、硝酸银溶液、酸性高锰酸钾溶液等。
实验步骤:1. 醛类试剂的鉴定反应:取少量待测有机化合物溶于水,加入几滴甲醛试剂,观察是否出现银镜反应,若出现则有醛基。
2. 羧酸的鉴定反应:将少量待测有机化合物溶于水,加入几滴甲酸试剂,发生酢酸酐脱羧反应即为有羧基。
3. 酚类的鉴定反应:将待测有机化合物溶于水,加入几滴苯酚试剂,观察是否出现紫色溴仿层析反应,若出现则含有酚基。
4. 醇类的鉴定反应:取几滴待测有机化合物溶液,加入酒精试剂,加热,观察是否能够生成醚类物质,若能则含有醇基。
5. 卤代烷的鉴定反应:将待测有机化合物与碘水反应,观察是否出现红棕色沉淀,若出现则含有卤原子。
6. 酰氯的鉴定反应:将待测有机化合物溶于乙醇中,加入氯化亚铁试剂,观察是否出现紫色斑点,若出现则含有酰氯基。
实验数据分析:在完成上述官能团鉴定反应的实验过程中,我们记录了反应发生与否及观察结果,根据这些数据可以对有机化合物中存在的官能团进行分析。
例如,在实验步骤1中,若观察到反应溶液出现银镜反应,则可判断待测有机化合物中含有醛基;在实验步骤2中,若反应产生了酢酸酐,则代表有机化合物中有羧基;类似地,根据其他实验步骤的结果,我们可以判断是否有酚基、醇基、卤原子、酰氯基等官能团存在于有机化合物中。
官能团的存在可以为我们提供有机化合物的结构信息,进一步确定化合物的性质和用途。
因此,官能团鉴定反应与分析实验在有机化学领域中具有重要的应用价值。
结论:通过本实验的官能团鉴定反应与分析实验可以确定有机化合物中存在的官能团种类,进一步分析化合物的结构。
有机分析在医药学分析的应用

有机分析在医药学分析的应用有机分析是一种分析化学领域的重要分支,其涉及到许多医药学领域。
有机分析技术在医药学分析的应用主要是指药物成分的分析、活性成分的检测、药物质量控制等方面。
本文将阐述有机分析在医药学分析的应用。
一、药物成分的分析药物成分的分析是医药学领域中十分重要的一部分,以此来判断药物的主治功效及其副作用。
目前,针对药物成分的分析主要包括定量分析和定性分析两种。
在定量分析中,实验员通常使用比色法、重量法、电化学法等技术来确定药物分子的数量。
而在定性分析中,有机分析技术可以通过分子结构的比较、红外光谱分析、核磁共振谱分析等手段来确定药物化学成分的组成。
二、活性成分的检测检测活性成分主要是为了确定药物的有效成分及其浓度,其中,有机分析起到了重要的作用。
有机分析根据活性成分的结构和化学反应,可以选择不同的化学试剂。
例如,在食品和药品中检测含量高的维生素C,可以使用萤光光谱分析检测,通过添加某些化学试剂,药物中的维生素C分子会发出特定的荧光信号。
而在测定药物中抗氧化成分时,可以通过化学反应生成可测量的产物进行检测。
三、药物质量控制药品的质量控制涉及到药物的含量、纯度和稳定性等多个方面。
有机分析在药物质量控制方面也发挥了重要作用。
例如,在固态药物的生产过程中,有机分析可以通过X射线衍射分析和热分析等手段,对药物的晶体结构和热稳定性进行检测,并对药物的生产过程进行改进,确保药品质量的稳定性。
总之,有机分析在药物学分析中的应用非常广泛,从药物成分的分析、活性成分的检测到药物质量的控制,都发挥着重要的作用。
未来,有机分析技术将持续不断地进步和变革,为医药学分析领域的研究和发展做出更大贡献。
有机合成中的化学选择性例题和知识点总结

有机合成中的化学选择性例题和知识点总结在有机化学的广袤领域中,有机合成无疑是一座璀璨的宝库,而其中的化学选择性更是关键的核心概念之一。
化学选择性关乎着反应的精准性和有效性,决定了我们能否在复杂的分子体系中实现预期的转化。
接下来,让我们通过具体的例题来深入理解化学选择性,并对相关的知识点进行系统总结。
一、化学选择性的基本概念化学选择性是指在一个有机反应中,试剂或反应条件能够有选择地与分子中的某一官能团或部位发生反应,而对其他官能团或部位不产生影响。
简单来说,就是能够精准地“瞄准”我们想要反应的部位,避免“误伤”其他部分。
例如,在一个同时含有羟基和羧基的分子中,如果我们只想让羟基发生反应,而羧基保持不变,这就需要特定的试剂和条件来实现这种选择性。
二、化学选择性的类型1、区域选择性区域选择性是指试剂优先选择分子内的某一区域进行反应。
比如在苯环上有多个取代位置时,反应可能倾向于在特定的位置发生。
例题:当苯环上同时存在邻位、间位和对位取代基时,使用某种亲电试剂进行取代反应,结果主要发生在对位。
这是因为该亲电试剂对苯环的电子云密度分布有特定的要求,导致反应具有明显的区域选择性。
2、官能团选择性官能团选择性是指试剂对不同官能团的反应活性差异。
某些试剂可能更倾向于与某一类官能团反应,而对其他官能团反应活性较低或不反应。
例如,在一个同时含有醛基和酮基的分子中,使用特定的还原剂,可能只还原醛基,而酮基不受影响。
3、立体选择性立体选择性包括对映选择性和非对映选择性。
对映选择性是指反应生成特定手性构型的产物;非对映选择性则是在存在多个非对映异构体的情况下,优先生成其中一种或几种。
例如,在一个含有双键的分子中进行加氢反应,如果使用手性催化剂,可以选择性地得到某一种对映异构体。
三、影响化学选择性的因素1、反应物的结构分子中官能团的电子效应、空间位阻等都会影响反应的选择性。
例如,当一个官能团周围存在较大的取代基时,可能会阻碍试剂的接近,从而影响反应的发生。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
绪论Байду номын сангаас
1.通过第一章的学习,你认为有机试剂在分析中有什么样的地位?分析化学未来的发展方 向是什么? 答:①地位:分析试剂在分析化学中占有与分析仪器同等重要的位置。被测定物质和一个适 宜试剂的化学反应仍然是许多分离、检出和测定方法的基础,包括仪器分析,有机试剂在其 中起到不可替代的作用。 ②发展方向: 分析试剂仍然在不断发展, 不断推动分析化学朝着 “更灵敏、 更准确、 更快速” 的方向发展。 以有机试剂为主要内容的分析化学新反应与仪器分析新方法的进一步结合将成 为分析化学中最重要的研究方向,继续合成、开发研究、应用新的有机试剂仍然是分析化学 今后的主要任务之一。 2.有机试剂是如何分类的,如果提到“吸附显色反应类试剂”属于那种分类方式? 答:有机试剂可以按照以下三种方式分类
3
间的相互影响和π电子云的离域,引起分子内能降低、体系趋向稳定、键长趋于平均化,以 及某些性质的变化等效应。 ③取代基吸电子或推电子能力会改变成键原子上电子云密度, 影 响分析功能基的络合能力,吸电子基减弱试剂络合能力而推电子基加强试剂的络合能力。
第四章
分光光度分析中的有机试剂
1.简述有机化合物的生色团类型及其生色机理。 答:①类型:生色团有π→π*跃迁生色团(乙烯及其共轭烯衍生物色团,环多烯生色团)和 n→π*跃迁生色团。 ②π→π*跃迁生色团生色机理:含有多个相间π键的孤立生色团会生成离域π共轭体系, 电子流动性显著增加,各能级间的能量差较小,电子容易激发,随着共扼体系的变长, π →π*跃迁的能级差将逐渐变小,激发能⊿ E 逐渐降低,导致分子的最大吸收波长红移,生 色作用加强,颜色加深,吸光强度也有所增加。 ③n→π*跃迁生色团生色机理:n →π*跃迁发生在含有杂原子的不饱和化合物中,其最 大摩尔吸光系数εmax (表示物质对光吸收能力大小的参量)比较小,吸收峰随溶剂极性增加 而向短波方向移动,即产生蓝移。 2.什么是 → 共轭效应 ? 答:含有多个相间π键的孤立生色团会生成离域π共轭体系,电子流动性显著增加,各能级间 的能量差较小,电子容易激发的现象。 3.硼与姜黄为什么二者反应为何有很高的灵敏度? 答:硼与姜黄所形成的螯合物的反应之所以有很高的灵敏度(ε=1.85×l05),其原因就在于螯 合物形成时姜黄分子中的π-π共轭体系变长,且发生了质子化。 4.举例说明极性溶剂对π→π*跃迁和 n→π*跃迁的吸收峰产生何影响? 答:溶剂与试剂间常形成氢键;或者由于溶剂的偶极使试剂分子的极性增大,引起 n→π*或 π→π*吸收的迁移。对π- π*跃迁,激发态的极性比基态的强,因此极性溶剂能使激发态的偶 极矩变大,使激发态的能级降低,致使跃迁的激发能降低,导致试剂分子的吸收谱带红移; 对于 n-π*跃迁,试剂杂原子上的未成键电子对在基态时,易与极性溶剂形成氢键,致使 n-π *跃迁的激发能增加,导致试剂分子的吸收谱带紫移。 5.金属络合物的生色机理有哪些?举例说明。 答:络合物生色与中心离子及配位体的基本结构和性能有关,从生色机理讲,可分为三种类 型:①配位体微扰的金属离子 d-d 及 f-f 电子跃迁吸收光谱,例如 MnO4-呈现出紫红色,原 因是由于 O2-离子电荷向高氧化态 Mn7+离子迁移而产生了颜色。 氧化价态越高, 其色彩越深; ②电荷转移吸收光谱,包括 L→M 跃迁(电子从配位体移向金属离子,例如 Fe(III)与 8-羟基 喹啉、钛铁试剂及磺基水杨酸等形成的配合物)和 M→L 跃迁(d 电子从金属离子移向配位 体例如 Fe(II)与 8-羟基喹啉、 2, 2′-联吡啶、 2-吡啶羧酸、 1, 10-二氮菲等所形成的配合物) ; ③中心离子微扰络合物的配位体的吸收光谱, 具体分为络合物颜色接近显色剂在碱性条件下 离解的颜色(铬天青 S、铬天青 R 以及荧光酮类显色剂与金属离子形成的络合物) 、络合物 颜色接近显色剂质子化的颜色 (变色酸双偶氮化合物与金属离子形成化合物) 和络合物的颜 色深于显色剂离子化的颜色(单偶氮染料与金属离子形成的络合物)三种情况。对于某一金 属离子络合物生色来说,有时可能三种生色机理同时存在。 6.氨基离子化以后,为什么会使试剂的最大吸收波长紫移? 答:在试剂分子中若包含有推电子取代基性质的氨基(-NH2)时,其离子化常在酸性介质中进 行,-NH2 十 H+→NH3+,发生的不是阴离子化,而是阳离子化.其结果不是推电子的趋势加 强,而是氮原子上未共用的 p 电子消失,致使氨基的给电子能力消失.所以,氨基化合物的
第三章
影响有机试剂-金属络合物的形成及稳定性因素
1.什么是平行类比反应,其原则是什么? 答: 某含有不同配位原子的有机螯合试剂的反应性能与某些无机反应平行类似, 比如一些金 属离子亲 O,S,N 无机配体, 这些金属离子同样亲和具有 O,S,N 给与原子的有机试剂叫平行类 比反应。其原则是:金属离子与有机试剂反应,试剂分子含有-OH 者,类似于金属离子的 水解反应;若有-SH 或=S 者,类似于生成硫化物的反应;含有氮的基团者, 类似于形成氨 络合物的反应;含有-AsO3 H2 或-PO3 H 2 者,类似于生成无机砷酸盐或磷酸盐的反应等。 2.举例说明影响有机试剂-金属络合物形成及稳定的因素有哪些? 答: 有机试剂的络合反应性能及络合物稳定性与分子的整体结构及构成整个分子的各部分如 分子的母体、功能基、取代基以及立体结构有关,它们同时对有机试剂及其络合物的吸收光 谱及强度、选择性、溶解度等都有各自的贡献。同时一些外因如温度、介质、酸度及离子强 度和螯合效应等也会有一定影响。 例如含邻二羟基分析功能基的钛铁试剂与金属离子的反应 和邻苯二酚基本相同,但金属-钛铁试剂螯合物更稳定,只有 Cu、Fe、Ti、Os 等元素的高价 离子和一部分稀土元素能与钛铁试剂形成能溶于水的有色螯合物。同时有些金属离子( 如 Fe3+ )与钛铁试剂螯合物的组成与溶液的 pH 值有关。 3.试述取代基的诱导效应和共轭效应。 答:①诱导效应定义为在有机分子中,因某一原子或基团的极性,通过静电诱导作用,而引 起电子沿着原子链向某一方向移动的效应; ②共轭效应定义为在共轭体系分子中, 由于原子
1
②配合物的磁性: 配合物磁性大小与配离子中单电子数目有关。 可通过比较配离子的成对能 P 和分裂能△值相对大小,判断 d 电子在分裂后的 d 轨道中的排列状况,从而推知未成对电 子数目。 ③配合物的稳定性:配合物的稳定性由晶体场稳定化能(CFSE)【d 电子从未分裂的 d 轨道进 入分裂后的 d 轨道所产生的总能量下降值】的大小判定。 2.阐述红外光谱和拉曼光谱的区别和联系。 答: ①拉曼光谱与红外光谱都是源于分子的振动和转动, 但产生两种光谱的机理有本质的差 别, 红外光谱是分子对红外光源的吸收所产生的光谱, 吸收光谱中光子的能量必须等于分子 的某两个能级之间的能量差。 拉曼光谱是分子对可见单色光的散射所产生的光谱。 拉曼光谱 中入射光子的频率和分子跃迁所涉及的能量差之间并没有确定的关系, 拉曼光谱是通过测定 散射光相对于入射光频率的变化来获取分子内部结构信息。 红外光谱是来源于分子振动时偶 极矩的变化(分子的正、负电荷中心之间的距离不为零) ,主要适用于研究分子的非对称振 动;拉曼光谱是来源于分子振动时极化率的变化,表征分子的变形性(电荷的正、负两极分 化的程度) 。主要适用于研究分子的对称和非极性基团的振动。 ②红外及拉曼光谱法的相同点在于, 对于一个给定的化学键, 其红外吸收频率与拉曼位移相 等,均代表第一振动能级的能量。因此,对某一给定的化合物,某些峰的红外吸收波数与拉 曼位移完全相同,红外吸收波数与拉曼位移均在红外光区,两者都反映分子的结构信息。同 一振动的拉曼位移和红外吸收光谱的频率是相同的。 3.核磁共振谱中的化学位移指什么? 答:在有机化合物中,各种氢核 周围的电子云密度不同(结构中不同位臵)共振频率有差 异,即引起共振吸收峰的位移,这种现象称为化学位移。 4.拉曼散射与布里渊散射有什么区别? 答:拉曼散射定义为光通过透明溶液时,有一部分光被散射,其频率与入射光不同,频率位 移与发生散射的分子结构有关,这种散射称为拉曼散射,频率位移称为拉曼位移。拉曼散射 是光与光学波(不是光波,主要因为晶格的这种振动模对光能产生共振吸收而得名)相互作 用的结果,是非弹性散射,分为斯托克斯线和反斯托克斯线两种,散射频率与入射光的频率 之差与样品分子的振动、转动能级有关,可以提供分子结构的信息。布里渊散射定义为光通 过介质时,因其无规则热运动的弹性波引起的光散射现象,也是非弹性散射,是光与声学波 相互作用的结果。 布里渊散射也属于拉曼效应, 即光在介质中受到各种元激发的非弹性散射, 其频率变化表征了元激发的能量。 与拉曼散射不同的是, 在布里渊散射中是研究能量较小的 元激发,如声学声子和磁振子等。 5.你认为,要确定一个有机分子的组成和结构,需要进行采用哪些手段? 答:要确定一个有机分子的组成和结构,需要把该化合物的紫外吸收光谱、红外吸收光谱、 核磁共振波谱、 质谱以及其它化学的和物理化学的方法共同配合起来, 才能得出可靠得结论。 UV 能知道物质中分子轨道跃迁情况, 尤其是共轭体系,反应出分子中生色团及助色团的特性; IR 能知道物质中有什么官能团;NMR 能知道每个氢原子(碳)周围环境有什么不同;MS 能 知道物质可以拆成那些碎片。再结合其他化学及物理化学实验数据就能基本确定其结构。 6.何谓反馈键,它与分子轨道理论中的π键的区别是什么? 答:配体向中心原子给电子,结合在一起后,由于相距很近,中心原子的某些轨道会与配体 的某些轨道(空轨道,反键轨道)有部分重合,上面的电子会与配体成键,这就是反馈键, 即离域π键;π键是由π对称的原子轨道组成的分子轨道。 7.影响有机试剂络合物溶解度的因素有哪些? 答:①氢键的生成;②引入极性大的基团,溶解度增大,引入极性小的基团,溶解度减小; ③试剂含有能电离的基团,溶解度增加;④带电荷的有机试剂和它的络合物,如试剂离子化
“吸附显色反应类试剂”属于第三种分类方式即按反应类型分类。 3.为什么说,形成螯合物的反应在分析上具有比较重要的意义? 答:因为反应形成的螯合物具有下列一些特性:①大多数金属螯合物为难溶性沉淀;②有一 些金属螯合物具有较深的特征颜色, 且易溶于水或有机溶剂; ③形成的螯合物具有较高的稳 定性。故这类反应在分离、测定以及光度分析上有着重要的意义。 4.常见的有机试剂命名方法有哪些?它们各有何优缺点? 答:①系统命名法,优点是由试剂的名称即可知道其组成和结构。 缺点是当试剂复杂时,名字往往很长,使用不便,也没有突出试剂的特性和用途。 ②以试剂的特性和用途命名 ③商业和习惯名称 ④英文名称缩写表示法
