最新第4章红外吸收光谱法
红外吸收光谱法

由 V =0 V = 2 即 △V =2 V =0 V = 3 即 △V =3
3 2 1 V=0
基频吸收 倍频吸收
注:基态中不同的振动 能级用V=0,1,2,… 表示
红外吸收光谱法
5、红外光谱的概念 分子吸收红外光,由分子振动、转动发生能级的跃迁(
基态V=0至第一振动能级V=1,即△V=1)产生的光谱,称 为中红外光谱,简称红外光谱。
官能团区( 4000-1300 cm-1):在该区域内的红外吸收 均是各种基团的特征吸收峰,吸收峰比较稀。
指纹区 ( 1300-400 cm-1):在该区域内的红外吸收大 多是一些单键的伸缩振动和各种弯曲振动(如C-C、C-N、C-O )。振动类型复杂且重叠,受分子结构的影响十分敏感,任何 细致的差别都会引起光谱明显改变,如同人的指纹一样,很少 有两个化合物指纹区的吸收峰完全相同,用于确认有机化合物 是很可靠的。
红外吸收光谱法
2、红外、紫外、可见吸收光谱的区别
光谱区域 波长
分子运动形式
光谱类型
紫外可见 200-780nm 分子外层价电子跃迁 紫外可见吸收光谱
红外 0.78-500um 分子振动、转动
红外吸收光谱
△E电子 > △E振 > △E转
红外光的能量较小,分子吸收红外光不足以引起外层 价电子跃迁。
红外吸收光谱法
就得到该试样的红外吸收光谱图。
d
H
Cl
+q
-q
-q
O d
H
H
+q
+q
HCl、H2O 的偶极矩
红外吸收光谱法
三、红外光谱法的特点 除了单原子分子和同核分子如Ne、He、O2、H2等外,
红外吸收光谱与紫外荧光的区别

μ = q·d
10.2
第22讲
红外光谱基本原理
第8页
由于偶极子具有一定的原有振动频率,
显然,只有当辐射频率与偶极子频率相
匹配时,分子才与辐射发生相互作用
(振动偶合)而增加它的振动能,使振
动加激(振幅加大),即分子由原来的
基态振动跃迁到较高振动能级。可见,
并非所有的振动能级都会产生红外吸收,
只有发生偶极矩变化的振动才能引起可
第22讲
红外光谱基本原理
第1页
第四章 红外吸收光谱法
第22讲
红外光谱基本原理
第2页
§10-1 红外吸收光谱分析概述
一、定义:
利用物质对红外辐射的吸收所产生的红外吸收 光谱,对物质的组成、结构及含量进行分析测定 的方法叫红外吸收光谱分析法。红外吸收光谱又 称为分子振动转动光谱
二、与紫外可见吸收光谱法的比较
紫外 104~105 103~104 102~103
﹤102
第22讲
红外光谱基本原理
第4页
不同点 紫外可见吸收光谱 红外吸收光谱
光源
紫外可见光
红外光
起源
电子能级跃迁
振动能级跃迁
研究 范围
不饱和有机化合物
几乎所有有机化合 物;
共轭双键、芳香族等 许多无机化合物
特色
反映发色团、助色团 反映各个基团的振
的情况
动及转动特性
第22讲
红外光谱基本原理
第5页
• 波数为波长λ的倒数,即1cm中所含波的 个数
费米共振—当倍频或组合频与某基频峰位相近时, 由于相互作用产生强吸收带或发生峰的分裂,这 种倍频峰或组合频峰与基频峰之间的偶合称为费 米共振。
第22讲
第4章红外吸收光谱法

❖折合质量相同时,振动频率取决于化学键的 强度
单键 双键 三键
化学键 C-C C=C CC
键力常数N·cm-1 5 10 15
波数cm-1 1190 1683 2062
08:50:27
❖ 化学键的类型相同时,原子质量m大,化学键的 振动波数低。
化学键 单键 单键
基团 C-C C-H
波数cm-1 1190 2920
08:50:27
(二) 吸收谱带的强度
➢ 分子振动时偶极矩是否变化决定了该分子能
否产生红外吸收,而偶极矩变化的大小又决定了 吸收谱带的强弱。
➢ 根据量子理论,红外光谱的强度与分子振动
时偶极矩变化的平方成正比。
➢ 偶极矩的变化与固有偶极矩有关。一般极性
比较强的分子或基团吸收强度都比较大,极性比 较弱的分子或基团吸收强度都比较弱。
08:50:27
08:50:27
2. 弯曲振动(变角振动或变形振动):键 角发生周期性变化而键长不变。
面内弯曲:剪式振动,摇摆振动 面外弯曲:摇摆振动,扭曲振动 例如:亚甲基
08:50:27
(动画)红外四种振动方式
08:50:27
图4.7 水分子和CO2的简正振动形式
08:50:27
(四)分子的振动自由度
多原子分子振动形式的多少可以用 振动自由度来描述。
振动自由度就是独立的振动数目。 在三维空间中,每个原子都能沿x, y,z三个坐标方向独立运动,对于由n个 原子组成的分子则有3n个独立运动,即 3n个运动自由度。
08:50:27
但是,这些原子被化学键联结在一起,成为一 个整体,分子作为整体的运动状态可以分为三类 :平动、转动和振动。
第四章 红外吸收光谱法 Infrared Absorption Spectrometry,IR
红外吸收光谱分析法

红外吸收光谱分析法
一、红外吸收光谱分析法概述
红外吸收光谱分析法是一种利用物质的红外光吸收能力来探测它们的物质组成的技术。
它特别适用于有机化合物和无机化合物的光谱分析。
通过分析红外吸收光谱,可以检测物质中的有机键、C-H键、C-O键或N-H 键的存在和位置,从而鉴定出物质的化学结构和性质。
红外光吸收法的原理是,物质中的分子、晶体或其他结构会在不同的波长处吸收光,产生光谱,这些吸收光谱是物质的独特特征,反映出物质的特性。
根据这种特性,分析用不同波长的光照射样品,并从所得到的光谱中提取出电子激发、分子振动等信息,从而得到物质的结构和性质。
二、红外吸收光谱分析法基本原理
红外吸收光谱分析法的原理是,当物质受到红外幅射的照射时,它的分子会产生振动和旋转,这些振动和旋转的能量会转化为更高能量的电子跃迁。
这些电子跃迁会引起物质材料吸收一些具有特定波长的红外光,从而产生在不同波长的吸收光谱,通过分析这些吸收光谱,就可以求取物质分子的结构和性质。
红外吸收光谱分析法 红外谱图解析

顺式烯 乙烯基烯 亚乙烯基烯
08:12:21
R1 H R1 H R1 R2
1660cm-1
1660-1630cm-1
中强,尖
总结
ⅰ 分界线1660cm-1 ⅱ 顺强,反弱
ⅲ 四取代(不与O,N等相连)无υ
ⅳ 端烯的强度强
(C=C)峰
ⅴ共轭使υ
下降20-30 cm-1 (C=C)
H C C R R1 C C R2
08:12:21
υ υ
C C
2140-2100cm-1 (弱) 2260-2190 cm-1 (弱)
C C
c)C-H 变形振动(1000-700 cm-1 )
面内变形(=C-H)1400-1420 cm-1 (弱) 面外变形(=C-H) 1000-700 cm-1 (有价值)
R1 H R1 R2 R1 R2 C C R4
O—H,C—O
a)-OH 伸缩振动(>3600 cm-1) b)碳氧伸缩振动(1100 cm-1)
C Cα C Cα′ C C Cα″ β
υ
(C-O)
OH
υ
游 离 仲-OH 醇, 叔-OH 酚 酚-OH 伯-OH
(—OH) 3640cm-1 3630cm-1 3620cm-1 3610cm-1
1050 cm-1 1100 cm-1 1150 cm-1 1200 cm-1
第四章 红外吸收光谱分 析法
infrared absorption spec-troscopy,IR
一、红外谱图解析
analysis of infrared spectrograph
二、未知物结构确定
structure determination of compounds
第四章红外吸收光谱法3、CO的红外吸收光谱在2170cm-1处有一振动
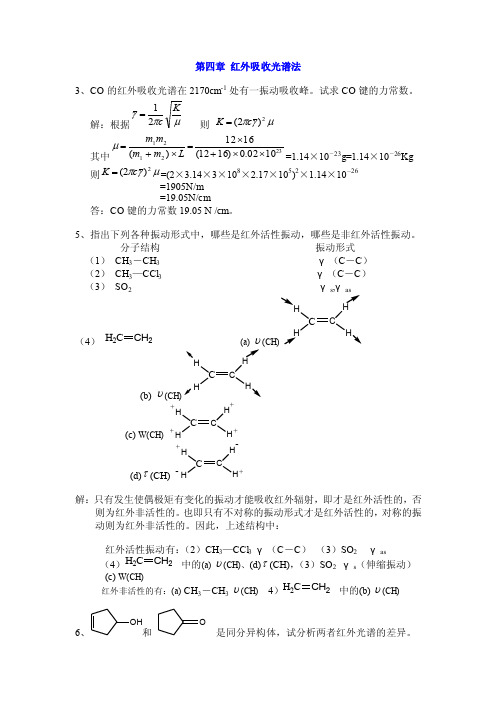
第四章 红外吸收光谱法3、CO 的红外吸收光谱在2170cm -1处有一振动吸收峰。
试求CO 键的力常数。
解:根据μπγKc 21= 则 μγπ2)2(c K = 其中2321211002.0)1612(1612)(⨯⨯+⨯=⨯+=L m m m m μ=1.14×10-23g=1.14×10-26Kg 则μγπ2)2(c K ==(2×3.14×3×108×2.17×105)2×1.14×10-26 =1905N/m=19.05N/cm答:CO 键的力常数19.05 N /cm 。
5、指出下列各种振动形式中,哪些是红外活性振动,哪些是非红外活性振动。
分子结构 振动形式(1) CH 3-CH 3 γ(C -C )(2) CH 3—CCl 3 γ(C -C )(3) SO 2 γs ,γ(4)H 2C CH 2 (a) υ(CH)CC(b) υ(CH)CH C (c) W(CH) C HHC H H ++++(d)τ(CH) C H H C H -++-解:只有发生使偶极矩有变化的振动才能吸收红外辐射,即才是红外活性的,否则为红外非活性的。
也即只有不对称的振动形式才是红外活性的,对称的振动则为红外非活性的。
因此,上述结构中:红外活性振动有:(2)CH 3—CCl 3 γ(C -C ) (3)SO 2 γas(4)H 2C CH 2 中的(a) υ(CH)、(d)τ(CH),(3)SO 2 γs (伸缩振动) (c) W(CH)红外非活性的有:(a) CH 3-CH 3 υ(CH) 4)H 2C CH 2 中的(b) υ(CH)6、OH 和 O是同分异构体,试分析两者红外光谱的差异。
答:由于OH中含有一个-OH 基团,因此在红外光谱中有一强吸收峰在3700~3100cm -1,且此分子中含有一个C=C 双键,因此在1680~1620cm -1也有一较弱的吸收峰。
仪器分析 第四章--红外吸收光谱法
章节重点:
分子振动基本形式及自由度计算;
红外吸收的产生2个条件;
各类基团特征红外振动频率;
影响红外吸收峰位变化的因素。
第八章 红外吸收光谱分 析法
第三节 红外分光光度计
1. 仪器类型与结构
2. 制样方法
3. 联用技术
1. 仪器类型与结构
两种类型:色散型 干涉型(傅立叶变换红外光谱仪)
弯曲振动:
1.4 振动自由度
多原子分子振动形式的多少用振动自由度标示。
三维空间中,每个原子都能沿x、y、z三个坐标方向独 立运动,n个原子组成的分子则有3n个独立运动,再除 掉三个坐标轴方向的分子平移及整体分子转动。
非线性分子振动自由度为3n-6,如H2O有3个自由度。 线性分子振动自由度为3n-5,如CO2有4个自由度。
某些键的伸缩力常数:
键类型: 力常数: 峰位:源自-CC15 2062 cm-1
-C=C10 1683 cm-1
-C-C5 1190 cm-1
-C-H5.1 2920 cm-1
化学键键强越强(即键的力常数K越大),原子折合 质量越小,化学键振动频率越大,吸收峰在高波数区。
1.2 非谐振子
实际上双原子分子并非理想的谐振子!随着振动量子 数的增加,上下振动能级间的间隔逐渐减小!
(1)-O-H,37003100 cm-1,确定醇、酚、酸 在非极性溶剂中,浓度较小(稀溶液)时,峰形尖锐 ,强吸收;当浓度较大时,发生缔合作用,峰形较宽。
注意区分: -NH伸缩振动:3500 3300 cm-1 峰型尖锐
(2)饱和碳原子上的-C-H -CH3 2960 cm-1 2870 cm-1 反对称伸缩振动 对称伸缩振动
四章红外吸收光谱法
Nicolet公司的 AVATAR 360 FT-IR
2. 傅里叶变换红外光谱仪结构框图Байду номын сангаас
(动画)
干涉仪
样品室
检测器
光源
计算机
显示器 绘图仪
干涉图 FTS
光谱图
2019/12/14
3. 傅里叶变换红外光谱仪工作原理图
(动画)
2019/12/14
迈克尔干涉仪工作原理图
(动画)
2019/12/14
第四章 红外吸收
光谱法
第三节 红 外 吸收 光谱仪
一、仪器类型
二、 色散型红外光谱仪
三、傅立叶变换红外光 谱仪
2019/12/14
一、仪器类型
两种类型:色散型 干涉型(傅立叶变换红外光谱仪)
2019/12/14
双光束红外分光光度计原理图(色散型)
2019/12/14
二、 色散型红外光谱仪主要部件
2019/12/14
(3) 检测器
真空热电偶:不同导体 构成回路时的温差电现象 涂黑金箔接受红外辐射;
傅立叶变换红外光谱仪 采用热释电(DTGS)和碲镉汞(MCT)检测器;
DTGS:氘代硫酸三苷肽单晶为热检测元件;极 化效应与温度有关,温度高表面电荷减少(热释电); 响应速度快;高速扫描;
2019/12/14
三、 傅立叶变换红外光谱仪的原理与特点
光源发出的辐射经干涉仪转变为干涉光,通 过试样后,包含的光信息需要经过数学上的傅立 叶变换解析成普通的谱图。 特点:(1) 扫描速度极快(1s);适合仪器联用;
(2)不需要分光,信号强,灵敏度很高; (3)仪器小巧。
2019/12/14
1. 内部结构
红外吸收光谱法(IR)
• 3、红外吸收光谱与分子结构的关系 一、基团的特征峰与相关峰 1、特征峰与相关峰 特征峰——具有能代表某基团存在并有较高强 度的特征频率的吸收峰。可用以鉴定官能团。 相关峰——某基团的一组特征峰构成该基团的 相关峰。 2、红外光谱的分区 常见有机物基团在4000~670cm-1有特征基团频 率。红外光谱划分为6个区域:
有些因素使红外吸收峰增多 (1)倍频和组合频的出现 (2)振动耦合 (3)费米(Fermi)共振 振动耦合——当两个基团位置相邻,且振动频率相近,有一个 公用原子连接,相应的特征峰发生分裂形成两个峰。 费米共振——泛频峰与基频峰的耦合 影响吸收峰强弱的因素:分子在振动能级之间的跃迁概率和振 动过程中的偶极矩的变化。 A、分子由基态振动能级(0=0)向第一激发态(1=0)跃迁的 概率较大,因此基频峰较强,倍频峰较弱或很弱。 B、极性基团(O-H、C=O、N-H 等)振动时,偶极矩变化 较大,有较强的吸收峰; 非极性基团(C-C、C=C等)的吸收峰较弱;分子越对称, 吸收峰越弱。
偶极矩() =分子所带电量(q)正负电荷中心距离(d) 非极性双原子分子(N2、O2、H2): 分子完全对称(d=0),无红外吸收。 极性分子( 0): 由于分子中的振动使d的瞬时值不断变化,从而不 断变化,有一个固定的变化频率。当照射的红外光 的频率与分子的偶极矩的变化频率相匹配时,分子 的振动(红外活性振动)与红外光发生振动偶合而 增加振动能,振幅加大,即分子由振动基态跃迁到 激发态。——吸收红外光
• (2).傅里叶变换红外吸收光谱仪(FTIR)简介 原理:检测器得到一个干涉强度对光程差和红外光频率的函 数图,经过电子计算机进行复杂的傅立叶变换,得到普通的 吸光度或透光率随波数变化的红外光谱图。
(2)傅里叶变换红外光谱仪 (FTIR)
仪器分析 第4章 红外吸收光谱法
4.2 基本原理
4.2.3 多原子分子的振动类型(P56)
伸缩振动 (υ):键长发生变化 1.简正振动基本形式 变形振动 (δ):键角发生变化
伸缩振动(υ)
对称伸缩振动(υs)
不对称伸缩振动(υas)
变形振动(δ)
面内变形振动(β)
面外变形振动(γ)
亚甲基的各种振动形式
2. 基本振动的理论数(分子振动自由度)
4.4 试样的处理和制备
4.4 试样的处理和制备
4.4.1 红外光谱法对试样的要求 (1)单一组分纯物质,纯度 > 98%; (2)样品中不含游离水; (3)要选择合适的浓度和测试厚度, 使大多数吸收峰透射比处于10%~80%。
4.4 试样的处理和制备
4.4.2 制样方法 1.气体样品的制备 2.液体和溶液样品的制备 3.固体样品的制备
分子振动自由度:多原子分子的基本振动
数目,也就是基频吸收峰的数目。
基频吸收峰:分子吸收一定频率的红外光后,
其振动能级由基态跃迁到第一
激发态时所产生的吸收峰。
2. 基本振动的理论数
线型分子振动自由度 = 3N – 5(如CO2)
非线型分子振动自由度 = 3N – 6(如H2O)
图5.12 CO2分子的简正振 动形式
来指导谱图解析。
基本概念
基团频率区: 在4000~1300cm-1 范围内的吸收峰,有一 共同特点:既每一吸收峰都和一定的官能 团相对应,因此称为基团频率区。
在基团频率区,原则上每个吸收峰都可以找到归属。
基本概念
指纹区: 在1300~400cm-1范围内,虽然有些吸收也对应 着某些官能团,但大量吸收峰仅显示了化合物 的红外特征,犹如人的指纹,故称为指纹区。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
15:17:48
二、红外光区的划分
表4.1 红外光谱区划分
区 域 /m 0.78~2.5 /cm-1 12820~4000 4000~200 能级跃迁类型
近红外(泛频区)
O-H、N-H和C-H键的 倍频吸收区
分子的振动、转动 分子的转动,骨架振 动
中红外(基本振动区) 2.5~50
远红外(转动区)
15:17:48
IR光谱用T-λ 曲线或T-曲线表示。纵坐标为
百分透射比T%,吸收峰向下,向上则为谷。横坐
标为波长λ (单位μ m)或波数 (单位cm-1)。
两者的关系是:/cm-1= 104/(λ /μ m) = 1/(λ /cm)
1。
中红外区的范围为4000-400cm-
用波数描述吸收谱带比较简单,且便于与Raman 光谱比较。
15:17:48
1 (频率) 2
1 k .......... ....... 或 (波数) 2c
k
以上两式称为分子简谐振动方程式。不仅
可以用于双原子分子振动的频率或波数,而且
也适用于复杂分子中一些化学键的振动频率或
波数的计算。
15:17:48
k为化学键的力常数(单位:N· cm-1 ),为双 原子折合质量(单位为g)
m1m2 m1 m2
若原子的质量用原子质量单位(u,1u=1.66×10-24g) 表示,则成键两原子的折合质量应为:
m1m2 (m1 m2 ) 6.021023
15:17:48
从分子简谐振动方程可知,分子振动频率与化 学键的键力常数、原子质量有关系.
折合质量相同时,振动频率取决于化学键的 强度
15:17:48
三、红外光谱的表示方法
当一束具有连续波长的红外光通过物质 时,其中某些波长的光就要被物质吸收。 物质分子中某个基团的振动频率和红外 光的频率一致时,二者发生共振,分子吸 收能量,由原来的基态振动能级跃迁到能 量较高的振动能级,将分子吸收红外光 的情况用仪器记录下来,就得到红外光谱 图。
15:17:48
aa'是谐振子位能曲线, bb'是真实双原子分子振动位能曲线
第四章 红外吸收光谱法 Infrared Absorption Spectrometry,IR
15:17:48
第一节
一、 定义
概
述
依据物质对红外辐射的特征吸收建立 起来的一种光谱分析方法。分子吸收 红外辐射后发生振动能级和转动能级 的跃迁,因而红外光谱又称分子振动转动光谱。
15:17:48
红外光谱属分子吸收光谱。样品受到频率 连续变化的红外光照射时,分子吸收其中一 些频率的辐射,分子振动或转动引起偶极 矩的净变化,使振-转能级从基态跃迁到激 发态,相应于这些区域的透射光强度减弱, 记录百分透过率T%对波数或波长的曲线, 即得红外光谱。
15:17:48
四、紫外吸收光谱与红外吸收光谱的区别
1. 光谱产生的机制不同
紫外:电子光谱;
红外:振-转光谱
2. 研究对象和使用范围不同
紫外:研究不饱和化合物,具有共轭体系; 红外:凡是在振动中伴随有偶极矩变化的化合 物都是红外光谱研究的对象。可研究几乎所有的有 机物。
15:17:48
五、红外光谱法的特点和应用
1 Ev (v )h (v = 0, 1, 2, · · · ) 2
式中, v 为振动量子数,ν为分子 振动频率。
15:17:48
在室温时,分子处于基态(v = 0),此时伸
缩振动振幅很小。当有红外辐射照射分子时,若
辐射光子所具有的能量恰好等于分子振动能级差
时,则分子吸收光子能量跃迁至振动激发态,导 致振幅增大。 分子的两个原子以其平衡点为中心,以很小 的振幅(与核间距相比)作周期性“简谐”振动, 其振动可用经典刚性振动描述。分子简谐振动频 率的计算公式为:
15:17:48
红外光谱的表示方法
红外光谱图:纵坐标为透光率(或吸光度),横坐标为波长
λ( m )和波数1/λ
,单位:cm-1。
10 4 / cm / m
1
15:17:48
图4.1 苯酚的IR吸收光谱
15:17:48
图4.2乌桕油的IR光谱
15:17:48
图4.3 聚苯乙烯红外光谱图
特点:与紫外-可见吸收光谱比较 (1) 除了单原子分子和同核双原子分子等少数 分子外,几乎所有化合物均可用红外吸收光谱法 进行研究。适用范围广。
(2)红外光谱可对物质的组成和结构特征提供
十分丰富的信息。其最重要和最广泛的用途是对
有机化合物进行结构分析。
15:17:48
(3)红外吸收可用于定量分析。但是由于 红外辐射能量较小,分析时需要较宽的光 谱通带,而物质的红外吸收峰又比较多, 难以找出不受干扰的检测峰,因此,定量 分析应用较少。 (4)红外吸收光谱是一种非破坏性分析 方法,对于试样的适应性较强。样品可以 是液体、固体、气体。
15:17:48
应 用:结构分析,定性,定量 具有快速,样品需要量少,气态、液 态、固态样品都可测等特点。与色谱等 联用(GC-FTIR)具有强大的定性功能 局限性:灵敏度低,样品必须纯制。15:17:48 第二节红外吸收基本原理
一 分子的振动 (一) 双原子分子振动
谐振子模型 双原子分子化学键的振动类 似于连接两个小球的弹簧 分子的振动总能量:
最常用的
50~1000
2.5~15
200~10
4000~650
15:17:48
3. 红外光谱特点 1)红外吸收只有振-转跃迁,能量低;
2)应用范围广:除单原子分子及单核分子外,几乎所有有
机物均有红外吸收; 3)分子结构更为精细的表征:通过IR谱的波数位置、波峰 数目及强度确定分子基团、分子结构; 4)定量分析; 5)固、液、气态样均可用,且用量少、不破坏样品; 6)分析速度快。 7)与色谱等联用(GC-FTIR)具有强大的定性功能。
化学键 单键 双键 C-C C=C 键力常数N· cm-1 5 10 波数cm-1 1190 1683
三键
CC
15
2062
15:17:48
化学键的类型相同时,原子质量m大,化学键的 振动波数低。
化学键 单键 单键 基团 C-C C-H 波数cm-1 1190 2920
(二) 非谐振子 实际上双原子分子并非理想的谐振子
