酸碱的电离常数(解离常数)
常见酸碱的电离常数(解离常数)
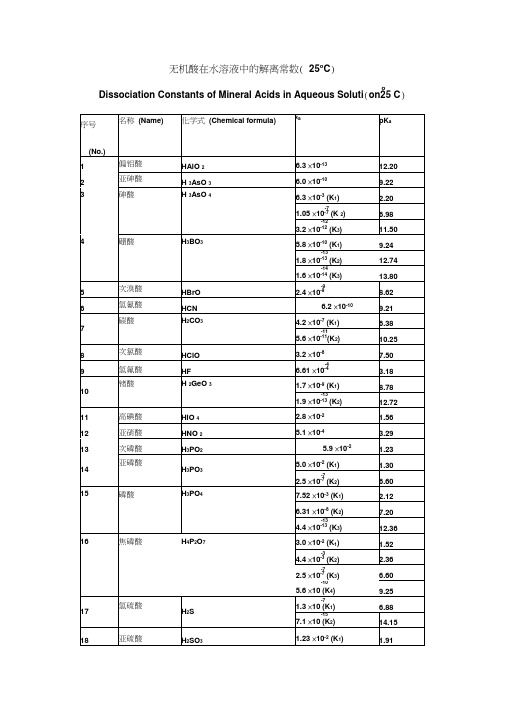
pKb
1
氢氧化铝
Al(OH)3
-9
1.38×10-9(K3)
8.86
2
氢氧化银
AgOH
-4
1.10×10-4
3.96
3
氢氧化钙
Ca(OH)2
-3
3.72×10-3
2.43
-2
3.98×10-2
1.40
4
氨水
NH3+H2O
-5
1.78×10-5
4.75
5
肼(联氨)
N2H4+H2O
-7
9.55×10-7(K1)
18
己胺
H(CH2)6NH2
-4
4.37×10-4
3.36
19
辛胺
H(CH2)8NH2
-4
4.47×10-4
3.35
20
苯胺
C6H5NH2
-10
3.98×10
9.40
21
苄胺
C7H9N
-5
2.24×10
4.65
22
环己胺
C6H11NH2
-4
4.37×10-4
3.36
23
吡啶
C5H5N
-9
1.48×10-9
5
乙二胺
H2N(CH2)2NH2
-5
8.51×10-5(K1)
4.07
-8
7.08×10-8(K2)
7.15
6
二甲胺
(CH3)2NH
-4
5.89×10-4
3.23
7
三甲胺
(CH3)3N
-5
6.31×10-5
4.20
解离平衡常数

解离平衡常数解离平衡常数(dissociation constant)是指一种物质在溶液中的解离程度,它表示溶液中物质的离解状态所占的比例。
解离平衡常数可以用来衡量一种物质在溶液中的溶解度,也可以用来衡量一种化合物的稳定性。
常见的解离平衡常数包括酸碱平衡常数(pH值)、离子解离常数(离子解离度)和离子解离平衡常数(离子解离程度)等。
解离平衡常数的大小可以通过实验测定,也可以用理论方法计算。
解离平衡常数在化学、生物学、药学等领域都有广泛的应用。
酸碱平衡常数(pH值)是衡量溶液中酸性或碱性程度的常数,它的大小可以反映溶液中的氢离子浓度。
pH值是以负数为单位表示的,常用pH计测定。
当pH值在7左右时溶液是中性的,pH值小于7时溶液是酸性的,pH值大于7时溶液是碱性的。
pH值对于生命的重要性是不言而喻的,它会影响生物体内的代谢过程,并且对人体的健康也有很大的影响。
离子解离常数(离子解离度)是衡量溶液中某种离子的解离程度的常数。
离子解离度的大小可以反映溶液中离子的溶解度,也可以反映溶液的电离度。
离子解离度是以正数为单位表示的,它的大小可以通过实验测定,也可以用理论方法计算。
离子解离度在化学、生物学、药学等领域都有广泛的应用。
离子解离平衡常数(离子解离程度)是衡量溶液中某种化合物的离解程度的常数。
离子解离程度的大小可以反映溶液中化合物的稳定性,也可以反映溶液的pH值。
离子解离程度是以正数为单位表示的,它的大小可以通过实验测定,也可以用理论方法计算。
离子解离程度在化学、生物学、药学等领域都有广泛的应用。
总之,解离平衡常数是衡量溶液中物质的解离程度的常数,它可以用来衡量物质的溶解度、电离度和稳定性。
解离平衡常数在化学、生物学、药学等领域都有广泛的应用。
常见酸碱的电离常数
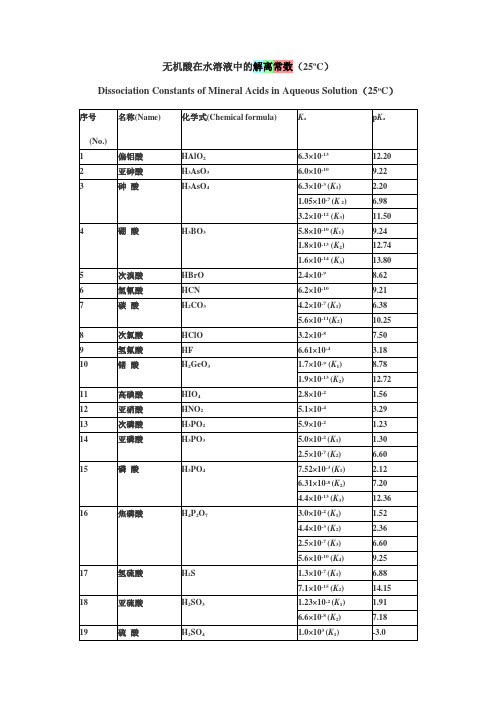
Dissociation Constants of Mineral Acids in Aqueous Solution(25oC)
序号
(No.)
名称(Name)
化学式(Chemical formula)
Ka
pKa
1
偏铝酸
HAlO2
6.3×10-13
12.20
2
亚砷酸
序号(No.)
名称(Name)
化学式(Chemical formula)
Kb
pKb
1
甲胺
CH3NH2
4.17×10-4
3.38
2
尿素(脲)
CO(NH2)2
1.5×10-14
13.82
3
乙胺
CH3CH2NH2
4.27×10-4
3.37
4
乙醇胺
H2N(CH2)2OH
3.16×10-5
4.50
5
乙二胺
H2N(CH2)2NH2
3.35
20
苯胺
C6H5NH2
3.98×10-10
9.40
21
苄胺
C7H9N
2.24×10-5
4.65
22
环己胺
C6H11NH2
4.37×10-4
3.36
23
吡啶
C5H5N
1.48×10-9
8.83
24
六亚甲基四胺
(CH2)6N4
1.35×10-9
8.87
25
2-氯酚
C6H5ClO
3.55×10-6
4.76
4.0×10-7(K3)
6.40
酸碱的电离常数(解离常数)

14
甘油酸
HOCH2CHOHCOOH
×10-4
15
丙酮酸
CH3COCOOH
×10-3
16
-丙胺酸
CH3CHNH2COOH
×10-10
17
-丙胺酸
CH2NH2CH2COOH
×10-11
18
正丁酸
CH3(CH2)2COOH
×10-5
19
异丁酸
(CH3)2CHCOOH
×10-5
20
3-丁烯酸
CH2═CHCH2COOH
8-HO—C9H6N
×10-5
35
二苯胺
(C6H5)2NH
×10-14
36
联苯胺
H2NC6H4C6H4NH2
×10-10(K1)
×10-11(K2)
有机酸在水溶液中的解离常数(25oC)
Dissociation Constants of Organic Acids in Aqueous Solution(25oC)
×10-4(K1)
×10-7(K2)
31
谷氨酸
HOCOCH2CH2CH(NH2)COOH
×10-3(K1)
×10-5(K2)
×10-10(K3)
32
正己酸
CH3(CH2)4COOH
×10-5
33
异己酸
(CH3)2CH(CH2)3—COOH
×10-5
34
(E)-2-己烯酸
H(CH2)3CH═CHCOOH
×10-5
21
异丁烯酸
CH2═C(CH2)COOH
×10-5
22
反丁烯二酸(富马酸)
HOCOCH═CHCOOH
碱解离常数kb公式

碱解离常数kb公式
碱的解离常数通常用Kb表示,计算公式为Kb = [BH+][OH-]/[B]。
其中,[BH+]、[OH-]和[B]分别表示碱的氢离子浓度、氢氧根离子浓度和碱的浓度。
Kb越大,pKb越小,碱性越强。
对于一对共轭酸碱对而言,通过公式推导可知pKa+pKb=pKw=14(25℃)。
例如当NH3做碱时pKb为4.75,生成共轭酸NH4+,NH4+的pKa为9.25,两者之和为14。
但人们有时依然习惯用pKa表示碱性的强弱,此处的pKa并不代表碱的pKa,而是指其共轭酸的pKa,共轭酸的pKa越大,则碱的pKb 越小,碱的碱性越强。
当然对于有些分子即可做酸,也可做碱,例如苯胺做酸时会电离产生H+,其pKa=28,此时的pKa指其作为酸的pKa。
当苯胺做碱时,其pKa=4.6,此时的Pka实际指的是其共轭酸的pKa。
以上信息仅供参考,如需了解关于化学公式的更多信息,建议查阅化学书籍或咨询化学专家。
醋酸的解离度和解离常数

醋酸的解离度和解离常数
醋酸是一元弱酸,在水溶液中存在以下电离平衡:HAC==H++AC-,在一定的温度下,这个过程很快达到了平衡,平衡常数的表达式为:K=[H+][AC-]/[HAC],此时,电离度α%=[H+]/c,式中[H+]、[AC-]、[HAC]分别为H+、AC-、HAC的平衡浓度。
设醋酸的初始浓度为C,如果忽略水电离所提供的[H+]量,则达到平衡时:
[H+ ]=[AC-] [HAC]=C-[H+]
K=[H+]2 /(C-[H+])
当α<5%时,K=[H+]2/C
因此,配制一系列已知浓度的醋酸溶液,测定其PH值,可求得一系列Ki值,其平均值为该温度下的Ki值。
意义
解离常数(pKa)是有机化合物非常重要的性质,决定化合物在介质中的存在形态,进而决定其溶解度、亲脂性、生物富集性以及毒性。
对于药物分子,pKa还会影响其药代动力学和生物化学性质。
精确预测有机化合物的pKa值在环境化学、生物化学、药物化学以及药物开发等领域都有重要意义。
采用电位滴定法测定物质解离常数时要注意数据处理的技巧,因为选择适当的数据处理方法能给实验数据的处理带来很大的方便,节省大量时间,同时能够提高数据的准确度。
电离度的概念以及公式

电离度的概念以及公式
电离度的概念是指一定温度下,弱电解质在溶液里达到电离平衡时,溶液中已电离的弱电解质分子数占弱电解质分子总数(包括已电离的和未电离的)的百分数。
电离度是表示弱电解质在水中电离程度的物理量,通常用电离度和电离常数来表示。
对于一元弱酸或一元弱碱,其电离度可以用以下公式计算:
对于一元弱酸:电离度α= [H+] / Ka
其中[H+]为溶液中的氢离子浓度,Ka为该物质的酸解离常数。
对于一元弱碱:电离度α= [OH-] / Kb
其中[OH-]为溶液中的氢氧根离子浓度,Kb为该物质的碱解离常数。
需要注意的是,对于多种离子同时存在的体系,如混合酸、混合盐等,电离度的计算较为复杂,需要考虑各种离子之间的相互作用。
常见酸碱的电离常数

6.0×10-10
9.22
3
砷酸
H3AsO4
6.3×10-3(K1)
2.20
1.05×10-7(K2)
6.98
3.2×10-12(K3)
11.50
4
硼酸
H3BO3
5.8×10-10(K1)
9.24
1.8×10-13(K2)
12.74
1.6×10-14(K3)
13.80
5
次溴酸
HBrO
2.4×10-9
4.19
35
二苯胺
(C6H5)2NH
7.94×10-14
13.1
36
联苯胺
H2NC6H4C6H4NH2
5.01×10-10(K1)
9.30
4.27×10-11(K2)
10.37
有机酸在水溶液中的解离常数(25oC)
Dissociation Constants of Organic Acids in Aqueous Solution(25oC)
2.0×10-5
4.70
28
3-戊烯酸
CH3CH═CHCH2COOH
3.0×10-5
4.52
29
4-戊烯酸
CH2═CHCH2CH2COOH
2.10×10-5
4.677
30
戊二酸
HOCO(CH2)3COOH
1.7×10-4(K1)
3.77
8.3×10-7(K2)
6.08
31
谷氨酸
HOCOCH2CH2CH(NH2)COOH
4.74
35
(E)-3-己烯酸
CH3CH2CH═CHCH2COOH
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
9.96
42
2,4,6-三硝基苯酚
2,4,6-(NO2)3C6H2OH
5.1×10-1
0.29
43
葡萄糖酸
CH2OH(CHOH)4COOH
1.4×10-4
3.86
44
苯甲酸
C6H5COOH
6.3×10-5
4.20
45
水杨酸
C6H4(OH)COOH
1.05×10-3(K1)
2.98
4.17×10-13(K2)
常见酸碱的电离常数
大学化学参考数据
无机酸在水溶液中的解离常数(25oC)
序号
(No.)
名称
化学式
Ka
pKa
1
偏铝酸
HAlO2
6.3×10-13
12.20
2
亚砷酸
H3AsO3
6.0×10-10
9.22
3
砷酸
H3AsO4
6.3×10-3(K1)
2.20
1.05×10-7(K2)
6.98
3.2×10-12(K3)
1.92
24
硅酸
H2SiO3
1.7×10-10(K1)
9.77
1.6×10-12(K2)
11.80
25
亚碲酸
H2TeO3
2.7×10-3(K1)
2.57
1.8×10-8(K2)
7.74
无机碱在水溶液中的解离常数(25oC)
序号
名称
化学式
Kb
pKb
1
氢氧化铝
Al(OH)3
1.38×10-9(K3)
8.86
15
丙酮酸
CH3COCOOH
3.2×10-3
2.49
16
-丙胺酸
CH3CHNH2COOH
1.35×10-10
9.87
17
-丙胺酸
CH2NH2CH2COOH
4.4×10-11
10.36
18
正丁酸
CH3(CH2)2COOH
1.52×10-5
4.82
19
异丁酸
(CH3)2CHCOOH
1.41×10-5
4.85
5.5×10-5
4.26
11
乳酸(丙醇酸)
CH3CHOHCOOH
1.4×10-4
3.86
12
丙二酸
HOCOCH2COOH
1.4×10-3(K1)
2.85
2.2×10-6(K2)
5.66
13
2-丙炔酸
HC≡CCOOH
1.29×10-2
1.89
14
甘油酸
HOCH2CHOHCOOH
2.29×10-4
3.64
3.36
11
1,3-丙二胺
NH2(CH2)3NH2
2.95×10-4(K1)
3.53
3.09×10-6(K2)
5.51
12
1,2-丙二胺
CH3CH(NH2)CH2NH2
5.25×10-5(K1)
4.28
4.05×10-8(K2)
7.393
13
三丙胺
(CH3CH2CH2)3N
4.57×10-4
3.34
2.6×10-5(K1)
4.59
2.6×10-6(K2)
5.59
55
乙二胺四乙酸(EDTA)
CH2—N(CH2COOH)2
∣
CH2—N(CH2COOH)2
1.0×10-2(K1)
2.0
2.14×10-3(K2)
2.67
6.92×10-7(K3)
6.16
5.5×10-11(K4)
10.26
序号(No.)
名称(Name)
化学式(Chemical formula)
Kb
pKb
1
甲胺
CH3NH2
4.17×10-4
3.38
2
尿素(脲)
CO(NH2)2
1.5×10-14
13.82
3
乙胺
CH3CH2NH2
4.27×10-4
3.37
4
乙醇胺
H2N(CH2)2OH
3.16×10-5
4.50
5
乙二胺
H2N(CH2)2NH2
4.10
6.6×10-6(K3)
5.18
53
苯基六羧酸
C6(COOH)6
2.1×10-1(K1)
0.68
6.2×10-3(K2)
2.21
3.0×10-4(K3)
3.52
8.1×10-6(K4)
5.09
4.8×10-7(K5)
6.32
3.2×10-8(K6)
7.49
54
癸二酸
HOOC(CH2)8COOH
8.51×10-5(K1)
4.07
7.08×10-8(K2)
7.15
6
二甲胺
(CH3)2NH
5.89×10-4
3.23
7
三甲胺
(CH3)3N
6.31×10-5
4.20
8
三乙胺
(C2H5)3N
5.25×10-4
3.28
9
丙胺
C3H7NH2
3.70×10-4
3.432
10
异丙胺
i-C3H7NH2
4.37×10-4
20
3-丁烯酸
CH2═CHCH2COOH
2.1×10-5
4.68
21
异丁烯酸
CH2═C(CH2)COOH
2.2×10-5
4.66
22
反丁烯二酸(富马酸)
HOCOCH═CHCOOH
9.3×10-4(K1)
3.03
3.6×10-5(K2)
4.44
23
顺丁烯二酸(马来酸)
HOCOCH═CHCOOH
1.2×10-2(K1)
4.76
4.0×10-7(K3)
6.40
38
苯酚
C6H5OH
1.1×10-10
9.96
39
邻苯二酚
(o)C6H4(OH)2
3.6×10-10
9.45
1.6×10-13
12.8
40
间苯二酚
(m)C6H4(OH)2
3.6×10-10(K1)
9.30
8.71×10-12(K2)
11.06
41
对苯二酚
(p)C6H4(OH)2
4.27
5
甘氨酸
CH2(NH2)COOH
1.7×10-10
9.78
6
一氯乙酸
CH2ClCOOH
1.4×10-3
2.86
7
二氯乙酸
CHCl2COOH
5.0×10-2
1.30
8
三氯乙酸
CCl3COOH
2.0×10-1
0.70
9
丙酸
CH3CH2COOH
1.35×10-5
4.87
10
丙烯酸
CH2═CHCOOH
序号(No.)
名称(Name)
化学式
(Chemical formula)
Ka
pKa
1
甲酸
HCOOH
1.8×10-4
3.75
2
乙酸
CH3COOH
1.74×10-5
4.76
3
乙醇酸
CH2(OH)COOH
1.48×10-4
3.83
4
草酸
(COOH)2
5.4×10-2(K1)
1.27
5.4×10-5(K2)
5.40
50
间苯二甲酸
(m)C6H4(COOH)2
2.4×10-4(K1)
3.62
2.5×10-5(K2)
4.60
51
对苯二甲酸
(p)C6H4(COOH)2
2.9×10-4(K1)
3.54
3.5×10-5(K2)
4.46
52
1,3,5-苯三甲酸
C6H3(COOH)3
7.6×10-3(K1)
2.12
7.9×10-5(K2)
11.50
4
硼酸
H3BO3
5.8×10-10(K1)
9.24
1.8×10-13(K2)
12.74
1.6×10-14(K3)
13.80
5
次溴酸
HBrO
2.4×10-9
8.62
6
氢氰酸
HCN
6.2×10-10
9.21
7
碳酸
H2CO3
4.2×10-7(K1)
6.38
5.6×10-11(K2)
10.25
8
次氯酸
2
氢氧化银
AgOH
1.10×10-4
3.96
3
氢氧化钙
Ca(OH)2
3.72×10-3
2.43
3.98×10-2
1.40
4
氨水
NH3+H2O
1.78×10-5
4.75
5
肼(联氨)
N2H4+H2O
9.55×10-7(K1)
6.02
1.26×10-15(K2)
14.9
6
羟氨
NH2OH+H2O
9.12×10-9
2.0×10-5
4.70
28
3-戊烯酸
CH3CH═CHCH2COOH
3.0×10-5
4.52
