最新中考化学化学计算题真题汇编(含答案)
九年级化学化学计算题题20套(带答案)及解析
九年级化学化学计算题题20套(带答案)及解析一、中考化学计算题1.小王同学为了测定某Na2CO3溶液中溶质的质量分数,取10g该溶液于烧杯中,然后将400g澄清石灰水分四次加入,烧杯中沉淀的质量与每次加入澄清石灰水的质量关系如表。
请计算:第一次第二次第三次第四次加入澄清石灰水100100100100的质量/g生成沉淀的质量0.4m 1.0 1.0/g(1)表中m的值为_____。
(2)Na2CO3溶液中溶质的质量分数_____(写出计算过程)。
【答案】0.8 10.6%【解析】【分析】第一次生成沉淀0.4g,而第三次不到0.4g的3倍,则第二次应该为0.4g的二倍,所以m=0.4g×2=0.8g,根据碳酸钙的质量和对应的化学方程式求算碳酸钠溶液中溶质的质量分数。
【详解】由分析可知,m=0.4g×2=0.8g设原Na2CO3溶液中溶质的质量分数为x。
106100=10g?x 1.0gx=10.6%答:(1)表中的m的值为 0.8。
(2)原Na2CO3溶液中溶质的质量分数是10.6%。
2.将含有杂质(不溶于水)的氯化钡样品12.5g放入39.6g水中充分搅拌,完全溶解后过滤。
取20g滤液与足量的稀硫酸完全反应,得到4.66g沉淀。
请计算:①配制的氯化钡溶液中溶质的质量分数。
②样品中氯化钡的质量分数。
【答案】20.8%;83.2%【解析】【详解】①设参加反应的氯化钡的质量为x 。
2244BaCl +H SO =BaSO +2H 208233x4Cl.66g208233=x 4.66gx= 4.16g则配制的氯化钡溶液中溶质的质量分数为 :4.16g20g×100%=20.8% ②由于20g 溶液中含有4.16g 氯化钡,则可设样品中氯化钡的质量为y 。
则4.16g y=20g-4.16g 39.6gy=10.4g样品中氯化钡的质量分数为:10.4g12.5g×100%=83.2%答:①氯化钡溶液中溶质的质量分数为20.8% ②样品中氯化钡的质量分数为83.2%。
【化学】中考化学化学计算题真题汇编(含答案)及解析

【化学】中考化学化学计算题真题汇编(含答案)及解析一、中考化学计算题1.某化学兴趣小组的同学在实验室配制溶质质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数。
下图表示用该氢氧化钠溶液与10g某稀盐酸发生反应时溶液温度的变化情况。
试计算稀盐酸中溶质的质量分数。
【答案】14.6%【解析】试题分析:由于中和反应放热,故随着反应的进行,溶液的温度逐渐升高,直至反应恰好完全,溶液温度达到最高,故根据图示可判断,当加入氢氧化钠那溶液的质量为20g时,反应恰好完全解:分析图知与10g稀盐酸恰好完全反应的氢氧化钠质量为:20g×8%=1.6g设稀盐酸中溶质的质量为xNaOH+HCl=NaCl+H2O40 36.51.6g x40:1.6g=36.5:xx=1.46g稀盐酸中溶质的质量分数为:1.46g/10g=14.6%答:稀盐酸中溶质的质量分数为14.6%考点:根据化学方程式计算2.现有碳酸钠和氯化钠的固体混合物12.6g,其中含氧元素4.8g,将该混合物加入到一定质量的稀盐酸中,恰好完全反应,得到137g氯化钠溶液。
计算:(l)原固体混合物中碳酸钠的质量分数(结果保留至0.1%)______;(2)所用稀盐酸中溶质的质量分数(结果保留至0.1%)______。
【答案】84.1% 5.7%【解析】【分析】【详解】(l)原固体混合物中碳酸钠的质量分数4.8g÷=10.6g;混合物中碳酸钠的质量分数为10.6g÷12.6g×100%≈84.1%;(2)设盐酸中溶质的质量为x,生成二氧化碳质量为y 2322Na CO+2HCl=2NaCl+H O+CO106734410.6g x y↑1067344==10.6g x yx=7.3gy=4.4g所用稀盐酸中溶质的质量分数7.3g÷(137g+4.4g-12.6g)×100%≈5.7%3.化学兴趣小组的同学用一瓶含有少量氯化钠和氯化钙的固体混合物进行下列实验:取样品14 g,放入烧杯中,加入96 g碳酸钠溶液恰好完全反应后过滤,称得滤液的总质量为100 g。
【化学】中考化学化学计算题题20套(带答案)及解析
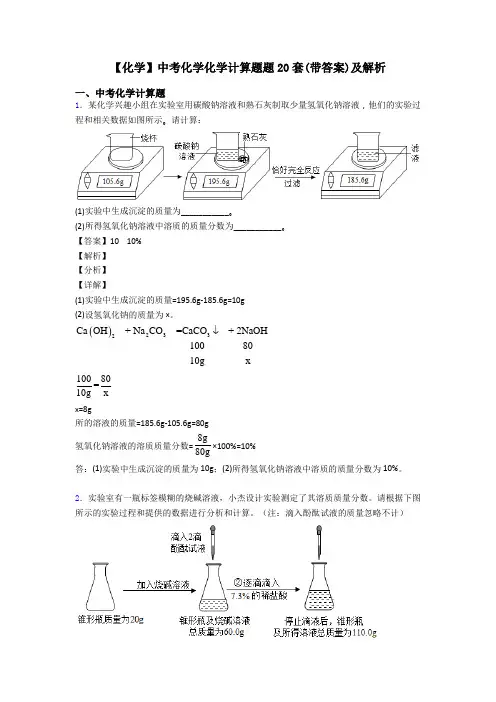
【化学】中考化学化学计算题题20套(带答案)及解析一、中考化学计算题1.某化学兴趣小组在实验室用碳酸钠溶液和熟石灰制取少量氢氧化钠溶液,他们的实验过程和相关数据如图所示。
请计算:(1)实验中生成沉淀的质量为___________。
(2)所得氢氧化钠溶液中溶质的质量分数为___________。
【答案】10 10%【解析】【分析】【详解】(1)实验中生成沉淀的质量=195.6g-185.6g=10g(2)设氢氧化钠的质量为x 。
()2332Ca OH + Na CO CaCO + =1002N 8xaOH10g ↓ 10080=10g xx=8g所的溶液的质量=185.6g-105.6g=80g氢氧化钠溶液的溶质质量分数=8g 80g×100%=10% 答:(1)实验中生成沉淀的质量为10g ;(2)所得氢氧化钠溶液中溶质的质量分数为10%。
2.实验室有一瓶标签模糊的烧碱溶液,小杰设计实验测定了其溶质质量分数。
请根据下图所示的实验过程和提供的数据进行分析和计算。
(注:滴入酚酞试液的质量忽略不计)(1)将稀盐酸逐滴滴入锥形瓶的过程中,应边滴加边摇动锥形瓶,当观察到溶液颜色恰好___________________时,停止滴加稀盐酸。
(2)通过计算确定该瓶烧碱溶液的溶质质量分数。
(写出计算步骤)___________。
【答案】无色 10%【解析】【分析】(1)根据酚酞溶液遇碱性溶液呈红色,遇中性溶液为无色解答;(2)根据化学方程式结合氢氧化钠的质量可以计算出稀盐酸的质量进而就算出其溶质的质量分数。
【详解】(1)在盛有烧碱溶液的锥形瓶中,滴加酚酞试液,溶液变红,逐滴滴入稀盐酸,稀盐酸会和氢氧化钠反应,当氢氧化钠被耗尽时,溶液变为无色。
故答案:无色(2)解:所取烧碱溶液的质量为:60g-20g=40g设烧碱溶液的溶质质量为x ,2NaOH +HCl =NaCl+H O4036.5x 50g 7.3%⨯ 4036.5507.3%x g =⨯ 0.4x g =该瓶烧碱溶液的溶质质量分数0.4100%10%40g g⨯== 答:该瓶烧碱溶液的溶质质量分数为10%。
中考化学真题分类汇编 计算题(含解析)-人教版初中九年级全册化学试题

综合计算题(一)1.(18某某)尿素[CO(NH2)2]是一种常见的氮肥,工业上制备反应如下:CO2+2NH3CO(NH2)2+H2O,请计算:(1)尿素中氮元素的质量分数。
(2)生产6t尿酸理论上需要氨气的质量是多少?化学试题参考答案及评分标准【答案】(1)46.7%t。
【解析】(1)尿素中氮元素的质量分数为:×100%=46.7%(2)设理论上需要氮气的质量为x。
CO2+2NH3CO(NH2)2+H2O3460x6tx tt。
2.(18某某)一种新型“人造树叶”可吸收二氧化碳并转化为乙醇(C2H5OH)燃料,化学方程式为2CO2+3H2O C2H5OH+3O2。
研究显示,一升“人造树叶”每天可从空气中吸收968gCO2。
(1)一升“人造树叶”工作一天可得到乙醇的质量是________?(2)若每天一棵树平均可吸收2,则一升“人造树叶”吸收的CO2相当于_______棵树吸收的CO2。
【答案】(1).506g(2).20【解析】根据反应的化学方程式计算解答。
(1)设一升“人造树叶”工作一天可得到乙醇的质量为x。
2CO2+3H2O C2H5OH +3O28846968gxx=506g(2)968g÷48.4g=20答:(1)一升“人造树叶”工作一天可得到乙醇的质量是506g;(2)若每天一棵树平均可吸收2,则一升“人造树叶”吸收的CO2相当于20棵树吸收的CO2。
3.(18某某)用溶质质量分数为5%的NaOH溶液中和73g的稀盐酸,反应过程中溶液的酸碱度变化如下图所示。
请计算:(1)用质量分数为10%的氢氧化钠溶液配制5%的氢氧化钠溶液100g,需要水__________克.(2)当a为80g时,所得溶液中溶质的质量分数是___________(结果精确到0.1%)?【答案】(1)50(2)3.8%【解析】(1)设需要水的质量为x,根据溶质在稀释前后质量不变。
100g×5%=(100g-x)×10%x=50g;(2)根据图像可知,当a为80g时,盐酸与氢氧化钠恰好完全反应。
最新中考化学试卷分类汇编化学化学计算题(及答案)
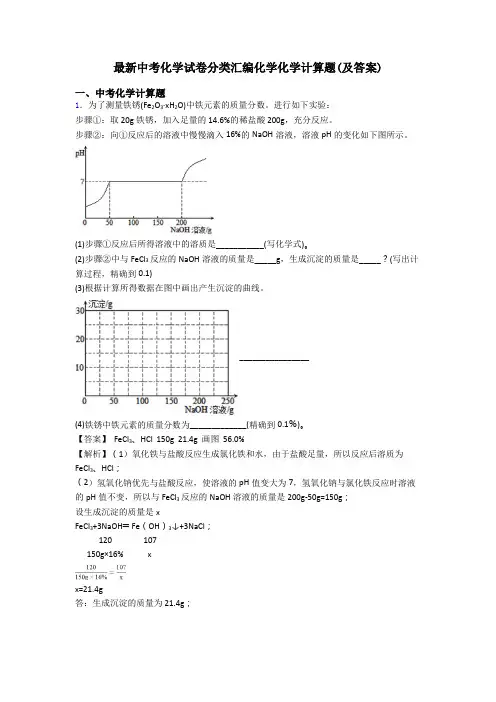
最新中考化学试卷分类汇编化学化学计算题(及答案)一、中考化学计算题1.为了测量铁锈(Fe2O3·xH2O)中铁元素的质量分数。
进行如下实验:步骤①:取20g铁锈,加入足量的14.6%的稀盐酸200g,充分反应。
步骤②:向①反应后的溶液中慢慢滴入16%的NaOH溶液,溶液pH的变化如下图所示。
(1)步骤①反应后所得溶液中的溶质是___________(写化学式)。
(2)步骤②中与FeCl3反应的NaOH溶液的质量是_____g,生成沉淀的质量是_____?(写出计算过程,精确到0.1)(3)根据计算所得数据在图中画出产生沉淀的曲线。
________________(4)铁锈中铁元素的质量分数为_____________(精确到0.1%)。
【答案】 FeCl3、HCl 150g 21.4g 画图 56.0%【解析】(1)氧化铁与盐酸反应生成氯化铁和水,由于盐酸足量,所以反应后溶质为FeCl3、HCl;(2)氢氧化钠优先与盐酸反应,使溶液的pH值变大为7,氢氧化钠与氯化铁反应时溶液的pH值不变,所以与FeCl3反应的NaOH溶液的质量是200g-50g=150g;设生成沉淀的质量是xFeCl3+3NaOH═Fe(OH)3↓+3NaCl;120 107150g×16% xx=21.4g答:生成沉淀的质量为21.4g;(3)所以产生沉淀的曲线为;(4)所以铁锈中铁的质量分数为 =56%。
2.某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下实验,取13.25g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8g水使其完全溶解,再向其中加入稀盐酸,测得反应放出气体的总质量与所加入稀盐酸的质量关系曲线如图所示,请回答:(1)当加入212g稀盐酸时,放出气体的质量为_____g。
(2)碳酸钠样品中碳酸钠的质量分数为多少?_____(写出计算过程)(3)加入106g稀盐酸(即A点)时烧杯中溶液的溶质质量分数为多少?_____(写出计算过程)【答案】4.4g 80% 5.6%【解析】【分析】【详解】(1)根据图像,可以看出当加入106g稀盐酸的时候,反应就结束,产生气体质量为4.4g,所以当加入212g稀盐酸时,放出气体的质量仍然为4.4g(2)发生反应:Na2CO3+2HCl=2NaCl+H2O+CO2↑,根据方程式中碳酸钠与二氧化碳的质量关系可算出碳酸钠的质量,进而可以计算碳酸钠样品中碳酸钠的质量分数,反应后得到的是NaCl溶液,所以也可根据方程式中NaCl与二氧化碳的质量关系,求出溶液中溶质的质量解:设碳酸钠的质量为x,生成的NaCl质量为y。
最新全国中考化学真题汇编——《计算题》专题(含答案,部分解析)

全国真题汇编《计算题》22. (2019·青海省)市售的某些银首饰是银、锌合金。
小庆同学取该合金样品20g ,加入100g 稀硫酸恰好完全反应,产生气体质量与反应时间的关系如图所示,计算:(1)该合金中锌的质量(精确到0.1g )。
_______(2)该稀硫酸中溶质的质量分数(精确到0.1% )。
______ 【答案】 (1). 6.5g (2). 9.8% 【解析】【详解】(1)由图可知,生成氢气的质量为0.2g ,设该合金中锌的质量为x ,参加反应的硫酸的质量为y ,则:244265982xyZn H SO ZnSO gH 0.2+=+↑65982x y 0.2g==x=6.5g y=9.8g(2)该稀硫酸中溶质的质量分数为:9.8g100%=9.8%100g⨯。
18. (2019·宁夏)中华文化源远流长,早在西汉时期《淮南万毕术》一书中就有“曾青得铁则化为铜”的记载,这是我国现代“湿法炼铜”的先驱。
某大型工厂利用此原理处理含硫酸铜的废液回收金属铜时,向100kg 的废液中加入足量的铁粉,得到金属铜6.4kg 。
(1)计算废液中硫酸铜的质量分数是多少?______(2)金属资源保护的有效途径之一是金属的回收再利用,其它有效途径还有_______(写一条)。
【答案】 (1). 16% (2). 防止金属锈蚀(或寻找金属替代品;有计划合理开采)(答案合理即得分) 【解析】 【分析】硫酸铜和铁反应生成硫酸亚铁和铜。
【详解】(1)设废液中硫酸铜的质量为x44CuSO +Fe =FeSO +Cu 16064x 6.4kg160x =64 6.4kgx=16kg废液中硫酸铜的质量分数为16kg×100%=16%100kg答:废液中含硫酸铜的质量分数为16%。
(2)金属资源保护的有效途径之一是金属的回收再利用,其它有效途径还有防止金属锈蚀(或寻找金属替代品;有计划合理开采)。
(化学)中考化学化学计算题题20套(带答案)
(15.6g-10.6g+11.7g)/111.2g×100%=15.0% (1分)
答:(1)产生二氧化碳4.4克
(2)所得溶液中溶质的质量分数是15.0%
【解析】
试题分析:根据质量差可以计算生成二氧化碳的质量,根据二氧化碳的质量可以计算碳酸钠、生成氯化钠的质量,进一步可以计算所得溶液中溶质的质量分数。
【详解】
(1)比较三组数据可以知道,12.5g合金最多只能生成0.2g氢气,其中的锌完全参加反应
设12.5g铜锌合金中含有锌的质量为x,生成硫酸锌的质量为y
解得:x=6.5g;y=16.1g
铜合金中铜的质量分数为: ;
铜锌合金中铜的质量分数为48%
(2)由第三次可知25g合金也生成0.2克氢气,说明100克稀硫酸最多消耗6.5g的锌,硫酸不足,根据(1)得出生成溶质硫酸锌的质量为16.1g;
答:(2)稀硫酸中溶质的质量分数为19.6%.
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算.
点评:本题主要考查学生运用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.
10.某化学兴趣小组为了粗略测定一批石灰石样品中CaCO3的质量分数,设计并进行如下实验。实验装置如图所示,称取研细的2.60g石灰石样品,分4次加入稀盐酸,充分反应至不再产生气体为止。测得反应前后的有关质量如表:
(3)设原60g稀盐酸中溶质质量分数为x
x=7.3%
答:原60g稀盐酸中溶质质量分数为7.3%。
【点睛】
观察表格,看每次加入盐酸,剩余固体量的变化情况,据此推出反应的盐酸的量和反应的碳酸钙的量。
初中化学计算题大全(含答案及解析)
2024年中考化学《必考经典》计算题大全(含答案及解析)1.实验室欲测定一瓶标签破损的稀硫酸中溶质的质量分数,现取10g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化情况如图所示。
分析并计算:(1)a点溶液中含有的离子是_____。
(2)当pH=7时,消耗氢氧化钠溶液中NaOH质量为_____g。
(3)计算稀H2SO4中溶质的质量分数。
_____(4)计算恰好完全反应时所得溶液的溶质质量分数。
_____【答案】Na+、H+、SO42- 0.8 稀H2SO4的溶质质量分数是9.8%;恰好完全反应时所得溶液的溶质质量分数是5.5%。
【解析】【详解】(1)由图示可知,在a点时溶液的pH小于7,说明加入的NaOH完全反应,有剩余的硫酸,所以,溶液中含有的离子为:Na+、H+、SO42-;(2)由图示可知,在溶液的pH等于7,消耗的NaOH溶液的质量为16g,溶质的质量为:16g×5%=0.8g;(3)10g稀硫酸样品含有H2SO4的质量为x,生成的硫酸钠的质量为y2NaOH+H SO=Na SO+2H O2424280981420.8g x y解得:x=0.98g y=1.42g稀H2SO4的溶质质量分数为:×100%=9.8%;(4)恰好完全反应时所得溶液的溶质质量分数:×100%≈5.5%。
2.某小组同学将530 g碳酸钠溶液加入到280 g石灰乳(水和氢氧化钙的混合物)中,使之恰好完全反应,所得溶液中溶质的质量分数为1%,计算加入的碳酸钠溶液中溶质的质量分数。
【答案】2%【解析】【详解】设原碳酸钠溶液中溶质的质量为xNa2CO3+ Ca(OH)2=CaCO3↓+ 2NaOH106 100 80X则解得x =10.6g所以加入的碳酸钠溶液中溶质的质量分数为答:加入的碳酸钠溶液中溶质的质量分数为2%。
3.取一定量的氯化钠与氢氧化钠的混合物,加一定量的水配成溶液,然后向其中滴加溶质质量分数为7.3%稀盐酸,直至恰好反应,共消耗稀盐酸50g。
最新九年级化学化学计算题真题汇编(含答案)
最新九年级化学化学计算题真题汇编(含答案)一、中考化学计算题1.化学兴趣小组的同学用一瓶含有少量氯化钠和氯化钙的固体混合物进行下列实验:取样品14 g,放入烧杯中,加入96 g碳酸钠溶液恰好完全反应后过滤,称得滤液的总质量为100 g。
(1)根据质量守恒定律,可知生成沉淀的质量为___________________________。
(2)固体混合物中氯化钙的质量是___________?(3)所得滤液中溶质的质量分数是__________?【答案】10 g 2.9 g 14.6%【解析】(1) 、根据质量守恒定律可知,反应前物质质量总和=反应后物质质量总和,即反应前所有混合物的总质量=滤液的总质量+生成沉淀的质量;(2)、根据化学方程式中各物质之间的质量比,利用碳酸钙沉淀的质量,列出比例式,即可计算出固体混合物中氯化钙的质量。
(3) 、根据题意,反应完全后过滤,所得滤液为氯化钠溶液,滤液中的溶质NaCl包括混合物中原有的NaCl和反应生成的NaCl;根据上述方程式可以求出生成NaCl的质量,而混合物中原有的NaCl的质量=混合物总质量-氯化钙的质量,据此可以计算出滤液中溶质的质量,然后根据溶质质量分数= 溶质质量溶液质量×100%计算即可。
解:(1) 、根据质量守恒定律,生成沉淀的质量=14g+96g-100g=10g;(2)、设固体混合物中含氯化钙的质量为x,反应后生成氯化钠的质量为y。
Na2CO3+CaCl2=CaCO3↓+2NaCl111 100 117x 10g y111100117=10x g y=解得,x=11.1g y=11.7g(3) 、原混合物中含氯化钠的质量=14g-11.1g=2.9g则所得滤液中溶质的质量分数=2.911.7100g gg+×100%=14.6%答:(2)、原固体混合物中氯化钙的质量为11.1g;(3) 、所得滤液中溶质的质量分数为14.6%。
初三化学化学计算题题20套(带答案)
初三化学化学计算题题20套(带答案)1. 假设有一块铁块,其质量为56克。
求该铁块中含有的铁原子数。
解答:我们需要知道铁的摩尔质量。
铁的摩尔质量约为56克/摩尔。
因此,该铁块中含有的铁原子数为56克 / 56克/摩尔 = 1摩尔。
由于1摩尔物质中含有6.022 x 10²³个原子,所以该铁块中含有的铁原子数为1摩尔x 6.022 x 10²³个/摩尔= 6.022 x 10²³个。
2. 某化学反应中,反应物A和反应物B的化学计量比为2:3。
如果反应物A的质量为24克,求反应物B的质量。
解答:我们需要根据化学计量比计算出反应物B的质量。
由于反应物A和反应物B的化学计量比为2:3,所以反应物B的质量为24克x (3/2) = 36克。
3. 在一定条件下,一定量的氧气与一定量的氢气完全反应,了36克水。
求反应中消耗的氧气和氢气的质量。
解答:我们需要根据水的化学式H₂O计算出水的摩尔质量。
水的摩尔质量为2 x 1.008克/摩尔 + 16.00克/摩尔 = 18.016克/摩尔。
因此,36克水的物质的量为36克 / 18.016克/摩尔 = 2摩尔。
由于水的化学计量比为2:1,所以反应中消耗的氢气的物质的量为2摩尔,质量为2摩尔 x 2.016克/摩尔 = 4.032克。
同样,消耗的氧气的物质的量为1摩尔,质量为1摩尔 x 32.00克/摩尔 = 32.00克。
4. 某溶液中,溶质的质量分数为10%。
如果该溶液的质量为500克,求溶质的质量。
数为10%,即溶质的质量占溶液总质量的10%。
因此,溶质的质量为500克 x 10% = 50克。
5. 在一定条件下,一定量的氢气和一定量的氧气完全反应,了水。
如果反应中消耗的氢气的质量为2克,求反应中消耗的氧气的质量。
解答:我们需要根据水的化学式H₂O计算出水的摩尔质量。
水的摩尔质量为2 x 1.008克/摩尔 + 16.00克/摩尔 = 18.016克/摩尔。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
最新中考化学化学计算题真题汇编 ( 含答案 )一、中考化学计算题1.取 CaCl 2和 CaCO 3的混合物 12.5g 于烧杯中,向其中滴加一定溶质质量分数的稀盐酸, 请加稀盐酸的质量与产生气体质量的关系如图所示。
求:(1) ___________________________ 混合物 CaCO 3 中的质量为 ; (2) ______________________________ 稀盐酸中的溶质质量分数为 ;(3) _______________________________________________________ 恰好完全反应时,所得不饱和溶液中溶质的质量分数为 _______________________________________________ ? (写出计算过程,计算试题分析:盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,由图可知:二氧化碳的质量为4.4g设碳酸钙的质量为 x ,稀盐酸中的溶质质量为 z ,生成氯化钙的质量为 y 。
CaCO 3+2HCl=CaC 2l+H 2O+CO 2↑ 100 73 111 44 x z y 4.4gx=10g z=7.3g y=11.1g1)混合物 CaCO 3 中的质量为2)稀盐酸中的溶质质量分数为3)恰好完全反应时,所得不饱和溶液中溶质的质量分数100%≈ 12.6%。
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算2.将 25.6 g NaCl 和 MgCl 2固体混合物完全溶于 126 g 水中配成溶液,再将 200 g 一定溶质 质量分数的 NaOH 溶液不断加入该溶液中。
充分反应后,测得的实验数据如下表。
求:实验次数 1 2 3 4 5 加入 NaOH404040404010g ;100%=7.3%;(1) ______________________________ 上表中m 的值为多少。
(2) ____________________________________________________ 恰好完全反应时,所得溶液中溶质的质量分数。
_____________________________________________________【答案】8.7 10%【解析】【分析】【详解】( 1)第一次加入40g 氢氧化钠溶液质量得到沉淀2.9g,第四次实验加入40g 氢氧化钠溶液生成沉淀增加了,说明第一次实验中40g 氢氧化钠完全反应只能生成2.9g 沉淀,所以第三次加入40g 氢氧化钠溶液也完全反应,生成沉淀的质量是 2.9g,所以m 的数值为5.8+2.9=8.7;(2)由表中数据分析可知,第4 次恰好完全反应。
设混合物中MgCl2的质量为x,生成NaCl 的质量为y。
MgCl2+ 2NaOH = Mg OH 2+ 2NaCl9558117x11.6g yx95=58 = 11.6gx=19 g58 = 11.6g117 = yy=23.4 g则原混合物中NaCl质量为25.6 g-19 g=6.6 g6.6g 23.4g 25.6g 126g 40g 4所以恰好反应时所得溶液中溶质的质量分数为× 100%=10%11.6g答:恰好完全反应时,所得溶液中溶质质量分数为10%。
3.某纯碱样品中含有少量氯化钠,现取该样品12g 溶解在100g 水中,再向其中逐滴加入氯化钙溶液,产生的沉淀与加入氯化钙溶液的质量关系如图所示:计算:(1)纯碱中碳酸钠的质量分数(结果精确到0.1%,下同);(2)恰好完全反应时,所得溶液中溶质的质量分数。
【答案】88.3% 5.4%【解析】【分析】碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钙。
反应方程式为:Na2CO3 +CaC2l ═ CaCO3 ↓ +2NaC。
l【详解】解(1)设纯碱样品中碳酸钠的质量为x,生成氯化钠的质量为y,106 100 117 ,x 10g y得x=10.6g,y=11.7g,纯碱样品中碳酸钠的质量分数:10.6× 100% 88.3%,12g(2)所得溶液中的溶质为氯化钠,来源为样品中的少量氯化钠和反应生成的氯化钠,其质11.7g (12g10.6g )量分数为× 100% 5.4%。
12g 100g 140g 10g答:(1)纯碱中碳酸钠的质量分数约88.3%;(2)恰好反应时,所得溶液中溶质的质量分数约为5.4%。
4.维生素C 又名抗坏血酸,易溶于水,易被氧化,遇热易被破坏,人体缺乏维生素C可能引发多种疾病,它的化学式是C6H8O6 。
计算:(1)维生素C 的相对分子质量为;(2)维生素C 中氢元素的质量分数为(结果保留一位小数)。
【答案】(1)176;(2)4.5%【解析】本题主要考查学生们对于相对分子质量、元素的质量分数计算的掌握程度。
(1)维生素C 的相对分子质量为:12×6+1×8+16×6=1;76(2)维生素C 中氢元素的质量分数=(1×8)/176×100%=4.5%5.侯氏制碱法生产的碳酸钠中常含有少量的氯化钠。
某学习小组对其组成展开探究。
取碳 酸钠和氯化钠的混合物样品 24g ,加入 100g 水使其完全溶解,再加入 96g 过量的氯化钙溶 液,反应过程中生成沉淀的质量与氯化钙溶液的质量关系如图所示:完全反应时,得到的沉淀质量是 _ 计算样品中 Na 2CO 3 的质量分数 ( 通过已知数据,可以求出的量有 _ A 反应后溶液的总质量 B 参加反应的氯化钙质量 C 氯化钙溶液中溶质的质量分数D 恰好完全反应时,溶液中氯化钠的溶质质量分数(4)取混合物样品 12g ,加入足量的稀盐酸,将生成的二氧化碳通入盛有8g 炽热碳粉的密闭容器中充分反应,在下图中画出二氧化碳的质量与容器中固体质量变化的关系图。
解析】 分析】 详解】1) 2) 3) g 。
写出计算过程,结果保留一位小数)。
(写字母)。
答案】 20 88.3% ABCD( 1)完全反应时,得到的沉淀质量是 20g 。
(2)设样品中 Na 2CO 3 的质量为 x CaCl 2 +Na 2CO 3 = CaCO 3↓+2NaCl106 100 x20g106 = 100 x = 20gx=21.2g21.2g样品中 Na 2CO 3 的质量分数为100% 88.3%24g(3)通过已知数据,可以求出的量有:A 反应后溶液的总质量B 参加反应的氯化钙质量C 氯化钙溶液中溶质的质量分数D 恰好完全反应时,溶液中氯化钠的溶质质量分数,故选6.实验室有一瓶未知浓度的 BaCl 2溶液,某同学取出 150g 该溶液于烧杯中,向其中逐滴加 入溶质质量分数为 26.5%的 Na 2CO 3 溶液。
反应过程中生成沉淀的质量与所用Na 2CO 3溶液质量的关系如图所示。
已知: BaCl 2+ Na 2CO 3=BaCO 3↓+2NaCl 。
请计算:(1)配制 26.5%的 Na 2CO 3溶液 80g ,需要 Na 2CO 3固体 ___g 。
(2)BaCl 2 溶液的溶质质量分数是 ____ ?(写出计算过程,结果保留到 0.1%)【答案】 (1) 21.2g ;( 2)13.9% 【解析】试题分析:( 1) 根据溶质质量分数计算的表达式:配制26.5%的 Na 2CO 3 溶液 80g ,需要Na 2CO 3 固体质量 =80g × 2.6 5%=21.2g(2)从图甲中获知,当 BaCl 2 完全转化为沉淀时消耗 Na 2CO 3 溶液的质量为 40g,再根据化学ABCD 。
反应方程式: BaCl 2+Na 2CO 3=BaCO 3↓+2NaCl 中 Na 2CO 3 与 BaCl 2 的质量关系,可求出 的质量,进而可求解 BaCl 2 溶液的溶质质量分数 解:设 BaCl 2 的质量为 xBaCl 2+ Na 2CO 3= BaCO 3↓+ 2NaCl 208 106 x40g × 2.6 5%208∶106=X ∶(40g × 2.6 5%) x =208× 40g ×.265%/106=20.8g该 BaCl 2溶液的溶质质量分数=( 20.8g/150g )× 100%=1.3 9% 答:该 BaCl 2 溶液的溶质质量分数为13.9% 考点:溶质质量分数计算,根据化学方程式计算(1)生成氧气的质量。
(2)过氧化氢溶液的溶质质量分数。
【答案】 (1) 0.8g (2)3.4%【解析】 试题分析:依据质量守恒定律化学反应前后物质的总质量不变,那么减少的质量为生成的 氧气的质量;再利用化学方程式,根据氧气的质量可求出过氧化氢中溶质的质量; 解: ⑴氧气的质量为: 3g+50g-52.2g=0.8g⑵设过氧化氢溶液中溶质质量为x 。
2H 2O 2 2H 2O + O 2↑68 32x0.8g x=1.7g则过氧化氢溶液的溶质质量分数 = 答:略。
考点:8.金属单质 A 与非金属单质硫( S )发生如下反应: 2A + S A 2S 。
甲、乙、丙三组学生 在实验室分别进行该实验,加入的 A 和硫的质量各不相同,但总质量均为 6 g 。
充分反应时,实验数据记录如下:BaCl27.某校化学实验室要测定过氧化氢溶液的溶质质量分数。
设计实验如下图所示。
根据上述信息,回答问题:(1)元素A的相对原子质量为。
(2)丙组实验中a∶b 为(结果以最简整数比表示,请写出计算过程)。
【答案】(1)64 ⋯⋯⋯⋯(1 分)(2)a∶b 为2∶3 或9∶1 ⋯⋯⋯⋯(2 分,写对1 个且过程正确的给1分)【解析】(1)由甲、乙的反应可知,4g A和1gB完全反应生成5g 的A2S,进行解答(2)生成3gA2S,一种情况时A全部反应,一种是S全部反应进行解答9.将铁粉和铜粉混合物7.0g,加入到盛有60.0 g 稀盐酸的烧杯中,恰好完全反应。
此时烧杯内各物质的总质量为66.8 g。
试计算:(1)原混合物中铁粉的质量分数。
(精确到0.1%)(2)反应后所得溶液中溶质的质量分数。
(精确到0.1%)【答案】解:生成H2的质量="7.0" g + 60 .0g—66.8 g =" 0.2" g (⋯1 ⋯分⋯)设原混合物中Fe的质量为x,生成FeCl2的质量为yFe + 2HCl = FeC2l+ H2↑ ⋯⋯(⋯1 分)56 127 2X y 0.2 g ⋯⋯⋯(1 分)56∶2 =x∶0.2 g x=5.6 g127∶2="y∶0.2" g y="12.7" g(1)原混合物中Fe的质量分数="5.6" g ÷7.0 g ×100% =80.0% (⋯1 ⋯分⋯)(2)反应后所得溶液中FeCl2的质量分数="12.7" g (÷5.6 g+60.0g—0.2 g)× 100% =19.4% ⋯⋯(⋯2分)答:略(其他合理解答也可酌情给分)【解析】分析:由于反应后生成的氢气从烧杯内逸出,因此由金属混合物的质量、稀硫酸的质量和反应后烧杯内该物质的总质量可以计算出生成的氢气的质量;由氢气的质量,根据铁与稀硫酸反应的化学方程式可以计算出参加反应的铁的质量和生成氯化亚铁的质量,进而计算出混合物中铁粉的质量分数和反应后所得溶液中溶质的质量分数.解:生成H2 的质量=7.0g+60.0g-66.8g=0.2g设原混合物中Fe 的质量为x,生成FeCl2的质量为yFe+2HCl=FeC2l+H2↑56 127 2x y 0.2g56 127 2 ,x y 0.2g x=5.6g,y=12.7g5.6g(1)原混合物中Fe 的质量分数= × 100%=80.0%7.0g12.7g(2)反应后所得溶液中FeCl2的质量分数= × 100%=19.4%5.6g 60.0g 0.2g答:(1)原混合物中铁粉的质量分数为80.0%.(2)反应后所得溶液中溶质的质量分数为19.4%.点评:本题主要考查有关化学方程式的计算和溶质质量分数的计算.进行化学方程式的计算时,必须找出反应物或生成物中一种纯物质的质量,然后根据这一质量计算出其它物质的质量.进行溶质质量分数的计算时,首先要计算出所得溶液中溶质的质量,然后再计算出所得溶液的质量.计算所得溶液的质量时,一般用反应前各物质的质量总和减去未反应的固体杂质的质量、再减去生成沉淀的质量和生成气体的质量.10.在人类历史发展过程中,金属元素的发现和使用深刻影响了我们的生活、生产等活动。
