C7-4-3洁净室洁净度测试记录
洁净室综合性能(常规项目)检测原始记录

第 第 共页
√悬浮粒子
粒径次数
测点 1 2 3 平均值(A)UCL
A max= 1294
5.0μm
(粒/m3)
L1 1412 2118 353 1294
3169
L2 706 353 706 588
L3
L4
L5
L6
L7
L8
A max= 14708
0.5μm
(粒/m3)
L1 14826 17297 12002 14708
14708 L2 10590 16944 16591 14708
L3
L4
L5
L6
L7
L8
计算公式:UCL=M+t×SE( 说明:M=(∑Ai)/L ; )
□自净时间基准粒子浓度N 污染粒子浓度N0T N0T
N T
T= T N-T N0 说明:T N0指粒子浓度在人工发烟污染1~2min后的时间,
T N为粒子浓度恢复至基准粒子浓度时的时间。
取样位置(测点)平面示意图图示符号:A 照度测点;B风速;C 温湿度测点;一光源;
D 悬浮粒子数测点;
E 微生物数测点;
F 噪声测点;
说明:①示意图中照度测点、温湿度测点、悬浮粒子数测点距地面的高度均为0.8m;
②对于非单向流洁净室,风量测定采用风口法,送风口即为风量的测点,故不再另外标示;
③对于单向流洁净室,风速测点距高效过滤器0.15m-0.3m,测点间距不大于0.6 m。
记录人:复核人:
送风口。
第 第 共页。
洁净室参数检查表

洁净车间技术参数检查记录表
检 查 项 目
18-26℃ 45-65% N m2 Nm N m3/h N m3/h 15次/h ≥10Pa (≥0.3um)99.9% 0.45m/s≤X≤1.0m/s ≤30min (≥0.5um) ≤10,500,000 (≥5um) ≤60,000 ≤10CFU/皿 ≥300Lx ≥30W/10m2
标
准
结果
备
注
温度 相对湿度 房间面积 房间高度 送风量 回风量 换风次数 压力差 高效过滤器效率 高效过滤器风速 自净时间 尘埃粒子数(粒/m3) 沉降菌数 光照度 紫外线消毒灯功率 检查人:
检精密模具有限公司
洁净车间技术参数检查记录表
检 查 项 目
18-26℃ 45-65% N m2 Nm N m3/h N m3/h 15次/h ≥10Pa (≥0.3um)99.9% 0.45m/s≤X≤1.0m/s ≤30min (≥0.5um) ≤10,500,000 (≥5um) ≤60,000 ≤10CFU/皿 ≥300Lx ≥30W/10m2
标
准
结果
备
注
温度 相对湿度 房间面积 房间高度 送风量 回风量 换风次数 压力差 高效过滤器效率 高效过滤器风速 自净时间 尘埃粒子数(粒/m3) 沉降菌数 光照度 紫外线消毒灯功率 检查人:
检查时间:
审核人:
审核时间:
具有限公司
具有限公司
洁净度测试记录表(J8-D级)
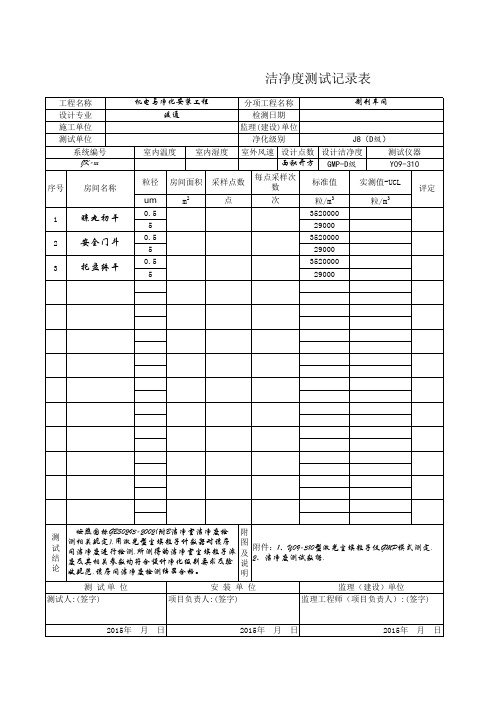
附 图 附件:1、Y09-310型激光尘埃粒子仪GMP模式测定. 及 2、洁净度测试数据. 说 明 监理(建设)单位 监理工程师(项目负责人):(签字)
测 试单 位 测试人:(签字)
安 装 单 位 项目负责人:(签字)
2015年
月
日
2015年
月
日
2015年
月
日
洁净度测试记录表
工程名称 设计专业 施工单位 测试单位 系统编号 JK-xx 序号 房间名称 机电与净化安装工程 暖通 制剂车间 分项工程名称 检测日期 监理(建设)单位 净化级别 J8(D级) 室外风速 设计点数 设计洁净度 测试仪器 面积开方 GMP-D级 Y09-310 每点采样次 数 次 标准值 粒/m 3520000 29000 3520000 29000 3520000 29000
3
室内温度
室内湿度
粒径 um
房间面积 m
2
采样点数 点
实测值-UCL 粒/m
3
评定
1 2 3
晾丸初干 安全门斗 托盘终干
0.5 论
按照国标GB50243-2002(附B洁净室洁净度检 测相关规定),用激光型尘埃粒子计数器对该房 间洁净度进行检测,所测得的洁净室尘埃粒子浓 度及其相关参数均符合设计净化级别要求及验 收规范,该房间洁净度检测结果合格。
洁净室测试记录(最新)
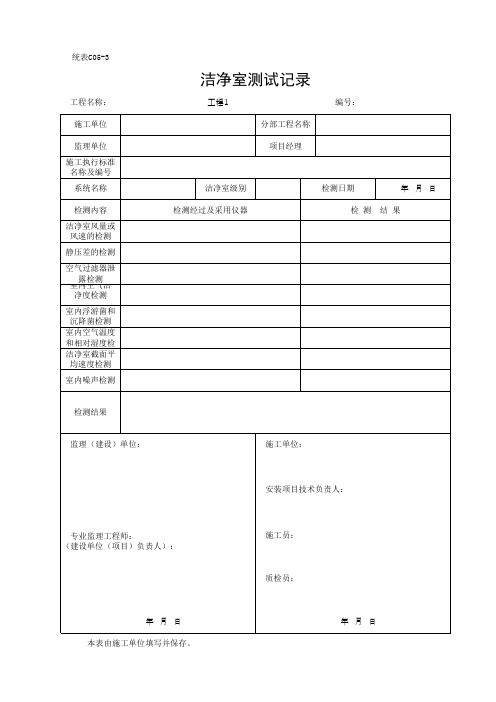
工程名称:
施工单位
监理单位 施工执行标准
名称及编号 系统名称
检测内容 洁净室风量或
风速的检测 静压差的检测 空气过滤器泄 室内露空检气测洁
净度检测 室内浮游菌和
沉降菌检测 室内空气温度 和相对湿度检 洁净室截面平
均速度检测 室内噪声检测
检测结果
监理(建设)单位:
洁净室测试记录
工程1 分部工程名称 项目经理
编号:
洁净室级别 检测经过及采用仪器
检测日期
年月日
检测 结果
施工单位:
安装项目ห้องสมุดไป่ตู้术负责人:
专业监理工程师: (建设单位(项目)负责人):
年月日 本表由施工单位填写并保存。
施工员: 质检员:
年月日
洁净室静压差测试记录

检测车间:
房间名称
设计值(Pa)
测试值(Pa)
结论
□合格□不合格
□合格□不合格
□合格□不合格
□合格□不合格
□合格□不合格
□合格□不合格
□合格□不合格
□合格□不合格
□合格□不合格
□合格□不合格
□合格□不合格
□合格□不合格
□合格□净区与非洁净区之间的压差应≥10Pa;不同洁净度级别之间的压差应≥5Pa;必要时,相同洁净度级别的不同功能区域(操作间)之间也应当保持适当的压差梯度;产尘大的操作间应保持相对的负压。
检测人:
复核人:
检测日期:
复核日期:
注:监测结果评定项在相应的□内打“√”。
实验室洁净度自检验检测报告模板

实验室洁净度自检验检测报告模板1.引言本报告是针对XXX实验室进行洁净度自检验检测的总结和分析。
实验室洁净度的检测是确保实验室环境符合卫生标准的重要措施之一,通过此次检测,旨在评估实验室洁净度的水平,并提出改进建议,以确保实验室操作的稳定性和结果的可靠性。
2.检测方法和仪器选择本次检测采用了XX方法,主要通过视觉观察和颜色比对来评估实验室的洁净度水平。
为了保证检测结果的准确性和可靠性,选用了XX品牌的洁净度检测仪器,该仪器具有高分辨率和精确度,能够提供准确的洁净度分析结果。
3.检测步骤和结果分析3.1检测点位的选择根据实验室的特点和实际情况,本次检测选择了实验室的重点区域作为检测点位,包括实验台面、试剂架、试剂柜、通风系统等。
共选择了X个检测点位进行检测。
3.2检测步骤在检测过程中,首先对每个检测点位进行视觉检查,观察是否有灰尘、污渍、杂物等。
然后,使用洁净度检测仪器进行颜色比对,将实验室的洁净度与已设定的标准进行对比。
3.3检测结果分析通过对每个检测点位进行检测和分析,得出了各个点位的洁净度分数。
根据实验室洁净度标准,分数大于等于X分表示洁净度良好,分数在X到Y之间表示洁净度一般,分数小于等于Y分表示洁净度较差。
根据本次检测的结果,实验室的洁净度总体评价为良好/一般/较差(请根据实际情况填写)。
XX个点位中,有X个点位达到或超过了良好/一般的标准,占比为X%。
X个点位洁净度较差,占比为X%。
4.结果分析和改进建议根据本次检测结果,针对洁净度较差的点位提出了改进建议,以提高实验室的洁净度水平。
具体建议如下:4.1清洁保养对于存在灰尘、污渍的点位,建议加强清洁保养,包括定期擦拭、清理和消毒等操作。
确保操作台面、试剂架等区域干净整洁。
4.2通风系统维护针对通风系统存在的问题,建议定期清理和维护,保持正常运行。
同时,监测通风系统的过滤器和换气次数,确保空气质量符合标准。
4.3实验操作规范提醒实验室工作人员加强实验操作规范,避免产生过多的污染源,例如避免在操作台上吃东西、留下垃圾等。
洁净室监测记录表
洁净室监测报告书申检单位:检测单位:监测区域:洁净车间报告日期:报告编号:监测报告书报告书编号:检测区域名称:洁净室区域面积高度洁净度级别级监测状态静态气流方式非单向气流监测依据YY0033-2000《无菌医疗器具生产质量管理规范》监测日期2012年8月26日报告日期2012年8月26日房间名称房间编号温度(℃)换气次数(次/h)沉降菌(个/皿)静压差(Pa)与非洁净区间相对湿度结果判定生产车间二更1 18.3 79.3 2.5 7.5 53%符合规定消毒缓冲间2 18.6 102 0.5 对同级别二更:3 53%符合规定清洗间 3 18.5 90 0.5 对同级别消毒缓冲间:456%符合规定洁具间 4 18.3 96 2.0 对同级别消毒缓冲间:255%符合规定操作间 5 18.5 36 1.0 对同级别消毒缓冲间:353%符合规定内包间 6 18.4 32.5 3.0 对同级别消毒缓冲间:454%符合规定实验室二更7 18.8 96 3.0 8 52%符合规定洁净走廊8 18.7 53 3.0 对同级别二更:2 53%符合规定阳性对照室9 18.8 55 1.5对同级别洁净走廊:-452%符合规定微生物限度室10 18.7 41 1.5对同级别洁净走廊:254%符合规定无菌室11 18.9 83 1.0 对同级别洁净走廊:353%符合规定结论判定:悬浮粒子均符合规定(报告另附)换气次数均符合规定沉降菌均符合规定温度均符合规定相对湿度均符合规定静压差均符合规定检测人员:XX XX授权人签字:悬浮粒子测定报告报告编号:200901测定状态静态测试日期2012年8月26日测定依据YY0033-2000《无菌医疗器具生产质量管理规范》报告日期2012年8月26日测试人XX 复核人XX 确认人XX房间名称房间编号净化级别(级)检测结果≥5um ≥0.5um判定平均值置信上限平均值置信上限生产车间二更0 52036 符合规定消毒缓冲间 2 3 8973 符合规定清洗间 3 3 0175 符合规定洁具间 4 3 8308 符合规定操作间 5 3 3688 628769 664630 符合规定内包间 6 3 10310 符合规定实验室二更7 3 7370 符合规定洁净走廊8 3 8910 符合规定阳性对照室9 3 9829 符合规定微生物限度室 1 752507 符合规定无菌室 1 0 521325 符合规定标准规定5um粒子,平均值和置信上限均<60000,0.5um粒子,平均值和置信上限均<10500000 结论上述洁净室悬浮粒子测定结果符合GMP对300000级洁净级别要求。
洁净区生产工艺卫生检查记录表
45%-65%
检查结论及处理意见
检查者: 日期:
洁净区生产工艺卫生检查记录
编号:
品名
规 格批Βιβλιοθήκη 号检查日期年 月 日
检查区域
负责人
检 查 内 容
检查项目
执行情况
结 果
符合
不符合
个人卫生
工衣穿戴
穿戴整齐,穿戴顺序符合要求。
个人清洁
头发、指甲符合要求,不化妆。
工作秩序
工作秩序符合相应的要求。
其它
其它个人卫生符合相应检查要求。
生产现场卫生
门窗
门、窗整洁、完整。
墙壁、天花、地面
不得有蜘蛛网且干净整洁。
工容器具
工容器具清洁。
生产设备
生产设备清洁且在上次清场有效期内。
物料摆放
物料摆放整齐且与生产工艺所需物料相符合。
进入物料外包装处理
堆放整齐,去除异物
非生产个人用品的控制
与生产无关的个人用品严禁进入生产区域。
其它
无其它影响产品质量因素
洁净度
压差
>5Pa
温度
18℃-28℃
洁净室布点 检测记录
测试房间
洁净级别
采点编号
检测结果
结论
男脱衣室
B级
男脱衣室
B级
女脱衣室
B级
女脱衣室
B级
洁具存放室(2楼)
B级
洁具存放室(2楼)
B级
洁具存放室(2楼)
B级
消毒液存放室(2楼)
B级
消毒液存放室(2楼)
B级
消毒液存放室(2楼)
B级
结晶离心室
B级
结晶离心室
B级
结晶离心室
B级
结晶离心室
B级
结晶离心室
B级
结晶离心室
干燥室
B级
干燥室
B级
走廊
B级
走廊
B级
走廊
B级
走廊
B级
走廊
B级
走廊
B级
0
检验者:核对者:
洁净室检测记录
车间
测试日期
培养时间
采样方法仪器
90mm平板菌落计数法
标准
A级
B级
C级
D级
测试房间
洁净级别
采点编号
检测结果
结论
走廊
B级
走廊
B级
走廊
B级
走廊
B级
楼梯间
B级
楼梯间
B级
器具存放室
B级
洁具存放室
B级
洁具存放室
B级
结晶离心室
B级
结晶离心室
B级
缓冲室(2楼)
B级
缓冲室(2楼)
B级
溶解过滤室
C级
溶解过滤室
C级
溶解过滤室
C级
溶解过滤室
C级
