异丙醇-环己烷双液系相图
2-双液系相图

3、实验步骤
1.已知浓度溶液折射率的测定 .
取异丙醇和环己烷以及环己烷摩尔 分数分别23.31%、45.85%、58.94%、 、 分数分别 、 、 74.80%四种组成的溶液,逐次用阿贝 四种组成的溶液, 四种组成的溶液 折射计测定其折射率。 折射计测定其折射率。 绘制组成一折射率的关系曲线 组成一折射率的关系曲线。 绘制组成一折射率的关系曲线。
2、基本原理
两种液态物质混合而成的二组分体系称为双液系 液体的蒸气压与外界压力相等时的温度—沸点 一定压力下,双液系的沸点与组成的T-x相图一般 有下列三种情况
完全互溶的双液系的沸点完全互溶的双液系的沸点-组成图
利用回流及分析的方法来绘制相图。 利用回流及分析的方法来绘制相图。取不同组成 的溶液在沸点仪中回流,测定其沸点及气、 的溶液在沸点仪中回流,测定其沸点及气、液相组 成。沸点数据可直接由温度计获得; 沸点数据可直接由温度计获得 数据可直接由温度计获得; 气、液相组成可通过测其折射率,然后由组成—— 折射率曲线中最后确定。 。
电阻丝不能露出液面,一定要浸没于溶液中,以 免通电红热后引起有机溶剂燃烧。电阻丝两端电 压不能过大,过大会引起有机溶剂燃烧或烧断电 阻丝。 测量过程中一定要达到气液平衡状态,即体系的 温度保持稳定,才能测定其沸点及气相冷凝液和 液相的折射率。
在测定其气相冷凝液和液相的折射率时要保持 温度一致。 使用阿贝折射仪 阿贝折射仪时,棱镜上不能接触硬物,擦 拭棱镜时需用擦镜纸等柔软的纸。 测定折射率时,动作要迅速,避免样品中易 挥发组分的损失
4. 数据记录和处理
1、绘制 ℃时的组成 、绘制25℃ 一折射率关系曲线 标准曲线) (标准曲线) 2、沸点值进行校正。假定 、沸点值进行校正。 特鲁顿( 特鲁顿(Trouton)规则适 ) 用于溶液井应用克劳修斯 一克拉贝龙方程则有
实验四异丙醇—环己烷双液系相

可编辑ppt
10
• 3.在测定其气相冷凝液和液相的折射率时 要保持温度一致。
• 4.使用阿贝折射仪时,棱镜上不能接触硬 物,擦拭棱镜时需用擦镜纸等柔软的纸。
可编辑ppt
11
阿贝折射仪的使用
1.阿贝折射仪 的构造原理
可编辑ppt
12
• 2.阿贝折射仪的使用方法 • (1)仪器安装: • (2)加样:顺单一方向轻擦镜面 (不可来回擦) • (3)调光明暗的界面恰好同十字线交叉处重合 • (4)读数 折射率 • 0~95% 糖溶液的百分数
分别测定气相冷凝液和液相的折射
率。按上述操作步骤分别测定加人
环已烷为1ml、 2ml、3ml、4ml、
5ml 、 10ml 时 各 液 体 的 沸 点 及 气 相
冷凝液和液相折射率。
可编辑ppt
6
(2)将蒸馏瓶内的溶液倒 人回收瓶中,并用环已烷 清洗蒸馏瓶。然后取25ml
环己烷注入蒸馏瓶内,按 (1)的操作步骤进行。以 后分别加人异丙醇0.2ml、 0.3ml、0.5ml、1.0ml、 4ml、5ml,测定其沸点及 气相冷凝液和液相折射率。
可编辑ppt
3
为了绘制沸点—组成图,可采取不同的方 法。比如取该体系不同组成的溶液,用化学分 析方法分析沸腾时该组成的气、液组成,从而 绘制出完整的相图。在本实验中的折射率的测 定,就是一种间接获取组成的办法。它具有简 捷、准确的特点。
本实验就是利用回流及分析的方法来绘制 相图。取不同组成的溶液在沸点仪中回流,测 定其沸点及气、液相组成。沸点数据可直接由 温度计获得;气、液相组成可通过测其折射率, 然后由组成—折射率曲线中最后确定。
实验四、 异丙醇—环己烷 双液系相图
可编辑ppt
环己烷-异丙醇双液系相图的绘制

宜宾学院 化学与化工学院
实验中心
实验目的
1 .了解物理化学实验手段中常用的物理方法— —光学方法的基本原理; 2.绘制异丙醇一环己烷双液系的气-液平衡相图, 了解相图和相律的基本概念; 3.进一步理解分馏原理; 4. 掌握测定双组分液体的沸点及正常沸点的方 法; 5.掌握阿贝折射计的原理及使用方法。
操作步骤
1.已知浓度溶液折 射率的测定(略)
取异丙醇和环己烷以 及环己烷摩尔分数分 别 23.31% 、 45.85% 、 58.94% 、 74.80% 四种 组成的溶液,逐次用 阿贝折射仪测定其折 射率。绘制组成一折 射率的关系曲线。
沸点仪结构图
2.溶液沸点及气、液相组成的测定
(1)取25mL异丙醇置于沸点测定仪之蒸馏瓶内。按图连 接好线路,打开回流冷却水,通电并调节变压器使液体加 热至沸腾,回流并观察温度计的变化,待温度恒定记下沸 腾温度。然后将调压变压器调至零处。停止加热,充分冷 却后,用吸液管分别从冷凝管上端的分馏液取样口及加液 口取样,用阿贝折射计分别测定气相冷凝液和液相的折射 率。按上述操作步骤分别测定加人环已烷为2mL、3mL、 4mL、5mL、10mL时各液体的沸点及气相冷凝液和液相折 射率。 (2)将蒸馏瓶内的溶液倒人回收瓶中,并用环已烷清洗蒸 馏瓶。然后取25mL环己烷注入蒸馏瓶内,按(1)的操作 步骤进行。以后分别加人异丙醇0.3mL、0.5mL、1.mL、 4mL、5mL,测定其沸点及气相冷凝液和液相折射率。
数据记录和处理
1、绘制环己烷-异 丙醇体系的组成一 折射率关系曲线 (工作曲线)略
1.44 1.43 1.42 1.41 1.4
1.39
1.38
异丙醇-环己烷气液平衡相图
实验七 异丙醇-环己烷气液平衡相图一、实验目的1. 了解绘制双液系相图的基本原理和方法;2. 采用回流冷凝法测定不同浓度的异丙醇-环己烷体系的沸点和气液两相平衡成分,绘制常压下环己烷-异丙醇双液系的T-x图,并找出恒沸点混合物的组成和最低恒沸点;3.学会使用阿贝折射仪。
二、实验原理 在常温下,任意两种液体混合组成的体系称为双液体系。
若两液体能按任意比例相互溶解,则称完全互溶双液体系;若只能部分互溶,则称部分互溶双液体系。
液体的沸点是指液体的蒸气压与外界大气压相等时的温度。
在一定的外压下,纯液体有确定的沸点。
而双液体系的沸点不仅与外压有关,还与双液体系的组成有关。
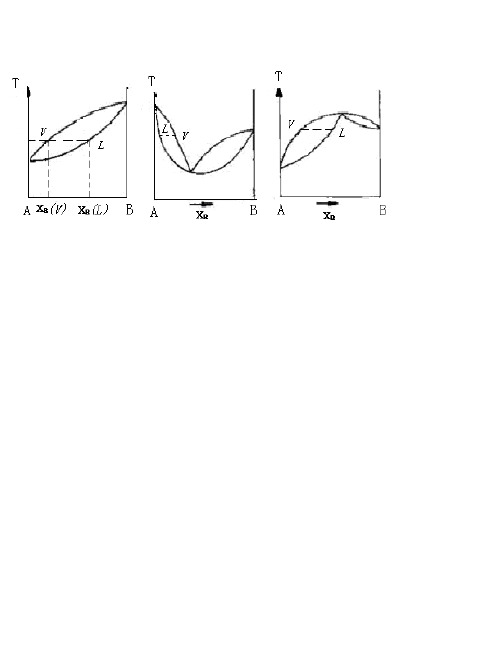
图17-1(a)是一种最简单的完全互溶双液系的T-x图(像苯与甲苯)。
图中纵轴是温度(沸点)T,横轴是液体B的摩尔分数xb (或质量百分组成),上面一条是气相线,下面一条是液相线,对应于同一沸点温度的二曲线上的两个点,就是互相成平衡的气相点和液相点,其相应的组成可从横轴上获得。
因此如果在恒压下将溶液蒸馏,测定气相馏出液和液相蒸馏液的组成就能绘出T-x图。
某些完全互溶的双液体系近似遵循拉乌尔定律,其正(或负)偏差不大,在T-x图上溶液的沸点介于A、B二纯液体的沸点之间(见图17-1(a)),如甲醇与水、二硫化碳与四氯化碳等。
大多数实际溶液由于A、B二组分的相互影响,常会与拉乌尔定律有较大偏差,在T-x图上会有最高或最低点出现,如图17-1(b)、(c)所示。
这些点称为恒沸点,其相应的溶液称为恒沸点混合物。
恒沸点混合物蒸馏时,所得的气相与液相组成不变,靠蒸馏无法改变其组成。
如HCl与水、丙酮与氯仿、硝酸与水等的体系具有最高恒沸点,苯与乙醇、异丙醇与环己烷、水与乙醇等的体系则具有最低恒沸点。
具有恒沸点的双液系与理想溶液或偏差很小的近似理想溶液的双液系的根本区别在于,体系处于恒沸点时气液两相的组成相同,因而也就不能像前者那样通过反复 蒸馏而使双液系的两个组分完全分离,因为对这样的溶液进行简单的反复蒸馏智能获得某一纯组分和组成为恒沸点的混合物。
异丙醇-环己烷双液系相图(精)

(二)粗品精制
冷却后,将混合物抽滤,固体每次用2—3ml水
洗涤两次。抽干后,在滤纸上进一步地压干。
用5ml乙醇做重结晶,得到白色晶体,熔点为
89-90℃。
称量,计算产率。
六 思考题
制备环己酮肟时,加入醋酸钠的目的是什么?
重结晶前用水洗两次,其目的是什么?
实验的反应类型是什么?弱酸在反应中如何起
到催化作用?
为什么?
(一)粗品制备
2. 反应
将醋酸钠溶液分批滴加至环己酮溶液中,加入的同时 不断振摇锥形瓶,此时有固体析出。加完后,用塞子 塞住瓶口,剧烈振摇锥形瓶10分钟,可以看到析出白 色粉状的环己酮肟结晶。
注意事项: 1) 产物在酸性中易水解,故不在较高温度下进行。
2)若反应中环己酮肟呈白色小球状,则表示还未完全反 应,应继续振摇。
沸点 155.65℃。无色可燃性液体,微溶于水, 能与醇、醚及其它有机溶剂混溶。本品是生产 聚酰胺的重要原料。 环己酮肟( cyclohexanone oxime ):分子量 113.14 ,熔点 89-90 ℃,棱柱体白色结晶。 不溶于水,溶于乙醇和乙醚,本品是有机合成
中间体。
五 实验步骤
(一)粗品制备 (二)粗品精制
(一)粗品制备
1. 取样: 分别取两个100ml烧杯制备样品溶液。
30 ml 水 7g 盐酸羟胺 7.5 ml 环己酮
20 ml 水 10 g 醋酸钠
(一)粗品制备
注意事项:
1) 加入的醋酸钠溶解慢,可研细后加入水中,或通 过加热促使其溶解。 2) 加入醋酸钠的作用: ① 使羟胺从盐的形式中游离出来。 ②调整PH值,形成CH3COONa — CH3COOH缓冲溶液,PH 约等于5。
异丙醇-环己烷气液平衡相图

实验七 异丙醇-环己烷气液平衡相图一、实验目的1. 了解绘制双液系相图的基本原理和方法;2. 采用回流冷凝法测定不同浓度的异丙醇-环己烷体系的沸点和气液两相平衡成分,绘制常压下环己烷-异丙醇双液系的T-x图,并找出恒沸点混合物的组成和最低恒沸点;3.学会使用阿贝折射仪。
二、实验原理 在常温下,任意两种液体混合组成的体系称为双液体系。
若两液体能按任意比例相互溶解,则称完全互溶双液体系;若只能部分互溶,则称部分互溶双液体系。
液体的沸点是指液体的蒸气压与外界大气压相等时的温度。
在一定的外压下,纯液体有确定的沸点。
而双液体系的沸点不仅与外压有关,还与双液体系的组成有关。
图17-1(a)是一种最简单的完全互溶双液系的T-x图(像苯与甲苯)。
图中纵轴是温度(沸点)T,横轴是液体B的摩尔分数xb (或质量百分组成),上面一条是气相线,下面一条是液相线,对应于同一沸点温度的二曲线上的两个点,就是互相成平衡的气相点和液相点,其相应的组成可从横轴上获得。
因此如果在恒压下将溶液蒸馏,测定气相馏出液和液相蒸馏液的组成就能绘出T-x图。
某些完全互溶的双液体系近似遵循拉乌尔定律,其正(或负)偏差不大,在T-x图上溶液的沸点介于A、B二纯液体的沸点之间(见图17-1(a)),如甲醇与水、二硫化碳与四氯化碳等。
大多数实际溶液由于A、B二组分的相互影响,常会与拉乌尔定律有较大偏差,在T-x图上会有最高或最低点出现,如图17-1(b)、(c)所示。
这些点称为恒沸点,其相应的溶液称为恒沸点混合物。
恒沸点混合物蒸馏时,所得的气相与液相组成不变,靠蒸馏无法改变其组成。
如HCl与水、丙酮与氯仿、硝酸与水等的体系具有最高恒沸点,苯与乙醇、异丙醇与环己烷、水与乙醇等的体系则具有最低恒沸点。
具有恒沸点的双液系与理想溶液或偏差很小的近似理想溶液的双液系的根本区别在于,体系处于恒沸点时气液两相的组成相同,因而也就不能像前者那样通过反复 蒸馏而使双液系的两个组分完全分离,因为对这样的溶液进行简单的反复蒸馏智能获得某一纯组分和组成为恒沸点的混合物。
异丙醇环己烷双液系相图

实验 异丙醇—环己烷双液系相图一、实验目的1.了解物理化学实验手段中常用的物理方法——光学方法的基本原理。
2. 绘制异丙醇-环己烷双液系的沸点-组成图,确定其恒沸物组成及恒沸温度。
3. 进一步理解分馏原理。
4. 掌握阿贝折射计的原理及使用方法。
二、实验背景根据相律绘制相图,通过相图的分析加深对所研究体系的认识,是热力学方法研究多相平衡体系的重要内容之一。
相平衡是物理化学的重要教学内容,其中气液平衡是最常见,也是讨论最多的内容之一。
各体系相图的绘制为生产和科研实践中对某些液体混合物的分离、提纯与精制、蒸馏、精馏等具有一定的指导意义。
完全互溶双液系的T-x图,按曲线的特征,体系可以分为三大类,理想体系,正偏差体系和负偏差体系。
其中,当偏差足够大时,会出现极大点和极小点,分别对应最大负偏差和最大正偏差,对应的极值点称为恒沸点,所对应的溶液称为恒沸混合物。
考虑综合因素,一般实验都选择具有最低恒沸点的异丙醇—环己烷或乙醇—环己烷体系,本实验选异丙醇—环己烷体系。
根据相平衡原理,对二组分体系,当压力恒定时,当气液两相平衡时,体系的自由度为1。
当体系的温度确定时,气液两相的组成也确定。
反过来,当气液两相的组成确定时,体系的平衡温度也确定。
沸点仪就是根据这个原理设计的。
本实验中气液相的组成通过测定对应样品的折射率来确定,因而两组分的折射率相差越大越好,同时为了避免组分因挥发而造成测量误差,还要求两组分的饱和蒸汽压相差越小越好。
目前实验教学中最常用的沸点仪如图8-2所示,结构简单,容易操作,但达到平衡时间较长。
另外一类型测定装置叫平衡釜,有陆志虞平衡釜、爱立斯平衡釜、罗斯平衡釜等,平衡釜结构比较复杂。
还有一种多功能沸点测定仪,具有沸点测定仪和平衡釜的双重功能,测定范围较广,除常规的气液平衡数据的测定外,还可用于含盐体系和部分互溶体系气液平衡的测定。
三、实验原理在常温下,任意两种液体混合组成的体系称为双液体系。
若两液体能按任意比例相互溶解,则称完全互溶双液体系;若只能部分互溶,则称部分互溶双液体系。
异丙醇环己烷双液系相图实验报告

异丙醇环己烷双液系相图实验报告实验目的:本实验旨在通过观察和分析异丙醇和环己烷双液系的相图,探究其相互溶解性和相变规律,为相关领域的研究提供实验数据和理论依据。
实验原理:相图是描述不同组分混合物在不同温度和压力下的相态变化规律的图表。
在本实验中,我们将异丙醇和环己烷两种液体混合,通过改变温度和浓度来观察它们的相变行为。
实验步骤:1. 准备实验所需的异丙醇和环己烷两种液体,保证其纯度和浓度。
2. 在实验室设备中,将异丙醇和环己烷按照一定比例混合,制备不同浓度的双液溶液。
3. 将制备好的双液溶液倒入实验容器中,并记录初始温度。
4. 缓慢升温,同时观察双液溶液的相变情况。
在每个温度点停留一段时间,直到相变达到平衡。
5. 记录每个温度下的相变情况,包括溶液的浑浊度、透明度、颜色等。
实验结果:通过实验观察和记录,我们得到了异丙醇和环己烷双液系的相图。
在低温下,异丙醇和环己烷两种液体是不相溶的,形成两个分散相;随着温度的升高,两种液体逐渐相互溶解,形成透明的单相溶液。
在一定温度范围内,双液溶液呈现出不同的浑浊度和颜色变化,这是由于溶液中两种液体的浓度变化引起的。
讨论与分析:通过对异丙醇和环己烷双液系相图的实验观察和分析,我们可以得到一些结论和启示。
首先,相图的形状和特征可以反映出两种液体的相互作用力和溶解性。
在本实验中,由于异丙醇和环己烷的化学性质和分子结构不同,它们之间的相互作用力较弱,因此在低温下不相溶。
随着温度的升高,两种液体的相互作用力增强,使得它们能够相互溶解。
其次,相图可以帮助我们确定混合物的最佳配比和工艺条件。
在实际应用中,我们常常需要将不同组分的液体混合,以获得特定性质和功能的溶液。
通过研究相图,我们可以确定最佳的配比和工艺条件,以提高产品的质量和效率。
最后,相图还可以为相关领域的研究提供理论依据和实验数据。
在化学工程、材料科学等领域,相图是研究和设计新材料、新工艺的重要工具。
通过实验观察和分析相图,我们可以了解混合物的相变规律和性质变化,为相关领域的研究提供理论指导和实验数据支持。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
渤海大学学生实验报告
课程名称:任课教师:
实验室名称:物理化学实验室(二)房间号实验时间: 2013 年月日
学院化学化工与食品安全学院专业班级
姓名学号同组人
实验项目异丙醇-环己烷双液系相图组别实验成绩
一、实验目的
1、了解物理化学实验中常用的物理方法-光学方法的基本原理
2、绘制异丙醇-环己烷双液系的沸点-组成图,确定其沸点组成及衡沸温度
3、进一步理解分馏原理
4、掌握阿贝折射计的原理及使用方法
二、实验原理
在常温下两种液态以任意比例相互溶解所组成的体系称之为完全互溶双液系。
在恒定压力下,表示溶液沸点与组成关系的图称之为沸点-组成图。
本实验利用回流及分析的方法来绘制相图。
取不同组成的溶液在沸点仪中回流,测定其沸点及其气液组成。
沸点数据可由温度计获得,气-液相组成可通过测其折射率,然后由组成-折射率曲线中最后确定。
三、仪器与试剂
沸点测定仪阿贝折射仪吸液管调压变压器温度计
移液管(1ml 10ml 25ml) 异丙醇环己烷
四、实验装置
渤海大学实验报告用纸(第页共页)
五、实验步骤
1.已知浓度溶液折射率的测定
取异丙醇和环己烷以及环己烷摩尔分数分别为0.2、0.4、0.6、0.8四种组成的溶液在25℃下,逐次用阿贝折射计测定其折射率,绘制组成-折射率的关系曲线;2,溶液沸点及气液组成的测定
(1)取25ml异丙醇于沸点测定仪之蒸馏瓶内,连好路线,打开回流冷却水,接通电源加热至沸腾。
待温度恒定后,记下温度将调压变压器调至零处,停止加热充分冷却后取样,用阿贝折射计分别测定气相和液相冷凝液的折射率,按上述步骤分别测各液体的沸点及气相冷凝液和液相折射率;
(2)将蒸馏瓶内的溶液倒入回馏瓶中,并用环己烷清洗蒸馏瓶,然后取25ml环己烷于蒸馏瓶内,按(1)的操作步骤进行,以后分别加入异丙醇
0.2ml,0.3ml,0.5ml,1ml,4ml,5ml,测定其沸点及气相冷凝液和液相折射
率。
六、数据记录和处理
大气压:大气压:101.56kpa; 压力校正因素:溶液沸点与大气压有关
沸点校正:△t=t/10 *(101.325-p)/101.325 t
b
=t+△t
编号
项目
1 2 3 4 5 6 7 8
t0c 66.4 64.6 63.9 64.1 64.3 64.6 65.7 71.6
气相n
y
1 1.4029 1.4027 1.401
2 1.4005 1.3995 1.3988 1.3962 1.3842
2 1.4027 1.4028 1.4010 1.4007 1.3994 1.3987 1.3964 1.3843
平均 1.4028 1.4027.5 1.4011 1.4006 1.39945 1.39875 1.3963 1.38425
x
g
41.4 42.2 45.0 45.8 47.9 49.6 61.4 69.0
液相
n
x
1 1.421
2 1.4191 1.4119 1.4106 1.3891 1.3831 1.3751 1.3637
2 1.4211 1.4190 1.4120 1.4108 1.3890 1.3832 1.3750 1.3635
平均 1.42115 1.41905 1.41195 1.4007 1.38905 1.38315 1.37505 1.3636
x
l
5.8 10.0 25.0 4
6.1 63.8 70.4 80.0 94.8 △t -0.0154 -0.0150 -0.0148 -0.0149 -0.0149 -0.0150 -0.0152 -0.0166
t
b
66.3846 64.585 63.8852 64.0851 64.2851 64.585 65.6848 71.5834
恒沸温度校正前63.95 后63.94 恒沸组成x
g = x
l
=45.7
渤海大学实验报告用纸(第页共页)
七结果讨论与分析
1.产生误差的原因:a.温度计的水银球应一半在液体中,一半在气相中,以确保气液达平衡,否则将影响实验结果。
b.滴管一定要用吹风机吹干,否则由于滴管上的残留液,而影响气相或液相的组成。
c.恒温槽中的水的温度应始终保持恒定,否则将影响气相或液相的折光率,从而影响气相或液相的组成。
d.气相或液相的折光率的测定准确与否,将直接影响实验结果。
七、思考题
1、折射率的测定为什么要在恒温下进行?
答:因为折射率与温度有关,所以测量时要在两棱镜的周围夹套内通入恒温水,保持恒温;
2、操作步骤中,在加入不同数量的各组分时,如发生了微小的偏差,对相图的绘制有无影响?为什么?
答:加入各组分时,如发生了微小的偏差,对相图的绘制五影响,因为最终液体的组成是通过对折光率的测定在工作曲线上得出,所以无影响;
3、对应某一组成测定沸点及气相冷凝液和液相折射率,如因某种原因缺少其中某一个数据,
应如何处理?它对相图的绘制有无影响?
答:沸点的数据不可以少,其他可以少,对于缺少的数据,可由它们的趋势找出其他点。
教师评语:
渤海大学实验报告用纸(第页共页)。
