中学计算常用:相对原子质量表(取整数)--免积分下载
中学计算常用:相对原子质量表(取整数)--免积分
62硫酸和碳酸钠反应:Na2CO3+H2SO4==Na2SO4+H2O+CO2↑
63硫酸和氯化钡溶液反应:H2SO4+BaCl2==BaSO4↓+2HCl
(7)碱+盐==另一种碱+另一种盐
64氢氧化钠与硫酸铜:2NaOH+CuSO4==Cu(OH)2↓+Na2SO4
74三氧化硫溶于水:SO3+H2O==H2SO4
75硫酸铜晶体受热分解:CuSO4·5H2O CuSO4+5H2O
76无水硫酸铜作于干燥剂:CuSO4+5H2O==CuSO4·5H2O
38氧化铜和稀盐酸反应:CuO+2HCl==CuCl2+H2O
39氧化铜和稀硫酸反应:CuO+H2SO4==CuSO4+H2O
40氧化镁和稀硫酸反应:MgO+H2SO4==MgSO4+H2O
41氧化钙和稀盐酸反应:CaO+2HCl==CaCl2+H2O
(4)酸性氧化物+碱==盐+水
42苛性钠暴露在空气中变质:2NaOH+CO2==Na2CO3+H2O
34锌和硫酸铜溶液反应:Zn+CuSO4==ZnSO4+Cu
35铜和硝酸汞溶液反应:Cu+Hg(NO3)2==Cu(NO3)2+Hg
(3)碱性氧化物+酸==盐+水
36氧化铁和稀盐酸反应:Fe2O3+6HCl==2FeCl3+3H2O
37氧化铁和稀硫酸反应:Fe2O3+3H2SO4==Fe2SO4+3H2O
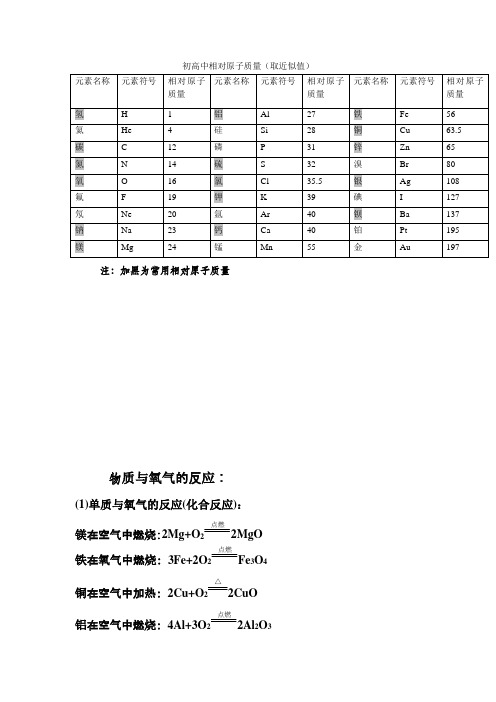
初中化学常用相对原子质量

初中化学常用相对原子质量嘿,朋友们,今天咱们聊聊初中化学里那些常用的相对原子质量。
别看这个话题好像有点儿高大上,其实没那么复杂,咱们轻松聊,绝对不让你打瞌睡。
你知道吗,相对原子质量就像是每个元素的“身份证”,它告诉我们这个元素有多重。
想想看,就像在学校里,大家的体重差异,各种身材各显神通,化学元素也是这样,千奇百怪,各有千秋。
举个例子,碳元素的相对原子质量是12。
这数字听起来简单,但其实它可了不得。
碳可是生命的基石,几乎所有的有机化合物里都有它的身影。
想想你身边的食物、植物,嘿,没错,都是因为碳在作怪。
还有氧元素,相对原子质量是16,这玩意儿可是让我们活着的关键,呼吸离不开它啊。
每次深呼吸,都是在和氧气做朋友。
水里那两个氢和一个氧,水的相对原子质量组合起来也得出奇的轻,形成我们生活中必不可少的水。
再说说氮,相对原子质量是14,听起来可能不如碳和氧那么闪亮,但氮的存在可真是无处不在。
空气里就占了大头,虽然它自己不太爱跟别的元素搭伙,但它在植物生长中可是个大功臣。
没有氮,植物可就“瘦骨嶙峋”了,像极了个儿不大的小孩,缺了营养,看着都可怜。
聊到这里,铁元素就不能不提了,相对原子质量是56,嘿,铁可是一位“壮汉”,在建筑和制造中可是不可或缺的主角。
想象一下,如果没有铁,咱们的生活该多无趣。
每当看到高楼大厦,桥梁,都是铁的功劳。
铁不光硬朗,还是我们的“血红蛋白”的重要成分,帮助我们运送氧气,真是个多才多艺的家伙。
说到这里,有必要提到一下铜,相对原子质量是63.5,铜在生活中也有不少妙用。
它在电缆里当“传送员”,给我们的家里带来电力。
咱们的电器、手机,离了铜可就麻烦大了。
而且铜还对咱们的身体有好处,虽然不多,但也是“点滴之恩”。
你可能会问,为什么相对原子质量会有小数点,比如铜的63.5呢?这和自然界里元素的同位素有关。
简单来说,就是这些元素可以有不同的“兄弟姐妹”,每种同位素的相对原子质量不一样,算出来就是小数了。
元素相对原子质量表

原子序数元素名称元素符号相对原子质量1 氢 H 1.007 94(7)2 氦 He 4。
002 602(2)3 锂 Li 6。
941(2)4 铍 Be 9.012 182(3)5 硼 B 10。
811(7)6 碳 C 12。
017(8)7 氮 N 14。
006 7(2)8 氧 O 15.999 4(3)9 氟 F 18.998 403 2(5)10 氖 Ne 20.179 7(6)11 钠 Na 22.989 769 28(2)12 镁 Mg 24。
305 0(6)13 铝 Al 26.981 538 6(8)14 硅 Si 28.085 5(3)15 磷 P 30.973 762(2)16 硫 S 32.065(5)17 氯 Cl 35.453(2)18 氩 Ar 39。
948(1)19 钾 K 39。
098 3(1)20 钙 Ca 40。
078(4)21 钪 Sc 44。
955 912(6)22 钛 Ti 47。
867(1)23 钒 V 50.941 5(1)24 铬 Cr 51.996 1(6)25 锰 Mn 54.938 045(5)26 铁 Fe 55。
845(2)27 钴 Co 58.933 195(5)28 镍 Ni 58.693 4(2)29 铜 Cu 63。
546(3)30 锌 Zn 65.409(4)31 镓 Ga 69。
723(1)32 锗 Ge 72.64(1)33 砷 As 74.921 60(2)34 硒 Se 78。
96(3)35 溴 Br 79。
904(1)36 氪 Kr 83。
798(2)37 铷 Rb 85.467 8(3)38 锶 Sr 87.62(1)39 钇 Y 88.905 85(2)40 锆 Zr 91。
224(2)41 铌 Nb 92.906 38(2)42 钼 Mo 95.94(2)43 锝 Tc [97。
9072]44 钌 Ru 101.07(2)45 铑 Rh 102。
元素相对原子质量表

原子序数元素名称元素符号相对原子质量1 氢 H 1.007 94(7)2 氦 He 4.002 602(2)3 锂 Li 6.941(2)4 铍 Be 9.012 182(3)5 硼 B 10.811(7)6 碳 C 12.017(8)7 氮 N 14.006 7(2)8 氧 O 15.999 4(3)9 氟 F 18.998 403 2(5)10 氖 Ne 20.179 7(6)11 钠 Na 22.989 769 28(2)12 镁 Mg 24.305 0(6)13 铝 Al 26.981 538 6(8)14 硅 Si 28.085 5(3)15 磷 P 30.973 762(2)16 硫 S 32.065(5)17 氯 Cl 35.453(2)18 氩 Ar 39.948(1)19 钾 K 39.098 3(1)20 钙 Ca 40.078(4)21 钪 Sc 44.955 912(6)22 钛 Ti 47.867(1)23 钒 V 50.941 5(1)24 铬 Cr 51.996 1(6)25 锰 Mn 54.938 045(5)26 铁 Fe 55.845(2)27 钴 Co 58.933 195(5)28 镍 Ni 58.693 4(2)29 铜 Cu 63.546(3)30 锌 Zn 65.409(4)31 镓 Ga 69.723(1)32 锗 Ge 72.64(1)33 砷 As 74.921 60(2)34 硒 Se 78.96(3)35 溴 Br 79.904(1)36 氪 Kr 83.798(2)37 铷 Rb 85.467 8(3)38 锶 Sr 87.62(1)39 钇 Y 88.905 85(2)40 锆 Zr 91.224(2)41 铌 Nb 92.906 38(2)42 钼 Mo 95.94(2)43 锝 Tc [97.9072]44 钌 Ru 101.07(2)45 铑 Rh 102.905 50(2)46 钯 Pd 106.42(1)47 银 Ag 107.868 2(2)48 镉 Cd 112.411(8)49 铟 In 114.818(3)50 锡 Sn 118.710(7)51 锑 Sb 121.760(1)52 碲 Te 127.60(3)53 碘 I 126.904 47(3)54 氙 Xe 131.293(6)55 铯 Cs 132.905 451 9(2)56 钡 Ba 137.327(7)编辑本段——(57-71La-Lu 镧系)——原子序数元素名称元素符号相对原子质量57 镧 La 138.905 47(7)58 铈 Ce 140.116(1)59 镨 Pr 140.907 65(2)60 钕 Nd 144.242(3)61 钷 Pm [145]62 钐 Sm 150.36(2)63 铕 Eu 151.964(1)64 钆 Gd 157.25(3)65 铽 Tb 158.925 35(2)66 镝 Dy 162.500(1)67 钬 Ho 164.930 32(2)68 铒 Er 167.259(3)69 铥 Tm 168.934 21(2)70 镱 Yb 173.04(3)71 镥 Lu 174.967(1)编辑本段——(72-88 Hf-Re)——原子序数元素名称元素符号相对原子质量72 铪 Hf 178.49(2)73 钽 Ta 180.947 88(2)74 钨 W 183.84(1)75 铼 Re 186.207(1)76 锇 Os 190.23(3)77 铱 Ir 192.217(3)78 铂 Pt 195.084(9)79 金 Au 196.966 569(4)80 汞 Hg 200.59(2)81 铊 Tl 204.383 3(2)82 铅 Pb 207.2(1)83 铋 Bi 208.980 40(1)84 钋 Po [208.982 4]85 砹 At [209.987 1]86 氡 Rn [222.017 6]87 钫 Fr [223]88 镭 Re [226]编辑本段——(89-103 Ac-Lr 锕系)——原子序数元素名称元素符号相对原子质量89 锕 Ac [227]90 钍 Th 232.038 06(2)91 镤 Pa 231.035 88(2)92 铀 U 238.028 91(3)93 镎 Np [237]94 钚 Pu [244]95 镅 Am [243]96 锔 Cm [247]97 锫 Bk [247]98 锎 Cf [251]99 锿 Es [252]100 镄 Fm [257]101 钔 Md [258]102 锘 No [259]103 铹 Lr [262]编辑本段——(104-111 Rf-Rg)——原子序数元素名称元素符号相对原子质量104 钅卢 Rf [261]105 钅杜 Db [262]106 钅喜 Sg [266]107 钅波 Bh [264]108 钅黑 Hs [277]109 钅麦 Mt [268]110 钅达 Ds [271]111 錀 Rg [272]编辑本段——不确定——原子序数元素名称元素符号相对原子质量112 暂无 Uub [285]113 暂无 Uut [284]114 暂无 Uuq [289]115 暂无 Uup [288]116 暂无 Uuh [292]117 暂无 Uus [291]118 暂无 Uuo [293]可以在简单计算题中直接带数使用答案补充很简单的四舍五入么。
初三相对原子质量表

初三相对原子质量表是物理学家们制定的一种表,用于表示物质中原子的质量。
这个
表在化学和物理研究中有着重要的作用。
表中收录了一系列各种元素的相对原子质量,它们有助于了解元素内部的结构和物质的性质,对于研究物质的组成和性质也有很大的帮助。
初三相对原子质量表的基本原理是,以氢原子的质量为1,其他元素的原子质量按其
与氢原子的比例计算。
例如,氦原子的质量为4.0026,而铀原子的质量则为238.0289。
这些数字表明氦原子的质量是氢原子质量的4倍,而铀原子的质量是氢原子质量的238
倍。
初三相对原子质量表不仅仅可以用于研究元素内部的结构,而且可以用于计算物质中
原子的质量比例,用于分析物质的物理性质和化学性质,从而有助于深入研究物质的结构
和性质。
此外,初三相对原子质量表还有助于研究元素的放射性行为,以及其他各种化合
物的组成和特性。
总而言之,初三相对原子质量表是物理学家们研究物质结构和性质的重要工具,它在
理解物质结构和性质方面有着重要的作用,并可用于研究元素放射性和各种化合物的组成
和特性。
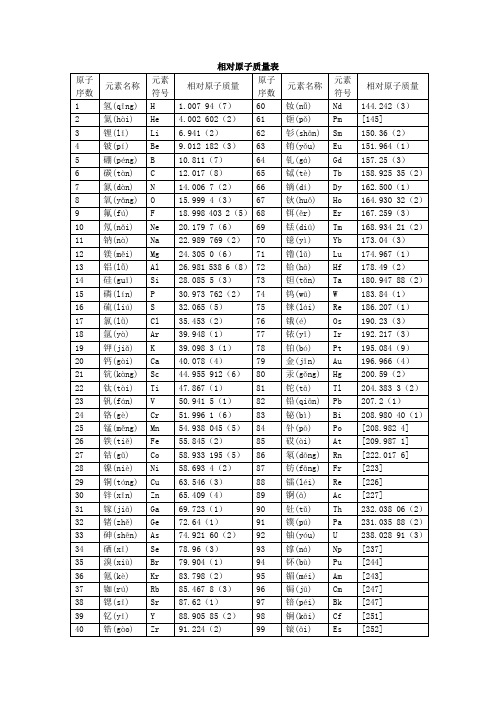
相对原子质量表
Uup
[288]
57
镧(lán)
La
138.905 47(7)
116
Uuh
[292]
58
铈(shì)
Ce
140.116(1)
117
Uus
[291]
59
镨(pǔ)
Pr
140.907 65(2)
118
Uuo
[293]
4
铍(pí)
Be
9.012 182(3)
63
铕(yǒu)
Eu
151.964(1)
5
硼(péng)
B
10.811(7)
64
钆(gá)
Gd
157.25(3)
6
碳(tàn)
C
12.017(8)
65
铽(tè)
Tb
158.925 35(2)
7
氮(dàn)
Nபைடு நூலகம்
14.006 7(2)
66
镝(dí)
Dy
162.500(1)
23
钒(fán)
V
50.941 5(1)
82
铅(qiān)
Pb
207.2(1)
24
铬(gè)
Cr
51.996 1(6)
83
铋(bì)
Bi
208.980 40(1)
25
锰(měng)
Mn
54.938 045(5)
84
钋(pō)
Po
[208.982 4]
26
铁(tiě)
Fe
55.845(2)
85
砹(ài)
相对原子质量表
原子序数
中学计算常用:相对原子质量表(取整数)--免积分下载

初高中相对原子质量(取近似值)注:加黑为常用相对原子质量物质与氧气的反应:(1)单质与氧气的反应(化合反应):镁在空气中燃烧:2Mg+O2点燃2MgO铁在氧气中燃烧:3Fe+2O2点燃Fe3O4铜在空气中加热:2Cu+O2△2CuO铝在空气中燃烧:4Al+3O2点燃2Al2O3氢气在空气中燃烧:2H2+O2点燃2H2O红磷在空气中燃烧:4P+5O2点燃2P2O5硫粉在空气中燃烧:S+O2点燃SO2碳在空气中燃烧:C+O2点燃CO2碳在空气中不充分燃烧:2C+O2点燃2CO(2)化合物与氧气的反应:一氧化碳在氧气中燃烧:2CO+O2点燃2CO2(化合反应)甲烷在空气中燃烧:CH4+2O2点燃CO2+2H2O酒精在空气中燃烧:C2H5OH+3O2点燃2CO2+3H2O二.几个分解反应:水在直流电的作用下分解:2H2O 通电2H2↑+O2↑加热高锰酸钾:2KMnO4△K2MnO4+MnO2+O2↑碳酸不稳定分解:H2CO3==H2O+CO2↑加热氧化汞:2HgO △2↑分解过氧化氢制取氧气:2H2O2 2H2O+O2↑高温煅烧石灰石:CaCO3高温CaO+CO2↑三.几个氧化还原反应:氢气还原氧化铜:H2+CuO △Cu+H2O木炭还原氧化铜:C+2CuO 高温2Cu+CO2↑焦炭还原氧化铁:3C+2Fe2O3高温4Fe+3CO2↑一氧化碳还原氧化铜:CO+CuO△一氧化碳还原氧化铁:3CO+Fe2O3高温2Fe+3CO2四.单质氧化物酸碱盐的相互关系:(1)金属单质+酸==盐+氢气(置换反应)锌和稀硫酸反应:Zn+H2SO4==ZnSO4+H2↑铁和稀硫酸反应:Fe+H2SO4==FeSO4+H2↑27镁和稀硫酸反应:Mg+H2SO4==MgSO4+H2↑28铝和稀硫酸反应:2Al+3H2SO4==Al2(SO4)3+3H2↑29锌和稀盐酸反应:Zn+2HCl==ZnCl2+H2↑30铁和稀盐酸反应:Fe+2HCl==FeCl2+H2↑31镁和稀盐酸反应:Mg+2HCl==MgCl2+H2↑32铝和稀盐酸反应:2Al+6HCl==2AlCl3+3H2↑(2)金属单质+盐(溶液)==另一种金属+另一种盐33铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu34锌和硫酸铜溶液反应:Zn+CuSO4==ZnSO4+Cu35铜和硝酸汞溶液反应:Cu+Hg(NO3)2==Cu(NO3)2+Hg (3)碱性氧化物+酸==盐+水36氧化铁和稀盐酸反应:Fe2O3+6HCl==2FeCl3+3H2O 37氧化铁和稀硫酸反应:Fe2O3+3H2SO4==Fe2SO4+3H2O 38氧化铜和稀盐酸反应:CuO+2HCl==CuCl2+H2O39氧化铜和稀硫酸反应:CuO+H2SO4==CuSO4+H2O40氧化镁和稀硫酸反应:MgO+H2SO4==MgSO4+H2O41氧化钙和稀盐酸反应:CaO+2HCl==CaCl2+H2O(4)酸性氧化物+碱==盐+水42苛性钠暴露在空气中变质:2NaOH+CO2==Na2CO3+H2O43苛性钠吸收二氧化硫气体:2NaOH+SO2==Na2SO3+H2O44苛性钠吸收三氧化硫气体:2NaOH+SO3==Na2SO4+H2O45消石灰放在空气中变质:Ca(OH)2+CO2==CaCO3↓+H2O46消石灰吸收二氧化硫:Ca(OH)2+SO2==CaSO3↓+H2O(5)酸+碱==盐+水47盐酸和烧碱起反应:HCl+NaOH==NaCl+H2O48盐酸和氢氧化钾反应:HCl+KOH==KCl+H2O49盐酸和氢氧化铜反应:2HCl+Cu(OH)2==CuCl2+2H2O50盐酸和氢氧化钙反应:2HCl+Ca(OH)2==CaCl2+2H2O51盐酸和氢氧化铁反应:3HCl+Fe(OH)3==FeCl3+3H2O52氢氧化铝药物治疗胃酸过多:3HCl+Al(OH)3==AlCl3+3H2O 53硫酸和烧碱反应:H2SO4+2NaOH==Na2SO4+2H2O54硫酸和氢氧化钾反应:H2SO4+2KOH==K2SO4+2H2O55硫酸和氢氧化铜反应:H2SO4+Cu(OH)2==CuSO4+2H2O56硫酸和氢氧化铁反应:3H2SO4+2Fe(OH)3==Fe2(SO4)3+6H2O 57硝酸和烧碱反应:HNO3+NaOH==NaNO3+H2O(6)酸+盐==另一种酸+另一种盐58大理石与稀盐酸反应:CaCO3+2HCl==CaCl2+H2O+CO2↑59碳酸钠与稀盐酸反应:Na2CO3+2HCl==2NaCl+H2O+CO2↑60碳酸镁与稀盐酸反应:MgCO3+2HCl==MgCl2+H2O+CO2↑61盐酸和硝酸银溶液反应:HCl+AgNO3==AgCl↓+HNO362硫酸和碳酸钠反应:Na2CO3+H2SO4==Na2SO4+H2O+CO2↑63硫酸和氯化钡溶液反应:H2SO4+BaCl2==BaSO4↓+2HCl (7)碱+盐==另一种碱+另一种盐64氢氧化钠与硫酸铜:2NaOH+CuSO4==Cu(OH)2↓+Na2SO4 65氢氧化钠与氯化铁:3NaOH+FeCl3==Fe(OH)3↓+3NaCl 66氢氧化钠与氯化镁:2NaOH+MgCl2==Mg(OH)2↓+2NaCl 67氢氧化钠与氯化铜:2NaOH+CuCl2==Cu(OH)2↓+2NaCl 68氢氧化钙与碳酸钠:Ca(OH)2+Na2CO3==CaCO3↓+2NaOH (8)盐+盐==两种新盐79氯化纳溶液和硝酸银溶液:NaCl+AgNO3==AgCl↓+NaNO3 70硫酸钠和氯化钡:Na2SO4+BaCl2==BaSO4↓+2NaCl 五.其它反应:71二氧化碳溶解于水:CO2+H2O==H2CO372生石灰溶于水:CaO+H2O==Ca(OH)273氧化钠溶于水:Na2O+H2O==2NaOH74三氧化硫溶于水:SO3+H2O==H2SO475硫酸铜晶体受热分解:CuSO4·5H2O △4+5H2O76无水硫酸铜作于干燥剂:CuSO4+5H2O==CuSO4·5H2O。
相对原子质量表

氖(nǎi)
Ne
20.179 7(6)
69
铥(diū)
Tm
168.934 21(2)
11
钠(nà)
Na
22.989 769(2)
70
镱(yì)
Yb
173.04(3)
12
镁(měi)
Mg
24.305 0(6)
71
镥(lǔ)
Lu
174.967(1)
13
铝(lǚ)
Al
26.981 538 6(8)
72
33
砷(shēn)
As
74.921 60(2)
92
铀(yóu)
U
238.028 91(3)
34
硒(xī)
Se
78.96(3)
93
镎(ná)
Np
[237]
35
溴(xiù)
Br
79.904(1)
94
钚(bù)
Pu
[244]
36
氪(kè)
Kr
83.798(2)
95
镅(méi)
Am
[243]
37
铷(rú)
Rb
113
Uut
[284]
55
铯(sè)
Cs
132.905 451(2)
114
Uuq
[289]
56
钡(bèi)
Ba
137.327(7)
115
Uup
[288]
57
镧(lán)
La
138.905 47(7)
116
Uuh
[292]
58
铈(shì)
Ce
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初高中相对原子质量(取近似值)注:加黑为常用相对原子质量
物质与氧气的反应:
(1)单质与氧气的反应(化合反应):
镁在空气中燃烧:2Mg+O2点燃
2MgO
铁在氧气中燃烧:3Fe+2O2点燃
Fe3O4
铜在空气中加热:2Cu+O2△
2CuO
铝在空气中燃烧:4Al+3O2点燃
2Al2O3
氢气在空气中燃烧:2H2+O2点燃
2H2O
红磷在空气中燃烧:4P+5O2点燃
2P2O5
硫粉在空气中燃烧:S+O
2点燃
SO2
碳在空气中燃烧:C+O2点燃
CO2
碳在空气中不充分燃烧:2C+O2点燃
2CO
(2)化合物与氧气的反应:
一氧化碳在氧气中燃烧:2CO+O
2点燃
2CO2(化合反应)
甲烷在空气中燃烧:CH
4+2O2
点燃
CO2+2H2O
酒精在空气中燃烧:C
2H5OH+3O2
点燃
2CO2+3H2O
二.几个分解反应:
水在直流电的作用下分解:2H
2O
通电
2H2↑+O2↑
加热高锰酸钾:2KMnO
4△
K2MnO4+MnO2+O2↑
碳酸不稳定分解:H2CO3==H2O+CO2↑
加热氧化汞:2HgO△2Hg+O
2
↑
分解过氧化氢制取氧气:2H
2
O22H2O+O2↑
高温煅烧石灰石:CaCO
3高温
CaO+CO2↑
三.几个氧化还原反应:
氢气还原氧化铜:H2+CuO △
Cu+H2O
木炭还原氧化铜:C+2CuO高温2Cu+CO
2
↑
焦炭还原氧化铁:3C+2Fe
2O3
高温
4Fe+3CO2↑
一氧化碳还原氧化铜:CO+CuO△
一氧化碳还原氧化铁:3CO+Fe
2O3
高温
2Fe+3CO2
四.单质氧化物酸碱盐的相互关系:
(1)金属单质+酸==盐+氢气(置换反应)
锌和稀硫酸反应:Zn+H2SO4==ZnSO4+H2↑
铁和稀硫酸反应:Fe+H2SO4==FeSO4+H2↑
27镁和稀硫酸反应:Mg+H2SO4==MgSO4+H2↑
28铝和稀硫酸反应:2Al+3H2SO4==Al2(SO4)3+3H2↑
29锌和稀盐酸反应:Zn+2HCl==ZnCl2+H2↑
30铁和稀盐酸反应:Fe+2HCl==FeCl2+H2↑
31镁和稀盐酸反应:Mg+2HCl==MgCl2+H2↑
32铝和稀盐酸反应:2Al+6HCl==2AlCl3+3H2↑
(2)金属单质+盐(溶液)==另一种金属+另一种盐
33铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu
34锌和硫酸铜溶液反应:Zn+CuSO4==ZnSO4+Cu
35铜和硝酸汞溶液反应:Cu+Hg(NO3)2==Cu(NO3)2+Hg (3)碱性氧化物+酸==盐+水
36氧化铁和稀盐酸反应:Fe2O3+6HCl==2FeCl3+3H2O 37氧化铁和稀硫酸反应:Fe2O3+3H2SO4==Fe2SO4+3H2O 38氧化铜和稀盐酸反应:CuO+2HCl==CuCl2+H2O
39氧化铜和稀硫酸反应:CuO+H2SO4==CuSO4+H2O
40氧化镁和稀硫酸反应:MgO+H2SO4==MgSO4+H2O
41氧化钙和稀盐酸反应:CaO+2HCl==CaCl2+H2O
(4)酸性氧化物+碱==盐+水
42苛性钠暴露在空气中变质:2NaOH+CO2==Na2CO3+H2O 43苛性钠吸收二氧化硫气体:2NaOH+SO2==Na2SO3+H2O
44苛性钠吸收三氧化硫气体:2NaOH+SO3==Na2SO4+H2O
45消石灰放在空气中变质:Ca(OH)2+CO2==CaCO3↓+H2O 46消石灰吸收二氧化硫:Ca(OH)2+SO2==CaSO3↓+H2O (5)酸+碱==盐+水
47盐酸和烧碱起反应:HCl+NaOH==NaCl+H2O
48盐酸和氢氧化钾反应:HCl+KOH==KCl+H2O
49盐酸和氢氧化铜反应:2HCl+Cu(OH)2==CuCl2+2H2O
50盐酸和氢氧化钙反应:2HCl+Ca(OH)2==CaCl2+2H2O
51盐酸和氢氧化铁反应:3HCl+Fe(OH)3==FeCl3+3H2O
52氢氧化铝药物治疗胃酸过多:3HCl+Al(OH)3==AlCl3+3H2O 53硫酸和烧碱反应:H2SO4+2NaOH==Na2SO4+2H2O
54硫酸和氢氧化钾反应:H2SO4+2KOH==K2SO4+2H2O
55硫酸和氢氧化铜反应:H2SO4+Cu(OH)2==CuSO4+2H2O
56硫酸和氢氧化铁反应:3H2SO4+2Fe(OH)3==Fe2(SO4)3+6H2O 57硝酸和烧碱反应:HNO3+NaOH==NaNO3+H2O
(6)酸+盐==另一种酸+另一种盐
58大理石与稀盐酸反应:CaCO3+2HCl==CaCl2+H2O+CO2↑
59碳酸钠与稀盐酸反应:Na2CO3+2HCl==2NaCl+H2O+CO2↑60碳酸镁与稀盐酸反应:MgCO3+2HCl==MgCl2+H2O+CO2↑61盐酸和硝酸银溶液反应:HCl+AgNO3==AgCl↓+HNO3
62硫酸和碳酸钠反应:Na2CO3+H2SO4==Na2SO4+H2O+CO2↑63硫酸和氯化钡溶液反应:H2SO4+BaCl2==BaSO4↓+2HCl (7)碱+盐==另一种碱+另一种盐
64氢氧化钠与硫酸铜:2NaOH+CuSO4==Cu(OH)2↓+Na2SO4 65氢氧化钠与氯化铁:3NaOH+FeCl3==Fe(OH)3↓+3NaCl 66氢氧化钠与氯化镁:2NaOH+MgCl2==Mg(OH)2↓+2NaCl 67氢氧化钠与氯化铜:2NaOH+CuCl2==Cu(OH)2↓+2NaCl 68氢氧化钙与碳酸钠:Ca(OH)2+Na2CO3==CaCO3↓+2NaOH (8)盐+盐==两种新盐
79氯化纳溶液和硝酸银溶液:NaCl+AgNO3==AgCl↓+NaNO3 70硫酸钠和氯化钡:Na2SO4+BaCl2==BaSO4↓+2NaCl 五.其它反应:
71二氧化碳溶解于水:CO2+H2O==H2CO3
72生石灰溶于水:CaO+H2O==Ca(OH)2
73氧化钠溶于水:Na2O+H2O==2NaOH
74三氧化硫溶于水:SO3+H2O==H2SO4
75硫酸铜晶体受热分解:CuSO4·5H2O △
CuSO4+5H2O
76无水硫酸铜作于干燥剂:CuSO4+5H2O==CuSO4·5H2O。
