高中化学专题1化学家眼中的物质世界第一单元丰富多彩的化学物质第4课时物质的分散系学案苏教版必修
01专题1 化学家眼中的物质世界 第一单元 丰富多彩的化学物质

三、气体摩尔体积 1、定义:1mol气体所占的体积,叫做气体摩尔体积,符 号是Vm,单位是L· mol—1。(定义中“1mol”严格的说是 “单位物质的量”) 2、标准状况(273K,101kPa)下,1mol任何气体所占的体 积都约为22.4 L。即标准状况下的气体摩尔体积(Vm)为 22.4 L· mol—1 。
3、对氧化物进行分类 (1)酸性氧化物:只能与碱反应生成盐和水,如CO2、SO2、SO3 、Mn2O7等。酸性氧化物又叫酸酐,大多数非金属氧化物、少数金 属氧化物是酸性氧化物。例如: 2NaOH + CO2(少量) === Na2CO3 + H2O。 (2)碱性氧化物:只能与酸反应生成盐和水,如Na2O、CaO、 MgO等,大多数金属氧化物是碱性氧化物。例如:CaO + HCl === CaCl2 + H2O。 (3)两性氧化物:既能与酸反应生成盐和水,又能与碱反应生成 盐和水,如Al2O3、ZnO等。例如:Al2O3 + 6HCl === 2AlCl3 + 3H2O,Al2O3 + 2NaOH === 2NaAlO2 + H2O。 (4)不成盐氧化物:既不能与酸反应生成盐和水,又不能与碱反 应生成盐和水,如CO、NO、H2O等。
课堂习题
2.盐是一类常见的物质,下列物质通过一定反应可直接 形成盐的是( ) ①金属单质 ②碱性氧化物 ③碱 ④非金属单质 ⑤ 酸性氧化物 ⑥酸 A.①②③ B.①④⑥ C.②⑤⑥ D.全部
4.下列反应不属于四种基本反应类型的是( ) A.2KClO3 2KCl+3O2↑ B.NH3+HCl===NH4Cl C.MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O D.Ba(OH)2+MgSO4===BaSO4↓+Mg(OH)2↓
高中化学必修一课时跟踪检测专题一化学家眼中的物质世界第1单元第4课时

专题1化学家眼中的物质世界第一单元丰富多彩的化学物质第4课时物质的分散系课时跟踪检测知识点一:分散系及分类比较1.下列关于分散系的说法不正确的是()A.分散系的稳定性:溶液>胶体>浊液B.分散质粒子的大小:溶液>胶体>浊液C.分散质粒子的直径为几纳米或几十纳米的分散系是胶体D.可以用过滤的方法将悬浊液中的分散质从分散剂中分离出来解析:溶液均一稳定,胶体属于介稳体系,浊液不能稳定存在,所以分散系的稳定性:溶液>胶体>浊液,A项正确;分散系中分散质粒子的大小顺序为浊液>胶体>溶液,故B项错误;分散质粒子的直径在1~100 nm之间的分散系为胶体,C项正确。
答案:B2.当光束通过下列分散系时,不能观察到丁达尔效应的是()A.豆浆B.牛奶C.蔗糖溶液D.烟、云、雾解析:豆浆、牛奶、烟、云、雾都属于胶体,均能产生丁达尔效应,而蔗糖溶液属于溶液,不能产生丁达尔效应。
答案:C3.下列分散系中的分散质粒子大小属于纳米级(1~100 nm)的是()A.Fe(OH)3胶体B.Fe(OH)3沉淀C.FeCl3溶液D.油水混合物答案:A4.下列关于胶体和溶液的说法中,不正确的是()A.胶体和溶液都是均一、稳定的分散系,静置不易产生沉淀B.胶体与纳米级微粒在直径上具有相同数量级C.光线通过时,胶体产生丁达尔效应,溶液则无丁达尔效应D.向Fe(OH)3胶体中逐滴加入稀硫酸无明显现象解析:胶体和溶液都是均一、稳定的分散系,静置不易产生沉淀,A正确;胶体与纳米级微粒在直径上具有相同数量级,都是10-9m,B正确;光线通过时,胶体产生丁达尔效应,溶液则无丁达尔效应,C正确;向Fe(OH)3胶体中逐滴加入稀硫酸先沉淀,后溶解,D错误,故选D。
答案:D知识点二:胶体的性质及制备5.下列叙述与胶体知识无关的是()A.“卤水点豆腐”B.明矾可用作净水剂C.在电影院看电影,会看到从放映室到银幕的光柱D.向氯化铁溶液中加入过量氢氧化钠溶液会看到红褐色沉淀解析:在豆浆里加入盐卤做豆腐,盐卤(主要成分为MgCl2)是电解质溶液,利用的是胶体的聚沉,A错误;明矾溶解后会产生氢氧化铝胶体,具有较大面积有吸附性,可以净水,与胶体性质有关,B错误;胶体能发生丁达尔现象,在电影院看电影,会看到从放映室到银幕的光柱,和胶体的性质有关系,C错误;FeCl3溶液中加入NaOH溶液出现红褐色沉淀是发生了复分解反应,生成红褐色沉淀氢氧化铁,与胶体性质无关,D正确。
苏教版高中化学电子课本下载

苏教版高中化学电子课本下载篇一:高中化学教材目录--苏教版高中化学--苏教版目录? 必修1专题一化学家眼中的物质世界第一单元丰富多彩的化学物质第二单元研究物质的实验方法第三单元人类对原子结构的认识专题二从海水中获得的化学物质第一单元氯、溴、碘及其化合物第二单元钠、镁及其化合物专题三从矿物到基础材料第一单元从铝土矿到铝合金第二单元铁、铜的获取及应用第三单元含硅矿物与信息材料专题四硫、氮和可持续发展第一单元含硫化合物的性质和应用第二单元生产生活中的含氮化合物附录一相对原子质量表附录二常见酸、碱和盐的溶解性表(20?) 附录三中英文名词对照表元素周期表高中化学--苏教版目录? 必修21专题一微观结构与物质多样性第一单元原子核外电子排布与元素周期律第二单元微粒之间的相互作用力第三单元从微观结构看物质多样性专题二化学反应与能量转化第一单元化学反应速率与反应限度第二单元化学反应中的热量第三单元化学能与电能的转化第四单元太阳能、生物质能和氢能的利用专题三有机化合物的获得与应用第一单元化石燃料与有机化合物第二单元食品中的有机化合物第三单元人工合成有机化合物专题四化学科学与人类文明第一单元化学是认识和创造物质的科学第二单元化学是社会可持续发展的基础附录一相对原子质量表附录二中英文名词对照表元素周期表高中化学--苏教版目录? 选修1 化学与生活专题一洁净安全的生存环境第一单元空气质量的改善第二单元水资源的合理利用第三单元生活垃圾的分类处理第四单元化学品的安全使用专题二营养均衡与人体健康第一单元提取人体必需的化学元素第二单元提供能量与营养的食物第三单元优化食物品质的添加剂第四单元造福人类的化学药物专题三丰富多彩的生活材料2第一单元应用广泛的金属材料第二单元功能各异的无机非金属材料第三单元高分子材料和复合材料附录中英文名词对照表附录一相对原子质量表附录二常见酸、碱和盐的溶解性表(20?)附录三生活饮用水水质标准附录四人体内常量元素和微量元素的含量附录五一些食物中的营养素含量附录六常见的食品添加剂附录七一些合成纤维的组成及特点元素周期表高中化学--苏教版目录? 选修2化学与技术专题一多样化的水处理技术第一单元水的净化与污水处理第二单元硬水软化第三单元海水淡化专题二从自然资源到化学品第一单元氨的合成第二单元氯碱生产第三单元硫酸工业第四单元镁和铝的冶炼专题三让有机反应为人类造福第一单元有机药物制备第二单元合成洗涤剂的生产第三单元纤维素的化学加工第四单元有机高分子合成专题四材料加工与性能优化专题五为现代农业技术添翼专题六从污染防治到绿色化学附录一中英文名词对照表元素周期表3高中化学--苏教版目录? 选修3物质结构与性质专题一揭示物质结构的奥秘专题二原子结构与元素的性质第一单元原子核外电子的运动第二单元元素性质的递变规律专题三微粒间作用力与物质性质第一单元金属键金属晶体第二单元离子键离子晶体第三单元共价键原子晶体第四单元分子间作用力分子晶体专题四分子空间结构与物质性质第一单元分子结构与物质的性质第二单元配合物的形成和应用专题五物质结构的探索无止境附录一中英文名词对照表元素周期表高中化学--苏教版目录? 选修4化学反应原理专题一化学反应与能量变化第一单元化学反应中的热效应第二单元化学能与电能的转化第三单元金属的腐蚀与防护专题二化学反应速率与化学平衡第一单元化学反应速率第二单元化学反应的方向和限度第三单元化学平衡的移动专题三溶液中的离子反应4第一单元弱电解质的电离平衡第二单元溶液的酸碱性第三单元盐类的水解第四单元难溶电解质的沉淀溶解平衡附录一中英文名词对照表附录二常见酸、碱和盐的溶解性表(20?) 附录三难溶电解质的溶度积常数(25?)附录四弱电解质在水中的电离平衡常数(25?) 元素周期表高中化学--苏教版目录? 选修5有机化学基础专题一认识有机化合物第一单元有机化学的发展与应用第二单元科学家怎样研究有机物专题二有机物的结构与分类第一单元有机化合物的结构第二单元有机化合物的分类与命名专题三常见的烃第一单元脂肪烃第二单元芳香烃专题四烃的衍生物第一单元卤代烃第二单元醇酚第三单元醛羧酸专题五生命活动的物质基础第一单元糖类油脂第二单元氨基酸蛋白质核酸附录一中英文名词对5照表元素周期表高中化学--苏教版目录? 选修6实验化学专题一物质的分离与提纯课题1 海带中碘元素的分离及检验拓展课题1-1 茶叶中某些元素的鉴定课题2 用纸层析法分离铁离子和铜离子拓展课题1-2 菠菜的叶绿体中色素的提取和分离拓展课题1-3 用粉笔进行层析分离课题3 硝酸钾晶体的制备拓展课题1-4 粗盐的提纯专题二物质性质的研究课题1 铝及其化合物的性质拓展课题2-1 铝热反应课题2 乙醇和苯酚的性质拓展课题2-2 苯酚与甲醛的反应专题三物质的检验与鉴别课题1 牙膏和火柴头中某些成分的检验拓展课题3-1 新装修居室内空气中甲醛浓度的检测拓展课题3-2 汽车尾气成分的检验课题2 亚硝酸钠和食盐的鉴别拓展课题3-3 真假碘盐的鉴别专题四化学反应条件的控制课题1 硫代硫酸钠与酸反应速率的影响因素拓展课题4-1 “蓝瓶子”实验课题2 催化剂对过氧化氢分解反应速率的影响拓展课6题4-2 过氧化氢酶的催化作用拓展课题4-3 蔗糖的燃烧课题3 反应条件对化学平衡的影响拓展课题4-4 淀粉与碘显色现象的探究拓展课题4-5 压强对化学平衡的影响专题五电化学问题研究课题1 原电池拓展课题5-1 干电池模拟实验课题2 电解与电镀拓展课题5-2 阿佛伽德罗常数的测定拓展课题5-3 用铜电极电解饱和食盐水专题六物质的定量分析课题1 食醋总酸含量的测定拓展课题6-1 配制并标定氢氧化钠溶液课题2 镀锌铁皮镀锌层厚度的测定拓展课题6-2 水果中维生素C含量的测定专题七物质的制备与合成课题1 硫酸亚铁铵的制备拓展课题7-1 用制氢废液制备硫酸锌晶体课题2 阿司匹林的合成拓展课题7-2 对氨基苯磺酸的合成附录一实验规则附录二实验室安全守则附录三实验室事故的处理附录四常见酸、碱和盐的溶解性表(20?) 附录五常见指示剂附录六基本操作和气体发生装置图附录七误差和有效数字运算规则附录八元素的相对原子质量表附录九7中英文名词对照表元素周期表篇二:苏教版语文电子课本目录费下载苏教版语文电子课本目录一年级上目录识字(一)1 一去二三里2 口耳目3 在家里4 操场上语文园地一有趣的游戏课文1 画2 四季3 小小竹排画中游4 哪座房子最漂亮5 爷爷和小树语文园地二我们的画6 静夜思7 小小的船8 阳光9 影子10 比尾巴语文园地三这样做不好识字(二)1 比一比2 自选商场3 菜园里84 日月明语文园地四我会拼图课文11 我多想去看看12 雨点儿13 平平搭积木14 自己去吧15 一次比一次有进步语文园地五该怎么办 16 小松鼠找花生17 雪地里的小画家18 借生日19 雪孩子20 小熊住山洞语文园地六小兔运南瓜生字表(一)生字表(二) 一.培养良好的学习习惯二.汉语拼音三.识字四.课文1 人有两个宝2 升国旗3 江南4 我叫神舟号5 家6 东方明珠97 秋姑娘的信8 看菊花五.识字六.课文9 大海睡了10 冰花11 北风和小鱼12 怀素写字13 小河与青草生字表一年级语文下目录一.培养良好的学习习惯二.识字三.课文1 春笋2 雨点3 小池塘4 春到梅花山5 草原的早晨6 蘑菇该奖给谁7 骑牛比赛108 小松树和大松树9 吃水不忘挖井人10 他得的红圈圈最多 11 奶奶的白发12 陈毅探母13 好学的爸爸四.识字五.课文14 鲜花和星星15 放小鸟16 这儿真好17 世界多美呀18 我叫足球19 三个小伙伴20 蚂蚁和蝈蝈21 古诗两首22 司马光23 鲁班和橹板24 乌鸦喝水25 咏华山26 小松鼠找花生果生字表苏教版二年级语文上册电子课本目录一.培养良好的学习习惯11二.识字三.课文1 秋游2 2008,北京~3 英英学古诗4 乡下孩子5 送给盲婆婆的婚姻6 一抹紫丁香7 有趣的发现8 小鹰学飞9 青蛙看海10 狼和小羊11 狐狸和乌鸦四.识字五.课文12 要好好学字13 来德扁担14 梅兰芳学艺15 大禹治水16 孔繁森17 登鹳雀楼18 青松19 小动物过冬1220 美丽的丹顶鹤21 水乡歌22 云房子23 夕阳真美生字表苏教版二年级语文下册电子课本目录一.培养良好的学习习惯二.识字三.课文1 古诗两首2 蚕姑娘3 月亮湾4 快乐的节目5 雨后6 谁的本领大7 蜗牛的奖杯8 狐假虎威9 母亲的恩情10 沉香救母(一) 11 沉香救母(二) 12 木兰从军四.识字五.课文13 学棋1314 黑板跑了15 晚上的太阳16 闪光的金子17 歌唱二小放牛郎 18 鸟岛19 台湾的蝴蝶谷20 欢乐的泼水节21 真想变成大大的荷叶 22 猴子种果树23 会走路的树24 问银河生字表苏教版三年级语文上册电子课本目录一.培养良好的学习习惯二.课文1 让我们荡起双桨2 学会查无字词典3 古诗两首4 做一片美的叶子三.课文5 北大荒的秋天6 西湖7 拉萨的天空四.课文8 蒲公英149 三袋麦子10 哪吒闹海五.课文11 第八次12 卧薪尝胆13 世界上第一个听诊器六.课文14 东方之珠15 小露珠16 石榴七.课文17 石头书18 小稻秧脱险记19 航天飞机八.课文20 军神21 掌声22 奎子九.课文23 每逢佳节倍思亲 24 孙中山破陋习生字表15苏教版三年级语文下册电子课本目录一.培养良好的学习习惯二.课文1 长城和运河2 美丽的南沙群岛3 庐山的云雾三.课文4 微笑着承受一切5 雪儿6 花瓣飘香四.课文8 蒲公英9 三袋麦子10 哪吒闹海五.课文11 赶海12 荷花13 古诗两首六.课文篇三:苏教版高一化学必修一教材整合苏教版高一化学必修一教材整合(共4个专题10个单元31节)16专题1 化学家眼中的物质世界一、教材整合的整体思路是:由于第一单元丰富多彩的化学物质一、物质的分类及转化(移去“氧化还原反应的判断”) 学生基础底,知识薄,教学中特别注重二、物质的量初中知识的复习与高中知识的衔接。
高中化学专题1化学家眼中的物质世界第1单元丰富多彩的化学物质第4课时物质的分散系

(3)③⑧电离方程式为③_________________________________________,
⑧___________________________________________________________。
【答案】 (1)④⑧⑨ (2)③⑤⑧
(3)HCl===H++Cl- KNO3===K++NO- 3
第十六页,共三十八页。
2.纳米材料是粒子直径在1~100 nm之间的材料,其研究成果已应用于医
学、化工、军事等领域。纳米碳就是其中的一种,若将纳米碳均匀地分散到蒸
馏水中,下列有关形成的物质的判断正确的是( )
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过
滤纸 ⑥静置后会析出黑色沉淀
2021/12/11
第九页,共三十八页。
[合 作 探 究·攻 重 难]
胶体的主要性质及应用
[背景材料] 〈实验 1〉 把盛有 CuSO4 溶液和 Fe(OH)3 胶体的烧杯置于暗处,分别用激 光笔(或手电筒)照射烧杯中的液体,在与光束垂直的方向进行观察。 〈实验 2〉 在两只烧杯中分别加入相同量的含有悬浮颗粒物的浑浊污水, 再向其中一只烧杯中加入 10 mL 氢氧化铁胶体,搅拌后静置、观察。
2021/12/11
第八页,共三十八页。
2.现有以下物质:①氮气 ②液态 CO2 ③氯化氢气体 ④铜片 ⑤硫酸 钡晶体 ⑥蔗糖 ⑦酒精 ⑧熔化的 KNO3 ⑨NaOH 溶液,请回答下列问题(填 序号):
(1)以上物质能导电的是________。
(2)以上物质中属于电解质的是___________________________________。
①非金属氧化物 ②非酸性气态氢化物 ③多数有机物
苏教版高中化学必修一知识点(全)
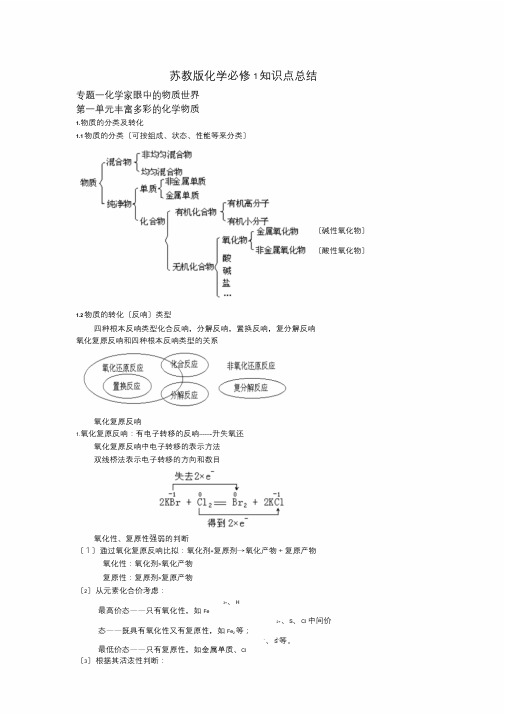
苏教版化学必修1知识点总结专题一化学家眼中的物质世界第一单元丰富多彩的化学物质1.物质的分类及转化1.1物质的分类〔可按组成、状态、性能等来分类〕〔碱性氧化物〕〔酸性氧化物〕1.2物质的转化〔反响〕类型四种根本反响类型化合反响,分解反响,置换反响,复分解反响氧化复原反响和四种根本反响类型的关系氧化复原反响1.氧化复原反响:有电子转移的反响-------升失氧还氧化复原反响中电子转移的表示方法双线桥法表示电子转移的方向和数目氧化性、复原性强弱的判断〔1〕通过氧化复原反响比拟:氧化剂+复原剂→氧化产物+复原产物氧化性:氧化剂>氧化产物复原性:复原剂>复原产物〔2〕从元素化合价考虑:3+、H最高价态——只有氧化性,如Fe2+、S、Cl 中间价态——既具有氧化性又有复原性,如Fe2等;-、S2-等。
最低价态——只有复原性,如金属单质、Cl〔3〕根据其活泼性判断:①根据金属活泼性:对应单质的复原性逐渐减弱KCaNaMgAlZnFeSnPb(H)CuHgAgPtAu对应的阳离子氧化性逐渐增强②根据非金属活泼性:对应单质的氧化性逐渐减弱Cl2Br2I2S对应的阴离子复原性逐渐增强(4)根据反响条件进展判断:不同氧化剂氧化同一复原剂,所需反响条件越低,说明氧化剂的氧化剂越强;不同复原剂复原同一氧化剂,所需反响条件越低,说明复原剂的复原性越强。
如:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O△MnO2+4HCl(浓)==MnCl2+Cl2↑+2H2O前者常温下反响,后者微热条件下反响,故物质氧化性:KMnO4>MnO2(5)通过与同一物质反响的产物比拟:如:2Fe+3C2l=2FeC3l Fe+S=FeS可得氧化性Cl2>S离子反响〔1〕电解质:在水溶液中或熔化状态下能导电的化合物,叫电解质。
酸、碱、盐都是电解质。
在水溶液中或熔化状态下都不能导电的化合物,叫非电解质。
化学必修一 专题1 化学家眼中的物质世界

专题1 化学家眼中的物质世界第一单元丰富多彩的化学物质一物质的分类及转化知识·运用·归纳知识点1 物质的分类对物质进行分类是按照物质的进行的,常见的分类依据有、、、。
常见的分类方法有树状分类法,如:按组成元素的差别纯净物可分为和。
例1、请根据所学的物质分类的方法填空。
混合物单质物质有机化合物强酸纯净物化合物酸弱酸强碱碱无机化合物弱碱正盐碱酸式盐碱式盐酸性氧化物氧化物碱性氧化物两性氧化物例2、判别正误:1、酸性氧化物均为非金属氧化物。
()2、碱性氧化物均为金属氧化物。
()3、金属氧化物均为碱性氧化物。
()巩固练习1、按物质的分类方法,下列各组中,前者包含后者的是()A.有机物、混合物B.纯净物、化合物C.化合物、单质D.单质、金属2、现有①空气②醋酸③碳酸氢铵④铜⑤硫酸钠⑥氢气⑦石墨⑧食盐水⑨泥浆水⑩蒸馏水十种物质,若根据物质的组成将它们进行分类,则(1)属于均匀混合物的有(填编号,下同)(2)属于非均匀混合物的有(3)属于金属单质的有(4)属于非金属单质的有(5)属于无机化合物的有(6)属于有机化合物的有(7)若将醋酸、碳酸氢铵、蒸馏水分为一类,你认为分类的依据可能是知识点2 物质转化的分类在一定的条件下物质可发生变化,由一种物质转化为另一种物质,这种转化遵循一定的规律,如:酸不能转化为碱,金属不能转化为非金属。
(1)转化为单质的反应有①化合物的分解②置换反应③化合物间的反应(2)转化为酸的反应有①非金属氧化物与水②盐和酸的反应③金属单质与非金属单质的反应(3)转化为碱的反应有①金属与水的反应②金属氧化物与水的反应③盐和碱的反应(4)转化为盐的反应有①单质与酸反应②碱与酸反应③碱性氧化物与酸反应④碱性氧化物与酸性氧化物反应(5)转化为氧化物的反应有①单质与氧气反应②酸分解反应③盐分解反应④碱分解反应例3、请举出含氧酸盐转化为无氧酸盐的三种类型,并写出化学方程式。
例4、现有生石灰、食盐、高锰酸钾、铜片、硝酸银和水六种物质,请选用其中部分物质为反应物,按下列要求各写一个化学方程式。
【金识源专版】高中化学 专题一 化学家眼中的物质世界 第一单元 丰富多彩的化学物质 物质的分类与

物质的分类和转化【教学目标】1、能根据物质的组成和性质对常见物质进行分类,并了解比较和分类对化学研究的作用。
2、掌握单质、氧化物、酸、碱、盐之间的转化关系,并了解通过化学反应实现物质转化的重要意义。
【教学重点】培养学生学会从不同角度、不同的标准对物质进行分类。
【教学难点】引导学生从物质的宏观性质的学习和研究转入从微观角度分析研究问题。
【教学过程】[导入新课]阅读P2图片,思考化学与人类社会发展的关系。
[强调]人类生活离不开各种各样的化学物质。
化学物质种类繁多,且新分子和新材料还在飞速增长。
[[设问]世界上的物质如此繁多,为了简明有序地掌握其性质及变化规律,常采用的方法之一是进行分类研究。
那么,我们是如何来对不同物质进行分类的呢?[板书]一、物质的分类[交流与讨论]在我们日常生活中,常会接触到下列物质:空气、乙醇、水、硫酸铵、铜、碘酒、碘、氧气、石墨、食盐水请你将上述物质进行分类,并说明分类的依据。
将你的分类结果与同学交流讨论。
[归纳]分类标准:(1)混合物和纯净物;(2)单质和化合物;(3)导体和非导体;(4)气体、液体和固体;(5)易溶物、微溶物和难溶物。
[板书]1、研究物质常采用的方法之一是分类研究。
2、对于若干种同样的物质,若分类的依据不同,则得到的分类结果不同。
对物质进行分类的常见依据有组成、状态、性能等。
化学上,根据组成对物质进行分类是最常用的方法。
[思考]下图是根据物质的组成对物质进行分类的一种结果,试填写其中空格:[提问]请说出上述概念“混合物、纯净物、单质、化合物”的含义。
[问题解决]实验室中有下列物质,请根据物质的组成对它们进行分类。
①钠(Na );②氯气(Cl 2);③氯化铁(FeCl 3)溶液;④硫酸(H 2SO 4);⑤碳酸钙(CaCO 3);⑥氧化钙(CaO );⑦氢氧化钠(NaOH );⑧葡萄糖(C 6H 12O 6)。
[阅读并思考]什么叫酸性氧化物?什么叫碱性氧化物?[问题解决]1、SO 2属于酸性氧化物,请写出SO 2与足量KOH 溶液反应的化学方程式。
高中化学专题1化学家眼中的物质世界第一单元丰富多彩的化学物质第4课时物质的分散系课时作业课件苏教版

9.溶液、胶体和浊液这三种分散系的根本区别是( ) A.分散质的粒子是否为大量分子或离子的集合体 B.分散质微粒直径的大小 C.能否透过滤纸 D.是否均一、稳定、透明
答案 B
答案
解析 C、D都是B的表现形式。对于A,胶体与浊液中分散质的粒子都 是大量分子或离子的集合体,故不是根本区别。分散质微粒直径的大小决定 了它们应有的各种特征和性质。
光束,穿过这些水雾会产生丁达尔效应
答案
2021/4/17
高中化学专题1化学家眼中的物质世界第一单元丰富多
34
彩的化学物质第4课时物质的分散系课时作业课件苏教
结束 语 同学们,你们要相信梦想是价值的源泉,相信成
功的信念比成功本身更重要,相信人生有挫折没 有失败,相信生命的质量来自决不妥协的信念,
考试加油。
二、非选择题 14.电解质是指在__________或__________下能够导电的__________。 电解质导电的根本原因在于它在这种状态下能够__________出自由移动的离 子。科学家从这个角度对化合物进行了分类,根据这种分类,酸、碱、盐都 属于__________。 答案 水溶液里 熔融状态 化合物 电离 电解质
8.下列分散系属于胶体的是( )
A.有色玻璃
B.食盐水
C.石灰乳
D.碘酒
答案 A
答案
休息时间到啦
同学们,下课休息十分钟。现在是休息时间,你们休息一 下眼睛,
看看远处,要保护好眼睛哦~站起来动一动,久坐对身体 不好哦~
解析 A项中是某些金属氧化物分散在玻璃中形成的胶体;B项与D项 是溶液;而C项则是悬浊液。
答案 C
答案
解析 当液体呈红褐色时要停止加热,加热过度会破坏胶体,生成 Fe(OH)3沉淀。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第4课时 物质的分散系一 分散系1.分散系概念及分类 (1)概念分散系是指由一种或几种物质分散到另一种物质中形成的混合体系。
(2)组成分散系⎩⎪⎨⎪⎧分散质:被分散的物质分散剂:容纳分散质的物质(3)分类依据分散质粒子直径大小分为三类分散系。
分散系⎩⎪⎨⎪⎧溶液:分散质粒子直径小于1 nm (或10-9m )浊液:分散质粒子直径大于100 nm (或10-7m )浊液又分为悬浊液和乳浊液胶体:分散质粒子直径在1~100 nm (或10-9~10-7 m )之间(4)除去NaCl 溶液或Fe(OH)3胶体中的泥沙采用什么方法?答案 根据三种分散系中粒子的直径大小、结合滤纸的孔隙大小可知,溶液、胶体中的分散质粒子能透过滤纸,浊液不能透过,因此除去NaCl 溶液或Fe(OH)3胶体中的泥沙时应用过滤的方法。
2.胶体的性质和应用 (1)胶体的性质把盛有CuSO 4溶液和Fe(OH)3胶体的烧杯置于暗处,分别用激光笔(或手电筒)照射烧杯中的液体,在与光束垂直的方向进行观察。
当光束通过CuSO 4溶液时,无光路现象出现。
当光束通过Fe(OH)3胶体时,可以看到形成一条光亮的通路。
这是由于胶体粒子对光线的散射作用形成的,叫作丁达尔效应。
丁达尔效应是区分胶体与溶液的一种常用物理方法。
(2)胶体的应用在两只烧杯中分别加入相同量的含有悬浮颗粒物的浑浊污水,再向其中一只烧杯中加入10 mL 氢氧化铁胶体,搅拌后静置、观察到的现象是加入Fe(OH)3胶体的烧杯中溶液变得澄清而透明。
归纳总结分散系及胶体的理解(1)分散质微粒直径的大小与分散系类别的关系:分散系间的本质区别是分散质粒子直径的大小。
分散系的性质,如是否透明、均一、稳定都由此决定。
(2)胶体粒子直径在10-9~10-7m之间,能透过滤纸。
(3)丁达尔效应是胶体的特有性质,区别溶液和胶体最简单的方法是丁达尔效应。
(4)氢氧化铁胶体具有吸附性,能够吸附水中悬浮的颗粒而沉降,因此常作净水剂。
1.科学家用DNA制造出一种臂长只有7 nm的纳米级镊子,这种镊子能钳起分子或原子,并对它们随意组合。
下列分散系中分散质的微粒直径与纳米粒子具有相同数量级的是( ) A.溶液B.胶体C.悬浊液D.乳浊液答案 B解析按照分散系中分散质微粒大小将分散系分为溶液、胶体、浊液。
溶液中分散质微粒直径小于1 nm;胶体中分散质微粒直径在1~100 nm之间;悬浊液、乳浊液中分散质微粒直径大于100 nm,B正确。
2.下列叙述正确的是( )A.直径介于1~100 nm之间的粒子称为胶体B.用过滤的方法可以将胶体和溶液分离C.利用丁达尔效应可以区别溶液与胶体D.胶体区别于其他分散系的本质特征是丁达尔效应答案 C解析胶体是一类分散质直径介于1~100 nm之间的分散系,A项错误;胶体和溶液都能通过滤纸,无法将二者分离,B项错误;胶体区别于其他分散系的本质特征是分散质粒子直径的大小,直径在1~100 nm之间,D项错误;丁达尔效应是区别溶液与胶体的简单、便捷的方法。
理解感悟胶体的概念是从分散质粒子的直径这一角度给出的,分散质粒子的直径介于1~100 nm之间正是胶体区别于其他分散系的本质特征,也是胶体具有丁达尔效应等特有性质的根本原因。
丁达尔效应是区别溶液和胶体的最简便方法。
二电解质和非电解质1.电解质和非电解质(1)以氯化钠为例,分析电解质溶液为什么能够导电?答案氯化钠晶体中的Na+和Cl-存在着静电作用,不能自由移动,因此氯化钠晶体不导电。
氯化钠晶体溶于水(或受热熔化)时,晶体中Na+与Cl-之间的静电作用被破坏,从而离解成能够自由移动的Na+和Cl-。
在外加电场的作用下,Na+和Cl-分别作定向移动而导电。
(2)电解质与非电解质的概念①电解质:在水溶液中或熔融状态下能够导电的化合物。
如:酸、碱、盐、金属氧化物、水。
②非电解质:在水溶液中和熔融状态下均不能导电的化合物。
如:蔗糖、乙醇、非金属氧化物等。
2.电解质在水溶液中能够导电,是因为它们在溶液中发生了电离,产生了能够自由移动的离子,其过程常用电离方程式来表示。
电离方程式是表示电解质电离过程的式子。
试写出下列各组物质的电离方程式:(1)HCl、H2SO4HCl===H++Cl-;H2SO4===2H++SO2-4。
(2)NaOH、Ba(OH)2NaOH===Na++OH-;Ba(OH)2===Ba2++2OH-。
(3)BaCl2、Na2CO3、Al2(SO4)3BaCl2===Ba2++2Cl-;Na2CO3===2Na++CO2-3;Al2(SO4)3===2Al3++3SO2-4。
归纳总结1.电解质和非电解质比较2.①符合客观事实,不能随意书写离子符号,离子所带电荷等于该元素或原子团在该化合物中的化合价;②质量守恒,即电离方程式左右两侧元素的种类、原子的个数相等;③电荷守恒,即电离方程式左右两侧的正负电荷数相加呈电中性。
[提醒] (1)电解质和非电解质都是化合物,单质、混合物既不是电解质,也不是非电解质。
(2)自身能够电离出离子的化合物才是电解质,如NH3、CO2、SO2、SO3等自身不能电离出自由移动的离子,而与水反应的生成物能电离,NH3、CO2、SO2、SO3均属于非电解质,相对应的NH3·H2O、H2CO3、H2SO3、H2SO4属于电解质。
(3)绝大多数盐属于电解质。
某些难溶于水的盐如硫酸钡(BaSO4)等,由于它们溶解度太小,其水溶液的导电性很弱,但溶于水的那一部分完全电离,且在熔融状态下能导电,因此它们是电解质。
(4)能导电的物质不一定是电解质,电解质不是在任何状态下都能导电。
3.下列属于电解质的是( )A.酒精B.蔗糖C.硝酸钾D.铜丝答案 C解析酒精、蔗糖是有机物,本身不能电离,为非电解质,A、B错误;硝酸钾是盐,属于电解质,C正确;铜丝为单质,既不是电解质,也不是非电解质,D错误。
4.下列电离方程式书写正确的是( )A.H2SO4===H2+2+SO2-4B.NaHCO3===Na++H++CO2-3C.Ba(OH)2===Ba2++2(OH)-D.Na3PO4===3Na++PO3-4答案 D解析A项中将H2SO4的电离写成了简单的分离,没有H2+2这样的离子,应该表示成H+;B项中NaHCO3在水溶液中电离出的离子主要是Na+和HCO-3,而不是H+和CO2-3;C项中不应该保留括号,应写成2OH-;D项中属于可溶性盐的电离,是正确的。
1.胶体⎩⎪⎨⎪⎧本质特征:胶体微粒直径在1~100 nm 之间鉴别:区别胶体与其他分散系的最简单方法是丁达尔效应2.电解质⎩⎨⎧判断依据:化合物溶于水或受热熔化发生电离物质鉴别:酸、碱、多数盐、活泼金属氧化物和水等电离方程式:原子守恒,电荷守恒1.下列家庭小实验不能制得溶液的是( )答案 B解析 食盐和蔗糖都能够溶于水形成溶液,植物油能够溶于汽油形成溶液,而泥土不溶于水,与水混合后会形成悬浊液。
2.下列关于硫酸铜溶液和氢氧化铁胶体的说法中,正确的是( ) A .前者是混合物,后者是纯净物 B .两者都具有丁达尔效应C .分散质的粒子直径均在1~100 nm 之间D .前者可用于杀菌,后者可用于净水 答案 D3.把下列四组物质分别溶于水,得到的四组水溶液中,含有的离子种类完全相同的是( ) ①NH 4Cl KNO 3 Na 2SO 4 ②K 2SO 4 NaNO 3 NH 4Cl③NH 4NO 3 K 2CO 3 (NH 4)2SO 4 NaCl ④NaCl (NH 4)2SO 4 K 2SO 4 NaNO 3 A .①②④ B .②③④ C .③④ D .①③答案 A解析 以上四组物质均为易溶性盐,溶于水后全部电离产生阴、阳离子,其中①②④组物质溶于水后得到的溶液电离产生相同的阳离子:NH +4、Na +、K +,相同的阴离子:SO 2-4、Cl -、NO -3,所以①②④组物质的水溶液含有的离子种类完全相同。
4.根据中学对电解质、非电解质的定义判断下列叙述正确的是( )A.虽然石墨有较好的导电性,但它属于非电解质B.实验测定NH3、CO2的水溶液均能导电,所以NH3、CO2均是电解质C.实验测定液态HCl、固体NaCl均不能导电,所以HCl、NaCl均是非电解质D.蔗糖(纯净物)在水溶液和熔融状态下均不能导电,所以蔗糖属于非电解质答案 D解析A项,石墨是单质,不属于非电解质;B项,NH3、CO2的水溶液导电的原因是二者与水反应生成了电解质NH3·H2O和H2CO3,NH3、CO2为非电解质;C项,HCl的水溶液、NaCl的水溶液能导电,HCl、NaCl为电解质。
5.下列叙述中正确的是________(填字母)。
A.固体氯化钠不导电,但氯化钠是电解质B.金刚石不能导电,所以金刚石是非电解质C.盐酸、稀硫酸都能导电,所以盐酸、稀硫酸都是电解质D.三氧化硫溶于水能导电,所以三氧化硫是电解质E.氨水能导电,所以氨是电解质F.有机化合物都是非电解质G.不是电解质(非电解质)的物质一定是非电解质(电解质)H.MgCl2、H2SO4、NaOH都是电解质,它们在水溶液中和熔融状态下都能导电I.Na2CO3和NaHCO3的电离方程式分别是Na2CO3===2Na++CO2-3、NaHCO3===Na++H++CO2-3 J.CaCO3、BaSO4均难溶于水,它们属于非电解质答案 A解析金刚石是单质,盐酸和稀硫酸是混合物,它们既不是电解质,也不是非电解质;SO3和NH3的水溶液能导电是由于H2SO4和NH3·H2O电离产生自由移动的离子的缘故,SO3和NH3都是非电解质;有机化合物中的CH3COOH及其钠盐等属于电解质;H2SO4是共价化合物,是由分子组成的,在熔融状态下以分子形式存在,不导电;NaHCO3电离出Na+和HCO-3,但HCO-3不能完全电离;难溶盐如CaCO3、BaSO4等虽然难溶于水,但溶于水的那部分是完全电离的,且在熔融状态下能够导电,属于电解质。
6.现有下列物质:A.淀粉溶液B.食盐水C.铜D.硝酸E.氢氧化钠固体F.泥水G.二氧化碳H.水I.硫酸钠固体J.硫酸氢钠(1)请将它们的序号或所属类别填到下列横线上。
物质⎩⎪⎪⎨⎪⎪⎧混合物⎩⎪⎨⎪⎧溶液: :淀粉溶液浊液:纯净物⎩⎪⎨⎪⎧单质: 化合物⎩⎪⎨⎪⎧酸: 碱: 盐::二氧化碳、水(2)所给物质中属于电解质的是___________________________________________,属于非电解质的是________________。
(3)写出I 、J 的电离方程式____________,_________________。
