有机化学--不饱和(脂肪)烃.
有机化学--第三章 不饱与烃烯烃与炔烃

2020/3/11
7
3.1.3 π键的特性
1. π键是由两个p轨道从侧面平行交盖而成的,轨道交盖程度一般比σ
键要小,另外,π键的电子云不像σ键的电子云那样集中于两个成键 原子核之间的联线上,而是在成键原子周围分散成上下两层,这样 原子核对π电子的束缚力较小,所以π电子云具有较大的流动性,易 受外界电场影响而发生极化,因此,与σ键比较, π键不如σ键牢固, 不稳定而容易断裂,表现较大的化学活泼性。
2020/3/11
3
3.1.1 碳原子轨道的sp2杂化
H
H
CC
H
H
1/3s +2/3p
2020/3/11
4
3.1.2 碳碳双键的组成
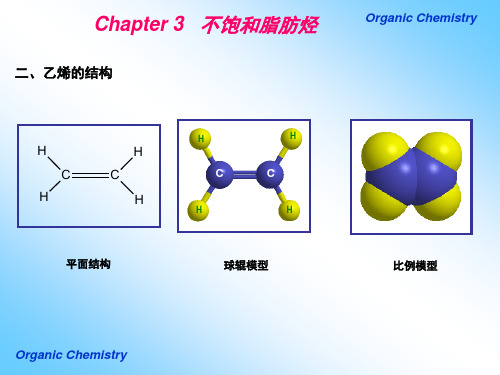
在乙烯中,成键的两碳原子各以一个sp2杂化轨道彼 此交盖形成一个C—C σ键,并各以两个sp2杂化轨道分 别与两个氢原子的1s轨道形成两个C—H σ键,这样形成 的五个σ键其对称轴都在同一平面内。
构型异构体:(I)和(Ⅱ)是由于构型不同而产生的异构体,称为构型异 构体(configurational isomers)。构型异构体具有不同的物理性质。
2020/3/11
17
顺反异构体:像(I)和(Ⅱ)这种构型异构体通常用顺、反 来区别,称为顺反异构体(cis and trans ismers),也称几 何异构体(geometric ismers)。
2020/3/11
5
由于每个碳原子上余下的p轨道的对称轴垂直于同一 平面,且彼此平行,这样两个p轨道就从侧面相互平行交 盖成键,组成新的轨道,称为π轨道。处于π轨道的电子称 为π电子,这样构成的共价键称为π键。
2020/3/11
6
π键的形成,若根据分子轨道理论的近似处理也一样, 两个碳原子的p轨道通过原子轨道的线性组合而形成两个分 子轨道,一个是比原来原子轨道能量低的成键轨道π,一个 是比原来原子轨道能量还要高的反键轨道π*。
不饱和脂肪烃—烯烃氧化(有机化学课件)

O RCOOH(过氧酸)
催化氧化
R
R"
C O+ O C
R'
OH
R
R"
CO+OC
R'
H
R R" R' C C H
OH OH
R
R"
CC
R'
H
O
酮、酸 邻二醇 酮、醛 环氧化物 环氧乙烷 酮、醛
学后释疑
产生乙烯
放置吸有某种成分的的H2
+
1 2
O2
PdCl 2-CuCl2 120~130 C °
O CH3C H —CH3
用 途 合成:工业上在氯化钯–氯化铜的作用下,生产乙醛、丙酮
小结
R C
R'
R" C
H
注意双键和H的变化
KMnO4(浓,热), OH 或 K2Cr2O7, H (1) O3
(2) H2O, Zn
被中性或碱性的高锰酸钾氧化——缓慢氧化
邻二醇
OH OH
KMnO4(稀,冷)
或
OsO4
反应的立体化学——顺式产物
HO OH
用 途 鉴别:紫红色褪去,常温下鉴别烯烃 合成:制备顺式邻二醇
烯烃的氧化反应 1. 与高锰酸钾反应
被酸性高锰酸钾氧化——剧烈氧化
浓,热 或
CH2= RCH= R R C=
产物特点 CO2 + H2O RCOOH R R C=O
酸性KMnO4溶液
HH
OO RRCCOOOOOHHH
RR
RR""
有机化学第三章不饱和烃

4 H +C
+
C
H
H
C
C
H H
H
+
H
C
.C
H H
• 键两部分电子云,象两块面包夹住圆柱型 键。
第三章 不饱和脂肪烃
学问如清泉,越掘越甘甜
(二)炔烃的结构
• 1、叁键上的碳原子以sp杂化。
2 S
2 P
2 Py 2 Pz SP
18O0
+
一个杂化
轨道
第三章 不饱和脂肪烃
学问如清泉,越掘越甘甜
2、乙炔分子中三个 键,2个π键的形成。
1)原子序数大的优先。
• Cl > F > O>N >C >B >H >孤电子对
2) 从离烯碳最近的原子
第二
(第一道弧线上)开始比
较, 如果都相同,依次比 较第二道弧线上的原子; H 3 C
如果还相同, 就比较第三道弧线上的 原子……
C l 第一
弧线
直到有一个优先。
弧线
H
H
H
HH
H
第三
H
弧线
H OH 第三章H不饱和脂肪烃
H+
C
+
C
+ H 三个 键
H
C
C
H
的形成
二个π键
+
的形成
HC
CH
三键的筒 状电 子云
第三章 不饱和脂肪烃
学问如清泉,越掘越甘甜
• 三.烯烃和炔烃的性质
• (一)烯烃和炔烃的物理性质
• 烯烃、炔烃物理性质与烷烃的相似。 ➢均不溶于水。 ➢2~4个碳原子的烯烃、炔烃在室温下为气体,
5~19个碳原子的烯烃在室温下为液体。
《有机化学》(第四版)第三章-不饱和烃(习题答案)

第三章 不饱和烃思考题习题3.1 写出含有六个碳原子的烯烃和炔烃的构造异构体的构造式。
其中含有六个碳原子的烯烃,哪些有顺反异构?写出其顺反异构体的构型式(结构式)。
(P69)解:C 6H 12有13个构造异构体,其中4个有顺反异构体:CH 2=CHCH 2CH 2CH 2CH 3CH 3CH=CHCH 2CH 2CH 3CH 3CH 2CH=CHCH 2CH 3(Z,E)(Z,E)CH 2=CCH 2CH 2CH 3CH 3CH 2=CHCHCH 2CH 3CH 3CH 2=CHCH 2CHCH 3CH 3CH 3C=CHCH 2CH 3CH 3CH 3CH=CCH 2CH 3CH 3CH 3CH=CH 2CHCH 3CH 3(Z,E)(Z,E)CH 2=CHCCH 3CH 3CH 3CH 2=CCHCH 3CH 3CH 3CH 3C=CCH 3CH 3CH 3CH 2=CCH 2CH 3CH 2CH 3C 6H 10有7个构造异构体:CH CCH 2CH 2CH 2CH 3CH 3C CCH 2CH 2CH 3CH 3CH 2C CCH 2CH 3CH CCHCH 2CH 3CH 3CH CCH 2CHCH 3CH 3CH CC(CH 3)3CH 3C CCHCH 3CH 3习题3.2 用衍生物命名法或系统命名法命名以下各化合物:(P74)(1) (CH 3)2CHCH=CHCH(CH 3)2对称二异丙基乙烯 or 2,5-二甲基-3-己烯(2)(CH 3)2CHCH 2CH=CHCHCH 2CH 3CH 3123456782,6-二甲基-4-辛烯(3)CH 3CH 2C CCH 2CH 3123456二乙基乙炔 or 3-己炔(4)CH 3CH 2C(CH 3)2C CH 12345 3,3-二甲基-1-戊炔(5)CH 2=CHCH 2C CH 123451-戊烯-4-炔(6) HCC C=CCH=CH 2CH 2CH 2CH 3CH 2CH 2CH 31234563,4-二丙基-1,3-己二烯-5-炔(7)CH 3CH 32,3-二甲基环己烯(8)CH 3CH 35,6-二甲基-1,3-环己二烯习题3.3 用Z,E-命名法命名以下各化合物:(P74)(1) ↑C=CCH 2CH 3H ClBr↑(Z)-1-氯-1-溴-1-丁烯(2) ↓C=CF CH 3ClCH 3CH 2↑(E)-2-氟-3-氯-2-戊烯 (3) ↑C=CCH 2CH 3CH 2CH 2CH 3HCH 3↓ (E)-3-乙基-2-己烯(4) ↓C=CCH(CH 3)2CH 2CH 2CH 3CH 3H↑ (E)-3-异丙基-2-己烯习题3.4 完成以下反应式:(P83)(1) C 3H 7C CC 3H7C=C H C 3H 7HC 3H 7(2)3C 3H 7C CC 3H 7C=C H C 3H 7C 3H 7H(3)+ Br 2C=C HC 2H 5C 2H 5H25(4)CCHOOC COOH C=CHOOCBr Br COOH+ Br 2习题3.5 以下各组化合物分别与溴进行加成反应,指出每组中哪一个反应较快。
有机化学不饱和脂肪烃
的 sp2杂化轨道。三个sp2 杂化轨道的轴在一个平面上,键角
120°,剩余的一个 p 轨道保持原状,垂直于sp2 杂化轨道平面
2p — — — 2p — — —
能
量 2s —
2s —
1s —
1s —
基态
激发态
—
———
sp2杂化态
Organic Chemistry
a C
b
a C
b
a C
b
a C
d
a C
b
d C
e
a C
a
b C
d
存在几何异构现象
Organic Chemistry
无几何异构现象
Chapter 3 不饱和脂肪烃
Organic Chemistry
④ 顺反异构的表示: 当两个双键碳上没有共同基团时,以顺反表示构型有困难,则用 Z(同)、E(对)来表示,即分别将双键碳原子上的两个原子或 基团按次序规则定出较优基团,如果较优基团在同侧,则以“ Z ” 表示;在异侧则以“ E ”表示
3
H
H3C1 C
2
H
Cl
C
2
C1 H3
(Z)—2—氯—2—戊烯
H
C
4
C
3
H
C6 H3 C
5
H
(2Z,4E)—2,4—己二烯
Organic Chemistry
Chapter 3 不饱和脂肪烃
⑤ 顺反异构体的数目
Organic Chemistry
Organic Chemistry
Chapter 3 不饱和脂肪烃
Chapter 3 不饱和脂肪烃
烃基饱和和不饱和

烃基饱和和不饱和
烃基饱和和不饱和是有机化学中的两个常见概念。
烃是指仅由碳氢元素构成的化合物,其中碳氢键是主要的键类型。
烃可以分为两类:饱和烃和不饱和烃。
饱和烃,也称为脂肪烃,是指分子中所有碳原子都与最大数量的氢原子相连。
这意味着它们没有任何双键或环状结构。
最常见的饱和烃是烷烃,其中所有碳原子都是以单键链接的。
例如,甲烷(CH4)、乙烷(C2H6)和丙烷(C3H8)都是饱和烃。
饱和烃通常是液体或固体,在常温下很少存在气态。
不饱和烃是指分子中存在一个或多个碳-碳双键或环状结构。
不饱和烃分为两类:烯烃和炔烃。
烯烃是指分子中至少有一个碳-碳双键,而炔烃则是指分子中至少有一个碳-碳三键。
例如,乙烯(C2H4)和丙烯(C3H6)是烯烃,而乙炔(C2H2)是炔烃。
不饱和烃通常是气态,在常温下很少存在液态或固态。
在化学反应中,烃基的饱和或不饱和性质会对反应的类型和速率产生影响。
例如,饱和烃更难被氧化,因此烷烃的燃烧反应需要更高的温度和氧气浓度。
另一方面,不饱和烃的双键或三键更容易参与化学反应,如加成反应和聚合反应。
总之,烃基的饱和和不饱和性质对于有机化学的研究和实际应用都具有重要意义。
了解这些概念可以帮助我们更好地理解烃化合物的性质和反应行为。
- 1 -。
《有机化学》第三章 不饱和烃

吸电子基团: +NR3>NO2>CN>COOH>F>Cl>Br>I>COOR>OR>
COR>SH>OH> C CR>C6H5>CH=CH2>H
诱导效应的特点:
(1)诱导效应的强弱取决于原了或基团的电负性的大小
的两原子可相对的自由旋转。 能相对自由旋转。Βιβλιοθήκη c.键的可极化度:较小。 较大
1.2 单烯烃的异构现象
1.2.1 结构异构
CH3 CH2 CH CH2 CH3 CH CH CH3
1-丁 烯
2-丁 烯
官能团碳碳双键 位置异构
CH3 C CH2 2-甲 基 丁 烯 CH3
碳链异构
结构异构是由于分子中各原子的结合顺序不同而引起的, 位置异构和碳链异构均属于结构异构。
(2) 与卤化氢的加成
CH3CH CHCH3 + HCl CH3CH2CHCH3
2–丁烯
HBr CH3CH2CH CH2
Markovnikov规则
Cl
2–氯丁烷
Br
CH3CHCH CH3
80 %
CH3CHCH2 CH2Br 20 %
当不对称的烯烃与卤化氢等极性试剂加成时,氢原总
是加到含氢较多的双键碳原子上,卤原子(或其子或
上相互重叠。
从侧面重叠。
电子云的分布情况 a. 电子云集中于两原子 电子云分布在 键所
核的连线上,呈圆柱形分布。 在平面的上下两方,呈块
状分布。
生物化学基础不饱和脂肪酸

– 短链(4-6个碳原子) – 中链(8-14个碳原子) – 长链(16个碳原子以上);20个碳以上的脂肪酸也被称为
超长链脂肪酸
• 按饱和度分:
– 饱和脂肪酸(Saturated fatty acid):烃类基团是全由单 键构成的烷烃基
– 单元不饱和脂肪酸(Monounsaturated fatty acid):烃类 基团是包含一个碳-碳双键的烯烃基
O
O
CH2 - O - C - R1
R2- C - O- C - H O
CH2 - O - P -O- CH2
OH H-C-OH
O
O
CH2 - O - P - O- CH2
R3- C - O- C - H
OH
O
CH2 - O - C - R4
磷脂酰肌醇
作为信使参与激素信号的放大
O
O
CH2 O C R
奇数碳脂肪酸和支链脂肪酸
• 在许多植物,海洋生物,微生物中存在奇 数碳脂肪酸。可能与生物的某些特殊生理 活性有关
• 在蔬菜,动物和微生物体内有发现一些带 支链的脂肪酸,常常用来区别不同的微生 物
脂肪醇与脂肪酮
• 最早的脂肪醇有鲸蜡中提取。脂肪醇通式为ROH, 具有两性,是制造表面活性剂的原料,通过还原 脂肪酸获得
– 必需脂肪酸中的亚油酸是前列腺素合成的前体,EFA缺乏将导致 前列腺素合成能力减退
– 动物精子的形成与EFA有关,长期缺乏EFA可导致不孕症 – EFA对X-射线引起的皮肤损伤有保护作用
• EFA缺乏的表现:可引起生长迟缓、生殖障碍、皮肤损伤 (出现皮疹等)以及肾脏、肝脏、神经和视觉方面的多种 疾病
H2C O C R3
H2C OH R1COONa HC OH + R2COONa H2C OH R3COONa
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
R
R C C H
>
H
>
RHC=CH2 >
H2C=CH2
总结:
◆双键碳上烷基越多越稳定
◆反式比顺式稳定。
氢化热的大小反映烯烃的相对稳定性。 双键碳原子上的烷基越多,烯烃越稳定。
R2C=CR2>R2C=CHR>RCH=CHR>RCH=CH2>CH2=CH2
2-甲基丙烯>反-2-丁烯>顺-2-丁烯>1-丁烯。
CH3CH2CH=CH2
CH3 C H C H CH3
㈡构型异构-顺反异构
CH3 C H C H CH3
(顺)—2—丁烯
(反)—2—丁烯的凯库勒模型
◆产生顺反异构的条件: (1)限制旋转的因素:(烷烃没有此因素,有构象异构) (2)同一个双键碳上不能连有相同的原子或基团
H H
C
C
a C b
CH3 C2H5
I > Br > Cl > S >F > N > C > H
②如果与双键碳直接相连原子的原子序数相同,则 比较其后一位原子的原子序数, 再相同,再顺次比较, 一直到比较出优先次序为止。比较时,按原子序数排 列,先比较各组中最大者;若仍相同,再依次比较。
-CH2Cl
-CHCH 3 OH
3 因为 Cl > O -CH2Cl > -CHCH OH
电负性: SP杂化碳> SP2杂化碳>SP3杂化碳 (1/2 S成份) (1/3 S成份) (1/4 S成份)
CH3 CH3 C C CH3 CH3 CH3 CH3 C C CH3 H
>
2、与酸的加成
酸中的H+ 是最简单的亲电试剂,能 与烯烃起加成反应。其反应通式如下:
C=C H-Nu C H Nu = -X -OSO3H -OH C Nu -OCOCH 3 等
1.顺式异构体有较大的密度。
H C C
Cl
2.顺式异构体有较大的溶解度。
3.顺式异构体有较高的沸点。 4.顺式异构体有较大的偶极矩。 H 5.反式异构体有较高的熔点。 6.反式异构体有较小的燃烧热。
H C C
Cl
Cl μ = 1.85
H Cl μ =0
§3 烯烃的化学性质
官能团是一类物质的代表,赋予有机化合 物特定的性质 烷烃:无官能团 烯烃:碳-碳双键、π键 ◆π键键能<σ键键能;电子云重叠程度小,易断裂。 ◆π键电子云受到亲电试剂进攻时易变形
◆烯烃加成反应的活性:双键碳上所连烷基越多 越活泼。
CH3 CH3 C C CH3 CH3 > CH3 CH3 C C CH3 H
>
CH3 CH3
CH2
CH2 < CH3CH
CH2 <
C
CH2
因为烷基有供电子作用,使π键上电子云密 度增加,利于亲电试剂的进攻。 双键碳为SP2杂化碳 烷基碳为SP3杂化碳
2,5-二甲基-2-己烯
CH3CH C=CH2 CH3 CH2CH3
3-甲基-2-乙基-1-丁烯
2.顺反异构体命名法
⑴ 顺反命名法
CH3 C H C H CH3
CH3 C H C
H
CH3
顺-2-丁烯
CH3 C H C Br Cl
反-2-丁烯
⑵ Z-E命名法(适用所有烯烃) Z、E命名法主要原则是根据“顺序规则”。 顺序规则是在表达某些立体化学关系时, 为决定 有关原子或基团的排列次序所提出的原则。 ①按直接连在双键碳上原子的原子序数大小排列,原 子序数大的排在序 列前面,称为次序优先基团;原子 序数小的排在后面,孤对电子排在氢之后。如下列原 子或基团的先后次序为:
第一节 烯 烃
一、双键的结构
1.实验现象 ① 现代物理手段测得所有原子在同一平面,每个碳原 子只和三个原子相连。键角120° ② 测键能:C—C 345.6 KJ/mol; C = C 610 KJ/mol 双键的键能不是两个单键键能之和:345.6 * 2 = 691.2 KJ/mol ③ 键长:
烯烃加成反应包括催化加氢和亲电加成反应
(一)催化加氢(催化氢化) cat H2 + RCH CH2
RCH2CH3
Cat.(Catalyst):Pt,Pd或Raney Ni(雷尼镍) 还原反应, 加氢反应机理:
CH3 CH3 H CH3 H CH3 CH3 CH3 H H H H H H H H
吸附 活泼氢原子 烯烃与被吸附 的氢原子接触
双键 同时加氢
完成加氢 脱离表面
因此:烯烃为平面分子,从烯烃双键平面的同 侧加氢,为顺式加氢 ◆氢化热:加氢反应是放热反应, 1 mol不饱和 烃催化加氢所放出的热量称为氢化热
C C + H H 435 Cat. C C
264 (611-347)
H H 2×414=828
断裂 :1个 π
1 个σ
生成: 2个σ
-CHCH 3 Cl
-CHF OH
因为 Cl > F
-CHCH 3 > -CHF Cl OH
③如果取代基是不饱和基团,则可认为与双键 或叁键碳原子直接连有两个或叁个相同的原子。如:
CH2=CH2 与 CH2-CH- 相当 C C
C=O 与 C O 相当 O
C -C CH 与 -C-C 相当 C
-C N
(二)亲电加成反应 (Electrophilic Addition Rxn) 亲电加成:亲电试剂进攻引起的加成反应为 亲电加成反应。 亲电试剂:带部分正电荷或缺电子的试剂为 亲电试剂,具有亲电子性质。
H
+
Cl
-
δ:part(部分) δ+:带部分正电荷 , δ- :带部分负电荷
1、与卤素反应
-
+
Cl
RCHCH3 Cl
符合马氏规则:不对称的烯烃与不对称试剂加成时, 氢加到连氢较多的双键碳上
◆若亲电试剂分子中不含H原子,又怎样来
表述“马氏规则”?如:
CH3 C = CH2 + OH
+
δ
+ δ δ CH3
Cl
δ
CH3 CH3 C CH2 OH Cl
不对称烯烃与极性试剂加成时,试剂中带有部分正 电荷的原子或基团总是加到带有部分负电荷的双键碳原 子上,而试剂中带有部分负电荷的原子或基团总是加到 带有部分正电荷的双键碳原子上。
烯烃的反应位置: ◆π键断裂(加成反应,氧化反应,聚合反应) ◆受碳-碳双键的影响α -氢易被取代或氧化
α-位:与官能团相连的第一个碳,为α-碳; α-碳上的氢为α-氢
α
C 2
H
C 1
C
H
H C C H
一.加成反应
H
C
C
+ X
Y
C X
C Y
x=y: H2 ;Br2 x≠y:H-Cl, HO-Cl,H-OH,(H-BH2)2 , H2SO4 次氯酸 硼烷
H3CH2C C H3 C C CH(CH3)2 CH2CH2CH3
顺-3-甲基-2-戊烯 (E)- 3-甲基-2-戊烯
(E) 3-甲基-4-异丙基-3-庚烯
5.重要的烯基:
CH 2=CH
CH 3CH=CH
CH 2=CHCH 2
乙烯基
丙烯基
烯丙基
二 烯烃的物理性质
弱极性,熔点、沸点同烷烃相似。
(一)、与烷烃相似,随着C原子数的增加而 递变 (二)、顺反异构的物理性质有如下的规律性
C
≡
c
H H
a≠ b
C
c≠ d
C
C2H5 CH3
d
三、 烯烃的命名
1、 烯烃的系统命名 (1).选择含有双键在内的最长而连续的碳链作为主链 (2).主链编号时,从距双键较近一端开始 (3).写出名称
CH3 CH3CCH=CH 2 CH3
CH3C=CHCH 2CHCH3 CH3 CH3
3, 3-二甲基-1-丁烯
B.由碳正离子反应历程解释
按反应历程,反应的第一步要生成碳正离子。 以丙烯为例,则有两种可能:
CH3 CH CH2
+
H+
CH3
CH =CH2
H+
CH3
CH
+
CH2 H
H (Ⅱ) 。 1 正离子
(Ⅰ) 。 2 正离子
反应的速率和方向往往取决于反应活性中间体生成
N 与 -C-N 相当 N
Z-E 命名原则:如果一个双键碳原子上连接的较 优基团与另一个双键碳原子上连接的较优基团在双 键同侧,其构型用Z表示,反之用E表示。
H3 C Br C C
H Cl
CH3 C H C
Cl
Br
(Z)1-氯-2-溴丙烯
H3 C C H C CH2CH3 CH3
( E)1-溴-1-氯-丙烯
电负性不同而引起整个分子电子云向电负性强的方向偏
移的效应。 分为供电子诱导效应(+I)及吸电子诱导效应(-I)
A.给电子基和吸电子基 给电子基团:电负性比氢小的,如烷基、负离子等。
-O > -C(CH 3)3 > (CH 3)2CH- > CH 3CH2- > CH 3-
吸电子基团:电负性比氢大的,如正离子、卤原子、 带氧或带氮的基团、不饱和烃基。
C
溴鎓离子
实验证据1:
CH2 CH2 + Br2 NaCl H2O CH2 CH2 Br Br + CH2CH2 Br Cl
两步反应,先生成
CH2-CH2
+
Cl
-
Br
形成环状溴鎓离子
实验证据2:
+ Br2 Br H
