门捷列夫发现元素周期律
元素周期表的历史

元素周期表的历史化学发展到18世纪,由于化学元素的不断发现,种类越来越多,反应的性质越来越复杂。
化学家开始对它们进行了整理、分类的研究,以寻求系统的元素分类体系。
一、门捷列夫发现元素周期律前对元素分类的研究⒈1789年,法国化学家拉瓦锡在他的专著《化学纲要》一书中,列出了世界上第一张元素表。
他把已知的33种元素分成了气体元素、非金属、金属、能成盐之土质等四类。
但他把一些物,如光、石灰、镁土都列入元素。
⒉1829年,德国化学家德贝莱纳(Dobereiner,J.W.1780-1849)根据元素的原子量和化学性质之间的关系进行研究,发现在已知的54种元素中有5个相似的元素组,每组有3种元素,称为“三元素组”,如钙、锶、钡、氯、溴、磺。
每组中间一种元素的原子量为其它二种的平均值。
例如,锂、钠、钾,钠的原子量为(69+39.1)/2=23。
⒊1862年,法国的地质学家尚古多(Chancourtois,A.E.B.1820-1886)绘出了“螺旋图”。
他将已知的62个元素按原子量的大小次序排列成一条围绕圆筒的螺线,性质相近的元素出现在一条坚线上。
他第一个指出元素性质的周期性变化。
⒋1863年,英国的化学家纽兰兹(Newlands,J.A.R.1837-1898)排出一个“八音律”。
他把已知的性质有周期性重复,每第八个元素与第一个元素性质相似,就好象音乐中八音度的第八个音符有相似的重复一样。
二、元素周期律的发现1869年3月,俄国化学家门捷列夫(1834-1907)公开发表了论文《元素属性和原子量的关系》,列出了周期表,提出了元素周期律——元素的性质随着元素原子量的递增而呈周期性的变化。
他在论文中指出:“按照原子量大小排列起来的元素,在性质上呈现明显的周期性。
”“原子量的大小决定元素的特征。
”“无素的某些同类元素将按他们原子量的大小而被发现。
”1869年12月,德国的化学家迈耶尔(Meyer,J.L.1830-1895)独立地发表了他的元素周期表,明确指出元素性质是它们原子量的函数。
元素周期律知识点总结

元素周期律知识点总结一、元素周期律的发现历程元素周期律是指化学元素按照一定规律排列的周期表。
在19世纪末,俄国化学家门捷列夫发现了元素周期律的规律,他将元素按照原子量的大小排列,发现了一些规律性的现象,比如元素的性质会随着原子量的增大而周期性地变化。
这一发现为后来的元素周期表的建立奠定了基础。
二、元素周期律的基本规律1. 原子序数元素周期律是根据元素的原子序数所排列的。
原子序数是指元素原子核中质子的数量,也是元素在周期表中的位置。
原子序数的增大决定了元素的性质的变化。
2. 周期性元素周期律的核心规律是周期性。
即元素的性质会随着原子序数的增大而周期性地变化。
这一规律可以用周期表中元素的位置来很好地解释。
3. 周期性表现元素周期律的周期性表现在以下方面:(1)元素的化学性质:比如金属元素和非金属元素的相互转变,电子亲和力、电负性等性质的周期变化。
(2)物理性质:原子半径、离子半径、电离能等。
(3)氧化物的性质:比如元素氧化物与水的反应性随着周期的增加而发生变化。
(4)化合价:元素的化合价随周期性地增加而变化。
三、周期表的结构元素周期表是由俄国化学家门捷列夫在1869年发现的,现在该表是由7行18列组成。
其中,横着排列的称为周期,纵向排列的称为族。
周期表的左侧是金属元素,右侧是非金属元素,中间是过渡元素。
周期表中有主族元素、副主族元素、过渡元素和稀有元素等。
四、周期表中的规律1. 周期性规律周期表中最基本的规律就是原子量的周期性变化。
比如,原子序数为3、11、19、37、55等元素的性质非常相似,因为它们在同一个周期内。
这些元素的外层电子数相同,因此具有相似的化学性质。
这一规律逐渐得到了发展,形成了更加完备的元素周期律。
2. 周期表的周期性规律周期表中的元素周期性地排列,列代表着元素的性质与它们的电子排布有关。
比如,同一族元素的外层电子数相同,因此它们的化学性质会有相似之处。
周期表中元素的周期性变化也与元素的原子结构有关,因为原子的结构决定了元素的性质。
化学元素周期律及其应用

化学元素周期律及其应用化学是探究物质结构和化学反应规律的学科。
化学元素是化学研究的基础,而元素周期律是我们了解化学元素和其规律的关键。
元素周期律的发现和发展1869年,俄罗斯化学家门捷列夫发现了元素周期律,并将元素按照其原子量和阶数分别放在周期表的同一行和同一列中。
随着科学技术的发展,逐渐发现新元素,而新元素的发现和周期表的不断完善推动了元素周期律的进一步发展。
目前,元素周期表已知元素118种。
元素周期律按照原子序数排列元素,并按照其电子构型将元素分为周期性的数值。
元素的电子数目决定了其物理和化学性质。
周期表中周期数即是原子轨道能级的数目,而周期表中同周期的元素的化学性质有一定的相似性。
元素周期律的应用元素周期律的应用非常广泛。
一个常见的用法是预测物质的化学性质。
通过周期律,我们可以预测具有相同电子构型的原子的化学行为往往相似。
例如,氧、硫和硒等元素都属于同一周期中,它们的化学性质都有一些相似之处,例如酸碱反应和氧化还原反应。
周期表也可以用来预测元素的物理性质。
例如,元素周期表的上方为金属,下方为非金属。
金属的特点是高导电性和高热传导性,而非金属则通常是非导体或半导体。
多个元素周期表上相邻的分析元素通常在许多方面也是物理相似的,例如电离能和原子半径。
元素周期律还可以用于设想新材料的组成,研究电子能带等。
最近几十年来,周期表的应用已经扩展到纳米科技、生物学、医学、材料科学、能源行业、环境科学、计算机科学等诸多领域。
对于研究人员和设计人员而言,元素周期律是一种强大的科学工具,可以用来预测或合成新能源、新材料和新工艺的创新思路。
此外,元素周期律还在化学教育中发挥着重要作用。
它帮助学生更好地了解化学并推动教育的发展。
孩子们可以通过自己的实践、科学活动和化学实验,体验到化学色彩丰富的世界。
总结元素周期表是研究化学元素和其规律的基础。
使用元素周期表,我们可以更好地理解元素的化学性质和物理性质,为各种类型的研究领域和工作提供新的思考方式和方法。
元素周期表的起源和应用

4f3 6s2 60 Nd 4f4 6s2 61 Pm 4f5 6s2 62 Sm 4f6 6s2 63 Eu 4f7 6s2 64 Gd
1 H 1s1 2 He 1s2 3 Li 2s1 4 Be 2s2 5 B 2s2 2p1 6 C 2s2 2p2 7 N 2s2
2p3 8 O2s2 2p4 9 F 2s2 2p5 10 Ne 2s2 2p6 11 Na 3s1 12 Mg 3s2 13 Al
4p3 34 Se 4s2 4p4 35 Br 4s2 4p5 36 Kr 4s2 4p6 37 Rb 5s1 38 Sr 5s2 39
Y 4d1 5s2 40 Zr 4d2 5s2 41 Nb 4d4 5s1 42 Mo 4d5 5s1 43 Tc 4d5 5s2 44
4f7 5d1 6s2 65 Tb 4f9 6s2 66 Dy 4f10 6s2 67 Ho 4f11 6s2 68 Er 4f12 6s2
69 Tm 4f13 6s2 70 Yb 4f14 6s2 71 Lu 4f14 5d1 6s2 72 Hf 5d2 6s2 73 Ta
A:质量数 (Mass number) ,即在数量上等于原子核(质子加中子)的粒子数目。 Z:原子序数,即是质子的数目。由于它是固定的,一般不会标示出来。
e:净电荷,正负号写在数字后面。
n:原子数目,元素在非单原子状态(分子或化合物)时的数目。除此之外,部份较高级的周期表更会列出元素的电子排布、电负性和价电子数目。
钕(nǚ) 61 钷(pǒ) 62 钐(shān) 63 铕(yǒu) 64 钆(gá) 65 铽(tè) 66 镝(dī) 67 钬(huǒ) 68
元素周期律知识点总结

元素周期律知识点总结1.元素周期律的历史:元素周期表最早由俄罗斯化学家门捷列夫发现,他将已知的元素按照重量递增的顺序进行排列,并注意到一些元素会在一定的重复间隔后再次出现,从而提出了元素周期性的概念。
后来,英国化学家门德里耶夫将元素按照电子结构进行排列,更加完善了元素周期表。
2.元素周期表的结构:元素周期表由横行称为周期,纵列称为族。
周期表中的元素按照原子序数递增排列,每个周期分为两个部分:s区和p区。
s区第一个元素是碱金属,最后一个元素是碱土金属,p区的最后一位元素是卤素。
3.原子序数和原子量:原子序数是元素周期表中每个元素的唯一标识,表示原子核中的质子数量。
原子序数从左到右递增,每增加一个元素,质子数量增加一、原子量是元素中质子和中子的总和,它的单位是原子质量单位(amu)。
4.周期表中的元素周期性:元素周期表的最重要特征之一是元素周期性,即元素性质随着原子序数的增加而周期性变化。
例如,原子半径和离子半径在一个周期内是递减的,而在一个族内则是递增的。
5.元素的分类:元素可以按照性质和位置进行分类。
按性质分类,元素可以分为金属、非金属和半金属。
按位置分类,元素可以分为主族元素、过渡金属和稀土金属。
6.周期表的块:周期表分为s区、p区、d区和f区。
s区包含1A和2A族元素,它们容易失去或共享一个或两个电子成为正离子。
p区包含3A到8A族元素,它们容易获得电子成为负离子。
d区包含过渡金属元素,它们填充在外层d轨道上的电子。
f区包含稀土金属元素,它们填充在内层f轨道上的电子。
7.周期表的周期性规律:周期表中的元素具有许多周期性规律。
其中一些重要的规律包括:-电离能:元素失去一个电子所需的能量。
电离能在周期内是递增的,而在一个族内是递减的。
-电负性:元素吸引和结合电子的能力。
电负性在周期内递增,而在一个族内递减。
-原子半径:元素原子的大小。
原子半径在周期内是递减的,在一个族内是递增的。
-金属性和非金属性:金属元素在左侧,非金属元素在右侧。
门捷列夫是怎样发现元素周期律的

门捷列夫是怎样发现元素周期律的门捷列夫是化学上不容忽视的人物,他提出的元素周期律是化学上重要的发现之一。
他的周期表告诉我们关于元素的结构和化学性质的基本信息。
本文将重点介绍门捷列夫是如何发现元素周期律的。
门捷列夫的早期工作门捷列夫出生于1834年,他早年的教育得到的是传统的化学知识,既是实验又是理论。
他通过工作变成了专业的化学家。
他开始研究化学中的定量关系,这些定量关系是许多反应中的重要组成部分。
他进一步将这些设计建立在一些基本假设上。
门捷列夫在他的定量关系的研究中发现了一些有趣的事情,这些事情导致了他对元素周期律的兴趣。
例如,他发现一些元素的性质与它们的分子量之间存在某种比例关系。
他发现基于元素的原子量,每个元素都有一些特定的化学性质。
在同一行或同一列中,他发现元素的性质也是类似的。
门捷列夫的周期律在他的研究中,门捷列夫提出了一种元素排列方式,这种排列方式使相似的元素出现在一起。
他通过将元素按照原子量逐一排列,然后根据相似性将它们分类,他发现了元素的周期律。
门捷列夫的周期表显示,元素是由原子质量逐渐增加而排列的。
然后,他将元素组成周期性表,以使相似元素出现在表中的同一行或同一列中。
此表充满了关于元素的结构和化学性质的信息,这意味着化学反应可以预测和理解。
例如,周期表的排列方式可以用来预测新元素的性质。
门捷列夫周期表的成功门捷列夫的周期表在当时的化学界引起了广泛的讨论,很快就得到了很多化学家的认可。
门捷列夫的周期表被证明是一个非常有用的工具,因为它可以用来预测化学反应以及新元素的性质。
随着时间的推移,门捷列夫的周期表逐渐得到了完善。
化学家们逐渐了解到,元素的周期性取决于它们的原子结构。
元素周期表的成功的一个关键因素是化学家们对元素结构的理解的提高。
总结门捷列夫的发现引起了化学界的轰动。
他发现的元素周期律是化学中最基本的规律之一。
他的工作为其他化学家提供了一个框架,他们可以使用门捷列夫的周期表来解决许多化学问题。
化学元素周期律(最新整理)
19 K 20 Ca 21 Sc 22 Ti 23 V 24 Cr 25 Mn 26 Fe 27 Co 28 Ni 29 Cu 30 Zn 31 Ga 32 Ge 33 As 34 Se 35 Br 36 Kr
4钾
钙 钪 钛
钒
铬
锰
铁
钴
镍
铜
锌镓锗砷 硒
溴
氪
39.098 40.08 44.956 47.9 50.9415 51.996 54.938 55.84 58.9332 58.69 63.54 65.38 69.72 72.5 74.922 78.9 79.904 83.8
57 La 镧
镧 系
138.905
58 Ce 铈
140.12
59 Pr 镨
140.91
60 Nd 钕
144.2
61 Pm 钷 147
89 Ac 锕
锕 系
227.03
90 Th 钍
232.04
91 Pa 镤
231.04
92 U 铀 238.03
93 Np 镎
237.05
62 Sm 钐
150.4 94 Pu
ⅠA ⅡA ⅢB ⅣB ⅤB
ⅥB
ⅦB
Ⅷ
ⅠB ⅡB ⅢA ⅣA ⅤA ⅥA ⅦA
0Байду номын сангаас
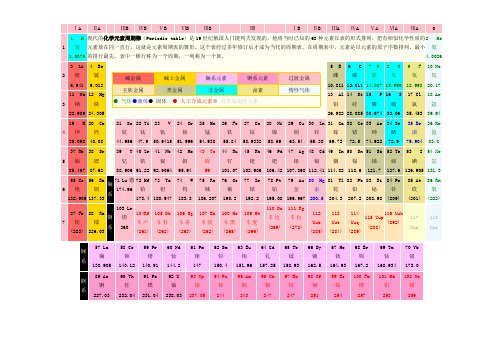
1 H 现代的化学元素周期律(Periodic table)是 19 世纪俄国人门捷列夫发现的。他将当时已知的 63 种元素以表的形式排列,把有相似化学性质的 2 He
1 氢 元素放在同一直行,这就是元素周期表的雏形。这个表经过多年修订后才成为当代的周期表。在周期表中,元素是以元素的原子序数排列,最小 氦
科学家门捷列夫

门捷列夫
生平简介:
德米特里〃门捷列夫,19世纪俄国化学家,他发现了 元素周期律,(但是真正第一位发现元素周期律的是 纽兰兹,门捷列夫是后来经过总结,改进得出现在使 用的元素周期律的),并就此发表了世界上第一份元 素周期表。1907年2月2日,这位享有世界盛誉的俄 国化学家因心肌梗塞与世长辞,那一天距离他的73岁 生日只有六天。他的名著、伴随着元素周期律而诞生 的《化学原理》,在十九世纪后期和二十世纪初,被 国际化学界公认为标准著作,前后共出了八版,影响 了一代又一代的化学家。
门捷列夫
研究领域:
1、化学,特别是无机化学、物理化学 2、门捷列夫除了发现元素周期律外,还研究过气体定律、气象学、石油工业、 农业化学、无烟火药、度量衡,由于他的辛勤劳动,在这些领域都不同程度地 做出了成绩。
最大贡献:
门捷列夫对化学这一学科发展最大贡 献在于发现了化学元素周期律。他在 批判地继承前人工作的基础上,对大 量实验事实进行了订正、分析和概括 ,总结出这样一条规律:元素(以及 由它所形成的单质和化合物)的性质 随着原子量(现根据国家标准称为相 对原子质量)的递增而呈周期性的变 化,既元素周期律。他根据元素周期 律编制了第一个元素周期表,把已经 发现的63种元素全部列入表里,从而初步完成了使元素系统化的任务。他还 在表中留下空位,预言了类似硼、铝、硅的未知元素(门捷列夫叫它类硼、 类铝和类硅,即以后发现的钪、镓、锗)的性质,并指出当时测定的某些元 素原子量的数值有错误。而他在周期表中也没有机械地完全按照原子量数值 的顺序排列。若干年后,他的预言都得到了证实。门捷列夫工作的成功,引 起了科学界的震动。人们为了纪念他的功绩,就把元素周期律和周期表称为 门捷列夫元素周期律和门捷列夫元素周期表。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
门捷列夫发现元素周期律
到1869年止,已有63种元素被人们所认识。
进一步寻找新元素成为当时化学家最热门的课题。
但是地球上究竟有多少元素?怎样去寻找新的元素?却没有人能作比较科学的回答。
寻找新元素的工作也固缺乏正确的理论指导,而带有很大的盲目性,常常白白地耗费了许多精力。
在对物质、元素的广泛研究中,关于各种元素的性质的资料,积累日愈丰富,但是这些资料却是繁杂纷乱的,人们很难从中获得清晰的认识。
整理这些资料,概括这些感性知识,从中摸索总结出规律,这是摆在当时化学家面前一个急待解决的课题,同时也是科学和生产发展的必然要求。
在这样的科学背景下,从事元素分类工作和寻找元素之间内在联系的许多化学家,经过长期的共同努力,取得了一系列研究成果,其中最辉煌的成就是俄国化学家门捷列夫和德国化学家迈尔先后发现的化学元素周期律。
化学元素周期律的发现
道尔顿提出了科学的原子论后,许多化学家都把测定各种元素的原子量当作一项重要工作,这样就使元素原子量与性质之间存在的联系逐渐展露出来,1829年德国化学家德贝莱纳提出了“三元素组”观点,把当时已知的44种元素中的15种,分成5组,指出每组的三元素性质相似,而且中间元素的原子量等于较轻和较重的两个元素原子量之和的一半。
例如钙、锡、钡,性质相似,铬的原子量大约是钙和钡的原子量之和的一半。
氯、溴、碘以及银、钠、钾等元素也有类似的关系。
然而只要认真一点,就会发现这样分类有许多不能令人满意的地方,所以并没有引起化学家们的重视。
1862年,法国化学家尚古多提出一个“螺旋图”的分类方法。
他将已知的62种元素按原子量的大小顺序标记在绕着圆柱体上升的螺旋线上,这样某些性质相近的元素恰好出现在同一母线上。
因此他第一个指出了元素性质的周期性变化。
可是他的报告照样无人理睬。
1864年,德国化学家迈尔在他的《现代化学理论》一书中刊出一个“六元素表”。
可惜他的表中只列出了已知元素的一半,但他已明确地指出:“在原子量的数值上具有一种规律性,这是毫无疑义的”。
1865年,英国化学家纽兰兹提出了“八音律”一说。
他把当时已知的元素按原子量递增顺序排列在表中,发现元素的性质有周期性的重复,第八个元素与第一个元素性质相近,就好像音乐中八音度的第八个音符有相似的重复一样。
纽兰兹的工作同样被否定,当时的一些学者把八音律斥之为幼稚的滑稽戏,有人甚至挖苦说:“为什么不按元素的字母顺序排列呢?那样,也许会得到更加意想不到的美妙效果。
”“六元素表”、“八音律”是存在许多错误,但是应该看到,从三元素组”到“八音律”都从不同的角度,逐步深入地探讨了各元素间的某些联系,使人们一步步逼近了科学的真理。
以前人工作所提供的借鉴为基础,门捷列夫通过顽强努力的探索,于1869年2月先后发表了关于元素周期律的图表和论文。
在论文中,他指出:
(1)按照原子量大小排列起来的元素,在性质上呈现明显的周期性。
(2)原子量的大小决定元素的特征。
(3)应该预料到许多未知元素的发现,例如类似铝和硅的,原子量位于65一75之间的元素。
(4)当我们知道了某些元素的同类元素后,有时可以修正该元素的原子量。
这就是门捷列夫提出的周期律的最初内容。
门捷列夫深信自己的工作很重要,经过继续努力,1871年他发表了关于周期律的新的论文。
文中他果断地修正了1869年发表的元素周期表。
例如在前一表中,性质类似的各族是横排,周期是竖排;而在新表中,族是竖排,周期是横排,这样各族元素化学性质的周期
性变化就更为清晰。
同时他将那些当时性质尚不够明确的元素集中在表格的右边,形成了各族元素的副族。
在前表中,为尚未发现的元素留下4个空格,而新表中则留下了6个空格。
由此可见,门捷列夫的研究有了重要的进展。
经受实践的验证
实践是检验真理的唯一标准。
门捷列夫发现的元素周期律是否能站住脚,必须看它能否解决化学中的一些实际问题。
门捷列夫以他的周期律为依据,大胆指出某些元素公认的原子量是不准确的,应重新测定,例如当时公认金的原子量为169.2,因此,在周期表中,金应排在饿、铱、铂(当时认为它们的原子量分别是198.6、196.7、196.7)的前面。
而门捷列夫认为金在周期表中应排在这些元素的后面,所以它们的原子量应重新测定。
重新测定的结果是:饿为190.9,铱为193.1,铂为195,2,金为197.2。
实验证明了门捷列夫的意见是对的。
又例如,当时铀公认的原子量是116,是三价元素。
门捷列夫则根据铀的氧化物与铬、铂、钨的氧化物性质相似,认为它们应属于一族,因此铀应为六价,原子量约为240。
经测定,铀的原子量为238.07。
再次证明门捷列夫的判断正确。
基于同样的道理,门捷列夫还修正了铟、镧、钇、铒、铈的原子量。
事实验证了周期律的正确性。
根据元素周期律,门捷列夫还预言了一些当时尚未发现的元素的存在和它们的性质。
他的预言与尔后实践的结果取得了惊人的一致。
1875年法国化学家布瓦博德朗在分析比里牛斯山的闪锌矿时发现一种新元素,他命名为镓,并把测得的关于它的主要性质公布了。
不久他收到了门捷列夫的来信,门捷列夫在信中指出关于镓的比重不应该是4.7,而是5.9一6.0。
当时布瓦傅德朗很疑惑,他是唯一手里掌握金属镓的人,门捷列夫是怎样知道它的比重的呢?经过重新测定,镓的比重确实为5.9。
这结果使他大为惊奇。
他认真地阅读了门捷列夫的周期律论文后,感慨他说:“我没有可说的了,事实证明门捷列夫这一理论的巨大意义。
”下表是个最有力的说明:
类铝镓
原子量69 69.72
比重 5.9-6.0 5.94
熔点低30.1
和氧气反应不受空气的侵蚀灼热时略起氧化
灼热时能分解水汽灼热时确能分解水汽
能生成类似明矾的矾类能生成结晶较好的镓矾
可用分光镜发现其存在用分光镜发现的
镓的发现是化学史上第一个事先预言的新元素的发现,它雄辩地证明了门捷列夫元素周期律的科学性。
1880年瑞典的尼尔森发现了钪,1885年德国的文克勒发现了锗。
这两种新元素与门捷列夫预言的类硼、类硅也完全吻合。
门捷列夫的元素周期律再次经受了实践的检验。
事实证明门捷列夫发现的化学元素周期律是自然界的一条客观规律。
它揭示了物质世界的一个秘密,即这些似乎互不相关的元素间存在相互依存的关系,它变成了一个完整的自然体系。
从此新元素的寻找,新物质、新材料的探索有了一条可遵循的规律。
元素周期律作为描述元素及其性质的基本理论有力地促进了现代化学和物理学的发展。
