总甲状腺素(TT4)校准品产品技术要求华科泰
总甲状腺素测定试剂盒(磁微粒化学发光免疫分析法)产品技术要求rejing

总甲状腺素测定试剂盒(磁微粒化学发光免疫分析法)
适用范围:用于体外定量测定人血清、血浆样本中总甲状腺素(TT4)的含量。
1.1包装规格:
A型:60人份/盒,100人份/盒;
B型:100人份/盒。
1.2 主要组成成分:
校准品靶值批特异,详见标签。
2.1 外观
试剂盒外观应整洁,文字符号标识清晰、内容完整;液体组分无沉淀或絮状物。
2.2 准确度
检测购自中国食品药品检定研究院甲状腺素(T4)国家标准品(编号:150551),其测量结果与理论值之比应在0.850-1.150之间。
2.3空白限
试剂盒空白限应不高于10ng/mL。
2.4 线性
在[10,240]ng/mL范围内,相关系数应不低于0.9900。
2.5 精密度
2.5.1 测定高、低两个水平的样本,批内变异系数(CV)应不大于8.0%。
2.5.2 测定高、低两个水平的样本,批间变异系数(CV)应不大于15.0%。
2.6 特异性
表1 与其它物质的交叉反应
2.7 溯源性
根据GB/T 21415有关规定提供校准品的来源、溯源过程及测量不确定度等内容,溯源至中国食品药品检定研究院甲状腺素(T4)国家标准品(编号:150551)。
2.8校准品开封稳定性
采用开封15天后的校准品,重新校准曲线,检测准确度,结果应符合上述2.2的要求。
2.9 稳定性
2℃~8℃保存12个月,取到效期后两个月内的产品进行检测,测定结果应符合上述2.2、2.3、2.4、2.5.1、2.8的要求。
甲状腺素(T4)作业指导书

校准品:
Cal 1 定标液(白盖),2瓶,1ml/瓶,T4的浓度约为50nmol/l,牛血清, 含防腐剂
Cal 2 定标液(黑盖),2瓶,1ml/瓶,T4的浓度约为230nmol/l,牛血清,含防腐剂
Elecsys1010或2010、e411分析仪所需耗品:
Elecsys 系统缓冲液(ProCell)货号11662988
Elecsys测量池清洗液(CleanCell)货号11662970
Elecsys 添加剂液(SysWash)货号11930346
Elecsys 系统清洗液(SysClean)货号11298500
6.质量控制
Elecsys 通用质控品(PreciControl)1和2。质控品1和质控品2至少每24小时或每一次定标后测定一次。质控间隔期应适用于各实验室的具体要求。检测值应落在确定的范围内,如出现质控值落在范围以外,应采取校正措施。
7.计算方法
对每一个标本,仪器会自动计算TSH的含量,单位是nmol/l、μg/dl。
5.1 校准操作步骤:
在编缉各项目的参数时,已经在Application—Calib菜单中定义好了定标类型和几点定标。因此在对各项目进行定标时,只需在定标菜单Calibration中进行即可。进入Calibration—Status菜单,用鼠标选择需定标的项目,再根据需要点单点定标(BLANK键)或两点定标(TWO POINT键)、跨距定标(SPAN键)、多点定标(FULL键),再选择其它项目进行相应选择,最后点SAVE,将定标物放入在Calibration—Calibrator中定义好的位置,点Start,再点Start,仪器开始定标。
T4 甲状腺素化学发光试剂盒使用说明书

T4甲状腺素化学发光试剂盒使 用 说 明 书济南杏恩生物科技有限公司T4甲状腺素化学发光试剂盒说明书【临床意义】通过化学发光酶免疫法定量分析人血清或血浆中的总T4甲状腺素(Total Thyroxine,tT4)的浓度。
T4增高见于甲抗、T4型甲抗、亚急性甲状腺炎、高TBG血症、甲状腺激素不敏感综合症;减低见于甲减、地方性甲状腺肿、慢性淋巴性甲状腺肿、甲亢治疗期、严重肝病、TBG降低。
【原理】 酶免疫分析测试【试剂存放方式】(所有试剂保存在2-8℃)【试剂盒组成】1. T4 包被板:1板,可拆板,8×12孔。
2. T4 标准品: 6小管,0.3ml/管3. 各个标准品浓度分别为0, 2,5,10,15,25 ug/dl。
4. 浓缩的 T4 标记偶合液(11×):1小管,0.5ml/管。
5. T4 偶合稀释液:1瓶,5ml/瓶。
6. T4低质控对照品:0.3ml/管7. T4高质控对照品:0.3ml/管8. 发光底物 1:5ml/瓶,含有H2O2的缓冲液。
9. 发光底物 2:5ml/瓶,含有发光触酶的缓冲液。
10. 产品说明书一份。
适用机器: 国内外所有板式化学发光仪 .【样本采集】本测试的样品为血清或血浆。
样品可保存在2-8℃下48小时,如需长期保存需冷冻在-20℃。
样品在解冻后需混合均匀后再进行测试简易操作步骤样品化学发光标记偶合液反应时间 15分钟 (室温25+/-2度)洗板Mediators PHL TM 选定程序 机器自动加底液发光底物1反应时间5分钟(室温25+/-2度发光底物2立即测读(1秒钟之内)计算样品浓度。
总甲状腺素(TT4)测定试剂盒(电化学发光免疫分析法)产品技术要求lztk

总甲状腺素(TT4)测定试剂盒(电化学发光免疫分析法)适用范围:本试剂盒用于体外定量测定人体血清样本中总甲状腺素(TT4)的含量。
1.1产品型号/规格:100人份/盒、200人份/盒。
1.2主要组成试剂盒由磁分离试剂(M)、试剂a(Ra)、试剂b(Rb)和定标品(TT4-Cal)(选配)组成。
组成及含量如下:2.1 外观2.1.1 试剂盒各组分应齐全、完整、液体无渗漏;2.1.2 磁分离试剂摇匀后应为棕色含固体微粒的均匀悬浊液,无明显凝集、无絮状物;2.1.3 其它液体组分应澄清,无异物,沉淀物或絮状物;2.1.4 包装标签应清晰、无磨损、易识别。
2.2 空白限应不大于0.420μg/dL 。
2.3 准确度用T4国家标准品(150551)进行检测,实测值与理论值之比应在0.850-1.150之间。
2.4 线性在[1.0,24.86]μg/dL范围内,线性相关系数的绝对值(|r|)应不小于0.9900。
2.5 精密度2.5.1 分析内精密度在试剂盒的线性范围内,浓度为(5.0±1.0μg/dL)和(20.0±4.0μg/dL)的样品检测结果的变异系数(CV)应不大于8%。
2.5.2 批间精密度在试剂盒的线性范围内,用3个批号试剂盒分别检测浓度为(5.0±1.0μg/dL)和(20.0±4.0μg/dL)的样品,检测结果的变异系数(CV)应不大于15%。
2.6 特异性2.6.1与三碘甲状腺原氨酸(T3)测定浓度不低于500ng/mL的T3样品,其测定结果应不高于1.5μg/dL;2.6.2 与反三碘甲状腺原氨酸(rT3)测定浓度不低于50ng/mL的rT3样品,其测定结果应不高于1.5μg/dL。
2.7 效期末稳定性本产品效期为15个月,试剂盒在2~8℃下保存至有效期末进行检测,检测结果应符合2.1、2.2、2.3、2.4、2.5.1的要求。
2.8 溯源性依据GB/T21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求,校准品溯源至国家标准品(编号150551)。
总甲状腺素(TT4)测定试剂盒(化学发光免疫分析法)产品技术要求kr

总甲状腺素(TT4)测定试剂盒(化学发光免疫分析
法)
2.1外观和性状
试剂盒各组分应齐全、完整、液体无渗漏;包装标签应清晰,准确、牢固;R1 组分应为棕色含固体微粒的液体,无板结、无絮状物。
R2 和R3 组分应为清澈透明的液体,无沉淀、无悬浮物、无絮状物。
2.2装量
应不少于试剂瓶的标示装量值。
其中R1≥5.6mL,R2≥6.0mL,R3≥6.0mL。
2.3准确性
用T4 国家标准品配制成与试剂盒对应校准品定标曲线中相应的5 个浓度点进行分析测定,用双对数或其他适当的数学模型拟合,要求两条剂量-反应曲线不显著偏离平行(t 检验);以T4 国家标准曲线为对照,试剂盒定标曲线校准品的实测值与标示值的效价比在0.900~1.100 之间。
2.4最低检出限
最低检出限应不大于0.5 μg/dL。
2.5线性
试剂盒在0.5-24 μg/dL 区间内,其相关系数(r)应不低于0.9900。
2.6重复性
变异系数CV 应≤ 8%。
2.7批间差
变异系数CV 应≤ 15%。
2.8特异性
浓度不低于500ng/mL 的TT3,检测结果应不高于15.0ng/mL。
浓度不低于50ng/mL 的rT3,检测结果应不高于最低检出限。
甲状腺功能复合定值质控品产品说明书 (3)

甲状腺功能复合定值质控品产品说明书
以下是甲状腺功能复合定值质控品的产品说明书:
产品名称:甲状腺功能复合定值质控品
产品型号:XXXXXXXX(根据具体产品而定)
生产商:XXXXXXXX(根据具体产品而定)
产品介绍:
甲状腺功能复合定值质控品是一种用于评估甲状腺功能检测方法准确性的标准物质。
该产品包含了各种甲状腺相关的生化指标,如TSH、T3、T4等,具有稳定性好、准确性高的特点。
产品特点:
1. 稳定性好:甲状腺功能复合定值质控品经过严格的制备工艺,能够保持长期的稳定性,确保每次使用的结果准确可靠。
2. 准确性高:该产品与国际标准物质进行比对,保证了结果的准确性。
3. 使用方便:甲状腺功能复合定值质控品提供了详细的使用说明,操作简便,适用于各种甲状腺功能检测方法。
适用范围:
甲状腺功能复合定值质控品适用于各种临床实验室、检验机构以及医疗机构中进行甲状腺功能检测方法的质量控制和准确性评估。
可以用于监测各种甲状腺功能检测方法的日常检测结果是否准确,并提供比对结果。
注意事项:
1. 请按照使用说明书中的指导操作,确保结果的准确性。
2. 在使用前,请检查产品的外观是否完好,如果有破损或其他异常情况,请勿使用。
3. 请在规定的温度和时间范围内存储该产品,避免受潮或高温等情况。
以上是甲状腺功能复合定值质控品的产品说明书,如有其他需要,请联系生产商进行咨询。
总甲状腺素(T4)测定试剂盒(化学发光免疫分析法)产品技术要求mairui
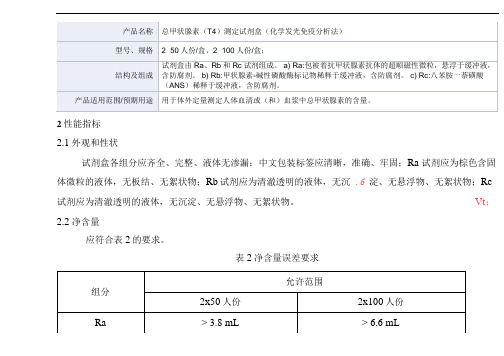
2性能指标
2.1外观和性状
试剂盒各组分应齐全、完整、液体无渗漏;中文包装标签应清晰,准确、牢固;Ra 试剂应为棕色含固体微粒的液体,无板结、无絮状物;Rb试剂应为清澈透明的液体,无沉.6 淀、无悬浮物、无絮状物;Rc 试剂应为清澈透明的液体,无沉淀、无悬浮物、无絮状物。
Vt;
2.2净含量
应符合表2的要求。
表2净含量误差要求
2.3准确度
对由国家标准品制备的两个浓度水平的正确度控制品进行检测,检测结果与标定浓度的相对偏差应在±10%范围内。
2.4最低检测限
应不大于0.5卩g/dL。
2.5线性
试剂盒在1卩g/dL〜30卩g/dL范围内,其相关系数(r)应不低于0.9900□
2.6重复性
变异系数CV应<10%0
2.7批间差
变异系数CV应<10%o
2.8分析特异性
当样品中甘油三酯浓度与1800 mg/dL,胆红素浓度匕10 mg/dL,血红蛋白浓度%500 mg/dL时,测试结果的干扰偏差在±10%范围内。
样品中反T3浓度为100卩g/dL时,交叉反应率应<10%,当样品中L-三碘甲状腺氨酸浓度为500卩g/dL, —碘酪氨酸浓度为5000卩g/dL,二碘酪氨酸浓度为5000 gg/dL时,交叉反应率应<3%o。
总甲状腺素(Total T4)标准操作规程

总甲状腺素(Total T4)标准操作规程1.【实验目的】为了保证总甲状腺素(Total T4)测定结果的准确性,以及可靠性。
2.【职责】2.1 实验室工作人员均应熟知并严格遵守本SOP,室负责人监督落实。
2.2 本SOP的改动,可由任一使用本SOP的工作人员提出,并报经下述人员批准签字:室负责人、科主任。
3.【样品类型及实验前准备】3.1 样本类型:血清和血浆,稳定性:如果检测时间超过24小时,则将血清或血浆从凝集物,血清分离器或红细胞中取出。
2-8℃可稳定6天,如需存放大于6天时,请于-20℃或更低的温度下保存。
3.2 患者准备:实验前正常饮食,晨起空腹,安静状态下抽取静脉血,条件特殊情况下可非空腹抽血检测。
3.3 容器,添加剂类型:血清(包括在血清分离器管中采集的血清),血浆(EDTA三钾、肝素锂、肝素钠),使用玻璃管或塑料管分离样本。
3.4 仪器设备:雅培ARCHITECT i1000SR, 低速离心机3.5 实验试剂:试剂盒(6C49)3.5.1.1 ARCHITECT Total T4(绵羊)包被的磁性微粒子抗T4T3吖啶标志物结合物3.5.1.2其他试剂:激发液、预激发液、清洗缓冲液(需另行配置)3.5.2校准品:名称:美国雅培i1000SR 总T3校准品 LIST NO.: 6C49--01规格:CAL 1: 0.0 (μg/dL) 1LX4ml CAL 2: 18.0 (μg/dL) 1LX4ml 3.5.3质控品名称:美国雅培i1000SR T4质控品 LIST NO:6C49-10水平浓度范围体积质控L 4.2 μg/dL 2.73 - 5.43 μg/dL 8ml质控M 7.4 μg/dL 5.44 - 9.92μg/dL 8ml 质控H 14.6 μg/dL 9.93 - 19.71μg/dL 8ml4.【实验原理】Architect i1000SR 总T4是采用化学发光微粒子免疫分析(ChemiluminesentMicroparticle ImmunoAssay, CMIA)技术,竞争两步法对人血清和血浆中的甲状腺素(总T4)进行定量检测。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
总甲状腺素(TT4)校准品
组成:
总甲状腺素(TT4)校准品S0-S5,校准品S0含添加0.1%生物防腐剂的牛血清,校准品S1-S5为在含0.1%生物防腐剂的牛血清中添加总甲状腺素(TT4)抗原。
适用范围:总甲状腺素(TT4)校准品与本公司总甲状腺素(TT4)测定试剂盒(磁微粒化学发光法)配套使用,用于人血清中总甲状腺素(TT4)测定系统的校准。
2.1 外观
校准品包装标签应清晰,无磨损;呈澄清透明的液体,无沉淀或絮状物,液体无渗漏。
2.2 装量
装量应不少于标示值。
2.3 溯源性
根据GB/T 21415-2008的有关规定,提供所用校准品的来源、赋值过程及测量不确定度等内容,溯源至中国食品药品检定研究院提供的国家标准品(编号:150551)。
2.4 准确度
检测中国食品药品检定研究院所提供的标准品(编号:150551),其测量结果的相对偏差应在±10%范围内。
2.5 均匀性
2.5.1 瓶内均匀性
各浓度点(除零外),变异系数(CV)应不高于10%。
2.5.2 瓶间均匀性
各浓度点(除零外),变异系数(CV)应不高于15%。
2.6 稳定性
2.6.1 首次开封后稳定性
校准品开瓶后,2℃~8℃储存,有效期15天,在效期内赋值结果的变化趋势不显著。
2.6.2 效期稳定性
校准品原包装2℃~8℃储存,有效期12个月,在效期内赋值结果的变化趋势不显著。
