孕酮校准品产品技术要求mairui
孕酮检测试剂注册技术审查指导原则

孕酮检测试剂注册技术审查指导原则本指导原则旨在指导注册申请人对孕酮检测试剂注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。
本指导原则是对孕酮检测试剂的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
本指导原则是供申请人和审查人员使用的指导文件,不涉及注册审批等行政事项,亦不作为法规强制执行,如有能够满足法规要求的其他方法,也可以采用,但应提供详细的研究资料和验证资料。
应在遵循相关法规的前提下使用本指导原则。
本指导原则是在现行法规、标准体系及当前认知水平下制定的,随着法规、标准体系的不断完善和科学技术的不断发展,本指导原则相关内容也将适时进行调整。
一、适用范围从方法学考虑,在本文中孕酮检测试剂是指采用化学发光免疫分析技术,以竞争法为基本原理,利用全自动、半自动化学发光免疫分析仪,在医学实验室对人体样本中孕酮的含量进行体外定量分析的试剂。
依据《体外诊断试剂注册管理办法》(国家食品药品监督管理总局令第5号)、《体外诊断试剂注册管理办法修正案》(国家食品药品监督管理总局令第30号)和《食品药品监管总局关于印发体外诊断试剂分类子目录的通知》(食药监械管〔2013〕242号),孕酮检测试剂管理类别为Ⅱ类医疗器械,分类编码为6840。
本指导原则不适用于:(一)单独申请注册的孕酮校准品和质控品。
(二)化学发光免疫分析法原理之外的其他孕酮检测试剂。
二、注册申报材料要求(一)综述资料孕酮是一种重要的孕激素,属于类固醇激素,相对分子量314.5,主要由卵巢黄体和妊娠期胎盘生成,是睾酮、雌激素及肾上腺皮质激素的前体。
正常男性和女性卵泡期产生的孕酮水平很低,分泌入血后主要结合于白蛋白和性激素结合蛋白在体内进行循环。
孕酮水平与黄体的发育和萎缩有关。
孕酮的主要功能是使子宫为受精卵的着床做好准备,并维持妊娠。
孕酮(P)测定试剂盒(磁微粒化学发光免疫分析法)产品技术要求beiaikang

孕酮(P)测定试剂盒(磁微粒化学发光免疫分析法)适用范围:用于体外定量测定人血清或血浆中孕酮(P)的含量。
1.1产品规格100管份/盒。
1. 1.2 主要组成成分校准品靶值批特异,详见标签。
质控品质控范围批特异,详见标签。
2.1 外观a)试剂盒中的组份应澄清,应无沉淀和絮状物,内外标签、标识清晰,易识别;b)分离试剂摇匀后,应为均匀悬浊液,无明显凝集;c)冻干组分呈白色或淡黄色疏松体,加水后应在3分钟内完全溶解,所得液体应无沉淀和不溶物质。
2.2 校准品溯源根据GB/T21415及有关规定提供校准品的来源、赋值过程及测量不确定度等内容,溯源至企业工作标准品,并与贝克曼孕酮试剂盒比对赋值。
2.3 净含量试剂盒各液体组份的体积不得少于标称体积。
2.4 最低检出限最低检出限不高于0.15ng/ml。
2.5 线性在(0,40ng/ml)范围内剂量-反应曲线相关系数(r)的绝对值应≥0.9900。
2.6 重复性和批间差2.6.1 重复性:用高低两个浓度水平的样本,各重复检测10次其变异系数(CV)应不大于10%。
2.6.2 批间差:用三个批号试剂盒检测同一样本,则三个批号试剂盒试剂盒之间的变异系数(CV)应不大于15%。
2.7 冻干粉瓶间差质控品按照规定复溶后,瓶间浓度变异系数CV≤15%。
2.8 准确度按照EP9-A2文件要求与贝克曼化学发光免疫法孕酮试剂进行比对,本试剂和比对试剂测定样本的浓度相关系数大于0.95,回归系数在0.8-1.2之间。
2.9 质控品测定值质控品的测定结果应在质控范围内。
2.10 特异性试剂盒与表中有关潜在交叉反应物应无显著的交叉反应。
2.11稳定性2.11.1效期稳定性:试剂盒在规定的贮存条件2℃~8℃下保存,有效期12个月,效期后两个月内应符合2.1、2.4、2.5、2.6.1、2.8的要求。
2.11.2冻干粉复溶后的稳定性:质控品在复溶后24小时测定,实测浓度在质控品质控范围内。
孕酮(PROG)测定试剂盒(化学发光免疫分析法)产品技术要求mairui
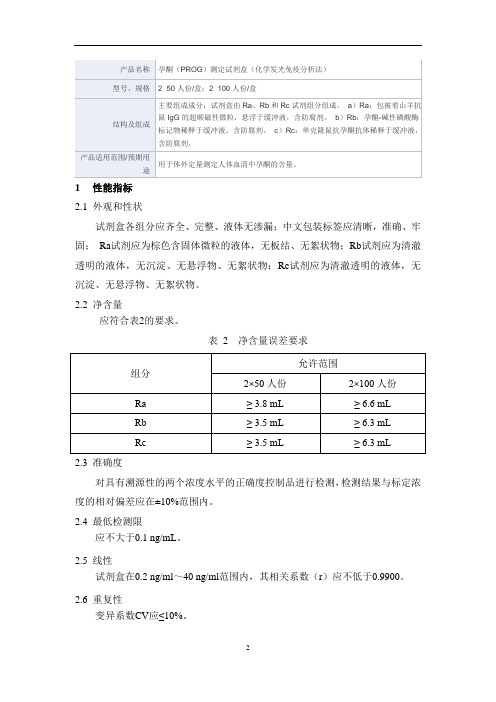
1性能指标
2.1外观和性状
试剂盒各组分应齐全、完整、液体无渗漏;中文包装标签应清晰,准确、牢固;Ra试剂应为棕色含固体微粒的液体,无板结、无絮状物;Rb试剂应为清澈透明的液体,无沉淀、无悬浮物、无絮状物;Rc试剂应为清澈透明的液体,无沉淀、无悬浮物、无絮状物。
2.2净含量
应符合表2的要求。
表 2 净含量误差要求
2.3准确度
对具有溯源性的两个浓度水平的正确度控制品进行检测,检测结果与标定浓度的相对偏差应在±10%范围内。
2.4最低检测限
应不大于0.1 ng/mL。
2.5线性
试剂盒在0.2 ng/ml~40 ng/ml范围内,其相关系数(r)应不低于0.9900。
2.6重复性
变异系数CV应≤10%。
2.7批间差
变异系数CV应≤10%。
2.8分析特异性
当样品中甘油三酯浓度≤450mg/dL,胆红素浓度≤10mg/dL,血红蛋白浓度≤500mg/dL时,测试结果的干扰偏差在±10%范围内。
当样品中孕烯醇酮浓度为200 ng/mL、皮质醇浓度为600 ng/mL、17-β雌二醇浓度为10 ng/mL、雌三醇浓度为10 ng/mL、睾酮浓度为10 ng/mL、雄烯二酮浓度为1000 ng/mL、11-脱氧皮质酮浓度为250 ng/mL时,交叉反应率应≤3%;当样品中甲孕酮浓度为100 ng/mL时,交叉反应率应≤6%。
酮体质控液产品技术要求怡成

酮体质控液
结构组成:
水平1 D-3-羟基丁酸钠0.38%
磷酸二氢钾0.68%
磷酸氢二钾1.17%
ProClin 300 0.0344%
浓度范围:0.50mmol/L~0.70mmol/L
质控范围:每批定值,批特异
水平2 D-3-羟基丁酸钠1.26%
磷酸二氢钾0.68%
磷酸氢二钾1.17%
ProClin 300 0.0344%
浓度范围:1.80mmol/L~2.20mmol/L
质控范围:每批定值,批特异
预期用途:公司生产的酮体测试系统配套使用,用于酮体测试系统的质量控制。
2.1 外观:瓶盖密闭性好,无渗漏,溶液无色,澄清无杂质。
2.2 装量:实际装量应不小于标称体积。
2.3 赋值有效性:对酮体质控液进行20次测试,95%的结果落在规定的质控范围之内。
2.4 均一性:
2.4.1 瓶内精密度:
2.5 稳定性:2℃~30℃保存,生产日期起有效期12个月。
酮体质控液有效期到期后一个月内的产品,应符合2.1、2.3、2.4的要求。
多项免疫复合定值质控品产品技术要求mairui

性能指标
2.1外观和性状
2.1.1颜色性状
质控品应为清澈透明液体,无沉淀、无悬浮物、无絮状物。
2.1.2包装
分装瓶应为透明塑料管,应盖有塑料外盖;盒贴、瓶贴、标签标识、说明书、参考值表应完整、清晰牢固。
塑料外盖与塑料管身配合后应无渗漏;塑料外盖应无明显划痕、崩缺。
2.2装量
每瓶质控品容量应不少于2.0 mL。
2.3测量准确度
2.3.1质控参考值表
质控品应可提供一份参考值表,包含适用型号的迈瑞化学发光免疫分析系统
的检测项目参考值及参考范围。
2.3.2赋值准确性
经校准的迈瑞全自动化学发光免疫分析仪检测质控品所包含的检测项目,结果应在参考范围内(不同批次的质控品参考范围参见参考值表)。
2.4均一性
2.4.1瓶内均一性
质控品瓶内均一性应满足变异系数CV≤8.0%。
2.4.2瓶间均一性
质控品瓶间均一性应满足变异系数CV≤5.0%。
2.5生物安全性
使用国家权威管理机构认可的、且不低于我国法定用于血源筛查体外诊断试剂
灵敏度的检测试剂,对质控品中乙型肝炎病毒表面抗原、人类免疫缺陷病毒抗体(HIV-I型和HIV-II型)、丙型肝炎病毒抗体、梅毒螺旋体抗体的检测应为阴性。
1。
孕酮(P)测定试剂盒(化学发光免疫分析法) 产品技术要求--性能指标

孕酮测定试剂盒(化学发光免疫分析法)1.性能指标2.1 试剂性能指标2.1.1外观和物理检查试剂盒应组分齐全,内外包装均应完整,标签清晰,液体试剂无渗漏。
其中:酶标记物应为清澈均匀的液体,无沉淀,无絮状物;磁微粒应无板结,液体内无絮状物,无异物;2.1.2装量试剂盒各组分装量应不少于标示量。
2.1.3 检出限检出限应不高于0.48nmol/L;空白限应不高于0.32nmol/L。
2.1.4 准确度相对偏差应在±10%范围内。
2.1.5 线性范围在[0.48,127] nmol/L,相关系数r应不小于0.99002.1.6 重复性使用同一批试剂盒测试浓度[2,14]nmol/L和[46,85]nmol/L的样品,其测试结果的变异系数(CV)应不大于8.0 %。
2.1.7 批间差用三批试剂盒测试浓度[2,14]nmol/L和[46,85]nmol/L的样品,其测试结果的变异系数(CV)应不大于15.0 %。
2.1.8 质控品测定值测试试剂盒内高低值质控品,其测定结果应均在质控品靶值范围内。
2.1.9 特异性分别添加潜在干扰物于含有孕酮的样本中,获得待测样本中孕酮目标浓度为64nmol/L(允许相对偏差为±15%),干扰物浓度如下,各个样本测量结果的均值应在M±2SD范围内。
(M为目标浓度平均值,SD为标准差)干扰物配制浓度分别为11-去氧皮质酮600ng/mL、孕烯醇酮200ng/ mL、皮质酮1000ng/mL、17a-羟基孕酮50ng/ mL、17β-雌二醇10ng/ mL、雌酮为0.1ug/mL、雌三醇10ng/ mL、醛甾酮50ng/ mL、丹那挫100 ng/ mL、11-脱氧皮质醇100 ng/ mL、强的松龙200ng/ mL、皮质醇为1ug/mL、睾酮为1μg/mL、克罗米酚为25μg/mL、保泰松为25μg/mL2.2校准品性能指标2.2.1外观和性状校准品应为澄清液体,无肉眼可见杂质。
免疫多项复合质控品产品技术要求mairui

质控品(低值)复溶前为浅黄色冻干粉末,复溶后为清澈浅黄色泌
复溶前为黄色冻干粉末,复溶后为清澈黄色液体;均无沉淀、悬浮物和絮状物;
2. 1.2包装
分装瓶为棕色硬质玻璃瓶,盖有橡胶瓶内塞和铝盖;盒贴、瓶贴、标签标识应完整、
清晰。
橡胶瓶内塞与玻璃配合后应无泄漏;外盖应无明显划痕、崩缺。
2. 2装量
质控品质量(含瓶重)均应不少于14 go 2. 3均一性项目名称
检测方法学
单位
高值)
质控品瓶内均一性应不大于表2的要求(SD和CV值满足其一即可)。
表1质控品瓶内均一性要求
质控品瓶间均一性应不大于表3的要求(SD和CV值满足其一即可)。
表3质控品瓶间均一性要求
每批质控品均应提供本批产品的参考值和参考范围表,并应提供赋值方法程序文件。
2. 5生物安全性
质控品使用国家权威管理机构认可的、且不低于我国法定用于血源筛查体外诊断试剂
灵敏度的检测试剂,HBsAg、HIV抗体、HCV抗体、TP抗体检测应为阴性。
孕酮(Prog)测定试剂盒(光激化学发光法)产品技术要求kemei
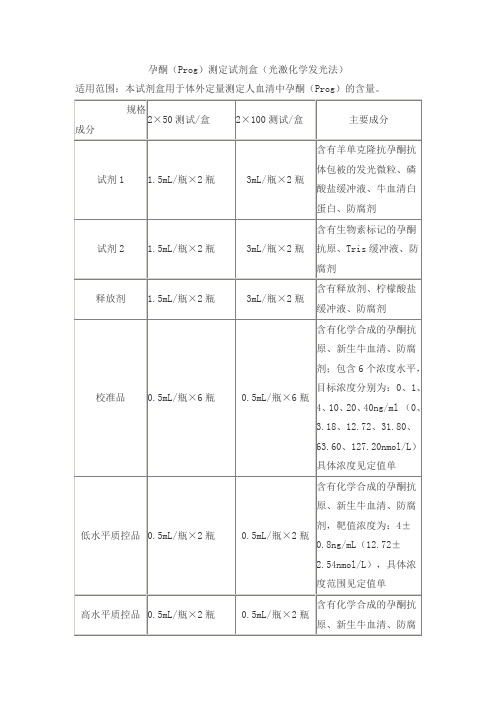
孕酮(Prog)测定试剂盒(光激化学发光法)适用范围:本试剂盒用于体外定量测定人血清中孕酮(Prog)的含量。
说明:1.校准品靶值批特异,详见定值单。
2.质控品质控范围批特异,详见定值单。
2.1 外观外观检查试剂盒组分齐全,内外包装均完整,标签清晰,液体试剂无渗漏。
2.2 检出限试剂盒的检出限不高于0.37ng/mL(1.2nmol/L)。
2.3 准确度用国家参考物质GBW09197、GBW09199作为样本进行检测,其测量结果的相对偏差应该在±15%内。
2.4 线性区间在[0.37,40]ng/mL([1.2,127.2]nmol/L)区间内,试剂盒的相关系数|r|应≥0.9900。
2.5 精密度2.5.1 批内精密度重复检测同一样本10次,测定结果的变异系数(CV)应不大于10.0%。
2.5.2 批间精密度用三个不同批次产品测定同一样本,测定结果的变异系数(CV)应不大于15.0%。
2.6 质控品测定值同一套质控品的测定结果应在本试剂盒规定的范围之内。
2.7 特异性分别添加潜在干扰物于含有孕酮的样本中,获得待测样本中孕酮目标浓度为20 ng/mL (64 nmol/L)(允许相对偏差为±15%),潜在干扰物浓度分别为10ng/mL 的皮质酮和10ng/mL的17α-羟孕酮。
各个样本测量结果的均值应在目标浓度平均值(M)±2标准差(SD)范围内。
2.8 稳定性试剂盒在2℃~8℃保存至效期末后3个月内,检验结果应符合2.1、2.2、2.3、2.4、2.5.1、2.6、2.7规定。
2.9 溯源性依据GB/T 21415-2008 依据GB/T 21415-2008及有关规定提供所用校准品的来源、赋值过程以及测量不确定度等内容,本试剂盒配套校准品溯源至国家标准物质GBW09199。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1.性能指标
2.1外观和性状
2.1.1颜色性状
校准品应为清澈透明液体,无沉淀、无悬浮物、无絮状物。
2.1.2包装
分装瓶应为白色塑料瓶,盖有塑料外盖;盒贴、瓶贴、标签标识、说明书、校准卡应完整、清晰牢固。
塑料外盖与塑料瓶身配合后应无泄漏;塑料外盖应无明显划痕、崩缺。
2.2装量
每瓶校准品容量应不少于2.0 mL。
2.3溯源性
2.3.1校准信息卡
校准品应可提供一份校准卡,包含校准品有效期和校准品各浓度水平的信息。
2.3.2赋值准确性
经校准品校准的迈瑞全自动化学发光免疫分析仪检测迈瑞内部参考血清,结果的偏倚应满足表2要求。
表 2 校准品赋值准确性的允许偏倚范围
2.3.3程序文件
应提供相应的赋值程序文件、至少一个批次的赋值记录,测量不确定度计算及校准品的互换性技术文件。
技术文件中计算的校准品测量不确定度应不大于8%。
2.4均一性
2.4.1瓶内均一性
校准品瓶内均一性以变异系数CV或标准偏差SD为指标,其中之一满足表3的要求即可。
表 3 校准品瓶内均一性的指标要求
2.4.2瓶间均一性
校准品瓶间均一性以变异系数CV或标准偏差SD为指标,其中之一满足表4的要求即可。
表 4 校准品瓶间均一性的指标要求
2.5生物安全性
使用国家权威管理机构认可的、且不低于我国法定用于血源筛查体外诊断试剂灵敏度的检测试剂对校准品中乙型肝炎病毒表面抗原、人类免疫缺陷病毒抗体(HIV-I型和HIV-II型)、丙型肝炎病毒抗体、梅毒螺旋体抗体的检测应为阴性。
