硼族元素
高中化学竞赛-硼族元素
高中化学奥林匹克竞赛辅导硼族元素一、硼族元素简介硼族元素包括硼(B)、铝(Al)、镓(Ga)、铟(In)、铊(Tl),在周期表中处于第Ⅲ A族。
硼族元素的价电子构型为n s2n p1,除硼外其余元素均为金属元素,金属性随原子序数的增加而增强。
B的半径较小,失去三个电子非常困难,因此硼不能形成简单阳离子B3+,只能通过共用电子对形成共价化合物。
Al、Ga、In、Tl在水溶液中可以形成M3+。
因为惰性电子对效应,Tl3+具有强氧化性。
在硼族元素形成的共价分子中,中心原子最外层只有6个电子,未达到8电子的外层结构,属于缺电子化合物,它们具有一个空p轨道,可以接受孤对电子形成配位键,是强的路易斯酸。
硼族元素的性质二、硼及其化合物1.硼的单质硼的非金属单质以原子晶体形式存在。
单质硼有无定形硼和晶体硼两种,无定形硼为棕色粉末,晶体硼为黑灰色原子晶体。
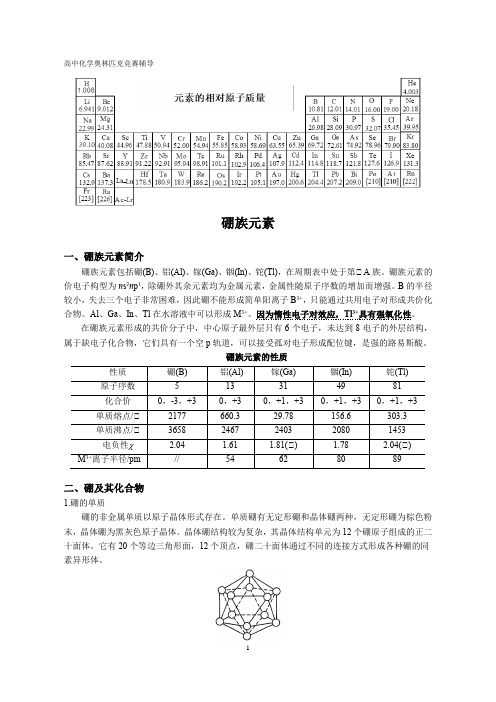
晶体硼结构较为复杂,其晶体结构单元为12个硼原子组成的正二十面体。
它有20个等边三角形面,12个顶点,硼二十面体通过不同的连接方式形成各种硼的同素异形体。
晶体硼的化学活性较低,无定形硼较活泼。
常温下,硼能与F 2反应,高温下能与N 2、O 2、S 等非金属单质反应。
无定形硼可被热的浓硝酸、浓硫酸氧化成硼酸,也能与强碱作用放出氢气。
2B+N 22BN(与金刚石C 2互为等电子体,是原子晶体) B+3HNO 3(浓)B(OH)3+3NO 2↑2B+2NaOH+2H 2O2NaBO 2+3H 2↑(与Al 的性质相似)2.硼的氧化物及含氧酸硼最重要的氧化物是B 2O 3,熔融B 2O 3能溶解许多金属氧化物,形成具有特征颜色的偏硼酸盐,这个反应用于定性分析,称为硼珠实验:CuO+B 2O 3Cu(BO 2)2(蓝色) NiO+B 2O 3Ni(BO 2)2(绿色) B 2O 3的水化物为硼酸H 3BO 3或B(OH)3。
H 3BO 3是白色的片状晶体,具有片层结构,层和层 之间存在范德华力,容易发生滑动,其中氢键对其结构的形成具有支配的作用。
无机化学-第六章-硼族元素

1
3
4
2
5
6
9
8
10
7
11
12
23-мар-22
无机化学
硼的化学性质
晶体硼较惰性
(1)无定形硼较活泼,高温下能与N2、O2、 S、X2发 生反应,显还原性。
R.T. 973K
2B(s) + 3F2(g) ══ 2BF3 4B(s) + 3O2(g) ══ 2B2O3
B-O Si-O C-O 键能/kJ·mol-1 560-690 > 452 > 358
CuBO2
红
Cu(BO2)2
蓝
Fe(BO2)2
绿
Fe(BO2)3
棕
23-мар-22
无机化学
(1) BX3结构:
硼的卤化物
B:sp2杂化
(2) BX3性质:
BF3
室温下 聚集态
g
熔点/( /℃) -127.1
沸点/( /℃) -100.4
23-мар-22
BCl3 g
-107 12.7
BBr3
BI3
23-мар-22
无机化学
硼的制备 ➢ -菱形硼 12 BI3 = B12(s) + 18 I2(g) ➢无定形硼 Na2B4O7·10H2O+ 2HCl=4H3BO3+ 2NaCl+ 5H2O 2H3BO3 = B2O3 + 3H2O (800K) B2O3 + Mg = 3MgO + 2B (800K)
结构: B:sp2杂化
硼酸 H3BO3
引 导 语 : 心得 体会是 指一种 读书、 实践后 所写的 感受性 文字。 语言类 读书心 得 同 数 学 札 记相近 ;体会 是指将 学习的 东西运 用到实 践中去 。下面 是小编 为你带 来 的 医 生 的 岗前培 训心得 体会, 希望对 你有所 帮助。 从 那 天 起 ,我们 开始了 胸 科 医 院 的 培训, 前三天 的课程 让我懂 得了很 多以前 在书上 学不到 的东西 ,有院 领 导 的 亲 身 经历和 他们的 所见所 闻,对 医院的 故障制 度有了 一定认 识。这 次培训 中 我 学 到 了 很多知 识,但 感触最 深的是 每一位 领导基 本上都 提到一 个要求 ,那就 是 学 习 、 学 习、再 学习。 一刻也 不能放 松,不 仅要钻 研本专 业的知 识,还 要了解 其 他 专 业 的 知识, 比如说 我自己 ,就应 该多了 解医学 影像诊 断及技 术等方 面的知 识 ,这样 有利于 我提高 工作效 率与质 量。此 外,就 是希望 能尽快 地进入 工作状 态, 做 好 思 想 意 识的转 变,从 受者转 变成施 者。我 认为我 在这方 面做得 也比较 到位, 经 过 学 习 和 互动, 感觉现 在也慢 慢走上 正轨了 ,希望 我们能 脚踏实 地的工 作,养 成 良 好 的 工 作与生 活习惯 ,为自 己积累 资本、 为医院 创造价 值。 通 过 第 四和 第 五 天 的 培 训我明 白了什 么是沟 通,沟 通就是 人们在 互动过 程中通 过某种 途径将 一 定 的 信 息 从发送 者传递 给接收 者,并 获得理 解的过 程,双 方互动 的过程 。我们
硼族元素及其化合物

硼族元素及其化合物
一、硼的性质
硼(Boron)是一种族IIIb的元素,在化学元素周期表中第五位,原子序数为5,原子质量为10.81、硼元素是一种半金属元素,具有金属质地,保持着类似硅的结构。
硼具有极强的抗氧化、加热稳定性、腐蚀性,使其有着优良的电性能,适用于电子设备中的导电成份,还拥有稳定的介电性能,是线路板制作的上佳材料。
二、硼的化合物
(1)氢氧化硼
氢氧化硼(H₂BO₃)是硼元素的最常见的化合物。
它是一种无色粉末状的晶体,熔点为350℃,有特殊的稀酸味,非常溶于水,但在碳酸钠、碳酸氢钠水溶液中极难溶解。
氢氧化硼是一种电解质,是用作电缆、电池和电磁浮动的主要材料。
(2)硼酸
硼酸(HBO₂)是硼的重要的化合物之一,其有机半氧化物的形式为
H₃BO₃,通常以白色粉末的形式存在,溶于水,不溶于二氯甲烷,拥有特殊的稀酸性味道。
硼酸有着广泛的应用,主要用作农药、洗涤剂、轻工业中制作消光剂、染料、防腐剂和焊条等。
(3)硼酸钠
硼酸钠(Na₂B₂O₄·2H₂O)是一种水溶性的硼酸盐,主要用作染料、洗涤剂、消光剂、增塑剂、绝缘剂、涂料等。
硼族元素(硼铝镓铟铊)-化学方程式复习总结

第13章硼族元素硼1. 硼与氮气:2B+N高温2BN2. 硼与浓硫酸:2B+3H2SO4(浓) △2B(OH)3+3SO2↑3. 碘化硼分解:2BI31000K Ta2B+3I24. 乙硼烷与氧气:B2H6+3O自然B2O3+3H2O5. LiBH4+2H2O=LiBO2+4H2↑6. 三氧化二硼与水:3B2O3+3H2O(g)=2B3O3(OH)3(g)7. 氟化硼与水:BF3+3H2O=B(OH)3+3HF氟化硼与氟化氢:BF3+HF=H[BF4]8. 硼与硫:2B+3S高温B2S39. 硼与氯气:2B+3Cl高温2BCl310. 硼与水:2B+6H2O(g)=2B(OH)3+3H211. Na2B4O7+H2SO4+5H2O=4H3BO3+Na2SO412. 硼酸受热分解:2H3BO3△B2O3+3H2O13. 三氧化二硼与镁:B2O3+3Mg高温2B+3MgO14. 硼与浓硝酸:B+3HNO3(浓) △B(OH)3+3NO2↑15. 硼与浓硫酸:2B+3H2SO4(浓) △2B(OH)3+3SO2↑16. 硼与氢氧化钠:2B+2NaOH+3KNO熔融2NaBO2+3KNO2+H2O17. 三氯化硼与氢气:2BCl3+6H2无声放电B2H6+6HCl18. 3LiAlH4+4BCl乙醚中2B2H6+3LICl+3AlCl319. 乙硼烷与氯气:B2H6(g)+6Cl2(g)=2BCl3(l)+6HCl(g)20. 乙硼烷与甲醇:B2H6+6CH3OH=2B(OCH3)3+6H221. 4NaH+B(OCH3)3=NaBH4+3NaOCH322. 三氧化二硼与水:B2O3+3H2O=2H3BO3(aq)23. 三氧化二硼与氧化铜:B2O3+CuO熔融Cu(BO2)2(蓝色)24. 三氧化二硼与氧化铁:3B2O3+Fe2O3熔融2Fe(BO2)3(黄色)25. 硼酸与水:B(OH)3+H2O=[B(OH)4]-+H+26.硼酸与乙醇:B(OH)3+3C2H5OH浓H2SO4(C2H5O)3B+3H2O27. [B4O5(OH)4]2-+5H2O=2H3BO3+2[B(OH)4]-28. 氟化硼与氨气:BF3(g)+NH3=H3N→BF331. 三氯化硼与水:BCl3+3H2O=B(OH)3+3HCl32. 硼与氟气:2B+3F2=2BF333. 硼酸与磷酸:B(OH)3+H3PO4=BPO4+3H2O34. 偏硼酸钠与过氧化氢:NaBO2+H2O2=NaBO3·H2O35. B2O3+8CaF2+8H2SO4(浓)+3H2O=2B(OH)3+16HF+8CaSO4铝1. 铝与氢氧化钠:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H22. 偏铝酸钠与氯化铵:NaAlO2+NH4Cl+H2O=Al(OH)3+NH3+NaCl3. Al2O3+2NaOH+3H2O加压煮沸2Na[Al(OH)4]4. 2Na[Al(OH)4]+CO2=2Al(OH)3↓+Na2CO3+H2O5. 氢氧化钠受热分解:2Al(OH)3△Al2O3+3H2O6. 电解三氧化二铝:2Al2O通电熔融冰晶石4Al+3O2↑7. 铝与氯气:2Al+3Cl2△2AlCl38. 六水氯化铝受热分解:AlCl3·6H2O△Al(OH)2Cl+4H2O+2HCl↑9. 铝离子与氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+10. Na[Al(OH)4]+NH4Cl=Al(OH)3↓+NaCl+NH3+H2O11. 铝与三氧化二铁:2Al+Fe2O点燃镁条2Fe+Al2O312. 铝与盐酸:2Al+6HCl(aq)=2AlCl3+3H2↑13. 铝与硫单质:2Al+3S高温Al2S314. 氯化铝与氢化锂:3nLiH+nAlCl乙醚中(AlH3)n+3nLiCl15. 氢氧化铝与氢氧化钠:Al(OH)3+NaOH(aq)=Na[Al(OH)4]镓(Ga)1.镓与稀硫酸:2Ga+3H2SO4(稀)=Ga2(SO4)3+3H2↑2.镓与浓硝酸:Ga+6HNO3(浓)=Ga(NO3)3+3NO2↑+3H2O铟(In)1.铟与稀硫酸:2In+3H2SO4(稀)=In2(SO4)3+3H2↑铊(Tl)1.氢氧化铊与氯化钠:TlOH+NaCl=TlCl+NaOH2.三氯化铊与碘化钾:TlCl3+3KI=TlI+I2+3KCl3.三氯化铊与硫化钠:2TlCl3+3Na2S=Tl2S↓+2S↓+6NaCl4.氯化铊与氯气:TlCl+Cl2=TlCl35.铊与稀硫酸:2Tl+H2SO4(稀)=Tl2SO4+H2↑6.铊与稀硝酸:Tl+2HNO3(稀)=TlNO3+NO2↑+H2O7.硫酸铊与硫酸亚铁:Tl2(SO4)3+4FeSO4=Tl2SO4+2Fe2(SO4)38.硝酸铊与二氧化硫:Tl(NO3)3+SO2+2H2O=TlNO3+H2SO4+2HNO39.铊离子与硫离子:2Tl3++3S2-=Tl2S↓+2S↓。
硼族元素及其化合物

无机化学
硼族元素及其化合物
氢氧化铝(Al(OH)3)是两性物质,既溶于酸又溶于碱: Al(OH)3+NaOH → NaAlO2+2H2O 2Al(OH)3+6HCl → 2AlCl3+3H2O 氢氧化铝的碱性比酸性略强,故铝盐都易水解。
硼族元素及其化合物
铝的卤化物从氟化物到碘化物,键型由离子键过渡 到共价键,这是因为F-、Cl-、Br-、I-的变形性依次增强, 其中最重要的是AlCl3。无水氯化铝是无色晶体,常温下 有挥发性,经测定其蒸发密度知它的分子式相当于Al2Cl6, 是共价化合物,为双聚分子。AlCl3溶于所有的有机溶剂, 在水中也易溶,因水解作用,其溶液显较强酸性,水解 过程中有碱式盐生成,其水解过程如下:
3. 铝的重要化合物
铝的重要化合物有氧化物、氢氧化物及卤化物。
氧化铝(Al2O3)是一种难熔的且不溶于水的白色粉末, 经灼烧后的氧化铝也不溶于酸。刚玉是存在于自然界中的 结晶氧化铝,其硬度仅次于金刚砂(碳化硅),是很好的 磨料。经特殊处理的氧化铝粉末,疏松多孔,具有很大的 相对表面积,有很强的吸附性能,叫做活性氧化铝,广泛 用作层析工作中的吸附剂。
无机化学
硼族元素及其化合物
硼族元素位于周期表中第ⅢA族,主 要包括硼(B)、铝(Al)、镓(Ga)、 铟(In)、铊(Tl)五种元素。
硼族元素及其化合物
一、 硼族元素通性
硼族元素的价电子层结构为ns2np1,其氧化数为+3 和+1,以+3为主要特征,在+3氧化态时完全是共价化合 物。由于它们价电子层的四个轨道中只有三个电子,价电 子数少于价电子层轨道数,故称为缺电子原子,所形成的 化合物被称为缺电子化合物。因此硼族元素有极强的接受 电子的能力,易形成聚合型分子(如Al2Cl6)和配位键化 合物。表8-19是硼族元素的一些基本性质。
硼族元素

硼族元素n s2n p1B为非金属单质,Al、Ga、In、Tl是金属B,Al,Ga(+3)In (+1,+3)Tl(+1)最大配位数:B: 4 HBF4其他 6 Na3AlF6金属性:总的变化规律是由上而下逐渐增强不规则变化的IIIA族金属的熔点;镓的反常熔点与其存在Ga2有关! 元素Al Ga In Tlm.p./℃660 30 157 303存在和提取天然资源提取B硼砂等硼酸盐金属镁还原Al 铝土矿(Al2O3·xH2O)电解4Al(s)+3O2(g)=2Al2O3(g)m o lKJH Or/3339-=∆硼(Boron)单质硼有多种同素异形体,基本结构单元为B12二十面体;二十面体连接的方式不同导致至少三种晶体单质硼的性质无定形硼比较活泼,室温下与F2反应,与Cl2, Br2, O2, S 等反应需加热,高温下与C, N2反应生成碳化物和氮化物,以几个反应较重要:2B + 6H2O ∆2B(OH)3+ 3H2B + 3HNO3 =H3BO3 + 3NO22B + 2OH- + 2H2O= 2BO2- + 3H2单质硼的制备方法:酸法和碱法两种1酸法:Mg2B2O5·H2O+2H2SO4=2H3BO3+2MgSO4虽可直接得H3BO3,但需耐酸设备等苛刻条件2碱法:Mg2B2O5·H2O+2NaOH=2NaBO2+2Mg(OH)2(浓) ↓浓的水溶液↓通CO2调碱度4NaBO2+CO2+10H2O=2Na2B4O7·10H2O+NaCO3硼砂↓溶于水,用H2SO4调酸度Na2B4O7 + H2SO4 + 5H2O= 4H3BO3+ Na2SO4溶解度小↓Δ脱水2 H3BO3 =B2O3 + 3H2O↓MgB2O3+3Mg =3MgO+2B (粗硼)粗硼含金属氧化物、硼化物及未反应完的B2O3↓用HCl, NaOH, HF (l) 处理纯硼( 95 % ~ 98 % )↓I2BI3↓钽丝(1000~1300K)2BI3 =2B+3I2(>99.95%)3电解B2O3 :在KBF4中的融体可得晶态硼。
第讲硼族元素全解

第讲硼族元素全解硼族元素是周期表中位于第三主族的化学元素。
该族元素的原子结构特点、物理化学性质等方面有很多值得关注的地方。
原子结构特点硼族元素的原子结构特点有以下几点:原子半径硼族元素的原子半径在同一周期中逐渐减小,在同一族中则随着核电荷数增加而逐渐减小。
电子亲和能硼族元素的电子亲和能呈右下方向递减的趋势,其中铍的电子亲和能最小,铟的电子亲和能最大。
电离能硼族元素的电离能值,随着核电荷数增加而逐渐增大,在同一周期中的电离能值逐渐增大。
值得注意的是,三价铍电离能较小,因为可能存在相对稳定的三价氧化物,使得它不容易丧失一个电子。
化合价电子数硼族元素的化合价电子数为3个,因此大多数化合物都为三配位,分子为平面三角形或三棱柱形。
值得注意的是,硼族元素同样也会形成四、五、六价化合物。
物理化学性质硼族元素的物理化学性质主要表现为以下几个方面:电子构型硼族元素的电子构型为ns2np1,其中n依次为2、3、4、5、6,p轨道只有一个未被占据,因此硼族元素属于典型的半金属元素。
化合反应•与非金属的反应:硼族元素可与氧、氮等非金属元素发生化学反应,并有产物生成。
•与金属的反应:大多数硼族元素均能够和金属反应,生成非常具有特异性的异构体。
物理性质•密度:硼族元素的密度随着原子序数的增加而逐渐增大。
•熔点:硼族元素的熔点随着原子序数的增加而先增后降。
•固定化学反应:硼族元素的固定化学反应能力很强,是化学反应中经常用到的一种试剂。
典型代表元素硼族元素中,最典型的代表元素为硼、铝、镓和铟。
硼硼的存在形式有硼酸、硼砂和硼烷等。
其烷基化合物中的双止键和三角形构型具有独特的结构。
硼制品被广泛地应用于一些领域,如玻璃、烟花、橡胶和塑料的生产等。
铝铝是第三大产量金属,铝和铝合金引人瞩目的特性是轻、硬、耐腐蚀、导电和热传导性好。
因此铝及其合金被广泛应用于汽车、航空和建筑等各个领域。
镓镓是一种蓝黑色的金属元素,也称为“未来金属”。
其压电和半导体性质被广泛地运用于电子技术领域,如生物医学、计算和通讯应用等。
第16章-硼族元素

第16章硼族元素16.1 硼族元素的通性16.1.1 硼族元素的通性包括硼、铝、镓、铟、铊五种元素。
硼在自然界中有硼镁矿、硼砂等;铝在地壳中的含量仅次于氧和硅,占第三位,主要以长石、云母、高岭土等硅酸盐形式存在。
镓、铟、铊比较分散,没有单独矿藏,与其他矿物共生。
硼的原子半径最小,核电荷对外层电子的吸引较强,为非金属,其余四种元素为金属,从硼到铝是由非金属突变到金属,不是逐渐过渡的。
●硼族元素氧化物的酸碱性递变规律:硼的氧化物呈酸性,铝和镓的氧化物为两性,铟和铊的氧化物是碱性的。
●硼族元素的价电子构型为ns2np1,一般氧化态为+III。
“惰性电子对效应”,随着原子序数的递增,生成低氧化态的(+I)的倾向增强。
镓、铟、铊在一定的条件下能显示出+I氧化态,特别是Tl ,其+I氧化态常见,Tl(+I)的化合物具有较强的离子健特征。
●硼、铝两元素亲氧特性表现得突出。
●硼族元素价电子轨道(ns和np)数为4,而价电子仅为3,为缺电子原子,它们所形成的化合物有些为缺电子化合物。
有空的价键轨道,这些化合物有很强的接受电子的趋势,容易形成聚合分子(如:Al2Cl6)和配合物(如:HBF4)。
在此过程中,中心原子价轨道由sp2杂化过渡到sp3杂化,相应分子从平面结构过渡到立体结构。
硼原子最高配位数为4,而其它元素外层d轨道可参与成键,最高配位数可以为6。
16.2 硼族元素的单质及其化合物硼在自然界主要以含氧化合物的形式存在。
硼的重要矿石有硼砂Na2B4O7·10H2O,方硼石2Mg3B8O15•MgCl2,硼镁矿Mg2B2O5•H2O等。
铝在自然界分布很广,主要以铝矾土矿形式存在,它是一种含有杂质的水合氧化铝矿。
镓、铟、铊在自然界单独矿物,以杂质的形式分散在其它矿物中。
16.2.1 硼族元素的单质1. 单质硼(1) 单质硼的结构单质硼有多种同素异形体,包括无定形硼和晶体硼。
无定形硼为棕色粉末,晶体硼呈黑灰色。
