九年级中考复习:专题训练:计算题12(含答案)
中考数学总复习训练 多边形与平面镶嵌(含解析)-人教版初中九年级全册数学试题

多边形与平面镶嵌一、选择题1.一个多边形的内角和是900°,则这个多边形的边数是()A.6 B.7 C.8 D.92.若一个多边形的内角和为1080°,则这个多边形的边数为()A.6 B.7 C.8 D.93.正十边形的每个外角等于()A.18° B.36° C.45° D.60°4.正六边形的每个内角都是()A.60° B.80° C.100°D.120°5.一个多边形的内角和与外角和相等,则这个多边形是()A.四边形B.五边形C.六边形D.八边形6.如果一个多边形的内角和是其外角和的一半,那么这个多边形是()A.六边形B.五边形C.四边形D.三角形7.一个正多边形的每个外角都等于36°,那么它是()A.正六边形 B.正八边形 C.正十边形 D.正十二边形8.只用下列图形中的一种,能够进行平面镶嵌的是()A.正十边形 B.正八边形 C.正六边形 D.正五边形9.下列图形中,单独选用一种图形不能进行平面镶嵌的是()A.正三角形 B.正六边形 C.正方形D.正五边形10.一个多边形截取一个角后,形成另一个多边形的内角和是1620°,则原来多边形的边数是()A.10 B.11 C.12 D.以上都有可能11.如图,过正五边形ABCDE的顶点A作直线l∥BE,则∠1的度数为()A.30° B.36° C.38° D.45°12.如图,甲、乙两人想在正五边形ABCDE内部找一点P,使得四边形ABPE为平行四边形,其作法如下:(甲)连接BD、CE,两线段相交于P点,则P即为所求(乙)先取CD的中点M,再以A为圆心,AB长为半径画弧,交AM于P点,则P即为所求.对于甲、乙两人的作法,下列判断何者正确?()A.两人皆正确B.两人皆错误C.甲正确,乙错误D.甲错误,乙正确13.如图,小红做了一个实验,将正六边形ABCDEF绕点F顺时针旋转后到达A′B′C′D′E′F′的位置,所转过的度数是()A.60° B.72° C.108°D.120°二、填空题14.正n边形的一个外角的度数为60°,则n的值为.15.如图,∠1、∠2、∠3、∠4是五边形ABCDE的4个外角.若∠A=120°,则∠1+∠2+∠3+∠4=.16.△OAB是以正多边形相邻的两个顶点A,B与它的中心O为顶点的三角形,若△OAB的一个内角为70°,则该正多边形的边数为.17.一幅图案在某个顶点处由三个边长相等的正多边形镶嵌而成.其中的两个分别是正方形和正六边形,则第三个正多边形的边数是.18.用4个全等的正八边形进行拼接,使相等的两个正八边形有一条公共边,围成一圈后中间形成一个正方形,如图1,用n个全等的正六边形按这种方式进行拼接,如图2,若围成一圈后中间形成一个正多边形,则n的值为.19.如图,四边形ABCD中,若去掉一个60°的角得到一个五边形,则∠1+∠2=度.20.如图,六边形ABCDEF的六个内角都相等,若AB=1,BC=CD=3,DE=2,则这个六边形的周长等于.21.如图,在正八边形ABCDEFGH中,四边形BCFG的面积为20cm2,则正八边形的面积为cm2.22.如图,由7个形状、大小完全相同的正六边形组成网格,正六边形的顶点称为格点.已知每个正六边形的边长为1,△ABC的顶点都在格点上,则△ABC的面积是.23.如图,正六边形硬纸片ABCDEF在桌面上由图1的起始位置沿直线l不滑行地翻滚一周后到图2位置.若正六边形的边长为2cm,则正六边形的中心O运动的路程为cm.24.如图,将正六边形绕其对称中心O旋转后,恰好能与原来的正六边形重合,那么旋转的角度至少是度.多边形与平面镶嵌参考答案与试题解析一、选择题1.一个多边形的内角和是900°,则这个多边形的边数是()A.6 B.7 C.8 D.9【考点】多边形内角与外角.【专题】计算题.【分析】本题根据多边形的内角和定理和多边形的内角和等于900°,列出方程,解出即可.【解答】解:设这个多边形的边数为n,则有(n﹣2)180°=900°,解得:n=7,∴这个多边形的边数为7.故选:B.【点评】本题主要考查多边形的内角和定理,解题的关键是根据已知等量关系列出方程从而解决问题.2.若一个多边形的内角和为1080°,则这个多边形的边数为()A.6 B.7 C.8 D.9【考点】多边形内角与外角.【分析】首先设这个多边形的边数为n,由n边形的内角和等于180°(n﹣2),即可得方程180(n ﹣2)=1080,解此方程即可求得答案.【解答】解:设这个多边形的边数为n,根据题意得:180(n﹣2)=1080,解得:n=8.故选C.【点评】此题考查了多边形的内角和公式.此题比较简单,注意熟记公式是准确求解此题的关键,注意方程思想的应用.3.正十边形的每个外角等于()A.18° B.36° C.45° D.60°【考点】多边形内角与外角.【专题】常规题型.【分析】根据正多边形的每一个外角等于多边形的外角和除以边数,计算即可得解.【解答】解:360°÷10=36°,所以,正十边形的每个外角等于36°.故选:B.【点评】本题考查了正多边形的外角和、边数、外角度数之间的关系,熟记正多边形三者之间的关系是解题的关键.4.正六边形的每个内角都是()A.60° B.80° C.100°D.120°【考点】多边形内角与外角.【专题】常规题型.【分析】先利用多边形的内角和公式(n﹣2)•180°求出正六边形的内角和,然后除以6即可;或:先利用多边形的外角和除以正多边形的边数,求出每一个外角的度数,再根据相邻的内角与外角是邻补角列式计算.【解答】解:(6﹣2)•180°=720°,所以,正六边形的每个内角都是720°÷6=120°,或:360°÷6=60°,180°﹣60°=120°.故选D.【点评】本题考查了多边形的内角与外角,利用正多边形的外角度数、边数、外角和三者之间的关系求解是此类题目常用的方法,而且求解比较简便.5.一个多边形的内角和与外角和相等,则这个多边形是()A.四边形B.五边形C.六边形D.八边形【考点】多边形内角与外角.【分析】首先设此多边形是n边形,由多边形的外角和为360°,即可得方程180(n﹣2)=360,解此方程即可求得答案.【解答】解:设此多边形是n边形,∵多边形的外角和为360°,∴180(n﹣2)=360,解得:n=4.∴这个多边形是四边形.故选A.【点评】此题考查了多边形的内角和与外角和的知识.此题难度不大,注意多边形的外角和为360°,n边形的内角和等于180°(n﹣2).6.如果一个多边形的内角和是其外角和的一半,那么这个多边形是()A.六边形B.五边形C.四边形D.三角形【考点】多边形内角与外角.【专题】应用题.【分析】任何多边形的外角和是360度,内角和等于外角和的一半则内角和是180度,可知此多边形为三角形.【解答】解:根据题意,得(n﹣2)•180°=180°,解得:n=3.故选D.【点评】本题主要考查了已知多边形的内角和求边数,可以转化为方程的问题来解决,难度适中.7.一个正多边形的每个外角都等于36°,那么它是()A.正六边形 B.正八边形 C.正十边形 D.正十二边形【考点】多边形内角与外角.【分析】利用多边形的外角和360°,除以外角的度数,即可求得边数.【解答】解:360÷36=10.故选C.【点评】本题考查了多边形的外角和定理,理解任何多边形的外角和都是360度是关键.8.只用下列图形中的一种,能够进行平面镶嵌的是()A.正十边形 B.正八边形 C.正六边形 D.正五边形【考点】平面镶嵌(密铺).【分析】根据密铺的知识,找到一个内角能整除周角360°的正多边形即可.【解答】解:A、正十边形每个内角是180°﹣360°÷10=144°,不能整除360°,不能单独进行镶嵌,不符合题意;B、正八边形每个内角是180°﹣360°÷8=135°,不能整除360°,不能单独进行镶嵌,不符合题意;C、正六边形的每个内角是120°,能整除360°,能整除360°,可以单独进行镶嵌,符合题意;D、正五边形每个内角是180°﹣360°÷5=108°,不能整除360°,不能单独进行镶嵌,不符合题意;故选:C.【点评】本题考查了平面密铺的知识,注意几何图形镶嵌成平面的关键是:围绕一点拼在一起的多边形的内角加在一起恰好组成一个周角.9.下列图形中,单独选用一种图形不能进行平面镶嵌的是()A.正三角形 B.正六边形 C.正方形D.正五边形【考点】平面镶嵌(密铺).【分析】几何图形镶嵌成平面的关键是:围绕一点拼在一起的多边形的内角加在一起恰好组成一个周角.360°为正多边形一个内角的整数倍才能单独镶嵌.【解答】解:A、正三角形的一个内角度数为180﹣360÷3=60°,是360°的约数,能镶嵌平面,不符合题意;B、正六边形的一个内角度数为180﹣360÷6=120°,是360°的约数,能镶嵌平面,不符合题意;C、正方形的一个内角度数为180﹣360÷4=90°,是360°的约数,能镶嵌平面,不符合题意;D、正五边形的一个内角度数为180﹣360÷5=108°,不是360°的约数,不能镶嵌平面,符合题意.故选:D.【点评】本题考查了平面密铺的知识,注意掌握只用一种正多边形镶嵌,只有正三角形,正四边形,正六边形三种正多边形能镶嵌成一个平面图案.10.一个多边形截取一个角后,形成另一个多边形的内角和是1620°,则原来多边形的边数是()A.10 B.11 C.12 D.以上都有可能【考点】多边形内角与外角.【专题】压轴题.【分析】首先计算截取一个角后多边形的边数,然后分三种情况讨论.因为截取一个角可能会多出一个角,也可能角的个数不变,也可能少一个角,从而得出结果.【解答】解:∵内角和是1620°的多边形是边形,又∵多边形截去一个角有三种情况.一种是从两个角的顶点截取,这样就少了一条边,即原多边形为12边形;另一种是从两个边的任意位置截,那样就多了一条边,即原多边形为10边形;还有一种就是从一个边的任意位置和一个角顶点截,那样原多边形边数不变,还是11边形.综上原来多边形的边数可能为10、11、12边形,故选D.【点评】本题主要考查了多边形的内角和定理及多边形截去一个角有三种情况.11.如图,过正五边形ABCDE的顶点A作直线l∥BE,则∠1的度数为()A.30° B.36° C.38° D.45°【考点】平行线的性质;等腰三角形的性质;多边形内角与外角.【分析】首先根据多边形内角和计算公式计算出每一个内角的度数,再根据等腰三角形的性质计算出∠AEB,然后根据平行线的性质可得答案.【解答】解:∵ABCDE是正五边形,∴∠BAE=(5﹣2)×180°÷5=108°,∴∠AEB=(180°﹣108°)÷2=36°,∵l∥BE,∴∠1=36°,故选:B.【点评】此题主要考查了正多边形的内角和定理,以及三角形内角和定理,平行线的性质,关键是掌握多边形内角和定理:(n﹣2).180° (n≥3)且n为整数.12.如图,甲、乙两人想在正五边形ABCDE内部找一点P,使得四边形ABPE为平行四边形,其作法如下:(甲)连接BD、CE,两线段相交于P点,则P即为所求(乙)先取CD的中点M,再以A为圆心,AB长为半径画弧,交AM于P点,则P即为所求.对于甲、乙两人的作法,下列判断何者正确?()A.两人皆正确B.两人皆错误C.甲正确,乙错误D.甲错误,乙正确【考点】平行四边形的判定.【分析】求出五边形的每个角的度数,求出∠ABP、∠AEP、∠BPE的度数,根据平行四边形的判定判断即可.【解答】解:甲正确,乙错误,理由是:如图,∵正五边形的每个内角的度数是=108°,AB=BC=CD=DE=AE,∴∠DEC=∠DCE=×(180°﹣108°)=36°,同理∠CBD=∠CDB=36°,∴∠ABP=∠AEP=108°﹣36°=72°,∴∠BPE=360°﹣108°﹣72°﹣72°=108°=∠A,∴四边形ABPE是平行四边形,即甲正确;∵∠BAE=108°,∴∠BAM=∠EAM=54°,∵AB=AE=AP,∴∠ABP=∠APB=×(180°﹣54°)=63°,∠AEP=∠APE=63°,∴∠BPE=360°﹣108°﹣63°﹣63°≠108°,即∠ABP=∠AEP,∠BAE≠∠BPE,∴四边形ABPE不是平行四边形,即乙错误;故选C.【点评】本题考查了正五边形的内角和定理,等腰三角形的性质,三角形的内角和定理,平行四边形的判定的应用,注意:有两组对角分别相等的四边形是平行四边形.13.如图,小红做了一个实验,将正六边形ABCDEF绕点F顺时针旋转后到达A′B′C′D′E′F′的位置,所转过的度数是()A.60° B.72° C.108°D.120°【考点】旋转的性质;正多边形和圆.【分析】由六边形ABCDEF是正六边形,即可求得∠AFE的度数,又由邻补角的定义,求得∠E′FE 的度数,由将正六边形ABCDEF绕点F顺时针旋转后到达A′B′C′D′E′F′的位置,可得∠EFE′是旋转角,继而求得答案.【解答】解:∵六边形ABCDEF是正六边形,∴∠AFE==120°,∴∠EFE′=180°﹣∠AFE=180°﹣120°=60°,∵将正六边形ABCDEF绕点F顺时针旋转后到达A′B′C′D′E′F′的位置,∴∠EFE′是旋转角,∴所转过的度数是60°.故选A.【点评】此题考查了正六边形的性质、旋转的性质以及旋转角的定义.此题难度不大,注意找到旋转角是解此题的关键.二、填空题14.正n边形的一个外角的度数为60°,则n的值为 6 .【考点】多边形内角与外角.【专题】探究型.【分析】先根据正n边形的一个外角的度数为60°求出其内角的度数,再根据多边形的内角和公式解答即可.【解答】解:∵正n边形的一个外角的度数为60°,∴其内角的度数为:180°﹣60°=120°,∴=120°,解得n=6.故答案为:6.【点评】本题考查的是多边形的内角与外角,熟知多边形的内角和公式是解答此题的关键.15.如图,∠1、∠2、∠3、∠4是五边形ABCDE的4个外角.若∠A=120°,则∠1+∠2+∠3+∠4= 300°.【考点】多边形内角与外角.【专题】数形结合.【分析】根据题意先求出∠5的度数,然后根据多边形的外角和为360°即可求出∠1+∠2+∠3+∠4的值.【解答】解:由题意得,∠5=180°﹣∠EAB=60°,又∵多边形的外角和为360°,∴∠1+∠2+∠3+∠4=360°﹣∠5=300°.故答案为:300°.【点评】本题考查了多边形的外角和等于360°的性质以及邻补角的和等于180°的性质,是基础题,比较简单.16.△OAB是以正多边形相邻的两个顶点A,B与它的中心O为顶点的三角形,若△OAB的一个内角为70°,则该正多边形的边数为9 .【考点】正多边形和圆.【分析】分∠OAB=70°和∠AOB=70°两种情况进行讨论即可求解.【解答】解:当∠OAB=70°时,∠AOB=40°,则多边形的边数是:360÷40=9;当∠AOB=70°时,360÷70结果不是整数,故不符合条件.故答案是:9.【点评】此题主要考查正多边形的计算问题,属于常规题.17.一幅图案在某个顶点处由三个边长相等的正多边形镶嵌而成.其中的两个分别是正方形和正六边形,则第三个正多边形的边数是12 .【考点】平面镶嵌(密铺).【分析】正多边形的组合能否进行平面镶嵌,关键是看位于同一顶点处的几个角之和能否为360°.若能,则说明可以进行平面镶嵌;反之,则说明不能进行平面镶嵌.【解答】解:∵正方形的一个内角度数为180°﹣360°÷4=90°,正六边形的一个内角度数为180°﹣360°÷6=120°,∴需要的多边形的一个内角度数为360°﹣90°﹣120°=150°,∴需要的多边形的一个外角度数为180°﹣150°=30°,∴第三个正多边形的边数为360÷30=12.故答案为:12.【点评】此题主要考查了平面镶嵌,关键是掌握多边形镶嵌成平面图形的条件:同一顶点处的几个内角之和为360°;正多边形的边数为360÷一个外角的度数.18.用4个全等的正八边形进行拼接,使相等的两个正八边形有一条公共边,围成一圈后中间形成一个正方形,如图1,用n个全等的正六边形按这种方式进行拼接,如图2,若围成一圈后中间形成一个正多边形,则n的值为 6 .【考点】平面镶嵌(密铺).【专题】应用题;压轴题.【分析】根据正六边形的一个内角为120°,可求出正六边形密铺时需要的正多边形的内角,继而可求出这个正多边形的边数.【解答】解:两个正六边形结合,一个公共点处组成的角度为240°,故如果要密铺,则需要一个内角为120°的正多边形,而正六边形的内角为120°,故答案为:6.【点评】此题考查了平面密铺的知识,解答本题关键是求出在密铺条件下需要的正多边形的一个内角的度数,有一定难度.19.如图,四边形ABCD中,若去掉一个60°的角得到一个五边形,则∠1+∠2= 240 度.【考点】多边形内角与外角.【专题】压轴题;数形结合.【分析】利用四边形的内角和得到∠B+∠C+∠D的度数,进而让五边形的内角和减去∠B+∠C+∠D的度数即为所求的度数.【解答】解:∵四边形的内角和为(4﹣2)×180°=360°,∴∠B+∠C+∠D=360°﹣60°=300°,∵五边形的内角和为(5﹣2)×180°=540°,∴∠1+∠2=540°﹣300°=240°,故答案为:240.【点评】考查多边形的内角和知识;求得∠B+∠C+∠D的度数是解决本题的突破点.20.如图,六边形ABCDEF的六个内角都相等,若AB=1,BC=CD=3,DE=2,则这个六边形的周长等于15 .【考点】等腰梯形的性质;多边形内角与外角;平行四边形的性质.【专题】计算题.【分析】凸六边形ABCDEF,并不是一规则的六边形,但六个角都是120°,所以通过适当的向外作延长线,可得到等边三角形,进而求解.【解答】解:如图,分别作直线AB、CD、EF的延长线和反向延长线使它们交于点G、H、P.∵六边形ABCDEF的六个角都是120°,∴六边形ABCDEF的每一个外角的度数都是60°.∴△AHF、△BGC、△DPE、△GHP都是等边三角形.∴GC=BC=3,DP=DE=2.∴GH=GP=GC+CD+DP=3+3+2=8,FA=HA=GH﹣AB﹣BG=8﹣1﹣3=4,EF=PH﹣HF﹣EP=8﹣4﹣2=2.∴六边形的周长为1+3+3+2+4+2=15.故答案为:15.【点评】本题考查了等边三角形的性质及判定定理;解题中巧妙地构造了等边三角形,从而求得周长.是非常完美的解题方法,注意学习并掌握.21.如图,在正八边形ABCDEFGH中,四边形BCFG的面积为20cm2,则正八边形的面积为40 cm2.【考点】正多边形和圆.【专题】压轴题.【分析】根据正八边形的性质得出正八边形每个内角以及表示出四边形ABGH面积进而求出答案即可.【解答】解:连接HE,AD,在正八边形ABCDEFGH中,可得:HE⊥BG于点M,AD⊥BG于点N,∵正八边形每个内角为:=135°,∴∠HGM=45°,∴MH=MG,设MH=MG=x,则HG=AH=AB=GF=x,∴BG×GF=2(+1)x2=20,四边形ABGH面积=(AH+BG)×HM=(+1)x2=10,∴正八边形的面积为:10×2+20=40(cm2).故答案为:40.【点评】此题主要考查了正八边形的性质以及勾股定理等知识,根据已知得出四边形ABGH面积是解题关键.22.如图,由7个形状、大小完全相同的正六边形组成网格,正六边形的顶点称为格点.已知每个正六边形的边长为1,△ABC的顶点都在格点上,则△ABC的面积是2.【考点】正多边形和圆.【专题】压轴题.【分析】延长AB,然后作出过点C与格点所在的直线,一定交于格点E,根据S△ABC=S△AEC﹣S△BEC即可求解.【解答】解:延长AB,然后作出过点C与格点所在的直线,一定交于格点E.正六边形的边长为1,则半径是1,则CE=4,中间间隔一个顶点的两个顶点之间的距离是:,则△BCE的边EC上的高是:,△ACE边EC上的高是:,则S△ABC=S△AEC﹣S△BEC=×4×(﹣)=2.故答案是:2.【点评】本题考查了正多边形的计算,正确理解S△ABC=S△AEC﹣S△BEC是关键.23.如图,正六边形硬纸片ABCDEF在桌面上由图1的起始位置沿直线l不滑行地翻滚一周后到图2位置.若正六边形的边长为2cm,则正六边形的中心O运动的路程为4πcm.【考点】正多边形和圆;弧长的计算;旋转的性质.【分析】每次滚动正六边形的中心就以正六边形的半径为半径旋转60°,然后计算出弧长,最后乘以六即可得到答案.【解答】解:根据题意得:每次滚动正六边形的中心就以正六边形的半径为半径旋转60°,正六边形的中心O运动的路程∵正六边形的边长为2cm,∴运动的路径为:=;∵从图1运动到图2共重复进行了六次上述的移动,∴正六边形的中心O运动的路程6×=4πcm故答案为:4π.【点评】本题考查了正多边形和圆的、弧长的计算及旋转的性质,解题的关键是弄清正六边形的中心运动的路径.24.如图,将正六边形绕其对称中心O旋转后,恰好能与原来的正六边形重合,那么旋转的角度至少是60 度.【考点】旋转对称图形.【分析】本题考查旋转对称图形的概念,旋转的最小度数是解决本题的关键.【解答】解:将正六边形绕其对称中心O旋转后,恰好能与原来的正六边形重合,那么旋转的角度至少是=60度.【点评】根据旋转对称图形的概念:把一个图形绕着一个定点旋转一个角度后,与初始图形重合,这种图形叫做旋转对称图形,这个定点叫做旋转对称中心,旋转的角度叫做旋转角.。
(完整版)初中数学中考计算题复习(最全)-含答案

一.解答题(共30小题)1.计算题:①;②解方程:.2.计算:+(π﹣2013)0.3.计算:|1﹣|﹣2cos30°+(﹣)0×(﹣1)2013.4.计算:﹣.5.计算:.6..7.计算:.8.计算:.9.计算:.10.计算:.11.计算:.12..13.计算:.14.计算:﹣(π﹣3.14)0+|﹣3|+(﹣1)2013+tan45°.15.计算:.16.计算或化简:(1)计算2﹣1﹣tan60°+(π﹣2013)0+|﹣|.(2)(a﹣2)2+4(a﹣1)﹣(a+2)(a﹣2)17.计算:(1)(﹣1)2013﹣|﹣7|+×0+()﹣1;(2).18.计算:.(1)19.(2)解方程:.20.计算:(1)tan45°+sin230°﹣cos30°•tan60°+cos245°;(2).21.(1)|﹣3|+16÷(﹣2)3+(2013﹣)0﹣tan60°(1)计算:.22.(2)求不等式组的整数解.(1)计算:23.(2)先化简,再求值:(﹣)÷,其中x=+1.24.(1)计算:tan30°25.计算:(1)(2)先化简,再求值:÷+,其中x=2+1.26.(1)计算:;(2)解方程:.27.计算:.28.计算:.29.计算:(1+)2013﹣2(1+)2012﹣4(1+)2011.30.计算:.1.化简求值:,选择一个你喜欢且有意义的数代入求值.2.先化简,再求值,然后选取一个使原式有意义的x值代入求值.3.先化简再求值:选一个使原代数式有意义的数代入中求值.4.先化简,再求值:,请选择一个你喜欢的数代入求值.5.(2010•红河州)先化简再求值:.选一个使原代数式有意义的数代入求值.6.先化简,再求值:(1﹣)÷,选择一个你喜欢的数代入求值.7.先化简,再求值:(﹣1)÷,选择自己喜欢的一个x求值.8.先化简再求值:化简,然后在0,1,2,3中选一个你认为合适的值,代入求值.9.化简求值(1)先化简,再求值,选择你喜欢的一个数代入求值.10.化简求值题:(1)先化简,再求值:,其中x=3.(2)先化简,再求值:,请选一个你喜欢且使式子有意义的数字代入求值.(3)先化简,再求值:,其中x=2.(4)先化简,再求值:,其中x=﹣1.11.(2006•巴中)化简求值:,其中a=.12.(2010•临沂)先化简,再求值:()÷,其中a=2.13.先化简:,再选一个恰当的x值代入求值.14.化简求值:(﹣1)÷,其中x=2.15.(2010•綦江县)先化简,再求值,,其中x=+1.16.(2009•随州)先化简,再求值:,其中x=+1.17.先化简,再求值:÷,其中x=tan45°.18.(2002•曲靖)化简,求值:(x+2)÷(x﹣),其中x=﹣1.19.先化简,再求值:(1+)÷,其中x=﹣3.20.先化简,再求值:,其中a=2.21.先化简,再求值÷(x﹣),其中x=2.22.先化简,再求值:,其中.23.先化简,再求值:(﹣1)÷,其中x—.25.(2011•新疆)先化简,再求值:(+1)÷,其中x=2.26.先化简,再求值:,其中x=2.27.(2011•南充)先化简,再求值:(﹣2),其中x=2.28.先化简,再求值:,其中a=﹣2.29.(2011•武汉)先化简,再求值:÷(x ﹣),其中x=3. 30.化简并求值:•,其中x=21.. 2。
(完整版)初三中考数学计算题训练及答案

1 23 8 3 ﹣ ﹣1.计算:22+|﹣1|﹣ 9.2 计算:( 13)0 -( 2 )-2 + tan45°13.计算:2×(-5)+23-3÷2.4. 计算:22+(-1)4+(5-2)0-|-3|;5.计算: Sin 450 -+ 6.计算: - 2 + (-2)0 + 2 s in 30︒ .( 1)0 + ∣2 3∣ + 2sin 60° 7.计算 ,8.计算:a(a-3)+(2-a)(2+a)∣﹣5∣ + 22﹣( + 1)00 39.计算:10. 计算: -- (-2011) + 4 ÷(-2)11.解方程 x 2﹣4x+1=0.12.解分式方程2 =x + 23x - 23 13.解方程:x=2x-1.14.已知|a﹣1|+ab + 2=0,求方裎x+bx=1 的解.x 315.解方程:x2+4x-2=0 16.解方程:x - 1 - 1 - x = 2.{2x+3<9-x,) 17.(2011.苏州)解不等式:3﹣2(x﹣1)<1.18.解不等式组:2x-5>3x.⎧x - 2 6(x + 3) ⎧⎪x + 2 > 1, 19.解不等式组⎨( -1)- 6 ≥ 4(x +1) 20.解不等式组⎨x +1 < 2.⎩5 x ⎩⎪ 2初中计算题训练2 12 1 2 1 21 2 1 2答案1.解: 原式=4+1﹣3=22.解:原式=1-4+1=-2.3.解:原式=-10+8-6=-84.解:原式=4+1+1-3=3。
1 5.解:原式= -2 + 2 = 2 . 6. 解:原式=2+1+2× =3+1=4.2 27. 解:原式=1+2﹣ 3+2× 2 =1+2﹣ 3+ 3=3.8.解: a (a - 3)+ (2 - a )(2 + a )= a 2 - 3a + 4 - a 2 =4 - 3a9. 解:原式=5+4-1=810. 解:原式= 3 -1- 1=0.2211. 解:(1)移项得,x 2﹣4x=﹣1,配方得,x 2﹣4x+4=﹣1+4,(x ﹣2)2=3,由此可得 x ﹣2=± 3,x =2+3,x =2﹣ 3;(2)a=1,b=﹣4,c=1.b 2﹣4ac=(﹣4)2﹣4×1×1=12>0.4 ± 12x=2 =2± 3, x =2+ 3,x =2﹣ 3.12.解:x=-10 13.解:x=314. 解:∵|a﹣1|+1b + 2=0,∴a﹣1=0,a=1;b+2=0,b=﹣2.1 ∴x ﹣2x=1,得 2x 2+x ﹣1=0,解得 x =﹣1,x =2. 1 1经检验:x =﹣1,x =2是原方程的解.∴原方程的解为:x =﹣1,x =2. 15.解: x =-4 ±16 + 8 = -4 ± 2 6 = - 2 ± 2 216. 解:去分母,得 x +3=2(x -1) . 解之,得 x =5. 经检验,x =5 是原方程的解. 17. 解:3﹣2x+2<1,得:﹣2x <﹣4,∴x>2. 18.解:x <-519.解: x ≥ 1520. 解:不等式①的解集为 x >-1;不等式②的解集为 x +1<4 x <3故原不等式组的解集为-1<x <3.2 36。
中考总复习专题训练 电学计算题附答案

计算题(电学)专项训练
1、有一只电铃,它正常工作时的电阻是10Ω,正常工作时的电压是4V,但我们手边只有电压为6V的电源和几个10Ω的电阻,要使电铃正常工作,该怎么办?
解:电铃正常工作时,U电铃=4V,电路中的电流:
I=I电铃===0.4A
串联电阻两端的电压:U R=U﹣U电铃=6V﹣4V=2V
串联电阻的阻值:
R===5Ω
∴应该串联一个5Ω的电阻.
2、如右图示,电源电压U恒定,当开关S闭合时,电流表的示数为1.2A;当开关断开时,电流表的示数是0.4A,电压表的示数为6V。
求两个灯泡的阻值。
解:当S断开时,两电阻串联,电压表测总电压电压(U=6V),
电路中的总电阻为
当S闭合时,L1被短路,电路中只有L2,所以:
∴R1=R﹣R2=15Ω﹣5Ω=10Ω
3、某品牌的电子瓦罉标有“220V 110W”字样,将其接入家庭电路中。
求:(1)通过该用电器的电流多大?
(2)该用电器工作时的电阻多大?
(3)若它工作2h,消耗的电能是多少?
解:
4、标有“3V 1W”字样的灯泡,与18Ω的电阻R串联后接到6V的电源上。
求:(1)灯泡的实际功率
(2)电阻R在5分钟内产生的热量。
解:
★★如图所示的电路中,电源电压恒定,电阻R
的阻值为10Ω。
2
的读数为0.2A,电流表A的读数为
当开关S闭合时,电流表A
1
0.5A。
求:
(1)电源电压;
的阻值。
(2)电阻R
1
解:。
中考化学专题训练 计算题(含解析)-人教版初中九年级全册化学试题

计算题1.某班同学在做完“二氧化碳的制取和性质”实验后,废液缸中盛有大量的盐酸与氯化钙的混合溶液(不考虑其它杂质).为了对废液进行处理,某同学做了如下实验:取废液缸上层清液20.0g于烧杯中,逐滴滴入溶质质量分数为5.3%的碳酸钠溶液至过量,滴入碳酸钠溶液质量(/g)与生成沉淀的质量(/g)的变化关系如图所示.(计算结果精确到0.1%)求:(1)当废液中盐酸完全反应时,生成的二氧化碳的质量.(2)实验过程中实际参加反应的碳酸钠溶液的质量为多少?(3)当废液中两种物质刚好消耗完毕时,所得溶液中氯化钠的质量分数.2.将一些氧化铜粉末加入到100克质量分数为14%的硫酸溶液中,微热至氧化铜全部溶解,再向蓝色溶液中加入W克铁粉,充分反应后,过滤,烘干,得到干燥的固体物质仍是Wg,求:(1)原先氧化铜的质量是多少?(2)最后得到的溶液中溶质的质量分数为多少?(3)当W为何值时才能满足加入的铁粉和得到的固体质量相等?3.市场上某补钙制剂的说明书如图所示:请计算(不要求写计算过程):(1)葡萄糖酸钙的相对分子质量为;(2)葡萄糖酸钙中碳、氢、氧、钙四种元素的质量比为;(3)此钙片中含葡萄糖酸钙的质量分数为.4.20℃时硫酸的密度和溶质质量分数对照表:密度(克/厘米3)溶质质量分数(%)10 20 40 60 80 98为测定铜锌合金的组成,取试样5克,加入质量分数为10%的稀硫酸至恰好不再产生气体为止,收集到氢气.试计算:(1)铜锌合金中锌的质量分数是多少?(2)测定时用去10%的稀硫酸多少毫升?(3)要配制上述质量分数的稀硫酸500毫升,需98%的浓硫酸多少毫升?5.尿素是常用的一种化肥,其化学式为CO(NH2)2,根据其化学式进行计算(1)尿素的相对分子质量;(2)尿素中氮元素的质量分数是多少?(3)60克尿素中含有氮元素多少克?(4)多少克碳酸氢铵(NH4HCO3)中所含的氮元素与60克尿素中所含的氮元素质量相等?6.某水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水.)有关实验数据如下表:反应前反应后实验数据烧杯和稀盐酸的质量石灰石样品的质量烧杯和其中混合物的质量150g 12g(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为g.(2)求该石灰石中碳酸钙的质量分数.7.将氯酸钾与二氧化锰的混合粉末加热到不再放出氧气为止,得到固体残留物,试计算:(1)生成氧气多少克?(2)残留固体中都含有什么?各多少克?8.如图为某试剂公司出品的过氧化氢溶液(俗称双氧水)的标签.小达欲配制100g6%的过氧化氢溶液,需用该过氧化氢溶液多少克?9.学校课外活动小组为了测定某钢铁厂生铁样品中铁的质量分数,在实验室中称取生铁样品放入烧杯中(烧杯的质量为30g).然后再加入50g稀硫酸,使之充分反应后,称量,烧杯及烧杯中物质的总质量为(已知该反应中稀硫酸恰好反应完,杂质不参与反应).请计算:(1)产生氢气的质量是多少?(2)该生铁样品中铁的质量分数?(精确到0.1%)(3)反应后的溶液中溶质的质量分数?(精确到0.1%)10.石灰厂为了测定一批石灰石样品中碳酸钙的质量分数,取用4g石灰石样品,把20g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下表:稀盐酸的用量第一次加入5g 第二次加入5g 第三次加入5g 第四次加入5g剩余固体的质量3g 2g 1g 1g(1)该石灰石样品中碳酸钙的质量分数是;(2)计算该稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%).11.取一种可燃物充分燃烧,测得生成二氧化碳,水.试求:(1)该可燃物含有的元素各占多少克?(2)可燃物的相对分子质量为32,通过计算,写出该可燃物的化学式.12.小明同学将含杂质的纯碱样品(碳酸钠与氯化钠的混合物)与稀盐酸相混合,充分反应,测得反应生成气体的质量(m)与反应时间(t)的数据如下表所示:反应时间t/s t0t1t2t3t4t5t6气体质量m/g 0根据题目要求,回答下列问题:(1)碳酸钠完全反应后,生成CO2的质量为g(2)请在下面的坐标图中,画出反应时生成气体的质量(m)随时间(t)变化的曲线.(3)求完全反应后所得溶液中溶质的质量分数.(Na2CO3+2HCl=2NaCl+CO2↑+H2O).13.过氧化氢溶液长期保存会自然分解,使得溶质质量分数减小.小军从家中拿来一瓶久置的医用过氧化氢溶液,和同学们一起测定溶质质量分数.他们取出该溶液51g,加入适量二氧化锰,生成气的质量与反应时间的关系如图所示.(1)完全反应后生成氧气的质量为.(2)计算该溶液中溶质的质量分数.14.某同学为探究铁合金中铁的质量分数,先后进行了三次实验,实验数据如下表:第一次第二次第三次实验次数项目所取合金的质量/g 20 20 40所加稀硫酸的质量/g 100 120 80生成氢气的质量/g根据该同学的实验,试回答以下问题:(1)上表三次实验中,合金里的铁恰好完全反应时,消耗稀硫酸溶液的质量是g.(2)该铜铁合金中铁的质量分数是多少?15.取MnO2和KClO3的固体混合物,加热至不再产生气体为止,将加热后剩固体冷却到室温,把40g 水分4次加入剩余固体中充分溶解.加水的质量与剩余固体的质量见下表:(MnO2是不溶于水的固体粉末)编号l 2 3 4加水的质量(g)10 10 10 10剩余固体的质量(g)m 3试求:(1)表中m值为;(2)所制得氧气的质量;(3)剩余固体加入40g水后,形成溶液溶质的质量分数(计算结果精确到0.1%).16.某固体混合物由碳酸钾和硫酸钾组成,现取一定量的该固体于烧杯中,加入85g水,充分搅拌,使其完全溶解,然后向烧杯中加入200g一定溶质质量分数的氯化钡溶液,恰好完全反应,过滤后得到白色沉淀.经分析,该沉淀中有不溶于稀硝酸,其余全部能够溶解,且产生无色无味的气体.(1)该固体中碳酸钾的质量为多少?反应后,烧杯中所得溶液的溶质质量分数为多少?(计算结果精确到0.1%)17.某学习小组取氯酸钾与二氧化锰的混合物共,加热该混合物t时间后,冷却,称量剩余固体质量,重复以上操作,依次称得4个加热时间后剩余固体的质量,记录数据如下:反应时间t1t 2t 3t 4t 5剩余固体质量/g a请仔细分析实验数据,回答下列问题:(1)表中a值为,完全反应后产生氧气的质量为g.(2)该混合物中氯酸钾的质量是多少?二氧化锰的质量是多少?18.石灰厂为了测定一批石灰石样品中碳酸钙的质量分数,取用4g石灰石样品,把20g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如表:稀盐酸的用量第一次加入5g 第二次加入5g 第三次加入5g 第四次加入5g剩余固体的质量3g 2g 1g 1g(1)计算该石灰石样品中碳酸钙的质量分数.(2)计算该20g稀盐酸中含有HCl的质量.(精确到0.01)19.某校兴趣小组在实验室中完成制取氧气的实验.他们取氯酸钾和二氧化锰的混合物共放入大试管中加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):反应时间/min 0剩余固体质量/g分析表中数据,完成下列问题:(1)完全反应后,生成氧气的质量为g;(2)原混合物中氯酸钾的质量分数是多少?(精确到0.1%)20.某研究性学习小组为了测定某矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分成4份,进行实验,结果如下:(杂质不与稀盐酸反应)实验 1 2 3 4加入样品的质量/g 5 10 15 20生成CO2的质量/g m(1)哪次反应中矿石有剩余?(2)表格中m的数值是.(2)试计算这种样品中碳酸钙的质量分数.21.为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品20g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止.反应过程中生成的气体与所用硫酸溶液的质量关系如图所示.试计算:(1)样品中铜的质量分数;(2)反应所消耗的硫酸溶液质量;(3)反应后所得溶液中溶质的质量分数.22.取某碳酸钠样品放入烧杯中,加入水充分溶解,再向其中加入稀硫酸,反应放出气体的总质量与所加入稀硫酸的质量关系曲线如图所示,请根据题意解答问题:(1)当加入196g稀硫酸时,放出气体的质量为g.(2)计算加入的稀硫酸溶液溶质的质量分数为.(3)试通过计算求出加入98g稀硫酸(即A点)时烧杯中溶液溶质的质量分数.(写出计算过程)23.用“侯氏联合制碱法”制得的纯碱常含有少量的氯化钠.为测定某纯碱样品中碳酸钠的含量,小明称取该纯碱样品,充分溶解于水中,再滴加氯化钙溶液,产生沉淀的质量与加入氯化钙溶液的质量关系如图所示.求:(1)该纯碱样品中碳酸钠的质量分数.(精确到0.1%)(2)所加入氯化钙溶液的溶质质量分数.24.某学校的学习小组对当地的石灰石矿区进行调查,测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品16g,把80g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的二氧化硅等杂质不溶于水,不与稀盐酸反应).请计算:序号加入稀盐酸的质量/g 剩余固体的质量/g第1次20 11第2次20 6第3次20第4次20 n(1)上表中n的数值为.(3)求盐酸中溶质的质量分数.25.小明同学发现他家菜园中的蔬菜生长迟缓,到农资商店去买氮肥,他发现一种化肥的包装袋上的标签如图,试计算:(答案保留一位小数)(1)硝酸铵的相对分子质量;(2)硝酸铵中各元素的质量比;(3)100Kg此化肥中含氮元素的质量;(4)若小明家的菜园共需施用含氮元素10Kg的化肥,如果买此化肥,至少需买多少Kg?26.某石灰石中含有杂质(杂质不溶于水,也不与盐酸反应),一兴趣小组想测定该样品中碳酸钙的质量分数,他们将一块样品敲打粉碎后,称出6g放入质量为20g的烧杯中,然后加入50g稀盐酸,用玻璃棒搅拌至不再产生气泡(盐酸有剩余),反应所需时间和烧杯及其所盛物质的总质量变化如图所示:(1)将样品敲碎的目的是;(2)生成二氧化碳的质量;(3)求此石灰石的纯度及最后所得溶液的质量?27.有一种未知浓度的稀硫酸600g,向其中加入足量的锌粉,充分反应后过滤,反应中共收集到氢气,求:(1)有多少克锌粉参加反应?(3)所得滤液中溶质的质量分数是多少?计算题参考答案与试题解析1.某班同学在做完“二氧化碳的制取和性质”实验后,废液缸中盛有大量的盐酸与氯化钙的混合溶液(不考虑其它杂质).为了对废液进行处理,某同学做了如下实验:取废液缸上层清液于烧杯中,逐滴滴入溶质质量分数为5.3%的碳酸钠溶液至过量,滴入碳酸钠溶液质量(/g)与生成沉淀的质量(/g)的变化关系如图所示.(计算结果精确到0.1%)求:(1)当废液中盐酸完全反应时,生成的二氧化碳的质量.(2)实验过程中实际参加反应的碳酸钠溶液的质量为多少?(3)当废液中两种物质刚好消耗完毕时,所得溶液中氯化钠的质量分数.【考点】根据化学反应方程式的计算;有关溶质质量分数的简单计算.【专题】压轴实验题;溶液的组成及溶质质量分数的计算;有关化学方程式的计算.【分析】(1)产生沉淀前消耗碳酸钠溶液,这是与废液中盐酸反应的碳酸钠溶液的质量,由于盐酸反应的碳酸钠溶液的质量和质量分数,根据二者反应的化学方程式可以计算出生成氯化钠和二氧化碳的质量.(2)由沉淀质量碳酸钠溶液的质量分数,根据碳酸钠与氯化钙反应的化学方程式可以计算出与氯化钙反应的碳酸钠溶液的质量和生成氯化钠的质量.两部分碳酸钠溶液合起来就是实际参加反应的碳酸钠溶液的质量.(3)由两种反应生成的氯化钠的质量和除以所得溶液的质量就得到所得溶液中氯化钠的质量分数.【解答】解:(1)设与盐酸反应时,生成氯化钠的质量为x,生成二氧化碳的质量为y.Na2CO3+2HCl═2NaCl+CO2↑+H2O106 117 44×5.3% x y==x=,y=(2)设与氯化钙反应时,需要碳酸钠溶液的质量为z,生成氯化钠的质量为w.Na2CO3+CaCl2═CaCO3↓+2NaCl106 100 117z•5.3% 1g w==z=,w=实际参加反应的碳酸钠溶液的质量为+=(3)所得溶液中氯化钠的质量分数为×100%≈4.0%答:(1)生成二氧化碳.(2)实际参加反应的碳酸钠溶液的质量为.(3)所得溶液中氯化钠的质量分数为4.0%.【点评】本题主要考查含杂质物质的化学方程式计算和溶质质量分数的计算,难度较大.2.将一些氧化铜粉末加入到100克质量分数为14%的硫酸溶液中,微热至氧化铜全部溶解,再向蓝色溶液中加入W克铁粉,充分反应后,过滤,烘干,得到干燥的固体物质仍是Wg,求:(1)原先氧化铜的质量是多少?(2)最后得到的溶液中溶质的质量分数为多少?(3)当W为何值时才能满足加入的铁粉和得到的固体质量相等?【考点】根据化学反应方程式的计算;有关溶质质量分数的简单计算.【专题】溶质质量分数与化学方程式相结合的计算.【分析】(1)要使加入的铁粉和得到的固体质量相等必须使硫酸消耗多余的Fe:从CuSO4+Fe=FeSO4+Cu,可以看出铁转化出铜,这是一个使固体质量增加的过程,而题目明确的说明过滤后的固体质量与投入的铁粉质量相同,这只能说明氧化铜被溶解后,硫酸仍然有剩余,剩余的硫酸继续消耗铁粉,且消耗铁粉的质量与前一步固体增加的质量相等;利用这一等量关系,计算所加入氧化铜的质量;(2)最后生成的溶质是FeSO4,它是由两部分生成的.第一部分与CuSO4反应得到的FeSO4,第二部分是铁与剩余硫酸生成的FeSO4,反应后溶液中总共含有FeSO4为两部分的质量和;根据质量守恒定律,反应后所得溶液总质量=100g稀硫酸+氧化铜的质量+铁的质量﹣析出的铜的质量(与铁的质量相等)﹣氢气质量,由于参加反应铁的质量与析出固体的质量相等,所以,反应后所得溶液的总质量=100g稀硫酸+氧化铜的质量﹣氢气质量.则最后得到溶液的质量分数为生成FeSO4的总质量与反应后所得溶液总质量的比.(3)因为铁与硫酸铜反应生成铜,固体质量增加,根据加入Wg铁粉,与硫酸铜反应后得到固体物质为Wg可知,铁粉没有完全反应,剩余的铁粉与稀硫酸反应,最后得到的Wg固体物质为铜的质量,根据Wg铜完全来自氧化铜,故可以计算出W的值.【解答】解:(1)设原先氧化铜的质量为m,则与氧化铜反应的硫酸的质量x,生成硫酸铜的质量yCuO+H2SO4═CuSO4+H2O80 98 160m x y,则x=,则y=2m设加入铁粉与硫酸铜溶液充分反应固体增加的质量为a,生成硫酸亚铁的质量为c;与剩余稀硫酸反应的铁的质量为b,生成硫酸亚铁的质量为d.Fe+CuSO4═FeSO4+Cu 固体质量增加56 160 64 64﹣56=82m a,则a=Fe+H2SO4═FeSO4+H2↑56 98b 100g×14%﹣,b=8﹣反应前后固体质量不变,即与硫酸反应消耗铁的质量等于与硫酸铜反应固体增加的质量,即:a=,b=8﹣,因为a=b,解得m=10g,答:原先氧化铜的质量为10g;(2)方法一:设加入铁粉与硫酸铜溶液充分反应固体增加的质量1g时生成硫酸亚铁的质量为c;与剩余稀硫酸反应的1g铁生成硫酸亚铁的质量为d,同时放出氢气质量为wFe+CuSO4═FeSO4+Cu 固体质量增加56 160 152 64 64﹣56=8c 1g,解得c=19gFe+H2SO4═FeSO4+H2↑56 152 21g d w,解得d≈w≈最后得到溶液的质量分数=×100%≈19.73%答:最后得到溶液的质量分数为19.73%.方法二:由题意可知,硫酸最终全部转化为硫酸亚铁,设硫酸亚铁的质量为z:H2SO4~FeSO498 152100g×14% z则,解得Z=g≈,加入铁粉的质量W=×100%=8g;最后得到溶液的质量分数=×100%≈19.73%(3)Wg铜完全来自氧化铜,根据质量守恒定律的元素守恒,则W=×100%×10g=8g当W取值为等于或大于8g时,才能满足加入铁粉和得到固体质量相等的要求.故答案为:(1)10g;(2)19.73%;(3)8g.【点评】分析固体质量不变的原因是解决本题的关键:要使加入的铁粉和得到的固体质量相等必须使硫酸消耗多余的Fe,且消耗铁粉的质量与置换出铜固体增加的质量相等.3.市场上某补钙制剂的说明书如图所示:请计算(不要求写计算过程):(1)葡萄糖酸钙的相对分子质量为430 ;(2)葡萄糖酸钙中碳、氢、氧、钙四种元素的质量比为72:11:112:20 ;(3)此钙片中含葡萄糖酸钙的质量分数为8% .【考点】相对分子质量的概念及其计算;元素质量比的计算.【专题】化学式的计算.【分析】(1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.(3)根据物质的纯度计算方法,进行分析解答.【解答】解:(1)根据相对分子的质量为组成分子的各原子的相对原子质量之和,可得葡萄糖酸钙的相对分子质量为:12×12+1×22+16×14+40=430;故填:430;(2)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得葡萄糖酸钙中碳、氢、氧、钙四种元素的质量比为:(12×12):(1×22):(16×14):40=144:22:224:40=72:11:112:20;故填:72:11:112:20;(3)此钙片中含葡萄糖酸钙的质量分数为=8%;故填:8%.【点评】本题考查学生利用化学式进行简单计算,注重了对学生基础知识的考查.4.20℃时硫酸的密度和溶质质量分数对照表:密度(克/厘米3)溶质质量分数(%)10 20 40 60 80 98为测定铜锌合金的组成,取试样5克,加入质量分数为10%的稀硫酸至恰好不再产生气体为止,收集到氢气.试计算:(1)铜锌合金中锌的质量分数是多少?(2)测定时用去10%的稀硫酸多少毫升?(3)要配制上述质量分数的稀硫酸500毫升,需98%的浓硫酸多少毫升?【考点】根据化学反应方程式的计算;用水稀释改变浓度的方法;有关溶质质量分数的简单计算.【专题】综合计算(图像型、表格型、情景型计算题).【分析】锌和稀硫酸反应生成硫酸锌和氢气,根据氢气的质量可以计算锌的质量,进一步可以计算锌的质量分数;溶液稀释前后,溶质质量分数不变.【解答】解:(1)设锌的质量为x,反应的硫酸质量为y,Zn+H2SO4═ZnSO4+H2↑,65 98 2x y==,x=,y=,铜锌合金中锌的质量分数为:×100%=26%,答:铜锌合金中锌的质量分数为26%.(2)测定时用去10%的稀硫酸的体积为:÷10%÷/mL=18.3mL,答:测定时用去10%的稀硫酸的体积为18.3mL.(3)设需要浓硫酸的体积为z,根据题意有:/mL×500mL×10%=/mL×z×98%,z=29.7mL,答:要配制上述质量分数的稀硫酸500毫升,需98%的浓硫酸29.7mL.【点评】本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规X性和准确性.5.尿素是常用的一种化肥,其化学式为CO(NH2)2,根据其化学式进行计算(1)尿素的相对分子质量;(2)尿素中氮元素的质量分数是多少?(3)60克尿素中含有氮元素多少克?(4)多少克碳酸氢铵(NH4HCO3)中所含的氮元素与60克尿素中所含的氮元素质量相等?【考点】相对分子质量的概念及其计算;元素的质量分数计算;化合物中某元素的质量计算;物质组成的综合计算.【专题】化学式的计算.【分析】(1)根据尿素的化学式可知,它的相对分子质量=(碳的相对原子质量×碳原子个数)+(氧的相对原子质量×氧原子个数)+(氮的相对原子质量×氮原子个数)+(氢的相对原子质量×氢原子个数);(2)尿素中氮元素的质量分数=×100%;(3)根据“60克×尿素中氮元素的质量分数”计算即可;CO(NH2)2(4)先计算出碳酸氢铵中氮元素的质量分数,再根据所含的氮元素质量相等进行计算即可.【解答】解:(1)根据尿素的化学式可知,它的相对分子质量=12+16+14×2+1×4=60;(2)尿素中氮元素的质量分数=×100%≈46.7%;(3)60g×46.7%=28g;(4)碳酸氢铵中氮元素的质量分数=×100%≈17.7%,60g×46.7%÷17.7%=158g.答;(1)尿素的相对分子质量为60;(2)尿素中氮元素的质量分数是46.7%;(3)60克尿素中含有氮元素28g;(4)158g碳酸氢铵(NH4HCO3)中所含的氮元素与60克尿素中所含的氮元素质量相等.【点评】本题主要考查学生运用化学式进行计算的能力.6.某水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水.)有关实验数据如下表:反应前反应后实验数据烧杯和稀盐酸的质量石灰石样品的质量烧杯和其中混合物的质量150g 12g(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为4.4 g.(2)求该石灰石中碳酸钙的质量分数.【考点】根据化学反应方程式的计算;质量守恒定律及其应用.【专题】压轴实验题;有关化学方程式的计算.【分析】(1)根据质量守恒定律可知:反应后比反应前减少的质量是生成二氧化碳的质量;(2)根据化学方程式由二氧化碳的质量可以计算出石灰石中碳酸钙的质量,进而计算出石灰石中碳酸钙的质量分数.【解答】解:(1)根据质量守恒定律,二氧化碳的质量为:150g+12g﹣=.(2)设该石灰石样品中碳酸钙的质量为x.CaCO3+2HCl═CaCl2+H2O+CO2↑100 44x,x=10g此石灰石中碳酸钙的质量分数为:×100%≈83.3%答:该石灰石中碳酸钙的质量分数为83.3%.【点评】本题主要考查有关化学方程式的计算和质量分数的计算,难度较小.7.将氯酸钾与二氧化锰的混合粉末加热到不再放出氧气为止,得到固体残留物,试计算:(1)生成氧气多少克?(2)残留固体中都含有什么?各多少克?【考点】根据化学反应方程式的计算.【专题】有关化学方程式的计算.【分析】反应前后的质量差即为反应生成氧气的质量,根据氧气的质量可以计算氯化钾的质量,进一步可以计算二氧化锰的质量.【解答】解:(1)生成氧气的质量为:﹣=,(2)设氯酸钾的质量为x,2KClO32KCl+3O2↑,149 96xx=二氧化锰的质量为:﹣=4g答案:(1)生成氧气(2)残余固体是KCl质量,MnO2质量4克.【点评】本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规X性和准确性.8.(2007•某某)如图为某试剂公司出品的过氧化氢溶液(俗称双氧水)的标签.小达欲配制100g6%的过氧化氢溶液,需用该过氧化氢溶液多少克?【考点】有关溶质质量分数的简单计算;一定溶质质量分数的溶液的配制.【专题】标签图示型;压轴实验题;溶液的组成及溶质质量分数的计算.【分析】根据稀释前后溶液中溶质质量不变,利用溶质质量=溶液质量×溶液的溶质质量分数,由欲配制100g6%的过氧化氢溶液计算溶液中溶质质量,然后再利用上述公式由溶质质量和浓溶液的溶质质量分数(见标签)30%,计算出所需该过氧化氢溶液的质量.【解答】解:需用该过氧化氢溶液的质量==20g答:需过氧化氢溶液20g.【点评】利用溶质质量=溶液质量×溶液的溶质质量分数,已知其中任意两个量即可计算出第三个量.9.学校课外活动小组为了测定某钢铁厂生铁样品中铁的质量分数,在实验室中称取生铁样品放入烧杯中(烧杯的质量为30g).然后再加入50g稀硫酸,使之充分反应后,称量,烧杯及烧杯中物质的总质量为(已知该反应中稀硫酸恰好反应完,杂质不参与反应).请计算:(1)产生氢气的质量是多少?(2)该生铁样品中铁的质量分数?(精确到0.1%)(3)反应后的溶液中溶质的质量分数?(精确到0.1%)。
初三中考复习 专题练习题 含答案

参考答案:选择题1-5 B C B B A 6-10 B C B B C二、填空题11、1 12、-1 13、y=-x (答案不唯一) 14、(0,0)15、y=2x(答案不唯一) 16、m=-2三、解答题21、(1)y=3x-5(2)x=222、y=-3+2(x-2) y=-1224、p点坐标为(,4)或(-,-4)二、反比例基础训练2、3、4、5、三、计算题参考答案选择题1-5 AAAAD 6、C 填空题16、-3计算题22、S△aoc=一元二次函数专项训练4、5、6、4、5、6、解答题参考答案圆基础训练的是()参考答案1-5 ADDCC 6.60 7、AB⊥CD 8、8 9、10、11-13 BDD 14、0.115、16、方程组训练1.今有鸡兔同笼,上有三十五头,下有九十四足(问鸡有( )只,A.12B.23C.35D.49 答案:B2.一个长方形的长减少15cm,宽增加6cm,就成为一个正方形,并且这两个图形的面积相等.该长方形的面积是( )cm?(A.90B.100C.120D.150答案:B3.一支部队第一天行军4小时,第二天行军5小时,两天共行军98km,且第一天比第二天少走2km,第一天行军的平均速度是_____km/h. 第二天行军的平均速度_____ km/h.A.12、10B.10、12C.12.5、9.6D.9.6、12.5 答案:A4.某公司有大小两种货车,2辆大车和3辆小车可运货15.5吨,5辆大车和6辆小车可运货35吨.大车每辆运送( )吨,A.2.5B.3C.3.5D.4 答案:D5.某公司用30000元购进两种货物,货物卖出后,一种货物的利润是10%,另一种货物的利润是11%,共获得利润3150元.问两种货物各进货( )元,A.1500、28500B.15000、15000C.1500、2150D.10000、20000 答案:B6.一张方桌由1个桌面、4条桌腿组成(如果1m3木料可以做方桌的桌面50个或做桌腿300条,现有5m3木料,那么用立方米木料做桌面、立方米木料做桌腿,做出的桌面和桌腿,恰好能配成方桌,能配成张方桌,()A.2,3,100B.1,4,50C.3,2,150D.4,1,200 答案:C7.1号仓库与2号仓库共存粮450吨,现从1号仓库运出存粮的60%,从2号仓库运出存粮的40%,结果2号仓库所余的粮食比1号仓库所余的粮食多30吨,1号仓库与2号仓库原来各存粮( )吨,A.210,240B.240,210C.306,144D.126,324答案:B8.一个三位数的数字之和等于12,它的个位数比十位数字小2(若将它的百位数字与个位数字互换,所得的数比原来的数小99,则原数( )A.264B.453C.345D.642 答案:B相似三角形专项、5、6、参考答案1、2、4、5、第三次:平行四边形动态讨论1、已知y=ax+b与反比例函数交点为A(2,2)B(-1,-4),求:(1)表达式(2)C点坐标(-4,m)求S△ABC(3)是否存在一点D,使四边形ABCD若存在,写出来。
(完整版)中考复习化学计算题专题(含答案)
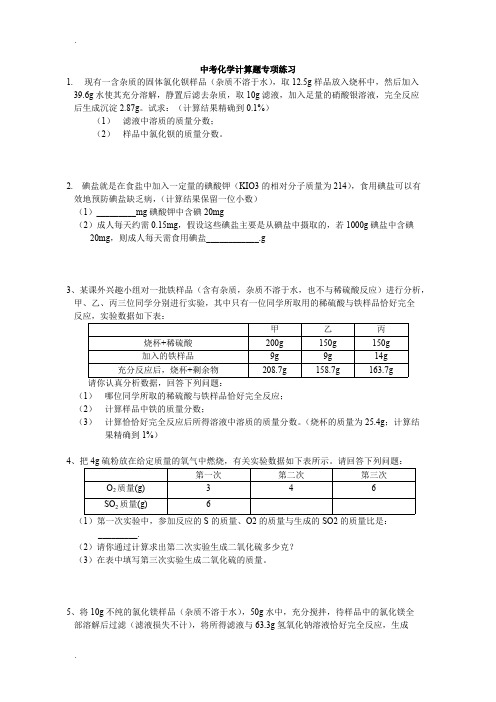
.5.8g白色沉淀。
求:(1)样品中氧化镁的质量。
(2)反应所得溶液中溶质的质量分数。
6、“骨质疏松症”是由人体缺钙引起的,可服用补钙剂来治疗。
乳酸钙(CaC6H10O6·5H2O)是一种常见的补钙剂,出售乳酸钙片剂每片含乳酸钙200mg.一个成年缺钙病人每天服用20片乳酸钙片剂可达到补钙目的。
计算:(计算结果保留整数)(1)乳酸钙中各元素的质量比。
(2)该成年缺钙病人改用喝牛奶(每100mg牛奶中含钙0.104g)来补钙,每天至少需喝多少毫升牛奶。
7、生铁和钢都是铁合金,生铁中碳的含量在2.0%~4.3%之间,钢中碳的含量在0.03%~2%之间。
将一块质量为10.0g的铁合金放入锥形瓶中,再向锥形瓶中加入100g稀H2SO4,恰好使铁合金中的铁完全反应(碳不熔于稀硫酸;铁合金中其他元素含量很低,可忽略不计),测得生成H2的体积为4.00L(H2在该条件下的密度为0.0880g/L)。
试根据计算回答:(计算结果保留三位效数字)(1)该铁合金是生铁还是钢?(2)反应后所得溶液的溶质质量分数。
8、将3.1克氧化钠加到质量为m的水中,完全反应后,得到溶质的质量分数为16%的溶液,在该溶液中加入50克稀盐酸,两者恰好完全反应。
(氧化钠与水反应的化学方程式为:Na2O+H2O==2NaOH)。
求:(1)m的值(2)所加盐酸中溶质的质量分数。
(3)若要使反应后的氧化钠溶液成为20ºC时的饱和溶液,至少要蒸发掉多少克水?(20ºC时,氧化钠的溶解度为36克)9、以下是我省生产的某种加钙食盐包装标签上的部分文字。
请仔细阅读后回答以下问题:摄入量?23、某校化学兴趣小组为测定空气中二氧化硫的含量,用NOH溶液吸收SO2,反应方程式如下:2NaOH+SO2=NaSO3+H2O用NaOH溶液吸收1000L已除去CO2的空气样品,溶液质量增重了0.64g。
已知此时空气的密度约为1.3g/L,求:(1)被吸收的SO2的质量。
【金牌学案】中考化学复习考点全突破专题训练卷 专题12 化学式、化学方程式专项计算

1 第三部分 物质的化学变化专题12 化学式、化学方程式专项计算(训练时间:90分钟 分值:100分)一、选择题(每题3分,共15分)1.下列关于耐高温新型陶瓷氮化硅(Si 3N 4)的叙述正确的是( )A .氮化硅中Si 、N 两种元素的质量比为3∶4B .氮化硅中氮元素的质量分数为40%C .140 g 氮化硅中含硅元素的质量为84 gD .氮化硅的相对分子质量为140 g【解析】此题借助新型耐高温陶瓷氮化硅考查化学式的计算。
氮化硅中Si 、N 元素质量比为(28×3)∶(14×4)=3∶2,A 错;氮化硅中N 元素的质量分数为56/140×100%=40%,B 正确;140 g 氮化硅中Si 元素的质量为140 g×84/140=84 g ,C 正确;氮化硅的相对分子质量为140,而不是140 g ,D 错误。
答案为BC 。
【答案】BC2.相同质量的下列物质中,所含氧元素质量最多的是( )A .H 2OB .H 2O 2C .COD .CO 2【解析】此题考查有关化学式的计算。
物质的质量乘以该物质中某元素的质量分数即为该元素的质量。
设H 2O 、H 2O 2、CO 、CO 2四种物质的质量均为1 g ,则所含氧元素的质量分别为:1 g×16/18×100%=0.89 g1 g×32/34×100%=0.94 g1 g×16/28×100%=0.57 g1 g×32/44×100%=0.78 g显然,H 2O 2中所含氧元素质量最多。
答案为B 。
另外,此题也可以通过变化化学式后比较得出答案,即四种物质的化学式分别变形为H 4O 2、H 2O 2、C 2O 2、CO 2,显然,四种物质中H 2O 2中氧元素质量分数最大,则相同质量的四种物质中它所含氧元素质量也是最大。
【答案】B3.孔雀石绿具有高残留和致癌等副作用,我国已将孔雀石绿列为水产养殖禁用药物。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
专题训练:计算题12
1、家里蒸馒头用的纯碱中含有少量的氯化钠,课外探究小组的同学欲测定纯碱中碳酸钠的含量。
他们取该纯碱样品11.0g ,全部溶解在100.0g 水中,再加入氯化钙溶液141.0g ,恰好完全反应。
过滤干燥后,称得沉淀质量为10.0g 。
请计算:
(1)纯碱样品中碳酸钠的质量;
(2)反应后所得滤液中溶质的质量分数。
【答案】(1)10.6g ;(2)5%
2、氯碱工业是指用电解饱和NaCl 溶液的方法来抽取NaOH 、Cl 2和H 2,并以它们为原料生产一系列化工产品,电解饱和NaCl 溶液的化学方程式为
2222NaCl 2H O Cl H 2NaOH +↑+↑+通电,请计算:
(1)烧碱中三种元素的质量比m (Na ):m (O ): m (H )= 。
(2)用这种方法制备40t 烧碱,需要NaCl 的质量为 。
(3)若用25%的NaCl 溶液按照上述方法电解并制取40t 烧碱,完全电解后所得溶液的质量分数。
( 假设生成的烧碱全溶,计算时若除不尽保留到1%) .
【答案】(1)23:16:1 (2)58.5t (32)20.3%
3、某学习小组收集一份铜锌合金样品,(设只含铜、锌),为认识其组成等,进行了以下实验:
(1)合金中铜、锌质量比为______
(2)稀硫酸质量分数是多少?(写出计算过程,结果精确到0.1%)
【答案】(1)33.5∶6.5或335∶65或67∶13(2)9.8%
4、现有碳酸钙和氯化钙的固体混合物16g,其中含碳元素1.2g,将该混合物加入到100 g 稀盐酸中,恰好完全反应。
计算:
(1)原固体混合物中碳酸钙的质量分数为多少?
(2)所得溶液溶质的质量分数(结果保留至0.1%)。
【答案】(1)10g (2)15.3%
5、氢氧化钠固体,因不慎敞口放置了一段时间,已经部分变质.化学课外兴趣小组的同学决定测定该瓶 试剂变质的程度,他们在知识回顾的基础上,依次进行了如下的实验操作:
【知识回顾】
氢氧化钠必须密封保存,理由是:①氢氧化钠固体会吸收水分而潮解;②氢氧化钠与二氧化碳反而变质, 发 生反应的化学方程式是: 。
【实验操作】
第一步:取该瓶中的试剂20g 加水配制成溶液;
第二步:向上述溶液中加入足量的稀盐酸,反应生成气体的质量变化如图所示。
根据实验步骤和图像进行分析与计算:
(1)20g 试剂与稀盐酸反应产生二氧化碳的质量 g .
(2)计算该20g 试剂中含有杂质Na 2CO 3的质量分数(写出计算过程)。
(结果精确到 0.1%) (3)如果第二步改为向第一步配制成的溶液中加入足量的澄清石灰水,则生成沉淀的质量为 g 。
【答案】22322NaOH+CO Na CO +H =O ; 2.2;26.5%;5
6、某化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,取用16g 石灰石样品,把80g 稀盐酸(氯化氢的水溶液)分4次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶解于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下:
(1)上表中n的数值为_____.由上表数据可知这四次实验中,第____次所加的盐酸没反应完.
(2)石灰石样品中碳酸钙的质量分数是?.
(3)如果该石灰厂煅烧50t这种石灰石,最多可得到二氧化碳气体多少吨?(本小题要求写出完整的计算过程,结果保留小数点后1位)
【答案】(1)3.2;三、四;(2)80%;(3)17.6t
7、现有50g氯化钙溶液与100g碳酸钠溶液恰好完全反应,将反应后的混合物过滤后得到溶液的质量为140g.
(1)生成沉淀的质量是_______g.
(2)求碳酸钠溶液中溶质的质量分数是多少?
【答案】(1)10(2)10.6%
8、【题文】
下图是广谱抗生素阿莫西林胶囊使用说明书的部分内容,根据说明书计算:
(1)阿莫西林它由种元素组成,其分子中碳、氢、氮原子的个数比为;
(2)阿莫西林中氧元素的质量分数为(精确到1%);
(3)如果一个体重25kg的儿童患病需要服用阿莫西林,每日要服粒.
【答案】(1)5,16:19:3;(2)22%;(3)6
9、色氨酸(C11H12N2O2)是氨基酸中的一种,在人体中含量太低会影响睡眠质量。
一般可通过食补黄豆、黑芝麻、海蟹和肉松等得以改善。
请回答:
(1)色氨酸属于(填“有机”或“无机”)化合物;
(2)色氨酸中碳、氢、氮和氧各元素的质量比是;
(3)g色氨酸中含6.4g氧元素。
【答案】(1)有机(2)33:3:7:8(3)40.8
10、向12g碳酸钙和氯化钙的固体混合物中滴加稀盐酸,反应过程中生成气体的质量与所用稀盐酸的质量关系如图所示。
请计算:
(1)混合物中碳酸钙的质量;
(2)恰好完全反应时,所得溶液中溶质的质量分数。
【答案】(1)10g(2)10%。
