高中化学选修四水溶液中的离子平衡
高二化学选修4第3章 水溶液中的离子平衡

第三章水溶液中的离子平衡一、选择题(每小题有1个或2个选项符合题意)1.下列关于盐酸与醋酸两种稀溶液的说法正确的是() A.相同浓度的两溶液中c(H+)相同B.100 mL 0.1 mol/L的两溶液均能中和等物质的量的氢氧化钠C.pH=3的两溶液稀释100倍,pH都为5D.两溶液中分别加入少量对应的钠盐,c(H+)均明显减少【解析】盐酸为一元强酸,醋酸为一元弱酸,浓度相同时,电离能力不同,所以A 项中c(H+)盐酸>c(H+)醋酸,但中和NaOH的能力相同。
C项稀释后,盐酸的pH=5,而醋酸电离平衡被促进,其pH<5;D项c(H+)酸酸几乎不变,故选B。
【答案】 B2.已知0.1 mol/L的醋酸溶液中存在电离平衡:CH3COOH CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)的值增大,可以采取的措施是() A.加少量烧碱溶液B.升高温度C.加少量冰醋酸D.加水【解析】本题提供的四种措施都会使醋酸的电离平衡正向移动,但A、C项会使c(H +)/c(CH3COOH)的值减小。
故选BD。
【答案】BD3.下列可用于测定溶液pH且精确度最高的是() A.酸碱指示剂B.pH计C.精密pH试纸D.广泛pH试纸【解析】A项酸碱指示剂只能测定溶液的酸碱性。
C项pH试纸只能比较粗略的测出溶液的pH。
D项广泛pH试纸只能测出整数的pH。
故选B。
【答案】 B4.取浓度相等的NaOH和HCl溶液,以3∶2体积比相混和,所得溶液的pH等于12,则原溶液的浓度为() A.0.01 mol/L B.0.017 mol/LC.0.05 mol/L D.0.50 mol/L【解析】设原溶液物质的量浓度为c mol/L,V(NaOH)=3 L,V(HCl)=2 L,二者混合后反应,混合溶液体积为5 L,二者混合后反应,所得溶液pH=12,则c(OH-)=10-2mol/L,3 L×c mol/L-2 L×c mol/L=10-2mol/L×5 L,则c=0.05 mol/L。
高中化学选修4第三章《水溶液中的离子平衡》单元测试(一)

1. 甲酸的下列性质中,可以证明它是弱电解质的是( )A. 1 mol ·L-1 的甲酸溶液中c(H+)约为1×10-2 mol/LB. 甲酸能与水以任意比例互溶C. 甲酸与盐酸都能与NaOH 发生反应D. 甲酸溶液的导电能力比盐酸溶液的导电能力弱2.硫化汞(HgS)难溶于水,在自然界中呈红褐色,常用于油画颜料,印泥及朱红雕刻漆器等。
某温度时,HgS 在水中的沉淀溶解平衡曲线如图所示。
下列说法正确的是( )A. 向硫化汞的浊液中加入硫化钠溶液,硫化汞的K sp 减小B. 图中a 点对应的是饱和溶液C. 向c 点的溶液中加入Hg(NO3)2 ,则c(S2-)减小D.升高温度可以实现c 点到b 点的转化3.氢氧化钙在80℃时的溶解度为xg ,20℃时的溶解度为yg 。
取20℃的氢氧化钙饱和溶液,蒸发掉Wg 水后再恢复到20℃ ,其溶液里面溶质的质量分数为z% ,则下列关系正确的是( )A.y>x ,y>zB.x>y>zC.y<x ,y<zD.x<y<z4.在-50℃时液氨中存在着下列平衡:2NH3(液) NH4++NH2- ,两种离子的平衡浓度均为 1.0×10-15mol ·L-1 。
以下有关-50℃时离子积的叙述中正确的是( )A.离子积为1.0×10-15B.离子积为1.0×10-30C. 向液氨中加入氨基钠(NaNH2),液氨的离子积增大D. 向液氨中加入NH4Cl ,c(NH4+)增大,离子积的数值也随之增大5.在氨水中,NH3 ·H2O 电离达到平衡的标志是( )A.溶液显电中性C.c(OH-)恒定不变B.溶液中检测不出NH3 ·H2O 分子的存在D.c( NH ) =c(OH-)6.对室温下pH 相同、体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是( )A.加适量的醋酸钠晶体后,两溶液的pH 均增大B.使温度都升高20℃后,两溶液的pH 均不变C.加水稀释2 倍后,两溶液的pH 均减小D.加足量的锌充分反应后,盐酸中产生的氢气速率快7.已知室温时,0. 1mo1/L 某一元酸HA 在水中有0.1%发生电离,下列叙述错误的是:( )A.该溶液的pH=4B.升高温度,溶液的pH 增大C.此酸的电离平衡常数约为1×10-7D. 由HA 电离出的c(H+)约为水电离出的c(H+)的106 倍8.下列物质的水溶液能导电,但其本身属于非电解质的是( )A.CH3COOHB.干冰C.酒精D.Cl29.已知CaCO3 的Ksp=2.8×10-9 ,现将浓度为2×10-4 mol •L- 1 的Na2CO3 溶液与CaCl2 溶液等体积混合,若要产生沉淀,则所用CaCl2 溶液的浓度至少应为( )A.2.8×10-2 mol •L- 1B. 1.4×10-5 mol •L- 1C.2.8×10-5 mol •L- 1D.5.6×10-5 mol •L- 110.下列事实能说明亚硝酸是弱电解质的是( )①25℃时亚硝酸钠溶液的pH 大于7 ②用HNO2 溶液做导电试验,灯泡很暗③HNO2溶液不与Na2SO4 溶液反应④0. 1mol ·L- 1HNO2 溶液的pH=2A.①②③B.②③④C.①④D.①②④11.关于浓度均为0. 1mol ·L- 1 的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是( )A.c(NH4+) :③>①B.水电离出的c(H+) :②>①C.①和②等体积混合后的溶液:c(H+)=c(OH-)+c(NH3 ·H2O)D.①和③等体积混合后的溶液:c(NH4+)>c(Cl-)>c(OH- >c(H+)12.25 ℃时,水电离出的H+浓度是5×10-13mol ·L-1 的硫酸溶液中,硫酸溶液的浓度为( )A.0.01mol ·L-1B.0.02 mol ·L-1C. 1×10-7mol ·L-1D. 1×10-12mol ·L-113.下列各式中属于正确的水解方程式的是( )A.NH4++H2O NH3 ·H2O+H+B.S2-+2H2O H2S+2OH-C.CH3COOH+H2O CH3COO-+H3O+D.CH3COOH+OH-===CH3COO-+H2O14.室温下,用0. 100 mol ·L- 1NaOH 溶液分别滴定20.00 mL 0. 100 mol ·L- 1 的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )A. Ⅰ表示的是滴定盐酸的曲线B.pH=7 时,滴定醋酸消耗的V(NaOH)小于20mLC.V(NaOH)=20mL 时,两份溶液中c(Cl-)=c(CH3COO-)D.V(NaOH)=10mL 时,醋酸溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)15.25℃时,将某强酸和某强碱溶液按1 ∶ 10的体积比混合后,溶液恰好呈中性,则混合前此强酸和强碱的pH 和为( )A. 12B. 13C. 14D. 1516.某温度(T℃)时,水的离子积为K w=1×10-13 。
《水溶液中的离子反应与平衡》 说课稿

《水溶液中的离子反应与平衡》说课稿尊敬的各位评委老师:大家好!今天我说课的题目是“水溶液中的离子反应与平衡”。
下面我将从教材分析、学情分析、教学目标、教学重难点、教法与学法、教学过程、板书设计以及教学反思这几个方面来展开我的说课。
一、教材分析“水溶液中的离子反应与平衡”是高中化学选修四《化学反应原理》中的重要内容。
这部分知识在化学学科中具有承上启下的作用,既是对必修课程中电解质溶液、离子反应等知识的深化和拓展,也为后续学习电化学基础等内容奠定了基础。
教材通过实验探究、理论分析等方式,引导学生认识水溶液中的离子平衡,包括弱电解质的电离平衡、水的电离和溶液的酸碱性、盐类的水解平衡以及难溶电解质的沉淀溶解平衡等。
这些内容不仅有助于学生理解化学反应的本质和规律,还能培养学生的科学思维和探究能力。
二、学情分析学生在必修课程中已经学习了电解质、离子反应等基础知识,对水溶液中的离子有了一定的认识。
但对于离子反应的平衡问题,学生的理解还比较肤浅,需要进一步深入学习和探究。
此外,学生在学习过程中可能会遇到抽象概念难以理解、数学计算能力不足等问题,这就需要教师在教学中采用合适的教学方法和策略,帮助学生突破难点。
三、教学目标1、知识与技能目标(1)理解弱电解质的电离平衡概念,能书写电离方程式。
(2)掌握水的离子积常数,能进行溶液酸碱性的判断和 pH 的计算。
(3)理解盐类水解的原理,能判断盐溶液的酸碱性。
(4)了解难溶电解质的沉淀溶解平衡,能运用溶度积规则判断沉淀的生成、溶解和转化。
2、过程与方法目标(1)通过实验探究和数据分析,培养学生观察、分析和解决问题的能力。
(2)通过对离子平衡概念的建立和应用,培养学生的逻辑思维和抽象概括能力。
3、情感态度与价值观目标(1)让学生体会化学知识与生活、生产的密切联系,激发学生学习化学的兴趣。
(2)培养学生严谨的科学态度和合作精神。
四、教学重难点1、教学重点(1)弱电解质的电离平衡、水的电离和溶液的酸碱性。
第三章 水溶液中的离子平衡 章末归纳与整理-高二化学(人教版选修4)
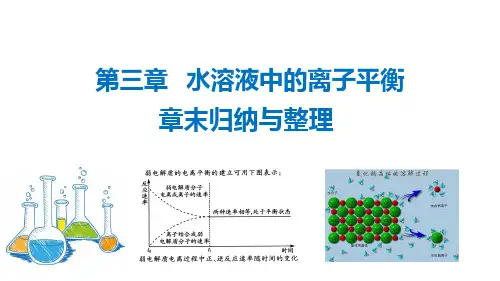
<7
c(H+)<c(OH-)
c(H+)<10-7mol·L-1
>7
pH=-lgc(H+) 常温下:①pH相同的酸(或碱),酸(或碱)越弱,其物质的量 浓度越大。②pH相同的强酸和弱酸溶液,加水稀释相同的 倍数时,强酸溶液的pH变化大。
2.酸碱中和滴定过程中的溶液的pH变化规律:在中和反应中,溶液
pH发生很大的变化,在滴定过程中会因pH突变而使指示剂发生颜色变
中和滴定
1.溶液的酸碱性规律:取决于溶液中c(H+)和c(OH-)的相对大小:
溶液 类别
中性 溶液 酸性 溶液 碱性 溶液 定义
规律
c(H+)与c(OH-)的 关系
室温(25 ℃)
数值
pH
c(H+)=c(OH-) c(H+)=c(OH-)=10-7mol·L-1 =7
c(H+)>c(OH-)
c(H+)>10-7mol·L-1
2.电离平衡的移动与电离平衡常数K、离子浓度的关系
实例 改变条件 加水稀释
CH3COOH CH3COO-+H+ ΔH>0
NH3·H2O
NH4++OH- H+)
c(OH-)
移动方 向
平衡常 数
c(OH-)
c(H+)
向右 不变 减小 增大 向右 不变 减小 增大
加HCl 加NaOH
盐的类别 溶液的酸碱性
原因
强酸 弱碱盐
强碱 弱酸盐
呈酸性, pH<7
呈碱性, pH>7
弱碱阳离子与H2O电离出的OH-结 水解实质:盐电
合,使c(H+)>c(OH-)
离出的阴离子、
弱酸根阴离子与H2O电离出的H+
阳离子与H2O电离 出的H+或OH-结
结合,使c(OH-)>c(H+)
化学选修第3章《水溶液中的离子平衡》知识点总结

化学选修第3章《水溶液中的离子平衡》知识点总结一、电解质、非电解质,强弱电解质的比较1.电解质、非电解质的概念2.强电解质与弱电解质的概念3.强弱电解质通过实验进行判断的方法(以醋酸HAc为例):(1)溶液导电性对比实验:相同条件下,HAc溶液的导电性明显弱于强酸(盐酸、硝酸)(2)测0.01mol/L HAc溶液的pH>2(3)测NaAc溶液的pH值:常温下,pH>7(4)测pH=a的HAc稀释100倍后所得溶液pH<a+2(5)将物质的量浓度相同的HAc溶液和NaOH溶液等体积混合后溶液呈碱性(6)中和10mL pH=1的HAc溶液消耗pH=13的NaOH溶液的体积大于10mL(7)将pH=1的HAc溶液与pH=13的NaOH溶液等体积混合后溶液呈酸性(8)比较物质的量浓度相同的HAc溶液与盐酸,分别与同样的锌粒反应产生气体的速率,后者快特别提醒:1.SO2、NH3、CO2的水溶液虽然能导电,但它们仍属于非电解质。
2.电解质强弱的判断,关键是看电解质在水溶液中是否完全电离。
电解质电离程度与溶解度无直接关系,溶解度大的不一定是强电解质(如醋酸),溶解度小的不一定是弱电解质(如硫酸钡)。
3.电解质溶液导电性取决于溶液中自由移动离子浓度和离子所带电荷数的多少。
一般来说,相同浓度的强电解质的导电性明显强于弱电解质。
弱酸(碱)与弱碱(酸)反应生成了强电解质,溶液的导电性明显增强。
4.电解质的强弱与溶液的导电性没有直接的关系。
如难溶物BaCO 3,它溶于水的部分能完全电离,故属于强电解质,但溶液的导电性几乎为零。
二、弱电解质电离平衡及电离平衡常数要点一:影响电离平衡的因素:1.温度:升高温度,促进电离(因为电离过程吸热),离子浓度增大2.浓度:溶液稀释促进电离,离子浓度反而变小3.同离子效应:加入与弱电解质具有相同的离子的物质,将抑制电离,相关离子浓度增大;4.加入能反应的物质,促进电离,但相关离子浓度降低。
2022届高考化学选修4知识纲要与发散思维训练:第三章 水溶液中的离子平衡知识纲要与变式训练(一)
一、弱电解质【学问纲要】要点1. 电解质与非电解质电解质非电解质定义在水溶液中或熔化状态下能导电的化合物在水溶液中和熔化状态下都不导电的化合物相同点都是与溶解性无关的化合物不同点在肯定条件下能电离不能电离在水溶液中或熔化状态下能导电在水溶液中和熔化状态下都不导电与常见物质类别的关系离子化合物和部分共价化合物全是共价化合物通常为酸、碱、盐、水、典型金属氧化物、某些非金属氢化物等通常为非金属氧化物、某些非金属氢化物、绝大多数有机物等特殊提示:(1)电解质和非电解质二者必需是化合物,单质和混合物既不是电解质也不是非电解质。
如Cu、Cl2等单质,既不属于电解质,也不属于非电解质。
(2)电解质在水溶液或熔融状态下能导电,两个条件满足其中一个即可,而非电解质在两种状况下均不导电。
电解质本身不肯定导电,电解质的导电是有条件的(水溶液或熔融状态)。
(3)电解质必需是电解质本身电离出离子,否则不是电解质。
某些物质的水溶液能导电,是由于它与水作用生成了能电离的物质(电解质),而非本身发生了电离,因而不是电解质,如CO2、SO2、SO3、NH3等是非电解质,而溶于水后生成的H2CO3、H2SO3、H2SO4、NH3·H2O等是电解质。
(4)溶于水后生成了新电解质的化合物也可能是电解质。
如:Na2O、CaO、Na2O2等,它们在熔融状态下即能导电,所以它们自身即为电解质。
(5)对于一些难溶的物质如BaSO4,由于溶解度太小,很难测出其溶液的导电性,但将BaSO4熔化成液态时,能电离出自由移动的Ba2+、SO2-4,能够导电,故BaSO4也是电解质。
要点2. 强电解质与弱电解质电解质强电解质弱电解质相同点都是电解质,在水溶液中都能电离,都能导电,与溶解度无关不同点键型离子键或极性键极性键电离程度完全电离部分电离电离过程不行逆可逆表示方法电离方程式用等号电离方程式用可逆号电解质在溶液中粒子形式水合离子分子、水合离子离子方程式中表示形式离子符号或化学式化学式特殊提示:(1)依据电解质在水溶液中是否全部电离,把电解质分为强电解质和弱电解质。
化学选修4_水溶液中的离子平衡_知识点归纳
第三章 水溶液中的离子平衡一、弱电解质的电离1、定义:电解质:在水溶液中或熔化状态下能导电的化合物,叫电解质。
非电解质:在水溶液中或熔化状态下都不能导电的化合物。
强电解质:在水溶液里全部电离成离子的电解质。
弱电解质: 在水溶液里只有一部分分子电离成离子的电解质。
2、电解质与非电解质本质区别:电解质——离子化合物或共价化合物 非电解质——共价化合物注意:①电解质、非电解质都是化合物 ②SO 2、NH 3、CO 2等属于非电解质 ③强电解质不等于易溶于水的化合物(如BaSO 4不溶于水,但溶于水的BaSO 4全部电离,故BaSO 4 为强电解质)——电解质的强弱与导电性、溶解性无关。
3、电离平衡:在一定的条件下,当电解质分子电离成 离子的速率 和离子结合成 时,电离过程就达到了 平衡状态 ,这叫电离平衡。
4、影响电离平衡的因素:A 、温度:电离一般吸热,升温有利于电离。
B 、浓度:浓度越大,电离程度 越小 ;溶液稀释时,电离平衡向着电离的方向移动。
C 、同离子效应:在弱电解质溶液里加入与弱电解质具有相同离子的电解质,会 减弱 电离。
D 、其他外加试剂:加入能与弱电解质的电离产生的某种离子反应的物质时,有利于电离。
9、电离方程式的书写:用可逆符号 弱酸的电离要分布写(第一步为主)10、电离常数:在一定条件下,弱电解质在达到电离平衡时,溶液中电离所生成的各种离子物质单质化合物电解质非电解质: 非金属氧化物,大部分有机物 。
如SO 3、CO 2、C 6H 12O 6、CCl 4、CH 2=CH 2……强电解质: 强酸,强碱,大多数盐 。
如HCl 、NaOH 、NaCl 、BaSO 4弱电解质: 弱酸,弱碱,极少数盐,水 。
如HClO 、NH 3·H 2O 、Cu(OH)2、H 2O ……混和物纯净物浓度的乘积,跟溶液中未电离的分子浓度的比是一个常数。
叫做电离平衡常数,(一般用Ka表示酸,Kb表示碱。
(完整word版)高二化学期末复习人教版选修四重难点专题突破:第三章水溶液中的离子平衡Word版汇总
《水溶液中的离子平衡》重难点专题突破学习目标定位]1•正确理解弱电解质的电离平衡及其平衡常数。
2•掌握溶液酸碱性规律与 pH 的计算。
3.掌握盐类水解的规律及其应用。
4•会比较溶液中粒子浓度的大小。
5•会分析沉淀溶解平衡及其应用。
弱电解质的电离平衡与电离常数1•弱电解质的电离平衡电离平衡也是一种动态平衡,当溶液的温度、浓度改变时,电离平衡都会发生移动,符合勒夏特列 原理,其规律是(1) 浓度:浓度越大,电离程度越小。
在稀释溶液时,电离平衡向右移动,而离子浓度一般会减小。
(2) 温度:温度越高,电离程度越大。
因电离是吸热过程,升温时平衡向右移动。
(3) 同离子效应:如向醋酸溶液中加入醋酸钠晶体,增大了 CH 3C00「的浓度,平衡左移,电离程度减小;加入稀盐酸,平衡也会左移。
(4)能反应的物质:如向醋酸溶液中加入锌或 NaOH 溶液,平衡右移,电离程度增大。
2•电离常数(电离平衡常数)它们的关系是 K i ? K 2? K 3,因此多元弱酸的强弱主要由 K i 的大小决定。
【例1】 下表是几种常见弱酸的电离方程式及电离平衡常数(25 C )。
酸 电离方程式电离平衡常数KCH 3COOHCH 3COOHCH 3COO 「+ H +1.76 10— 5H 2CO 3H ++ HCO 3K 1 = 4.31 10 7 H 2CO 3— + _ —HCO 3H + CO 2 K 2 = 5.61 10 11H 3PO 4H ++ H 2PO 4 K 1 = 7.52 10 —3H 3PO 4H 2PO 4H ++ HPO2 — 4K 2= 6.23 10 —8HPO*H + + PO*K 3= 2.20 10—13F 列说法正确的是( )A. 温度升高,K 减小B. 向0.1 mol L 71CH 3COOH 溶液中加入少量冰醋酸,C (H+)/C (CH 3COOH)将减小C. 等物质的量浓度的各溶液 pH 关系为pH(Na 2CO 3)>pH(CH 3COONa)>pH(Na 3PO 4)D. PO 47、HPO 2「和H 2PO 4在溶液中能大量共存3.电离平衡的移动与电离平衡常数 K 、离子浓度的关系以CH 3COOH 为例,C (CH3COO 「)c (H十)~(CH COOH )~K 的大小可以衡量弱电解质电离的难易, 有关。
高中化学选修4第三章水溶液中的离子平衡知识点和题型总结
水溶液中的离子平衡§1 知识要点一、弱电解质的电离1、定义:电解质、非电解质 ;强电解质 、弱电解质以下说法中正确的选项是〔 BC 〕A 、能溶于水的盐是强电解质,不溶于水的盐是非电解质;B 、强电解质溶液中不存在溶质分子;弱电解质溶液中必存在溶质分子;C 、在熔融状态下能导电的化合物一定是离子化合物,也一定是强电解质;D 、Na 2O 2和SO 2溶液于水后所得溶液均能导电,故两者均是电解质。
2、电解质与非电解质本质区别:在一定条件下〔溶于水或熔化〕能否电离〔以能否导电来证明是否电离〕 电解质——离子化合物或共价化合物 非电解质——共价化合物 离子化合物与共价化合物鉴别方法:熔融状态下能否导电 以下说法中错误的选项是〔 B 〕A 、非电解质一定是共价化合物;离子化合物一定是强电解质;B 、强电解质的水溶液一定能导电;非电解质的水溶液一定不导电;C 、浓度相同时,强电解质的水溶液的导电性一定比弱电解质强;D 、相同条件下,pH 相同的盐酸和醋酸的导电性相同。
3、强电解质与弱电质的本质区别:在水溶液中是否完全电离〔或是否存在电离平衡〕注意:①电解质、非电解质都是化合物 ②SO 2、NH 3、CO 2等属于非电解质③强电解质不等于易溶于水的化合物〔如BaSO 4不溶于水,但溶于水的BaSO 4全部电离,故BaSO 4为强电解质〕4、强弱电解质通过实验进行判定的方法(以HAc 为例):〔1〕溶液导电性比照实验; 〔2〕测0.01mol/LHAc 溶液的pH>2;〔3〕测NaAc 溶液的pH 值; 〔4〕测pH= a 的HAc 稀释100倍后所得溶液pH<a +2 〔5〕将物质的量浓度相同的HAc 溶液和NaOH 溶液等体积混合后溶液呈碱性 〔6〕中和10mLpH=1的HAc 溶液消耗pH=13的NaOH 溶液的体积大于10mL; 〔7〕将pH=1的HAc 溶液与pH=13的NaOH 溶液等体积混合后溶液呈酸性〔8〕比拟物质的量浓度相同的HAc 溶液与盐酸分别与同样的锌粒反响产生气体的速率最正确的方法是 和 ;最难以实现的是 ,说明理由 。
高二化学_第三章_水溶液中离子平衡(人教版选修4):重难点三_弱电离质在水溶液中的电离平衡
1.电离平衡概念一定条件(温度、浓度)下,分子电离成离子的速率和离子结合成分子的速率相等,溶液中各分子和离子的浓度都保持不变的状态叫电离平衡状态(属于化学平衡)。
任何弱电解质在水溶液中都存在电离平衡,达到平衡时,弱电解质具有该条件下的最大电离程度。
2.电离平衡的特征①逆:弱电解质的电离过程是可逆的,存在电离平衡;②等:弱电解质电离成离子的速率和离子结合成分子的速率相等;③动:弱电解质电离成离子和离子结合成分子的速率相等,不等于零,是动态平衡;④定:弱电解质在溶液中达到电离平衡时,溶液里离子的浓度、分子的浓度都不再改变;⑤变:外界条件改变时,平衡被破坏,电离平衡发生移动;3.影响电离平衡的因素(符合勒沙特列原理)(1)内因-电解质本身的性质,是决定性因素;(2)外因①温度-由于弱电解质电离过程均要吸热,因此温度升高,电离度增大;②浓度-同一弱电解质,浓度越大,电离度越小;在一定温度下,浓度越大,电离程度越小.因为溶液浓度越大,离子相互碰撞结合成分子的机会越大,弱电解质的电离程度就越小.因此,稀释溶液会促进弱电解质的电离;例如:在醋酸的电离平衡 CH3COOH⇌CH3COO-+H+A 加水稀释,平衡向右移动,电离程度变大,但c(CH3COOH)、c(H+)、c(CH3COO-)变小;B 加入少量冰醋酸,平衡向右移动,c(CH3COOH)、c(H+)、c(CH3COO-)增大但电离程度小;③外加物质若加入的物质电离出一种与原电解质所含离子相同的离子,则会抑制原电解质的电离,使电离平衡向生成分子的方向移动;若加入的物质能与弱电解质电离出的离子反应,则会促进原电解质的电离,使电离平衡向着电离的方向移动.以电离平衡CH3COOH⇌CH3COO-+H+为例,各种因素对平衡的影响可归纳为下表:(1)强电解质用“=”,弱电解质用“⇌”(2)多元弱酸分步电离,多元弱碱一步到位.H 2CO3H++HCO3-,HCO3-H++CO32-,以第一步电离为主.NH 3•H2O NH4++OH- Fe(OH)3Fe3++3OH-(3)弱酸的酸式盐完全电离成阳离子和酸根阴离子,但酸根是部分电离;NaHCO 3=Na++HCO3-,HCO3-H++CO32-(4)强酸的酸式盐如NaHSO4完全电离,但在熔融状态和水溶液里的电离是不相同的;熔融状态时:NaHSO4=Na++HSO4-;溶于水时:NaHSO4=Na++H++SO42-;5.电离平衡常数(相当于化学平衡常数)在一定温度下,当弱电解质的电离达到平衡状态时,溶液中电离产生的各种离子浓度的乘积与溶液中未电离的弱电解质分子浓度的比值是一个常数,这个常数叫做电离平衡常数,简称电离常数,通常用K a表示弱酸的电离常数;AB A++B-(1)K的意义:K值越大,则电离程度越大,电解质(即酸碱性)越强;K值越小,电离程度越小,离子结合成分子就越容易,电解质(即酸碱性)越弱.表达式中各组分的浓度均为平衡浓度;(2)K的影响因素:K的大小与溶液的浓度无关,只随温度的变化而变化.温度不变,K值不变;温度不同,K值也不同;(3)多元弱酸的K:多元弱酸的电离是分步电离的,每步电离平衡常数,通常用K1、K2、K3 分别表示,但第一步电离是主要的.如:磷酸的三个K值,K1>K2>K3 ,磷酸的电离只写第一步.说明:①一元弱酸、一元弱碱的电离常数表达式:CH 3COOH CH3COO-+H+一定温度下CH3COOH的电离常数为:NH 3•H2O NH4++OH-一定温度下NH3•H2O的电离常数为:②多元弱酸的电离特点及电离常数表达式:1°分步电离:是几元酸就分几步电离.每步电离只能产生一个H+,每一步电离都有其相应的电离常数.2°电离程度逐渐减小,且K1>K2>K3,故多元弱酸溶液中平衡时的H+主要来源于第一步.所以,在比较多元弱酸的酸性强弱时,只需比较其K1即可.例如25℃时,H3PO4的电离;H 3PO4H2PO4-+H+H 2PO4-HPO42-+H+HPO 42-PO43-+H+多元弱酸溶液中的c(H+)是各步电离产生的c(H+)的总和,在每步的电离常数表达式中的c(H+)是指溶液中H+的总浓度而不是该步电离产生的c(H+).6.电离度电离度(α)(相当转化率,与温度、浓度均有关)A 内因:电解质的本性.B 外因:温度和溶液的浓度等.(1)浓度的影响:醋酸稀释时电离度变化的数据:浓度(mol/L) 0.2 0.1 0.001电离度(%) 0.948 1.32 12.4可见,电离度随浓度的降低而增大.(因浓度越稀,离子互相碰撞而结合成分子的机会越少,电离度就越大.)【重难点指数】★★★★【重难点考向一】强酸和弱酸的鉴别【例1】室温下,对于pH和体积均相同的醋酸和盐酸两种溶液,分别采取下列措施,有关叙述正确的是( ) A.加适量的醋酸钠晶体后,两溶液的pH均增大B.温度都升高20℃后,两溶液的pH均不变C.加水稀释两倍后,两溶液的pH均减小D.加足量的锌充分反应后,两溶液中产生的氢气一样多【答案】A【重难点点睛】考查弱电解质电离,盐酸是强酸,醋酸是弱酸,所以醋酸溶液中存在电离平衡,升高温度能促进弱电解质电离,pH相同的醋酸和盐酸,醋酸的浓度大于盐酸,不同的酸和相同金属反应,生成氢气的速率与溶液中离子浓度成正比;易错选项是B,注意对于相同浓度的盐酸和醋酸溶液,升高温度,盐酸的pH不变,但醋酸的pH改变,为易错点。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
考点一弱电解质的电离(一)强、弱电解质1.概念[注意]①六大强酸:HCl、H2SO4、HNO3、HBr、HI、HClO4。
②四大强碱:NaOH、KOH、Ca(OH)2、Ba(OH)2。
③大多数盐包括难溶性盐,如BaSO4。
2.电离方程式书写(1)弱电解质①多元弱酸分步电离,且第一步电离程度远远大于第二步(通常只写第一步电离),如H2CO3的电离方程式:H2CO3H++HCO-3、HCO-3H++CO2-3。
②多元弱碱电离方程式一步写成,如Fe(OH)3电离方程式为Fe(OH)3Fe3++3OH-。
(2)酸式盐①强酸的酸式盐在溶液中完全电离,如NaHSO4的电离方程式为NaHSO4===Na++H++SO2-4。
②弱酸的酸式盐中酸根离子在溶液中不能完全电离,如NaHCO3===Na++HCO-3、HCO-3H++CO2-3。
(二)弱电解质的电离平衡1.电离平衡的建立2.电离平衡的特征(三)影响弱电解质电离平衡的因素1.影响电离平衡的内因弱电解质本身的性质是决定电离平衡的主要因素。
2.外界条件对电离平衡的影响以弱电解质HB的电离为例:HB H++B-。
(1)温度:弱电解质电离吸热,温度升高,电离平衡向正反应方向移动,HB的电离程度增大,c(H+)、c(B-)均增大。
(2)浓度:稀释溶液,电离平衡向正反应方向移动,电离程度增大,n(H+)、n(B-)增大,但c(H+)、c(B-)均减小。
(3)相同离子:在弱电解质的溶液中,加入与弱电解质具有相同离子的强电解质,电离平衡向逆反应方向移动,电离程度减小。
(4)加入能与电离出的离子反应的物质:电离平衡向正反应方向移动,电离程度增大。
(四)溶液的导电能力电解质溶液导电能力取决于溶液中自由移动离子浓度和离子所带电荷数。
自由移动离子浓度越大,离子所带电荷数越多,则导电能力越强。
将冰醋酸、稀醋酸加水稀释,其导电能力随加水的量的变化曲线如图所示。
[说明]①OA段导电能力随加水量的增多导电能力增强,原因是冰醋酸发生了电离,溶液中离子浓度增大。
②AB段导电能力减弱的原因,随水的加入,溶液的体积增大,离子浓度变小,导电能力减弱。
[拓展归纳]外界条件对电离平衡影响的四个不一定(1)稀醋酸加水稀释时,溶液中不一定所有的离子浓度都减小。
因为温度不变,K W=c(H+)·c(OH-)是定值,稀醋酸加水稀释时,溶液中的c(H+)减小,故c(OH-)增大。
(2)电离平衡右移,电解质分子的浓度不一定减小,如对于CH3COOH CH3COO-+H+,平衡后,加入冰醋酸,c(CH3COOH)增大,平衡右移,根据勒夏特列原理,只能“减弱”而不能消除,再次平衡时,c(CH3COOH)比原平衡时大。
(3)电离平衡右移,离子的浓度不一定增大,如在CH3COOH溶液中加水稀释或加少量NaOH固体,都会引起平衡右移,但c(CH3COOH)、c(H+)都比原平衡时要小。
(4)电离平衡右移,电离程度也不一定增大,加水稀释或增大弱电解质的浓度,都使电离平衡向电离方向移动,但加水稀释时弱电解质的电离程度增大,而增大弱电解质的浓度时弱电解质的电离程度减小。
[题点全练]1.某浓度的氨水中存在平衡:NH3·H2O NH+4+OH-,如想增大NH+4的浓度,而不增大OH-的浓度,应采取的措施是()①适当升高温度②加入NH4Cl固体③通入NH3④加入少量盐酸A.①②B.②③C.②④D.①④解析:选C升温平衡向右移动,c(NH+4)、c(OH-)都增大;加入NH4Cl固体,相当于增大c(NH+4),平衡向左移动,c(OH-)减小,但c(NH+4)仍较原来增大,因平衡移动只能减小其增大的程度,而不能完全抵消它增大的部分;通入NH3平衡向右移动,c(NH+4)、c(OH -)都增大;加入少量盐酸,H+与OH-反应使c(OH-)下降,平衡向右移动,使c(NH+4)增大。
2.(2018·山西五校第一次联考)下列关于醋酸性质的描述,不能证明它是弱电解质的是()A.1 mol·L-1的醋酸溶液中H+浓度约为10-3 mol·L-1B.醋酸溶液中存在CH3COOH分子C.10 mL pH=1的醋酸溶液与足量锌粉反应生成H2 112 mL(标准状况)D.10 mL 0.1 mol·L-1的醋酸溶液与10 mL 0.1 mol·L-1的NaOH溶液恰好完全中和解析:选D A项,1 mol·L-1的醋酸溶液中c(H+)约为10-3 mol·L-1,说明CH3COOH部分发生电离,则CH3COOH是弱电解质;B项,醋酸溶液中存在CH3COOH分子,说明CH3COOH未完全发生电离,则CH3COOH是弱电解质;C项,Zn与醋酸溶液发生的反应为Zn+2CH3COOH===(CH3COO)2Zn+H2↑,标准状况下112 mL H2的物质的量为0.005 mol,则参与反应的n(CH3COOH)=0.01 mol;10 mL pH=1的醋酸溶液中,CH3COOH电离产生的n(H+)=0.01 L×0.1 mol·L-1=0.001 mol,则有n(H+)<n(CH3COOH),说明CH3COOH部分发生电离,则CH3COOH是弱电解质;D项,10 mL 0.1 mol·L-1的醋酸溶液与10 mL 0.1 mol·L-1的NaOH溶液中,n(CH3COOH)=n(NaOH)=0.01 L×0.1 mol·L-1=0.001 mol,二者能恰好完全反应,只能说明CH3COOH为一元酸,不能证明CH3COOH 是弱电解质。
3.(2018·菏泽调研)H2S水溶液中存在电离平衡H2S H++HS-和HS-H++S2-。
若向H2S溶液中()A.加水,平衡向右移动,溶液中氢离子浓度增大B.通入过量SO2气体,平衡向左移动,溶液pH增大C.滴加新制氯水,平衡向左移动,溶液pH减小D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小解析:选C向H2S溶液中加水,平衡向右移动,溶液中n(H+)增大,由于溶液体积增大的程度大于n(H+)增大的程度,因此溶液中c(H+)减小,A错误。
通入SO2气体,发生的反应为2H2S+SO2===3S↓+2H2O,平衡向左移动;当SO2过量时,SO2与水反应生成H2SO3,H2SO3的酸性比H2S强,因此溶液的pH减小,B错误。
滴加新制氯水,发生的反应为H2S+Cl2===2HCl+S↓,溶液中c(H2S)减小,平衡向左移动;由于反应生成的HCl 为强酸,完全发生电离,溶液的pH减小,C正确。
加入少量CuSO4,发生的反应为CuSO4+H2S===CuS↓+H2SO4,溶液中c(S2-)减小,平衡向右移动,溶液中c(H+)增大,D错误。
[真题验收]下列关于电解质溶液的说法正确的是()A.(2016·四川高考)0.1 L 0.5 mol·L-1 CH3COOH溶液中含有的H+数为0.05N AB.(2016·江苏高考)室温下,稀释0.1 mol·L-1 CH3COOH溶液,溶液的导电能力增强C.(2016·全国卷Ⅲ)向0.1 mol·L-1 CH3COOH溶液中加入少量水,溶液中c(H+)c(CH3COOH)减小D .(2013·江苏高考)CH 3COOH 溶液加水稀释后,溶液中c (CH 3COOH )c (CH 3COO -)的值减小解析:选D A 项,CH 3COOH 为弱电解质,在水溶液中部分电离,0.1 L 0.5 mol·L -1 CH 3COOH 溶液中含有的H +数小于0.05N A ,错误;B 项,CH 3COOH 溶液中存在平衡,CH 3COOHCH 3COO -+H +,加水稀释,平衡右移,产生的离子数增加,但溶液的体积增大,c (CH 3COO -)、c (H +)减小,导电能力减弱,错误;C 项,加水稀释时,平衡CH 3COOHCH 3COO -+H +右移,n (H +)增大,n (CH 3COOH)减小,c (H +)c (CH 3COOH )=n (H +)/Vn (CH 3COOH )/V =n (H +)n (CH 3COOH ),故比值变大,错误;D 项,稀释时,n (CH 3COO -)增大,n (CH 3COOH)减小,故c (CH 3COOH )c (CH 3COO -)的值减小,正确。
考点二 电离度与电离常数(一)电离度1.概念:一定条件下,当弱电解质在溶液中达到电离平衡时,溶液中已经电离的电解质分子数占原来弱电解质总分子数的百分数。
注意:指已电离的电解质与未电离的电解质的分子数之和。
2.表达式:α=已电离的弱电解质的浓度弱电解质的初始浓度×100%。
3.意义:衡量弱电解质的电离程度,在相同条件下(浓度、温度相同),不同弱电解质的电离度越大,弱电解质的电离程度越大。
4.影响因素 温度的 影响 升高温度,电离平衡向右移动,电离度增大; 降低温度,电离平衡向左移动,电离度减小 浓度的 影响 当弱电解质溶液浓度增大时,电离度减小; 当弱电解质溶液浓度减小时,电离度增大(二)电离常数1.概念:在一定条件下,弱电解质在达到电离平衡时,溶液中电离所生成的各种离子浓度的乘积与溶液中未电离的分子浓度的比值是一个常数,这个常数叫做电离平衡常数。
用K(弱酸的用K a,弱碱的用K b)表示。
2.表达式(1)对于一元弱酸HA:HA H++A-电离常数K a =c(H +)·c(A-)c(HA)。
(2)对于一元弱碱BOH:BOH B++OH-电离常数K b=c(B+)·c(OH-)c(BOH)。
(3)对于多元弱酸,以H2CO3为例:H2CO3H++HCO-3K a1=c(H+)·c(HCO-3) c(H2CO3)HCO-3H++CO2-3K a2=c(H+)·c(CO2-3) c(HCO-3)3.意义相同条件下,K值越大,表示该弱电解质越易电离,所对应的酸性或碱性相对越强。
4.特点电离常数只与温度有关,与电解质的浓度、酸碱性无关,由于电离过程是吸热的,故温度升高,K增大。
多元弱酸是分步电离的,各级电离常数的大小关系是K1≫K2……,所以其酸性主要决定于第一步电离。
(三)电离常数的4个应用判断弱酸(或弱碱)的相对强弱电离常数越大,酸性(或碱性)越强。
如:常温下,CH3COOH的K a=1.8×10-5,H2CO3的K a1=4.3×10-7、K a2=5.6×10-11。
