第八章 羰基化过程
最新8羰基化过程汇总

8.3 烯烃的氢甲酰化 一.化学原理
(1)主、副反应(丙烯) 主:
副:a.异构醛
b.加氢生成丙烷
平行反应
c.醛加氢生成醇--连串反应
(2)热力学
放热反应,热效应较大 平衡常数大,热力学有利,动力学控制 副反应比主反应热力学有利,选择催化 剂和工艺条件促进主反应
d.催化剂 HRh(Co)x(PPh3)y
x+y=4
PPh3↑ ,正/异丁醛↑ ,r ↓
羰基化反应。
2 低压法甲醇羰化反应合成醋酸基本原理
Monsanto低压法采用铑碘催化剂体系,主要 化学反应如下:
动力学研究表明,与BASF高压法不同,Monsanto低 压法合成醋酸反应对甲醇与一氧化碳为零级,对铑 及碘为一级,反应速率的控制步骤为碘甲烷的氧化 加成。动力学方程式如下:
反应速度常数为3.5×106e-14.7/RTL/mol·s,式中活化 能的单位是kJ/mol。Leabharlann (3)催化剂①羰基钴
T ↑ ,PCO ↑ 催化剂↑ ,PCO ↑
缺点:正异构醛比例低,催化剂热稳定性差
②膦羰基钴
配位基膦(PR3) 特点:
a.稳定性增加,活性降低 b.直链产物选择性增加 C.加氢活性较高 d.副产物少 e.适应性差
③膦羰基铑
选择性好,活性高,异构化性能高 催化剂稳定,可在较低压力下操作
(3)氢酯化(与CO和ROH反应)
(4)不对称合成
生成单一对映体的醛 某些结构的烯烃进行羰基合成反应能生成含有对映 异构体的醛。若使用特殊的催化剂,使生成的两种 对映体含量不完全相等,理想情况下仅生成某种单 一对映体,这样的反应称作不对称催化氢甲酰化反 应。
8.羰基化过程

2 低压法甲醇羰化反应合成醋酸基本原理
Monsanto低压法采用铑碘催化剂体系,主要 化学反应如下:
动力学研究表明,与BASF高压法不同,Monsanto低 压法合成醋酸反应对甲醇与一氧化碳为零级,对铑 及碘为一级,反应速率的控制步骤为碘甲烷的氧化 加成。动力学方程式如下: 反应速度常数为3.5×106e-14.7/RTL/mol· s,式中活化 能的单位是kJ/mol。
二. 甲醇羰化制醋酸的工艺流程
1 BASF高压法生产工艺流程
2 Monsanto低压法生产工艺流程
3 甲醇低压羰基合成醋酸的优缺点
甲醇低压羰化法制醋酸在技术经济上的优越性很大,其优点在于:
(1) 利用煤、天然气、重质油等为原料,原料路线多样化,不受原油 供应和价格波动影响。 (2) 转化率和选择性高,过程能量效率高。 (3) 催化系统稳定,用量少,寿命长。 (4) 反应系统和精制系统合为一体,工程和控制都很巧妙,结构紧凑。 (5) 虽然醋酸和碘化物对设备腐蚀很严重,但已找到了性能优良的耐 腐蚀材料-哈氏合金C(Hastelloy Alloy C),是一种Ni-Mo合金,解决 了设备的材料问题。 (6) 用计算机控制反应系统,使操作条件一 直保持最佳状态。 (7) 副产物很少,三废排放物也少,生产环境清洁。 (8) 操作安全可靠。 主要缺点是催化剂铑的资源有限,设备用的耐腐蚀材料昂贵。
二 丙烯氢甲酰化合成丁、辛醇
1.丁、辛醇用途及合成路线 (1)用途 (2)合成路线
①乙烯为原料,乙醛缩合法 ②氢甲酰化法 a. 液相法 催化剂:羰基钴-高压 膦羰基铑-低压
Hale Waihona Puke b.在碱存在下缩合为辛烯醛
c.
2.丙烯低压氢甲酰化合成正丁醛 (1)反应条件
羰基化的定义

羰基化是指有机化合物中存在羰基(C=O)的反应或转化过程。
羰基是由碳和氧组成的官能团,常见于各种有机化合物中,如醛、酮、酸酐等。
羰基化过程可以是化学反应的一部分,其中羰基发生改变,通常与其他分子中的特定官能团进行反应。
以下是一些羰基化的例子:
1. 醛和酮的还原:醛和酮中的羰基可以被还原成相应的醇。
这种还原通常涉及氢气和催化剂,如氢气和铂催化剂。
2. 醇的氧化:醇中的羟基(-OH)可以被氧化为羰基,形成醛或酮。
这可以通过氧气或氧化剂来实现。
3. 酰基化反应:酸酐或酸氯等羰基化合物可以与其他化合物中的醇或胺反应,形成酯或酰胺。
4. 卡宾反应:卡宾是一种具有未成对电子对的碳的中间体,它可以与羰基化合物反应,形成新的有机化合物。
这些只是羰基化反应的一些例子,实际上,这一领域涉及到多种不同的反应和转化。
具体的羰基化定义可能会根据上下文和化学反应的类型而有所不同。
091104-10_第八章_羰基化合物的反应
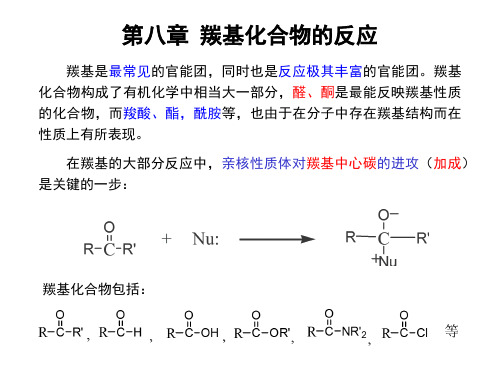
而在PH=6时,
以单负离子存在。
PH=6时的单负离子能产生亲核催化作用:
例8-4:
乙酰基水杨酸的水解动力学研究也显示出负离子质体水解比中性质体 快,这说明也存在分子内催化作用。可能存在以下方式 ①亲核催化:
这是一个亲核催化过程,但同位素标记法否定了这个过程,因为 酚还不是一个好的离去基团。
但乙酰水杨酸在H2O18中水解产物中没有18O进入。可见水杨酸与乙酸 的混合酸酐并不是乙酰水杨酸水解反应的中间体。
第八章 习题
判定下列分子可能有几种方式进行分子内催化酯水解反应,写出反应 机理及能体现该催化作用的过渡态:
中间体的稳定性降低金属锂试剂与羰基化合物的加成速度是与其聚合程度有关的二聚体比四聚体快10倍左右二聚体的反应一般是经过一个环状过度态
第八章 羰基化合物的反应
羰基是最常见的官能团,同时也是反应极其丰富的官能团。羰基 化合物构成了有机化学中相当大一部分,醛、酮是最能反映羰基性质 的化合物,而羧酸、酯,酰胺等,也由于在分子中存在羰基结构而在 性质上有所表现。 在羰基的大部分反应中,亲核性质体对羰基中心碳的进攻(加成) 是关键的一步:
8.2.2 含NH2化合物对羰基的加成
亲核性质体对羰基化合物加成产生的四面体中间体,通常是不稳 定的,会继续断裂形成新的双键。含氨基化合物对羰基的加成是此类 反应中较典型的:
这些反应都是可逆的,常常通过这些反应的逆反应即水解反应 来对其机理进行研究。
亚胺在酸性水溶液中极易水解,水解机理随底物及体系PH值而变化:
羧酸根负离子也可作为亲核催化剂,此时要求R’O- 的碱性< R’’CO2-。
在中间体中,如果R”CO2-的离去比-OR’快,则观察不到催化现象。
8.6 酯的胺解
羰基化过程

• 用这种方法改变催化剂的性能称之为催化剂的改 性,引入的新配体也叫作改性剂。改变配位体的研 究构成了羰基合成催化剂研究的重要方面。
化 学 工 程 与 工 艺 教 研 室
化 学 工 艺 学 电 子 教 案
8.2.2 配位体
• 三价膦(PR3)的改性效果最为优越,已被工业采用。 • 羰基钴催化剂的主要问题是在较高的CO压力下才能稳定, 且产物的n/i不高。改性目标首先是克服这两个缺点。与 CO配体相比,三价膦是强的δ电子给予体,弱的π电子接 受体,PR3取代CO与钴配位后,增大了钴原子上的负电荷 密度。钴将增强的负电荷密度再通过适当轨道反馈给未取 代的CO,从而加强了钴对CO的配合能力,使整个分子的 稳定性增加。从而使改性后的催化剂可以在较低的压力下 进行反应,但同时造成剐作用是反应速度下降很多,必须 以提高催化剂浓度等方法加以弥补。三价膦是一个不等性 sp3杂化轨道构型,配位后呈四面体结构,因此比原先直线 形的CO配体产生更强的定向效应。大的方向位阻有利于生 成正构醛,使反应的正异比增加。另外对于羰基钴来说, 三价膦改性剂大大增加催化剂的加氢活性,一方面可以使 生成的醛直接加氢为醇,省去了加氢步骤,另一方面烯烃 加氢成烷烃的副反应也明显增加。
化 学 工 程 与 工 艺 教 研 室
化 学 工 艺 学 电 子 教 案
8.3.1 甲醇羰化反应合成醋酸的基本原理 • BASF高压法与Monsanto低压法甲醇羰化反 应合成醋酸化学原理基本相同,反应过程大 同小异,也都有一个催化剂循环和一个助催 化剂循环。并且都采用第Ⅷ族元素为催化 剂,碘为助催化剂,但因具体金属元素不同. 活性、中间体组成相异,催化效果有差别, 反应动力学、反应速率控制步骤也有所不同。 化
化 学 工 程 与 工 艺 教 研 室
8 羰基化过程

化工工艺学
随着一碳化学的发展,有一氧化碳参与 的反应类型逐渐增多,通常将在过渡金 属配合物(主要是羰基配合物)催化剂存在 下,有机化合物分子中引入羰基的反应 均归入羰化反应的范围,其中主要有两 大类。
化工工艺学
过渡金属络合物(主要是羰基化合物)
催化剂下,有机化合物引入羰基。
均相反应,反应条件温和,选择性好。
(4)不对称合成生Fra bibliotek单一对映体的醛
化工工艺学
2.甲醇的羰化反应
(1)合成醋酸 孟山都法(Monsanto acetic acid process)
(2)合成醋酐
化工工艺学
(3)合成甲酸
(4)合成草酸酯、碳酸二甲酯、乙二醇
化工工艺学
8.2羰基化反应的理论基础
在催化反应中,凡催化剂以配合物的 形式与反应分子配位使其活化,反应分 子在配合物体内进行反应形成产物,产 物自配合体中解配,最后催化剂还原, 这样的催化剂称为配位(络合)催化剂,这 样的催化过程被称之为配位(络合)催化过 程。羰基合成反应是典型的配位催化反 应。
化工工艺学
b.在碱存在下缩合为辛烯醛
c.
化工工艺学
2.丙烯低压氢甲酰化合成正丁醛
(1)反应条件
a. 温度
T↑ ,r丁醛↑ ,r副↑ ,催化剂失活速度↑ T↓ ,催化剂活性低,用量大
100-110℃ b.压力
1.8MPa
c.原料配比
H2 ↑ ,丙烯↑ ,丙烷↑ ,原料损失↑ ∴ 控制H2和丙烯的量
压力
PCO ↑ ,r ↓ 总压不变: 钴: PCO ↑ ,正/异↑ 铑: PCO ↑ ,正/异↓ PH2 ↑ ,r ↑ ,正/异↑
第8章 羰基化过程
配位体: CO基团--HM (CO)m 改变配位体影响整个配位化合物的电子结构和空 间结构
配位体改性:大多是第V主族元素的三价化合物。 提供孤对电子与配合物的中心原子 配位。
HM(CO)m+L→HM(CO)m-1L+CO HM(CO)m-1L+L→HM(CO)m-2L2+CO HM(CO)m-2L2+L→HM(CO)m-3L3+CO
艺条件促进主反应
(3)催化剂
①羰基钴
2Co + 8CO
Co2(CO)8
H2 2HCo(CO)4
催化剂稳定,必须保持足够高的CO 分压
T ↑ ,催化剂稳定所需PCO ↑ 催化剂↑ ,催化剂稳定所需PCO ↑
T( ℃) 20 150 150
PCO(MPa) 0.05 4 8
催化剂用量 0.2% 0.2% 0.9%
采用水溶液膦配位体改性的水溶性铑膦催化剂
8.2 烯烃的氢甲酰化
1.化学原理
(1)主、副反应(丙烯)
主: CH3CH=CH2 + H2 + CO 副: a.异构醛
b.加氢生成丙烷
CH3CH2CH2CHO
平行反应
c.醛加氢生成醇、缩醛--连串反应
(2)热力学
放热反应,热效应较大 平衡常数大,热力学有利,动力学控制 副反应比主反应热力学有利,选择催化剂和工
催化剂:以过渡金属M为中心的羰基氢化物 HxMy(CO)zLn
羰基合成催化剂评价
活性: 单位金属浓度在单位时间内催化产生的目 的产物量
选择性:化学选择性 区域选择性(醛基的位置--正构醛和 异构醛的摩尔比) 对映体选择性(不对称合成)
中心原子
化学工艺学第八章-4丙烯羰基化合成丁醇、辛醇
化学工艺学第八章-4丙烯羰基化合成丁醇、辛醇第八章羰基化过程8(4 丙烯羰基化合成丁醇、辛醇 8(4(1 烯烃氢甲酰化反应的基本原理8(4(1(1 反应过程烯烃氢甲酰化主反应是生成正构醛,由于原料烯烃和产物醛都具有较高的反应活性,故有连串副反应和平行副反应发生。
平行副反应主要是异构醛的生成和原料烯烃的加氢,这两个反应是衡量催化剂选择性的重要指标。
主要连串副反应是醛加氢生成醇和缩醛的生成。
以丙烯氢甲酰化为例说明。
主反应CH= CHCH+CO+H?CHCHCHCHO (8—39) 232322副反应CH=CHCH+CO+H (CH3)CHCHO (8—40) 2222异丁醛CH2=CHCH+HCHCHCH (8—41) 22323CHCHCHCHO+H?CHCHCHCHOH (8—42) 322232222CHCHCHCHO?CHCHCHCH(OH)CH(CH())CHCH (8—43) 32232223缩二丁醛CHCHCHCHO+(CH)CHCHO ? 32232CHCH(CH)33CH(OH)CH(CHO)CHCH 23缩醛 (8—44)在过量丁醛存在下,在反应条件下,缩丁醛又能进一步与丁醛化合,生成环状缩醛、链状三聚物,缩醛很容易脱水生成另一种副产物烯醛CHCHCH(OH)CH(CHO)CHCH?CHCHCHCH—C(CH)CHO +HO CH32223322252(8—45) 8(4(1(2 催化剂各种过渡金属羰基配位化合物催化剂对氢甲酰反应均有催化作用,工业上经常采用的有羰基钴和羰基铑催化剂,现分别讨论如下。
1.催化剂及特性催化剂名称活性组分缺点HCO(CO) 羰基钴催化剂热稳定性差,容易分解析出钴而失去4活性HCO(CO).[P(n-R)] 膦羰基钴催化33剂可看作是[P(n-R)]取催化剂的热稳定性好,直链正构醛的3代了HCO(CO)中的选择性佳,加氢活性高、醛缩合及醇4CO.(R为烷基、芳基、醛缩合等连串副反应少等优点。
第八章 羰基化过程
CH≡CH+CO+H2O
CH2=CHCOOH
• (3)氢酯化(与CO和ROH反应)
RCH=CH2+CO+R’OH
CH≡CH+CO+ROH
RCH2CH2COOR’
CH2=CHCOOR
• (4)不对称合成
生成单一对映体的醛
2.甲醇的羰化反应
• • • • (1)合成醋酸 (2)合成醋酐 (3)合成甲酸 (4)合成草酸酯、碳酸二甲酯、乙二醇
催化剂浓度,%
生成烷烃量 产物 正/异比
0.1-1.0
低 醛/ 醇 3-4:1
0.6
明显 醇/ 醛 8-9:1
0.01-0.1
低 醛 12-15:1
(3)工艺流程
• • • • 反应 精制 轻组分回收 催化剂制备与再生
优缺点
优点 (1)原料多样化 (2 )S 和X 高 (3)催化系统稳定 (4)反应和精制系统合为一体 (5)Ni-Mo合金耐腐蚀 (6)计算机控制保持最佳 (7)副产物少 (8)操作安全可靠 缺点:铑资源少,设备昂贵
(3)催化剂
PPh3↑,正/异丁醛↑,r↓
x+y=4
(2)工艺流程
放空 合成气 丙烯 净化 反应 气液分离器
正丁醛 异丁醛
净化
(3)反应器
不锈钢釜式反应器
搅拌器、冷却装置、气体分布器
(4)低压法特点
优点: • 反应条件温和 • 副反应少,原料消耗少 • 催化剂易分离回收 • 污染少 缺点: 铑资源太少 配位体三苯基膦有毒
①羰基钴 2Co+8CO
Co2(CO)8 2HCo(CO)4
8.羰基化过程.
2 低压法甲醇羰化反应合成醋酸基本原理
Monsanto低压法采用铑碘催化剂体系,主要 化学反应如下:
动力学研究表明,与BASF高压法不同,Monsanto低 压法合成醋酸反应对甲醇与一氧化碳为零级,对铑 及碘为一级,反应速率的控制步骤为碘甲烷的氧化 加成。动力学方程式如下:
反应速度常数为3.5×106e-14.7/RTL/mol·s,式中活化 能的单位是kJ/mol。
d.催化剂 HRh(Co)x(PPh3)y
x+y=4
PPh3↑ ,正/异丁醛↑ ,r ↓
(2)工艺流程
合成气 净化
丙烯 净化
放空
反
气液
应
分离
器
异丁醛 正丁醛
(3)反应器
不锈钢釜式反应器 搅拌器、冷却装置、气体分布器
(4)低压法特点
优点: 反应条件温和 副反应少,原料消耗少 催化剂易分离回收 污染少 缺点:
1.不饱和化合物的羰化反应
(1)氢甲酰化(与CO和H2反应)
在双键两端的C原子上分别加上一个 氢和一个甲酰基(-HCHO)
①烯烃的氢甲酰化 CH2=CH2+CO+H2→CH3CH2CHO
②烯烃衍生物的氢甲酰化 (不饱和醇、醛、酯、醚,含卤素、含氮化合物)
(2)氢羧基化(与CO和H2O反应)
(3)氢酯化(与CO和ROH反应)
烯烃与合成气(CO/H2)或一定配比的一氧化碳及氢 气在过渡金属配合物的催化作用下发生加成反应,生 成比原料烯烃多一个碳原子的醛。这个反应被命名为 羰基合成 (oxo synthesis),也称作Röelen反应。
过渡金属络合物(主要是羰基化合物)催化剂下,有 机化合物引入羰基。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
进展1—催化剂的均相固相化
为了克服铑膦催化剂制备和回收复杂的缺点,↓消耗量,↓产 品分离步骤等,进行了均相催化剂固载化的研究,即把均相 催化剂固定在有一定表面的固体上,使反应在固定的活性位 上进行,催化剂兼有均相和多相催化的优点。 固 相 化 方 法 化学键合法
通过各种化学键合把络合催化剂负载于高分子载体上 (eg:苯乙烯和二乙烯基苯共聚物 、离子交换树脂 )
HxMy(CO)zLn
中心原子 配体
中心原子
工业上采用的羰基合成催化剂的中心原子主要为:
钴和铑
配位体
CO、PR3(膦)、 P(OR)3 (亚磷酸酯)、 AsR3 (胂)、 SbR3 (锑) R——烷基、芳基、环烷基、杂环基等
反应相
一类是将配位催化剂固载化,使用液体或气体原料进行多 相反应,最终实现产物与催化剂分离的目的。 另一类是催化剂和反应产物处于互不相溶的两种液相之中, 反应后只需进行简单的相分离,便可达到分离催化剂的目 的——两相催化体系。
物理吸附法
吸附于硅胶、氧化铝、活性炭、分子筛等无机载体 上,或将催化剂溶于高沸点溶剂后,再浸于载体上
目前活性金属流失问题成为阻碍固相络合催化剂实际应用的 主要障碍 !
进展2-非铑催化剂
铑是稀贵资源,故利用受到限制。 国外除对铑催化剂的回收利用进一步研究外,对 非铑催化剂的开发也非常重视。其中铂系催化剂 有很好的苗头:我国研究了Pt-Sn-P系催化剂。日
主要包括加氢和产品精制两个过程
2.丙烯低压氢甲酰化合成正丁醛
(1)反应条件
a. 温度
T↑ →r丁醛↑ ,r副↑ ,催化剂失活速度↑
T↓ →催化剂活性低,用量大
100-110℃
b.压力
1.8MPa (压力太高,丙烯和丙烷溶解度增大, 会增加稳定塔的负荷 )
c.原料配比Байду номын сангаас
H2 ↑ ,丙烯↑ →生成丙烷↑ ,原料损失↑
(2)催化剂
活性组分 [Rh+(CO)2I2]助剂:HI、CH3I、I2
(3)反应机理 自学
2、工艺流程
反应 精制 轻组分回收 催化剂制备与再生
优缺点
优点: (1)原料多样化 (2)S和X高 (3)催化系统稳定 (4)反应和精制系统合为一体 (5)Ni-Mo合金耐腐蚀 (6)计算机控制保持最佳 (7)副产物少 (8)操作安全可靠 缺点:铑资源少,设备昂贵
催化剂:未改性羰基钴 Natta于1955年报道
动力学方程
动力学方程
催化剂:HRh(CO)2L2
反应速度与烯烃浓度无关 控制步骤:HCORh(CO)L2与H2的反应
(5)烯烃结构的影响
①对反应速度影响 a.双键位置与反应速度密切相关,直链α –烯烃反应 最快 b.支链降低反应速度 ②对产物影响 a.环戊烯、环己烯反应无异构醛生成 b.双键位置对正/异比无影响 c.带支链:醛基加到α -碳原子
气体分布器
(4)低压法特点
优点: 反应条件温和 副反应少,原料消耗少(正/异醛比率
高达12~15:1 )
催化剂易分离回收(利用率高,损失少) 污染少,接近无公害工艺 缺点: 铑资源太少 配位体三苯基膦有毒
4.进展
低压氢甲酰化法有许多优越性,但因 铑价格昂贵,催化剂制备和回收复杂 等因素,目前正从开发新催化体系和 改进工艺二个方面加以革新。另外, 使用羰基合成方法生产的工业产品已 经突破了传统概念中的羰基合成醇类。
应类型逐渐增多,通常将在过渡金属络合物
(主要是羰基络合物)催化剂存在下,有机化合
物分子中引入羰基(>C=O)的反应均归入羰化
反应的范围,其中主要有两大类。
羰 化 反 应 的 类 型
甲醇的羰化反应
不饱和化合物的羰化反应
8.1 反应类型
1.不饱和化合物的羰化反应
(1)氢甲酰化(与CO和H2反应)
HCo(CO)4
HCo(CO)3P(n-C4H9)3
HRh(CO)(PPh3)3
140~180 20~30 0.1-1.0 低 醛/醇 3~4∶1
160~200 5~10 0.6 明显 醇/醛 8~9∶1
90~110 1~2 0.01-0.1 低 醛 12~15∶1
(4)反应机理与动力学
反应机理见P260(自学) 羰基合成是放热反应,放热量因原料结构的 不同而有所不同,反应的平衡常数很大。所 以氢甲酰反应在热力学上是有利的,反应主 要由动力学因素控制。
总结
放热反应,热效应较大
平衡常数大,热力学有利,动力学控制
副反应比主反应热力学有利,选择催化剂
和工艺条件促进主反应
(3)催化剂
①羰基钴
催化剂热稳定性差
T( ℃) 20 150 150
PCO(MPa) 0.05 4 8
催化剂用量 0.2% 0.2% 0.9%
T ↑ ,PCO ↑ 催化剂↑ ,PCO ↑
3.理论基础
催化剂以配合物的形式与反应分子配位使 其活化,反应分子在配合物体内进行反应 形成产物,产物自配合体中解配,最后催 化剂还原——称为配位(络合)催化剂; 该催化过程——配位(络合)催化过程。
羰基合成反应是典型的配位催化反应
Catalyst
羰基合成的催化剂往往是“原位”形成的。 所谓“原位(In situ)”是指加入反应体系中的化 合物或配合物在反应条件下就地形成催化剂, 同时产生催化作用。 羰基合成催化剂的典型结构是以过渡金属(M) 为中心原子的羰基氢化物,它可以被某种配 位体(L)所改性。
8.3 丙烯氢甲酰化合成丁、辛醇
1.丁、辛醇用途及合成路线 (1)用途 (2)合成路线
①乙烯为原料,乙醛缩合法 ②氢甲酰化法 a.丙烯氢甲酰化法合成丁醛 液相法 催化剂:羰基钴-高压 膦羰基铑-低压 包括氢甲酰化反应、催化剂的分离和醛的精制3个过程
b.在碱存在下缩合为辛烯醛
c.辛烯醛加氢合成2-乙基己醇(辛醇):
2.甲醇的羰化反应
(1)合成醋酸 (2)合成醋酐
CH 3 OH CO CH 3 COOH CH 3 COOCH CO CH 3 CO ) O ( 2
3
(3)合成甲酸
CH 3 OH CO HCOOCH
HCOOCH
3
3
H 2 O HCOOH
CH 3 OH
(4)合成草酸酯、碳酸二甲酯、乙二醇
反应体系中Co2(CO)8与 HCo(CO)4的比例由反应的T与P决定。
[ HCo ( CO ) 4 ] Co 2 ( CO ) 8
2
K pH
2
K 1 . 365
1900 T
优点:羰基钴催化剂的成本低 缺点:正异构醛比例低,催化剂热稳定性差
②膦羰基钴
配位基膦(PR3) 特点:
(6)影响反应的因素
温度
T↑ ,r ↑ ,正/异↓ ,重组分及醇↑ T不宜过高,钴: 140-180℃ ,铑:100-110 ℃
压力
PCO ↑ ,r ↓ 总压不变: 钴: PCO ↑ ,正/异↑ 铑: PCO ↑ ,正/异↓ PH2 ↑ ,r ↑ ,正/异↑
溶剂
a.溶解催化剂 b.反应在气相中进行,对气-液间传质有利 c.移走反应热
∴ 控制H2和丙烯的量
d.催化剂
HRh(Co)x(PPh3)y
PPh3↑ ,正/异丁醛↑ ,r ↓
三苯基膦
x+y=4
(2)工艺流程
放空 合成气 净化 反应 净化 气液分离器 正丁醛 异丁醛
丙烯
(3)反应器
不锈钢釜式反应器
带:搅拌器、冷却装置、气体分布器
冷却装置
1.催化剂进出口 3.反应物出口 5.喷射环 7.冷却盘管 2.原料进口 4.雾沫回流管 6.叶轮 8.搅拌器
a.稳定性增加,活性降低 b.直链产物选择性增加 c.加氢活性较高 d.副产物少 e.对于不同原料烯烃的氢甲酰化反 应的适应性差
③膦羰基铑
活性也比羰基氢钴高102~104倍
选择性好,活性高,异构化性能高
催化剂稳定,可在较低压力下操作
商品名:ROPAC
三种氢甲酰化催化剂性能比较
催化剂 温度,℃ 压力,MPa 催化剂浓度,% 生成烷烃量 产物 正/异比
Chemical Technology
第八章 羰基化反应
Carbonyl Reaction
烯烃与CO及H2在过渡金属配合物的催化作用 下发生加成反应,生成比原料烯烃多一个碳 原子的醛。这个反应被命名为羰基合成
(Carbonyl synthesis),也叫Röelen反应。
随着一碳化学的发展,有一氧化碳参与的反
本研究了螯形环铂催化剂,于0.5~10MPa、70~
100℃条件下,反应3小时烯烃100%转化为醛;另 外还报道了钌族离子型络合催化剂HRu3(CO)15丙 烯氢甲酰化,正/异醛比例达21.2。对钴膦催化剂 也在作进一步研究,该催化剂一步可得到醇。
8.3 甲醇低压羰化制醋酸
1.化学原理 (1)主副反应 主: CH3OH + CO CH3COOH 副: 酯 二甲醚 CO + H2O CO2 + H2
在双键两端的C原子上分别加上一个氢和 一个甲酰基(-HCHO)
①烯烃的氢甲酰化
②烯烃衍生物的氢甲酰化
(不饱和醇、醛、酯、醚,含卤素、含氮化合物等 中的双键都能进行羰基合成反应,但官能团不参 与反应。 )
(2)氢羧基化(与CO和H2O反应)
(3)氢酯化(与CO和ROH反应)
(4)不对称合成 某些结构的烯烃进行羰基合成反应能生成含有 对映异构体的醛。若使用特殊的催化剂,使生 成的两种对映体含量不完全相等,理想情况下 仅生成某种单一对映体,这样的反应称作不对 称催化氢甲酰化反应。
