水总硬度的测定计算公式
水硬度及测定方法

水硬度及测定水中有些金属阳离子,同一些阴离子结合在一起,在水被加热的过程中,由于蒸发浓缩,容易形成水垢,随着在受热面上而影响热传导,我们把水中这些金属离子的总浓度称为水的硬度。
如在天然水中最常见的金属离子是钙离子(Ca2+)和镁离子(Mg2+),它与水中的阴离子如碳酸根离子(Co32-)、碳酸氢根离子(HCO3-)、硫酸根离子(SO42-)、氯离子(Cl-)、以及硝酸根离子(NO3-)等结合在一起,形成钙镁的碳酸盐、碳酸氢盐、硫酸盐、氯化物、以及硝酸盐等硬度,水中的铁、锰、锌等金属离子也会形成硬度,但由于它们在天然水中的含量很少,可以略去不计。
因此,通常就把Ca2+、Mg2+的总浓度看作水的硬度。
一.锅炉水垢类别:锅炉的给水和锅水的组成、性质以及生成水垢的具体条件不同,使水垢在成分上有很大的差别。
如按其化学组成,水垢可以分为下列几种,其特性和结垢的部位简述如下:1、碳酸盐水垢碳酸盐水垢的成分以碳酸钙为主,也有少量的碳酸镁。
其特性按其生成条件不同。
有坚硬性的硬垢;也有疏松海绵状的软垢。
此类水垢具有多孔性。
比较容易清除:它常在锅炉水循环较嘎的部位和给水的进口处结生。
2、硫酸盐水垢硫酸盐水垢的主要成分是硫酸钙。
它的特性是特别坚硬和致密。
它常沉积在锅炉内温度最高。
蒸发率最大的蒸发面上。
3、硅酸盐水垢硅酸盐水垢的主要成分是硬硅钙石(5CaO·5Si02·H2O)或镁橄榄石(MgO.SiO2》:另一种是软质的硅酸镁。
主要成分是蛇纹石(3MgO·2SiO2·2H2O):一般二氧化硅的含量都在20%以上。
它的特性是非常坚硬,导热性非常小,它常常容易在锅炉温度高的蒸发面上沉积。
4、混合水垢混合水垢是由钙、镁的碳酸盐、硫酸盐、硅酸盐以及铁铝氧化物等组成,很难指出其中哪一种是最主要的成分。
主要是由于使用不同成分的水质生成的。
5、含油水垢硬度比较小的给水中混入油脂后,就会结成含油的水垢。
水总硬度

水总硬度是指水中Ca2+、Mg2+的总量,它包括暂时硬度和永久硬度。
水中Ca2+、Mg2+以酸式碳酸盐形式存在的部分,因其遇热即形成碳酸盐沉淀而被除去,称之为暂时硬度;而以硫酸盐、硝酸盐和氯化物等形式存在的部分,因其性质比较稳定,不能够通过加热的方式除去,故称为永久硬度。
硬度又分为钙硬和镁硬,钙硬是由Ca2+引起的,镁硬是由Mg2+引起的。
水硬度是表示水质的一个重要指标,对工业用水关系很大。
水硬度是形成锅垢和影响产品质量的主要因素。
因此,水的总硬度即水中钙、镁总量的测定,为确定用水质量和进行水的处理提供依据。
水的总硬度测定的方法一、原理测定自来水的硬度,一般采用络合滴定法,用EDTA标准溶液滴定水中的Ca2+、Mg2+、总量然后换算为相应的硬度单位。
用EDTA滴定Ca2+、Mg2+总量时,一般是在pH=10的氨性缓冲溶液进行,用EBT(铬黑体)作指示剂。
化学计量点前,Ca2+、Mg2+和EBT生成紫红色络合物,当用EDTA溶液滴定至化学计量点时,游离出指示剂,溶液呈现纯蓝色。
由于EBT与 Mg2+ 显色灵敏度高,与Ca2+显色灵敏度低,所以当水样中Mg2+含量较低时,用EBT 作指示剂往往得不到敏锐的终点。
这时可在EDTA标准溶液中加入适量的Mg2+(标定前加入Mg2+对终点没有影响)或者在缓冲溶液中加入一定量Mg2+—EDTA盐,利用置换滴定法的原理来提高终点变色的敏锐性,也可采用酸性铬蓝K-萘酚绿B混合指示剂,此时终点颜色由紫红色变为蓝绿色。
滴定时,Fe3+,Al3+ 等干扰离子,用三乙醇胺掩蔽;Cu2+,Pb2+,Zn 2+ 等重金属离子则可用KCN、Na2S 或硫基乙酸等掩蔽。
本实验以CaCO3 的质量浓度(mg/L)表示水的硬度。
我国生活饮用水规定,总硬度以 CaCO3计,不得超过450 mg/L。
计算公式:水的硬度= ×100.09(mg/L)式中C为EDTA的浓度,V为EDTA的体积,100.09为CaCO3的质量二、试剂1、EDTA标准溶液(0.01mo/L):称取2 g乙二胺四乙酸二钠盐(Na2H2Y.2H2O)于250 mL 烧杯中,用水溶解稀释至500mL 。
03实验3 水总硬度的测定(配位滴定法)

实验三水总硬度的测定(配位滴定法)实验日期:实验目的:1、学习EDTA标准溶液的配制方法及滴定终点的判断;2、掌握钙、镁测定的原理、方法和计算。
一、水硬度的表示法:一般所说的水硬度就是指水中钙、镁离子的含量。
最常用的表示水硬度的单位有:1、以度表示,1o=10 ppm CaO,相当10万份水中含1份CaO。
2、以水中CaCO3的浓度(ppm)计相当于每升水中含有CaCO3多少毫克。
M CaO—氧化钙的摩尔质量(56.08 g/mol),M CaCO3—碳酸钙的摩尔质量(100.09 g/mol)。
二、测定原理:测定水的总硬度,一般采用配位滴定法即在pH=10的氨性溶液中,以铬黑T作为指示剂,用EDTA标准溶液直接滴定水中的Ca2+、Mg2+,直至溶液由紫红色经紫蓝色转变为蓝色,即为终点。
反应如下:滴定前:EBT +Me(Ca2+、Mg2+)=Me-EBT(蓝色) pH=10 (紫红色)滴定开始至化学计量点前:H2Y2- + Ca2+= CaY2- + 2H+H2Y2- + Mg2+= MgY2- + 2H+计量点时:H2Y2- + Mg-EBT = MgY2- + EBT +2H+(紫蓝色)(蓝色)滴定时,Fe3+、Al3+等干扰离子用三乙醇胺掩蔽,Cu2+、Pb2+、Zn2+等重金属离子可用KCN、Na2S或巯基乙酸掩蔽。
三、主要试剂1、0.02mol/LEDTA2、NH3-NH4Cl缓冲溶液3、铬黑T:0.5%4、三乙醇胺(1:2)5、Na2S溶液 2%6、HCl溶液 1:17、CaCO3固体A.R.四、测定过程1、EDTA溶液的标定准确称取在120度烘干的碳酸钙0.5~ 0. 55g 一份,置于250ml 的烧杯中,用少量蒸馏水润湿,盖上表面皿,缓慢加1:1HCl 10ml,加热溶解定量地转入250ml容量瓶中,定容后摇匀。
吸取25ml,注入锥形瓶中,加20ml NH3-NH4Cl缓冲溶液,铬黑T指示剂2~3滴,用欲标定的EDTA溶液滴定到由紫红色变为纯蓝色即为终点,计算EDTA溶液的准确浓度。
水质硬度和碱度的测定
水的总硬度测定1、实验原理:水的总硬度是测定Ca2+、Mg2+总量,以钙的化合物表示。
本实验是用EDTA络合滴定法测定水的总硬度。
在pH=10的缓冲溶液中,以EBT为指示剂。
2、试齐:0.01mol·L-1EDTA溶液;氨性缓冲溶液(pH=10);20%三乙醇胺(可掩蔽Fe3+,Al3+);EBT指示剂。
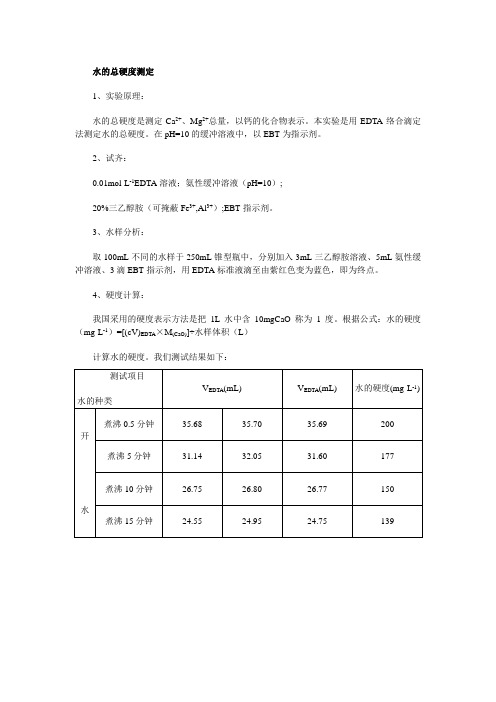
3、水样分析:取100mL不同的水样于250mL锥型瓶中,分别加入3mL三乙醇胺溶液、5mL氨性缓冲溶液、3滴EBT指示剂,用EDTA标准液滴至由紫红色变为蓝色,即为终点。
4、硬度计算:我国采用的硬度表示方法是把1L水中含10mgCaO称为1度。
根据公式:水的硬度(mg·L-1)=[(cV)EDT A×M(CaO)]÷水样体积(L)计算水的硬度。
我们测试结果如下:水硬度表μs/cm Ppm Mg/l。
f硬度0-1400-700-700-7非常软140-30070-15070-1507-15软300-500150-250150-25015-25微硬500-640250-320250-32025-32中度硬640-840320-420320-42032-42硬840以上420以上420以上42以上非常硬《锅炉水总碱度的测定》1原理用酸碱中和滴定法测定总碱量,反应产物为NaCl+H2CO3,选用甲基橙作指标剂,用标准H2SO4溶液滴定至溶液由黄色变橙色,即为终点。
2.1甲基橙指示剂:0.1%(m/v)gl22.2 标准H2SO4溶液:0.1N ofe^Z3测定步骤3.1量取100.0ml澄清水样,注入250 ml锥形瓶中;3.2加入2滴甲基橙指标剂;3.3用0.1N标准H2SO4溶液滴定至溶液由橙色变黄色,记下标准H2SO4溶液用量Vml。
4计算结果总碱度=C×V /0.1=10 C×V (毫克当量/升)公式中 C----标准H2SO4溶液浓度,V----标准H2SO4溶液用量V,ml;。
水的总硬度的测定实验报告

水的总硬度的测定实验报告水的总硬度的测定实验报告引言:水是人类生活中不可或缺的资源,而水的硬度是一个重要的水质指标,对于水的使用、处理和保护都具有重要意义。
本实验旨在通过测定水的总硬度,了解水质状况并探讨硬水对人类和环境的影响。
实验方法:1. 实验材料准备:- 高纯度去离子水- 0.02 mol/L EDTA(乙二胺四乙酸)溶液- 碳酸钙标准溶液- Eriochrome Black T指示剂- 硬度试剂盒- 烧杯、滴定管等实验器材2. 实验步骤:1) 取一定体积的水样,加入适量的Eriochrome Black T指示剂。
2) 用0.02 mol/L EDTA溶液滴定至溶液颜色由蓝色变为红色,记录滴定所需的EDTA溶液体积。
3) 用去离子水代替水样进行空白试验,重复步骤1和2。
4) 用硬度试剂盒中的碳酸钙标准溶液进行标定,记录滴定所需的EDTA溶液体积。
实验结果与分析:根据实验数据计算出水样的总硬度,可以通过以下公式计算:总硬度(mg/L)= (V2 - V1) × C × 1000 / V其中,V1为空白试验所需EDTA溶液体积,V2为水样试验所需EDTA溶液体积,C为碳酸钙标准溶液的浓度,V为取样体积。
通过实验测得的数据,我们可以得出水样的总硬度。
根据总硬度的不同范围,可以对水质进行评价:- 总硬度低于60 mg/L,水质属于软水,适合饮用和生活用水。
- 总硬度在60-120 mg/L之间,水质属于中硬水,对人体无明显危害。
- 总硬度在120-180 mg/L之间,水质属于硬水,可能会对人体健康产生一定影响。
- 总硬度高于180 mg/L,水质属于超硬水,对人体健康和环境都有不利影响。
结论:通过本实验的测定,我们了解了水的总硬度对水质的影响。
根据实验结果,我们可以评价水样的硬度水平,进而选择适合的水处理方法或选择合适的饮用水。
然而,本实验只是对水样总硬度的初步测定,仅能提供一个大致的硬度范围。
硬度常以CaCo3

硬度常以CaCo3(分子量=100)的当量来表示,并以水质中含1ppmCaCo3为1度。
计算硬度时,通常引起硬度的离子可用下列公式计算:硬度(ppmCaCo3)=M2+(ppm)×100/M2+的当量(公式中的M2+代表任一的二价金属离子)例如,若水质中含有10ppm的镁离子(Mg2+),以及15ppm的钙离子(Ca2+),则它的总硬度值计算如下:总硬度=镁硬度+钙硬度镁硬度=10ppm×100/24.4=41.0ppm 钙硬度=15ppm×100/40.0=37.5ppm 总硬度=41.0ppm+37.5ppm=78.5ppm(计算公式中的24.4为镁的当量重,40.0为钙的当量重)总硬度=c(EDTA)*V(EDTA用量)*M(CaCO3分子量)*1000/【V(水样体积)*10】将水的总硬度计算公式的右侧乘以碳酸钙的摩尔质量g/mol,再乘以1000即可(克到毫克的转换用的是德国度,就是得出EDTA消耗的体积然后怎么计算出硬度的实验目的1.了解配位滴定法基本原理和方法。
2.了解水的硬度的概念及其表示方法。
实验原理含有钙、镁离子的水叫硬水。
测定水的总硬度就是测定水中钙、镁离子的总含量,可用EDTA 配位滴定法测定:滴定前:M + EBT M-EBT(红色)主反应:M + Y MY终点时:M-EBT + Y MY + EBT(红色) (蓝色)滴定至溶液由红色变为蓝色时,即为终点。
滴定时,Fe3+、Al3+等干扰离子可用三乙醇胺予以掩蔽;Cu2+、Pb2+、Zn2+等重属离子,可用KCN、Na2S或巯基乙酸予以掩蔽。
水的硬度有多种表示方法,本实验要求以每升水中所含Ca2+、Mg2+总量(折算成CaO的质量)表示,单位mg·L-1。
器材和药品1.器材天平(0.1g、0.1mg),容量瓶(100mL),移液管(20mL),酸式滴定管(50mL),锥形瓶(250mL)等。
水的总硬度测定实验报告

水的总硬度测定实验报告一、实验目的1、掌握 EDTA 滴定法测定水的总硬度的原理和方法。
2、学会使用酸式滴定管、移液管等仪器进行准确的定量操作。
3、熟悉用铬黑 T 指示剂判断滴定终点。
二、实验原理水的总硬度通常指水中钙、镁离子的总含量。
在一定条件下,以铬黑 T 为指示剂,用 EDTA(乙二胺四乙酸二钠盐)标准溶液滴定水中的钙、镁离子。
当溶液中的钙、镁离子与 EDTA 完全反应时,溶液由酒红色变为蓝色,即为滴定终点。
反应式如下:Ca²⁺+ H₂Y²⁻⇌ CaY²⁻+ 2H⁺Mg²⁺+ H₂Y²⁻⇌ MgY²⁻+ 2H⁺三、实验仪器与试剂1、仪器酸式滴定管(50mL)移液管(25mL)锥形瓶(250mL)容量瓶(100mL、250mL)玻璃棒烧杯(500mL、100mL)电子天平2、试剂乙二胺四乙酸二钠盐(EDTA)氯化铵氨水缓冲溶液(pH=10)铬黑 T 指示剂碳酸钙基准试剂盐酸(1:1)四、实验步骤1、 001mol/L EDTA 标准溶液的配制与标定(1)配制称取约 4g EDTA 二钠盐于 500mL 烧杯中,加入约 200mL 水,温热溶解后,转入容量瓶中,用水稀释至刻度,摇匀。
(2)标定准确称取 025g 左右(精确至 00001g)基准碳酸钙于 250mL 烧杯中,用少量水润湿,盖上表面皿,从杯嘴边逐滴加入 1:1 盐酸至碳酸钙完全溶解,加 100mL 水,加热煮沸,以除去二氧化碳。
冷却后,加入10mL 氯化铵氨水缓冲溶液(pH=10),加入 3 滴铬黑 T 指示剂,用配制好的 EDTA 溶液滴定至溶液由酒红色变为纯蓝色,即为终点。
记录EDTA 溶液的用量。
平行标定三份,计算 EDTA 标准溶液的浓度。
2、水样的采集与预处理用干净的塑料瓶采集水样。
若水样中存在悬浮物或有机物,可先进行过滤或消解处理。
3、水样总硬度的测定用移液管准确吸取 2500mL 水样于 250mL 锥形瓶中,加入 5mL 氯化铵氨水缓冲溶液(pH=10),加入 3 滴铬黑 T 指示剂,用 EDTA 标准溶液滴定至溶液由酒红色变为纯蓝色,即为终点。
使用自动电位滴定仪测定水的总硬度

使用自动电位滴定仪测定水的总硬度和—DL-苹果酸含量测定1.相关标准《GB/T 5750.4-2006 生活饮用水标准检验方法感官性状和物理指标》《GB/T 14848-93 地下水质量标准》《GB/T1576-2001 工业锅炉水质标准》《GB7477-87 水质钙和镁总量的测定-EDTA滴定法》《ISO 6059-1984 水质钙和镁总量的测定EDTA滴定法》《CJ/T 206-2005 城市供水水质标准》2.测量原理当pH=10时,水样中的钙镁离子能与乙二胺四乙酸进行络合,形成稳定的螯合物,因此多采用溶解度大的乙二胺四乙酸钠滴定法来测定钙镁离子的总量,并经过换算,以每升水中碳酸钙的质量表示。
本方法使用水硬度电极作为指示电极。
水硬度电极对钙镁离子具有相同的选择性,对水溶液中游离态钙镁离子总量具有电位响应特性,在EDTA滴定过程中可以有效指示总硬度的滴定终点。
3.仪器设备3.1实验仪器:ZDJ-5型自动滴定仪,或其他型号自动电位滴定仪。
3.2实验电极:雷磁水硬度复合电极3.3其他一般实验室仪器。
4.试剂和溶液4.10. 01mol/L乙二胺四乙酸钠标准溶液:将EDTA在80℃下干燥2小时,准确称取 1.863g,去离子水定容至500ml,摇匀,实际浓度为0.0100mol/L。
乙二胺四乙酸钠标准溶液的浓度可按式(1)计算:(1)式中:c(Na2EDTA),乙二胺四乙酸钠标准溶液的浓度,单位为摩尔每升(mol/L);m,称取乙二胺四乙酸钠的质量,单位为克(g)V, 配制溶液的体积,单位为升(L)4.2pH=10的NH3-NH4Cl缓冲溶液:称取5.4g分析纯的氯化铵,溶解于去离子水中,移入100ml塑料容量瓶中,加入35mL浓氨水并用水稀释至刻度,摇匀。
5.操作过程5.1仪器准备参照ZDJ-5或其他型号自动滴定仪说明书安装和调试滴定仪。
根据水硬度电极说明书对水硬度电极的极差性能进行验证。
5.2参数设置(推荐参数)最小滴定体积:0.02ml。
