高考化学一轮复习 第23讲 化学平衡的移动作业
高考化学一轮复习:第23讲《化学平衡移动》

化学平衡移动(时间:45分钟满分:100分)考点题号化学平衡的移动1、3、5、7化学平衡图像分析2、4、6化学平衡移动原理综合应用及计算8、9、10、11一、选择题(本题共7个小题,每题6分,共42分。
每个小题只有一个选项符合题意) 1.(2013·郑州质检)一定温度下,1 mol X和n mol Y在体积为2 L的密闭容器中发生如下反应:X(g)+Y(g)2Z(g)+M(s),5 min后达到平衡,此时生成2a mol Z。
下列说法正确的是( )。
A.用X表示此反应的反应速率是(0.1-2a) mol·L-1·min-1B.当混合气体的质量不再发生变化时,说明反应达到平衡状态C.向平衡后的体系中加入1 mol M,平衡向逆反应方向移动D.向上述平衡体系中再充入1 mol X,v正增大,v逆减小,平衡正向移动解析由题给反应的化学方程式可知生成2a mol Z消耗a mol X,利用化学反应速率的定义可知v(X)=a mol(2 L×5 min)=0.1a mol·L-1·min-1;因M为固态,故平衡向右移动,气体质量变小;若平衡向左移动,气体质量增加,故当混合气体质量不再发生变化时,可说明反应达到平衡状态;增大M的量,平衡不发生移动;向平衡体系中再充入X,反应物浓度增大,平衡正向移动,v正、v逆都增大。
答案 B2.(2013·合肥调研)已知图一表示的是可逆反应CO(g)+H2(g)C(s)+H2O(g) ΔH>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)N2O4(g) ΔH<0的浓度(c)随时间t的变化情况。
下列说法中正确的是A.图一t2时改变的条件可能是升高了温度或增大了压强B.若图一t2时改变的条件是增大压强,则反应的ΔH增大C.图二t1时改变的条件可能是升高了温度或增大了压强D.若图二t1时改变的条件是增大压强,则混合气体的平均相对分子质量将减小解析由图一可知,t2时正、逆反应速率均加快且发生突变,化学平衡正向移动,可能是升高了温度也可能是增大了压强,根据ΔH所表示的意义,不管平衡如何移动,ΔH不变,所以A正确,B错;由图二可知,t1时改变平衡条件的瞬间,NO2和N2O4的浓度均增大,然后c(NO2)减小,c(N2O4)增大,平衡向正反应方向移动,改变的条件可能是给体系增大压强,但不可能是由温度改变引起的,选项C错;若增大压强,平衡正向移动,N2O4的体积分数增加,因此混合气体的平均相对分子质量增大,D错。
高考化学一轮复习化学平衡移动学案(含解析)
正误判断
(1)化学平衡发生移动,化学反应速率一定改变;化学反应速率改变,化学平衡也一定发生
移动(×)
(2)升高温度,平衡向吸热反应方向移动,此时 v 放减小,v 吸增大(×) (3)合成氨反应需要使用催化剂,说明催化剂可以促进该平衡向生成氨的方向移动,所以也
可以用勒夏特列原理解释使用催化剂的原因(×)
(3)下列措施中,有利于提高 αHCl 的有________。
ቤተ መጻሕፍቲ ባይዱ
A.增大 n(HCl)
B.增大 n(O2)
溶液的颜色变浅(×)
(8)对于 2NO2(g) 体的颜色变浅(×)
N2O4(g)的平衡体系,压缩体积,增大加强,平衡正向移动,混合气
2
深 度思考
根据化学平衡原理解答下列问题:
在体积不变的密闭容器中发生 N2(g)+3H2(g) 变一种外界条件,完成下表:
2NH3(g) ΔH=-92.4 kJ·mol-1,只改
改变的条件(其他条件不变)
化学平衡移动的方向
浓度
增大反应物浓度或减小生成物浓度 减小反应物浓度或增大生成物浓度
向正反应方向移动 向逆反应方向移动
反应前后气体体
增大压强
向气体分子总数减小的方向 移动
压强(对有气体 参加的反应)
积改变
减小压强
向气体分子总数增大的方向 移动
反应前后气体体 积不变
改变压强
平衡不移动
(4)平衡时,其他条件不变,分离出固体生成物,v 正减小(×) (5)C(s)+CO2(g) 2CO(g) ΔH>0,其他条件不变时,升高温度,反应速率 v(CO2)和 CO2
的平衡转化率均增大(√)
(6)化学平衡正向移动,反应物的转化率不一定增大(√)
高考化学一轮达标作业有详解化学平衡的移动化学反应进行的方向

高考化学一轮达标作业(有详解)-化学平衡的移动-化学反应进行的方向————————————————————————————————作者:————————————————————————————————日期:ﻩ2014届高三一轮达标作业(有详解)22 化学平衡的移动化学反应进行的方向一、选择题(本题共10个小题,每小题5分,共50分)1.在已经处于化学平衡状态的体系中,如果下列量发生变化,其中一定能表明化学平衡移动的是() A.反应混合物的浓度ﻩB.反应体系的压强C.正、逆反应的速率ﻩD.反应物的转化率解析:对于“等体反应”,缩小反应容器,压强增大,平衡不移动,但反应混合物的浓度增大,正逆反应速率增大,可知A、B、C错误。
答案:D2.对于反应4Fe(OH)2(s)+2H2O(l)+O2(g)===4Fe(OH)3(s)ΔH=-444.3kJ/mol,且熵减小,在常温常压下该反应能自发进行,对反应的方向起决定作用的是( )A.焓变B.温度C.压强ﻩD.熵变解析:化学反应的方向由(ΔH-TΔS)共同决定,该反应为熵减且能自发进行的反应,故对该反应方向起决定作用的是焓变。
答案:A3.下列反应中符合图像的是( )A.N2(g)+3H2(g)2NH3(g) ΔH=-Q1 kJ·mol-1(Q1>0)B.2SO3(g)2SO2(g)+O2(g)ΔH=+Q2 kJ·mol-1(Q2>0)C.4NH3(g)+5O2(g)4NO(g)+6H2O(g)ΔH=-Q3 kJ·mol-1(Q3>0)D.H2(g)+CO(g)C(s)+H2O(g)ΔH=+Q4 kJ·mol-1(Q4>0)解析:由左图知升高温度平衡正移,正反应为吸热反应;由右图知增大压强平衡向逆向移动,正反应为气体体积增大的反应。
答案: B4.对已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,下列有关叙述正确的是()①生成物的百分含量一定增加②生成物的产量一定增加③反应物的转化率一定增大④反应物的浓度一定降低⑤正反应速率一定大于逆反应速率⑥使用了适宜的催化剂A.②⑤ﻩB.①②C.③⑤D.④⑥5.COCl2(g)CO(g)+Cl2(g)ΔH>0,当反应达到平衡时,下列措施:①升温②恒容通入惰性气体③增加CO浓度④减压⑤加催化剂⑥恒压通入惰性气体,能提高COCl2转化率的是( )A.①②④ﻩB.①④⑥C.②③⑤ﻩD.③⑤⑥解析:该反应为吸热反应,升温则平衡正向移动,反应物转化率提高,①正确;恒容时,通入惰性气体,反应物与生成物浓度不变,平衡不移动,②错误;增加CO浓度,平衡逆向移动,反应物转化率降低,③错误;该反应正反应为气体分子数增大的反应,减压时平衡向正反应方向移动,反应物转化率提高,④正确;催化剂只能改变反应速率,不能改变平衡状态,⑤错误;恒压时,通入惰性气体,容器体积增大,反应物与生成物浓度降低,平衡向气体分子数增大的方向移动,即向正反应方向移动,反应物转化率提高,⑥正确。
高考化学大一轮复习 7.23 化学平衡的移动和化学反应进行的方向精讲课件

应用 1 [2012·安徽卷]一定条件下,通过下列反应可实
现燃煤烟气中硫的回收:
催化剂
SO2(g)+2CO(g)
2CO2(g)+S(l) ΔH<0
若反应在恒容的密闭容器中进行,下列有关说法正确的
是( )
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时,其他条件不变,分离出硫,正反应速率加快
第三十五页,共78页。
C.平衡时,其他条件不变,升高温度可提高 SO2 的转化 率
D.其他条件不变,使用不同催化剂,该反应的平衡常数 不变
第三十六页,共78页。
解析:本题主要考查外界条件对化学平衡的影响,同时 考查考生应用基础知识解决简单化学问题的能力。因反应前 后气体分子数不相等,达到平衡前容器内压强逐渐变小,A 项错误;硫为纯液体,减少硫的量不影响化学反应速率,B 项错误;升高温度,化学平衡逆向移动,SO2 的转化率降低, C 项错误;只有温度的改变,会影响反应的平衡常数,采用 不同的催化剂,只会改变化学反应速率,对化学平衡无影响, 化学平衡常数不变,D 项正确。
第二十七页,共78页。
核心考点(kǎo diǎn) 引领 通关
考点(kǎo diǎn)分类 点点 击破
第二十八页,共78页。
考点一 化学平衡移动的分析 1.实质 化学平衡移动的实质是外界条件(如浓度、温度、压强)破
坏了原平衡状态,使正、逆反应速率不再相等,当 v(正)>v(逆) 时,平衡向正反应方向移动,当 v(正)<v(逆)时,平衡向逆反 应方向移动,当 v(正)=v(逆)时,平衡不发生移动,然后在新 的条件下达到正、逆反应速率再次相等。
再 如 转 化 关 系 : AgNO3 ―C―l-→ AgCl ―B―r-→ AgBr ――I-→ AgI―S―2-→Ag2S↓得以进行,也是由于打破了各物质的溶解平 衡,生成了更难溶的物质。
高考化学一轮总复习《化学平衡移动》课时作业及答案

第六章化学反应速率和化学平衡第三节化学平衡移动一、单项选择题1.(2011·北京东城一模)在1 100 ℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g)Fe(s)+CO2(g)ΔH=a kJ·mol-1(a>0),该温度下K=0.263,下列有关该反应的说法正确的是() A.若生成1 mol Fe,则吸收的热量小于a kJB.若升高温度,正反应速率加快,逆反应速率减慢,则化学平衡正向移动C.若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态D.达到化学平衡状态时,若c(CO)=0.100 mol/L,则c(CO2)=0.026 3 mol/L2.在密闭容器中,在一定条件下,进行下列反应:NO(g)+CO(g) 12N2(g)+CO2(g)ΔH=-373.2 kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是()A.加催化剂同时升高温度B.加催化剂同时增大压强C.升高温度同时充入N2D.降低温度同时增大压强3.(2011·厦门模拟)I2在KI溶液中存在下列平衡:I2(aq)+I-(aq) I-3(aq)。
测得不同温度下该反应的平衡常数如下表:(aq)+I-(aq)I-3(aq)的ΔH>0A.反应IB.利用该反应可以除去硫粉中少量的碘单质C.在上述平衡体系中加入苯,平衡不移动D.25 ℃时,向溶液中加入少量KI固体,平衡常数K小于6804.在容积不变的密闭容器中,一定条件下发生反应:2A B(g)+2C(g),且达到平衡。
当升高温度时气体的密度增大,则下列叙述中正确的是()A.升高温度,正反应速率增大,逆反应速率减小B.若正反应是放热反应,则A为气态C.物质A一定为非气态,且正反应是吸热反应D.若向容器中充入惰性气体,则平衡向右移动5.(2012·河北模拟)一定条件下,在一密闭容器中,发生可逆反应:m A(g)+n B(g)q C(g)ΔH>0,C的体积分数变化如下图实线a所示,若开始只改变某一条件,C的体积分数如下图虚线b所示,则下列说法不正确的是()A.所改变的条件可能是加压B.所改变的条件可能是加入催化剂C.所改变的条件可能是升高温度D.增大压强该反应的平衡常数不变6.反应N 2O4(g)2NO2(g)在温度为T1、T2(T2>T1)时,平衡体系中NO2的体积分数随压强变化如下图所示。
高三化学苏教一轮复习教师用书 专题 第单元 化学平衡的移动 含答案
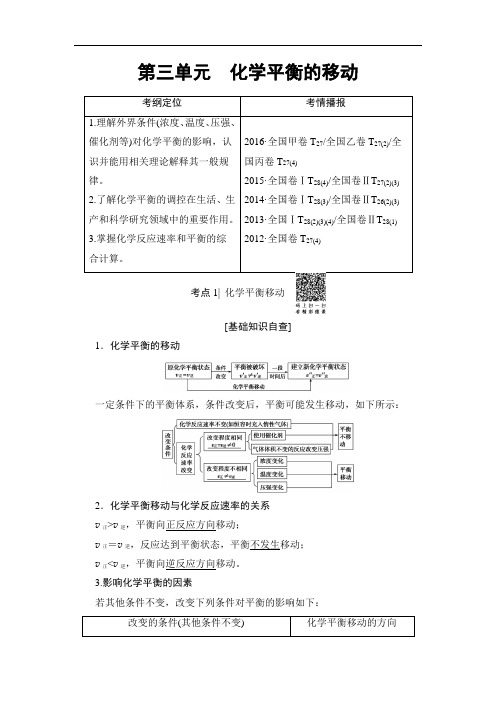
第三单元化学平衡的移动考纲定位考情播报1.理解外界条件(浓度、温度、压强、催化剂等)对化学平衡的影响,认识并能用相关理论解释其一般规律。
2.了解化学平衡的调控在生活、生产和科学研究领域中的重要作用。
3.掌握化学反应速率和平衡的综合计算。
2016·全国甲卷T27/全国乙卷T27(2)/全国丙卷T27(4)2015·全国卷ⅠT28(4)/全国卷ⅡT27(2)(3)2014·全国卷ⅠT28(3)/全国卷ⅡT26(2)(3)2013·全国ⅠT28(2)(3)(4)/全国卷ⅡT28(1)2012·全国卷T27(4)考点1| 化学平衡移动[基础知识自查]1.化学平衡的移动一定条件下的平衡体系,条件改变后,平衡可能发生移动,如下所示:2.化学平衡移动与化学反应速率的关系v正>v逆,平衡向正反应方向移动;v正=v逆,反应达到平衡状态,平衡不发生移动;v正<v逆,平衡向逆反应方向移动。
3.影响化学平衡的因素若其他条件不变,改变下列条件对平衡的影响如下:改变的条件(其他条件不变) 化学平衡移动的方向浓度增大反应物浓度或减小生成物浓度向正反应方向移动减小反应物浓度或增大生成物浓度向逆反应方向移动压强(对有气体参加的反应)反应前后气体体积改变 增大压强 向气体分子总数减小的方向移动减小压强 向气体分子总数增大的方向移动反应前后气体体积不变改变压强 平衡不移动温度升高温度 向吸热反应方向移动 降低温度向放热反应方向移动催化剂同等程度改变v (正)、v (逆),平衡不移动如果改变影响化学平衡的条件之一(如温度、压强以及参加反应的化学物质的浓度),平衡将向着能够减弱这种改变的方向移动。
4.充入惰性气体与平衡移动的关系 (1)恒温、恒容条件 原平衡体系――→充入惰性气体体系总压强增大→体系中各组分的浓度不变→平衡不移动。
(2)恒温、恒压条件[应用体验]1.已知在K 2Cr 2O 7的溶液中存在平衡取两试管各加入5 mL 0.1 mol/L 的K 2Cr 2O 7溶液。
高考化学一轮复习课时分层训练化学平衡状态衡移动

课时分层训练(二十二) 化学平衡状态和平衡移动(建议用时:45分钟)A级基础达标1.可逆反应N 2(g)+3H2(g)2NH3(g),在容积为10 L的密闭容器中进行,开始时加入2 mol N2和3 mol H2,达平衡时,NH3的浓度不可能达到( )A.0.1 mol·L-1B.0.2 mol·L-1C.0.05 mol·L-1D.0.15 mol·L-1B[2 mol N2和3 mol H2反应,假设反应能够进行到底,则3 mol H2完全反应,生成2 mol NH3,此时NH3的浓度为0.2 mol·L-1,但由于是可逆反应,不能完全反应,所以NH3的浓度达不到0.2 mol·L-1。
]2.对于反应2SO 2(g)+O2(g)2SO3(g),一定条件下达到平衡时,下列关于平衡状态的说法不正确的是( )A.v正(SO2)=2v逆(O2)B.n(SO2)∶n(O2)=2∶1C.c(SO2)的浓度不再变化D.恒温恒容下的体系压强不变B[平衡时,各组分的量保持恒定,但不一定为某一比值。
]3.对于反应:N 2O4(g)2NO2(g) ΔH>0,现将1 mol N2O4充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是( )D[从开始至平衡,由于容器容积增大,密度减小,达平衡后密度不变,A错;反应过程中,反应热不会变化,不是变量无法判断是否达到平衡状态,与图像不符,B错;N2O4的正反应速率逐渐减小,最后保持不变,NO2的反应速率应从零开始,逐渐增大,最后保持不变,C错;转化率一定时达到平衡,D对。
]4.一定温度下在容积恒定的密闭容器中,进行如下可逆反应:A(s)+2B(g) C(g)+D(g),下列叙述能表明该反应已达到平衡状态的是( )①混合气体的密度不再变化时②容器内气体的压强不再变化时③混合气体的总物质的量不再变化时④B的物质的量浓度不再变化时⑤混合气体的平均相对分子质量不再改变的状态⑥当v正(B)=2v逆(C)A.①④⑤⑥B.②③⑥C.②④⑤⑥D.只有④A[A为固态,反应正向进行时气体质量增大,逆向进行时气体质量减小,所以,密度不变时平衡,①正确;该反应前后气体体积不变,所以压强不变时不一定平衡,②错误;该反应前后气体物质的量相等,所以混合气体的总物质的量不变不一定平衡,③错误;B的浓度不变,说明反应达到平衡,④正确;混合气体的平均相对分子质量不再改变的状态,说明气体的质量不变,正、逆反应速率相等,反应达到平衡,⑤正确;v正(B)=2v逆(C)时,说明正、逆反应速率相等,反应达到平衡,⑥正确。
高中化学一轮复习第七章第23讲 化学平衡的移动和化学反应进行的方向 PPT100张

见学生用书P157
微考点 1 影响化学平衡移动的因素 一、对平衡移动概念的理解
二、影响化学平衡的外界因素 1.影响化学平衡的因素
条件的改变(其他条件不变) 增大反应物浓度或 减小生成物浓度
浓度 减小反应物浓度或 增大生成物浓度
化学平衡的移动 向 正 反应方向移动 向 逆 反应方向移动
压强(对有 气体存在 的反应)
解析 不导热的密闭容器中,等压时,通入惰性气体,体积增大,x(g) +3y(g) 2z(g)平衡逆向移动,放出热量,体系温度升高,a(g)+b(g) 2c(g) 平衡逆向移动,c 的物质的量减少;B 项,等压时,通入 z 气体,x(g)+ 3y(g) 2z(g)平衡逆向移动,体系温度升高;C 项,等容时,通入惰性气 体,反应物浓度不变,各反应速率不变;D 项,等容时,通入 z 气体,x(g) +3y(g) 2z(g)平衡逆向移动,y 的物质的量浓度增大。
A.升高温度
B.加水稀释
C.增大 Fe2+的浓度
D.常温下加压
解析 正反应放热,升高温度,平衡向逆反应方向移动,A 项错误; 加水稀释,平衡向离子数目增多的方向移动,平衡向逆反应方向移动,B 项错误;常温下加压对水溶液的平衡移动几乎无影响,D 项错误。
答案 C
2.为了探究外界条件对反应 aX(g)+bY(g) cZ(g)的影响,以 X 和 Y 物质的量之比为 a∶b 开始反应,通过实验得到不同条件下达到平衡时 Z 的 体积分数,实验结果如下图所示。以下判断正确的是( )
微诊断
判断正误,正确的画“√”,错误的画“×”。 1.温度改变,平衡一定发生移动。( √ ) 提示 任何反应都伴随着能量的变化,通常表现为吸热或放热,故温
度改变,化学平衡将发生移动。 2.只要 v(正)增大,平衡一定正向移动。( × ) 提示 平衡正向移动是因为 v(正)大于 v(逆),若 v(正)、v(逆)都增大,
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第23讲化学平衡的移动A组基础题组1.(2017北京朝阳期中,10)下列事实不能..用平衡移动原理解释的是( )A.蒸干AlCl3溶液,无法得到无水AlCl3B.用稀H2SO4洗涤BaSO4沉淀,可减少沉淀损失量C.氯水中加入少量CaCO3粉末,可以提高漂白能力D.滴加CuSO4溶液可以加快Zn与稀H2SO4反应的速率2.已知:xA(g)+yB(g) zC(g) ΔH=a kJ·mol-1。
将x mol A和y mol B充入密闭容器中,在不同温度(T1>T2)及压强(p1>p2)下,C的物质的量与反应时间的关系如图所示。
下列判断正确的是 ( )A.x+y=z;a>0B.x+y>z;a<0C.x+y<z;a<0D.x+y<z;a>03.(2017北京朝阳一模,11)探究浓度对化学平衡的影响,实验如下:Ⅰ.向5 mL 0.05 mol/L FeCl3溶液中加入5 mL 0.05 mol/L KI溶液(反应a),平衡后分为两等份Ⅱ.向一份中加入饱和KSCN溶液,变红(反应b);加入CCl4,振荡、静置,下层显极浅的紫色Ⅲ.向另一份中加入CCl4,振荡、静置,下层显紫红色结合实验,下列说法的是( )A.反应a为:2Fe3++2I- 2Fe2++I2B.Ⅱ中,反应a进行的程度大于反应bC.比较氧化性:Ⅱ中,I2>Fe3+D.比较水溶液中c(Fe2+):Ⅱ<Ⅲ4.诺贝尔化学奖得主乔治·欧拉教授率领团队首次采用金属钌作催化剂,从空气中捕获CO2直接转化为甲醇,为通往未来“甲醇经济”迈出了重要一步,并依据该原理开发如图所示转化。
(1)CO2中含有的化学键类型是键。
(2)将生成的甲醇(沸点为64.7 ℃)与水分离可采取的方法是。
(3)上图所示转化中,第1步至第4步的反应热(ΔH)依次是a kJ/mol、b kJ/mol、c kJ/mol、d kJ/mol,则该转化总反应的热化学方程式是。
(4)500 ℃时,利用金属钌作催化剂,在固定容积的密闭容器中可直接实现如(3)中转化得到甲醇。
测得该反应体系中X、Y浓度随时间的变化如下图。
①Y的化学式是,判断的理由是。
②下列说法正确的是(选填字母)。
a.Y的转化率是75%b.其他条件不变时,若在恒压条件下进行该反应,Y的转化率高于75%c.升高温度使该反应的平衡常数K增大,则该反应为吸热反应d.金属钌可大大提高该反应中反应物的转化率③从反应开始到平衡,用氢气表示的平均反应速率v(H2)= mol/(L·min)。
5.(2017北京海淀期中,18)煤制天然气工艺是煤高效洁净利用的新途径之一,其工艺流程简图如下:(1)反应Ⅰ:C(s)+H2O(g)CO(g)+H2(g) ΔH=+135 kJ·mol-1,通入的氧气会与部分碳发生燃烧反应。
请利用能量转化及平衡移动原理说明通入氧气的作用:。
(2)反应Ⅱ:CO(g)+H2O(g)CO2(g)+H2(g) ΔH=-41 kJ·mol-1。
下图表示不同温度条件下,煤气化反应Ⅰ发生后的汽气比(水蒸气与原料气中CO的物质的量之比)与CO平衡转化率的变化关系。
①判断T1、T2和T3的大小关系: 。
②若煤气化反应Ⅰ发生后的汽气比为0.8,经煤气化反应Ⅰ和水气变换反应Ⅱ后,得到CO与H2的物质的量之比为1∶3,则反应Ⅱ应选择的温度是(填“T1”“T2”或“T3”)。
(3)①甲烷化反应Ⅳ发生之前需要进行脱酸反应Ⅲ。
煤经反应Ⅰ和Ⅱ后的气体中含有两种酸性气体,分别是H2S和。
②工业上常用热碳酸钾法脱除H2S气体得到两种酸式盐,该反应的化学方程式是。
(4)已知:CO(g)+H2O(g)CO2(g)+H2(g)ΔH1=-41 kJ· mol-12H2(g)+O2(g)2H2O(g) ΔH2=-484 kJ· mol-1CH4(g)+2O2(g)CO2(g)+2H2O(g)ΔH3=-802 kJ· mol-1反应Ⅳ:CO(g)+3H2(g)CH4(g)+H2O(g) ΔH= 。
B组提升题组6.已知:2SO2(g)+O2(g) 2SO3(g) ΔH,有关数据如下:T(℃)527 627 727 827 927平衡常数K 910 42 3.2 0.39 0.12下列说法不正确...的是( )A.根据平衡常数随温度的变化关系,判断出ΔH<0B.保持其他条件不变,SO2的平衡转化率α(727 ℃)<α(927 ℃)C.增大压强、降低温度能提高SO2的转化率D.SO3的稳定性随温度的升高而降低7.某温度下,在一容积可变的密闭容器里,反应2A(g) B(g)+2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、2 mol、4 mol。
在保持温度和压强不变的条件下,下列说法正确的是( )A.充入1 mol稀有气体氦(He),平衡将不发生移动B.充入A、B、C各1 mol,平衡将向正反应方向移动C.将A、B、C的物质的量都减半,C的百分含量不变D.加入正催化剂,正、逆反应速率均加快,平衡向逆反应方向移动8.(2017北京东城期末,16)CH4超干重整CO2技术可得到富含CO的气体,用于生产多种化工产品。
该技术中的化学反应为:CH4(g)+3CO2(g) 2H2O(g)+4CO(g) ΔH=+330 kJ/mol。
(1)下图表示初始投料比n(CH4)∶n(CO2)为1∶3或1∶4时,CH4的转化率在不同温度(T1、T2)下与压强的关系。
(注:投料比用a1、a2表示)①a2= 。
②判断T1与T2的大小关系,并说明理由: 。
(2)CH4超干重整CO2的催化转化原理示意图如下:①过程Ⅰ中生成1 mol H2时吸收123.5 kJ热量,其热化学方程式是。
②过程Ⅱ,实现了含氢物种与含碳物种的分离。
生成H2O(g)的化学方程式是。
③假设过程Ⅰ和过程Ⅱ中的各步均转化完全,下列说法正确的是。
(填序号)a.过程Ⅰ和过程Ⅱ中均发生了氧化还原反应b.过程Ⅱ中使用的催化剂为Fe3O4和CaCO3c.若过程Ⅰ投料比=1,可导致过程Ⅱ中催化剂失效9.五氯化磷(PCl5)是有机合成中重要的氯化剂,可以由三氯化磷(PCl3)氯化得到:PCl3(g)+Cl2(g)PCl5(g) ΔH=-93.0 kJ·mol-1。
某温度下,在容积为2.0 L的密闭容器中充入2.0 mol PCl3和1.0 mol Cl2,一段时间后反应达平衡状态,实验数据如下表所示:t/s 0 50 150 250 350n(PCl5)/mol 0 0.24 0.36 0.40 0.40(1)0~150 s内的平均反应速率v(PCl3)= mol·L-1·s-1。
(2)该温度下,此反应的化学平衡常数的数值为(可用分数表示)。
(3)反应至250 s 时,该反应放出的热量为kJ。
(4)下列关于上述反应的说法中,正确的是(填字母序号)。
a. 无论是否达平衡状态,混合气体的密度始终不变b.300 s 时,升高温度,正、逆反应速率同时增大c.350 s 时,向该密闭容器中充入氮气,平衡向正反应方向移动d.相同条件下,若起始时向该密闭容器中充入1.0 mol PCl3和0.5 mol Cl2,达到化学平衡状态时,n(PCl5)<0.20 mol(5)温度T1时,混合气体中PCl5的体积分数随时间变化的示意图如下。
其他条件相同,请在下图中画出温度为T2(T2>T1)时,PCl5的体积分数随时间变化的曲线。
答案精解精析A组基础题组1.D 滴加CuSO4溶液可以加快Zn与稀H2SO4反应的速率是因为Zn和CuSO4溶液发生置换反应生成Cu,进而形成了Cu—Zn原电池,与平衡移动原理无关。
2.B 观察图像知,升高温度,n(C)减小,即平衡向逆反应方向移动,故a<0;增大压强,n(C)增大,即平衡向正反应方向移动,故x+y>z。
3.B A项,由实验Ⅱ可知,反应a为可逆反应,离子方程式为2Fe3++2I- 2Fe2++I2。
B项,加入饱和KSCN 溶液,溶液变红,则生成了较多的Fe(SCN)3;加入CCl4,振荡、静置,下层显极浅的紫色,则加入CCl4前的溶液中含有较少的I2,由此说明反应a进行的程度小于反应b。
C项,Ⅱ中反应a的平衡逆向移动,则氧化性I2>Fe3+。
D项,Ⅲ中反应a的平衡正向移动,Fe2+的浓度升高,Ⅱ中反应a的平衡逆向移动,Fe2+的浓度降低,所以水溶液中Fe2+的浓度:Ⅱ<Ⅲ。
4.答案(1)极性共价(2)蒸馏(3)CO2(g)+3H2(g) CH3OH(l)+H2O(l)ΔH=(a+b+c+d)kJ/mol(4)①CO2根据图像可知,Y为反应物,X为生成物,且相同时间内反应物减少量与生成物增加量相同,所以二者化学计量数相同②abc③0.225解析(1)CO 2中含有的化学键类型为极性共价键。
(2)分离沸点相差较大的互溶液体,应采用蒸馏的方法。
(3)根据盖斯定律可得,CO2(g)+3H2(g) CH3OH(l)+H2O(l) ΔH=(a+b+c+d)kJ/mol。
(4)②a项,α=×100%=75%;b项,若在恒压条件下进行,相当于对原平衡加压,平衡正向移动,Y的转化率提高;c项,K与温度成正比,所以正反应为吸热反应;d项,催化剂不影响转化率。
③v(H2)=mol/(L·min)=0.225 mol/(L·min)。
5.答案(1)氧气与碳发生燃烧反应放热,放出的热被可逆反应C(s)+H 2O(g)CO(g)+H2(g)吸收利用,促使平衡正向移动(2)①<T2<T3②T3(3)①CO2②K2C+H2S KHS+KHCO3(4)-207 kJ· mol-1解析(1)因煤气化反应是吸热反应,可以利用氧气与碳反应放出的热量使平衡正向移动,增大转化率。
(2)①水气变换反应是放热反应,汽气比相同时,温度越高,CO的转化率越低,故有T1<T2<T3;②反应Ⅰ发生后的汽气比为0.8,可设CO为1 mol,则H2O为0.8 mol,生成的氢气也是1 mol,设反应Ⅱ转化的CO为x mol,反应后剩余的CO为(1-x) mol,氢气共(1+x) mol,即(1-x)/(1+x)=1/3,x=0.5,所以,反应Ⅱ中CO的平衡转化率为50%,对照图中数据可知,此时的温度应是T3。
(3)①反应Ⅱ中生成的CO2也为酸性气体;②加热情况下H2S与碳酸钾反应得到两种酸式盐,化学方程式为K2CO3+H2S KHS+KHCO3。
