高等有机作业
16秋浙大《有机化学(A)》在线作业

B. CH3CHO
C. PhCOCH3
D. CH3COCH3
正确答案:
3. 下列各组物质一定是同系物的是
A. 符合通式(CH2)nO2 的酯
B. 甲酸和醋酸
C. 正丁烷和异戊烯
D. 硬脂酸和油酸
正确答案:
4. 已知甲、乙两种烃的含碳的质量分数相同,下列判断正确的是
D. 甲烷与氯气均在黑暗中混合
正确答案:
22. 下列化合物的沸点最高的是()。
A. 正已醇
B. 正已烷
C. 1-己炔
D. 1-氯己烷
正确答案:
23. 下列四个试剂,不跟CH3CH2COCH2CH3反应的是:
A. RMgX
B. NaHSO3饱和水溶液
C. PCl5
D. LiAlH4
A. 环丙烷
B. 环丁烷
C. 环戊烷
D. 环己烷
正确答案:
31. (R)-2-氯丁烷 与(S)-2-氯丁烷的哪种性质不同?
A. (A) 熔点
B. 沸点
C. 折射率
D. 比旋光度
正确答案:
32. (CH3)3CBr与乙醇钠在乙醇溶液中反应主要产物是:
A. (CH3)3COCH2CH3
A. 错误
B. 正确
正确答案:
3. 芳杂环化合物是平面形的,π电子数符合4n+2规则。
A. 错误
B. 正确
正确答案:
4. 卤素取代位置对反应的影响:卤素离羧基越近,诱导效应越强,酸性越弱。
A. 错误
B. 正确
正确答案:
5. 在农业上常用稀释的福尔马林来浸种,给种子消毒,因为该溶液中含有甲酸。
高等有机大作业:消除反应概述

大连理工大学高等有机化学课程论文消除反响概述Introduction of Elimination Reactions学院〔系〕:化学与环境生命学部专业:应用化学学生姓名:汪乐楠学号:202141348指导教师:评阅教师:完成日期:大连理工大学Dalian University of Technology摘要消除反响〔elimination reactions〕是有机化学中非常常见的一类反响,也是有机物合成中应用极广泛的一类反响,被用于不饱和有机分子的合成、有机物官能团与构型构象的转化等。
对各种类型消除反响的相关研究是有机合成领域长久以来的根底与热门课题。
本文试通过对消去反响的典型反响类型及其机理、影响反响的环境条件、反响的取向与竞争的简单综述,帮助读者深化全面地理解这一反响类型。
关键词:消除反响;概述;E1反响;E2反响;α-消除;γ-消除;立体化学;反响的竞争;本科生课程论文目录摘要 (III)引论 (1)1消除反响的分类 (2)E2反响 (2)E2反响机理 (2)E2反响的立体化学 (3)E1反响 (7)E1反响机理 (7)E1反响中的重排现象 (9)共轭碱单分子消除反响 (11)E1CB反响机理 (12)采取E1CB机理的条件 (12)β-羟基乙胺与α-羟基甲胺热消除反响 (13)楚加耶夫消除反响〔Chugaev Elimination〕 (13)α-消除反响 (15)γ-消除反响与其他消除反响类型 (16)2消除反响产物的区域选择性 (17)扎伊采夫规那么〔Saytzeff’s Rule〕 (17)霍夫曼规那么〔Hofmann’s Rule〕 (17)扎伊采夫取向与霍夫曼取向的竞争 (18)底物分子骨架与碱体积的影响 (18)α-官能团的影响 (18)β-官能团的影响 (20)潜在共轭体系 (20)小结:消除反响区域选择性的分析方法 (20)3消除与取代反响的竞争 (22)底物构造 (22)离去基团 (22)α-烷基与α-芳基 (22)β-烷基与β-芳基 (24)潜在共轭体系 (25)其他吸电子基团 (25)亲核试剂 (26)亲核试剂的碱性 (26)亲核试剂的体积〔空间位阻〕 (27)亲核试剂的浓度 (27)溶剂的极性 (28)反响温度 (30)小结:S N- E反响竞争的规律 (30)4总结 (33)参考文献 (34)致谢.............................................................................................. 错误!未定义书签。
高等有机化学作业及期末考试复习题(一)
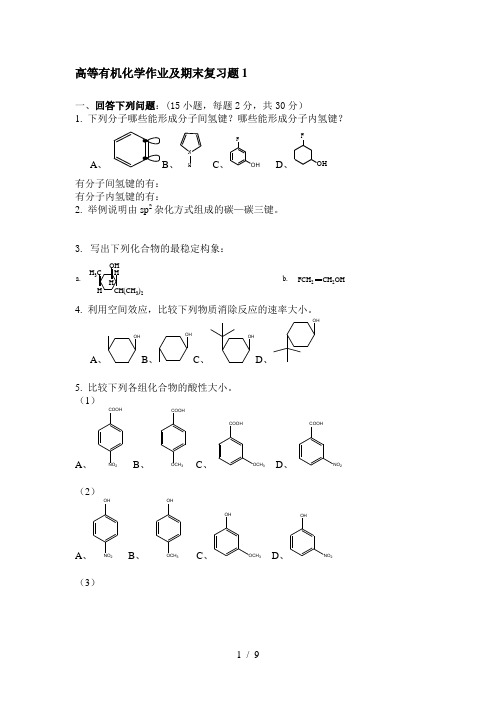
高等有机化学作业及期末复习题1一、回答下列问题:(15小题,每题2分,共30分)1. 下列分子哪些能形成分子间氢键?哪些能形成分子内氢键?A 、B 、NC 、FOHD 、FOH有分子间氢键的有: 有分子内氢键的有:2. 举例说明由sp 2杂化方式组成的碳—碳三键。
3. 写出下列化合物的最稳定构象:a.3)2H 3 b.FCH 2CH 2OH4. 利用空间效应,比较下列物质消除反应的速率大小。
A 、OHB 、OHC 、OHD 、OH5. 比较下列各组化合物的酸性大小。
(1)A 、 COOHNO 2B 、COOHOCH 3C 、COOH OCH 3D 、COOHNO 2(2)A 、OH NO 2B 、 OHOCH 3C 、OHOCH 3D 、OHNO 2(3)A 、 NH 2NO 2B 、NH 2OCH 3C 、NH 2OCH 3D 、NH 2NO 2(4)A 、 CH 3NO 2B 、CH 3OCH 3C 、CH 3OCH 3D 、CH 3NO 26. 下列化合物酸性最弱的是?OHNO 2OH NO 2OHNO 2OHABCD7. 下列醇与卢卡斯试剂反应活性最高的是?A CH 3CH 2CH 2CH 2OHB CH 3CH(OH)CH 2CH 3C (CH 3)2CHCH 2OHD (CH 3)3COH8. 下列物种中的亲电试剂是: ;亲核试剂是 。
a. H +;b. RCH 2+;c. H 2O ;d. RO —;e. NO 2+; f CN —; g. NH 3; h. R C =O +9. 下列化合物中有对映体的是: 。
a.CH 3CH =C =C(CH 3)2b.N C 6H 2H 5CH 3I c.d.3)2310. 预测下列各分子的形状和键角的大小:H 2C=C=CH 2NH 3C CH 3CH 3CH 3BeCl 2OH 3C CH 3CH 311. 按亲电加成反应活性大小排列的顺序是:( )>( )>( )>( )。
有机化学作业本答案(全)

H2C CH
H
3.
CC
H
CH3
H
4.
C
H3C
H C
C H
H C
CH3
5. 3-甲基-2-乙基-4-溴-1-丁烯 6、3,3-二甲基-1-丁炔银
二.完成下列反应
1. CH3CHCHBr CH3
2. CF3CH2CH2Cl
CH3 3. CH3CCH2CH3
Br
4. CH3COOH
5. CH3CCH2CH3 O
CHCH3 Br
2. A.
O CH3
B. CH3CH CH3
CHCH3 OH
C. H3CC CHCH3 CH3
B.
OH
C. CH3I
6. H2C CHCH2C CH Br Br
7. CH3CCH 3
O
OHC CH 2CH 2CHO
HCHO
8.
HOOC(CH 2)4COOH
9. CH3CH2COOH
CH3CCH 2COOH
CO 2
O
三. 判断正误
1.
2.
3.
4.
5.
6.
7.
8.
9、
四.选择题
1、C 2、A 3、A 4、A
五. 推断结构
1、 A. H2C CH CH2Br B. H2C CH CH2 CH2 CH CH2
C. HOOC CH2 CH2 COOH
D. H3C CH CH2 CH2 CH CH3
Br
Br
2. A. CH3CH2CH2CH2Br or CH3CHCH2Br
CH3
CH3
B. CH3CCH3 C. CH3CHCH2CH3
东北师范大学奥鹏《高等有机化学》(离线考核)作业考核答案

离线考核《高等有机化学》满分100分一、回答下列问题(共26分)1.化合物ClCH=CHCHBrCH2CH3有几个构型异构体?写出构型式、命名并标记其构型。
(12分)答:有四个异构体,它们分别是:(1E,3R)-1-氯-3-溴-1-戊烯(1Z,3R)-1-氯-3-溴-1-戊烯(1E,3S)-1-氯-3-溴-1-戊烯(1Z,3R)-1-氯-3-溴-1-戊烯2.由下列指定化合物合成相应的卤化物,是用Cl2还是Br2?为什么?(6分)a b答:a 用Br2,甲基环己烷伯、仲、叔氢都有,溴代反应的选择性比氯代反应的大,产物1-溴-1-甲基环己烷的产率要比1-氯-1-甲基环己烷高。
b 用Cl2还是Br2都可以,环己烷的12 个氢是都是仲氢。
3.叔丁基溴在水中水解,(1)反应的产物是什么?(2)写出反应类型,(3)写出反应历程,(4)从原料开始,画出反应进程的能量变化图,在图中标出反应物、产物、过渡态和活性中间体(若存在的话)(8分)。
答:(1)反应的产物叔丁醇(CH3)3COH(2)反应类型 S N1反应。
(3)反应历程:(4)反应进程的能量变化图:反应进程二、写出反应的主要产物,有构型异构体的产物,要写出产物的构型式(每小题2分,共20分。
)1.2.3.4.5.++6.7.8.9.10.三、按题中指定的项目,将正确答案填在()中。
(每小题3分,共30分。
)1.S N2反应速率的快慢(a>d>b>c)。
a b cd2.羰基化合物亲核加成反应活性的大小(b>d>e>c>a)。
a b c d e3.碳正离子稳定性的大小(c>b>a)。
a b c4.作为亲核试剂亲核性的强弱(b>c>a)。
a b c5.酯碱性水解反应速率的大小(c>a>d>b)。
a b c d6.化合物与1mol Br2反应的产物是()。
7.进行S N1反应速率的大小(b>a>c)。
苄基溴α-苯基溴乙烷β-苯基溴乙烷a b c8.下列化合物在浓KOH醇溶液中脱卤化氢,反应速率大小的顺序是(c>b>a)。
化学-高等有机化学-教学大纲

《高等有机化学》课程大纲Advanced Organic Chemistry(40学时)一、课程目标1. 教学目标本课程是面向化学专业(包括有机化学、无机化学、分析化学、物理化学、高分子化学及材料化学)的硕士研究生开设的一门基础课程。
高等有机化学是一门论述有机化合物的结构、反应、机理及它们之间关系的科学,对更深层次地理解和掌握有机化学起着理论指导作用。
通过本课程的学习使学生在“基础有机化学”的基础上,对一些在本科阶段教学中未能深入或来不及介绍的重要内容做专题讨论,进一步深化学生对有机化学理论的理解,对有机反应机理的认识,对立体化学知识的巩固,同时还针对有机化学领域的最新研究进展进行拓展介绍。
总之,通过比较系统、深入地介绍现代有机分子结构理论,有机化合物结构和性能之间的关系,有机反应机理及中间体结构与性质,从总体上巩固和加强学生对有机化学的认识和理解。
2. 学习目标掌握有机分子结构和反应性能的关系;掌握立体化学的基本原理,了解反应过程中的立体化学;初步掌握有机反应机理及研究方法,掌握取代基效应和线性自由能关系;掌握典型的有机反应类型和反应中间体的结构、产生和稳定性;掌握周环反应的基本类型和基本原理。
二、课程内容专题1:有机化合物的分子结构理论(12学时)第一章:共价键理论:定域键和离域键第二章:取代基效应第三章:芳香性理论第四章:比共价键弱的相互作用专题2:立体化学(10学时)第一章:分子的不对称性和旋光性第二章:外消旋体的拆分第三章:动态立体化学及不对称合成第四章:构象与构象分析专题3:有机反应机理基础知识(12学时)第一章:研究有机反应机理的方法第二章:动力学控制与热力学控制第三章:取代基效应和线性自由能关系第四章:有机酸碱第五章:有机反应中的溶剂效应第六章:碳正离子、碳负离子和自由基第七章:卡宾和苯炔专题4:周环反应(6学时)第一章:电环化反应及其理论解释第二章:σ- 键迁移反应及其理论解释第三章:环加成反应及其理论解释三、教学方式本门课程以教师讲授为主,学生课后自主讨论为辅,课堂教学采用多媒体授课形式。
有机-作业

《有机化学》作业-3.13第一章1.从某有机反应液中分离出少量白色固体,其熔点高于300℃。
能否用简单方法推测其是有机化合物还是无机化合物;2.写出下列化合物可能的凯库勒结构式:C3H8O;C2H7N;C2H4O2。
3.计算甲烷与溴反应生成溴甲烷的反应热;4.用楔线式表示甲醇的立体结构式。
第二章5.写出C7H16烷烃的所有构造异构体;6.用系统命名法命名下列化合物:7.写出围绕己烷C3-C4 σ键旋转的优势构象,分别用纽曼投影式和锯架式表示;8.写出下列反应的反应机制:第三章9.写出1-戊烯和异丁烯加HBr的主要产物,哪一个烯烃的加成速率快,并给予解释。
10.写出异丁烯与Br2/CCl4的加成产物。
11.烯烃(1)和(2)用高锰酸钾氧化,(1)得一种产物丙酸,而(2)的氧化产物为戊酸和二氧化碳,试写出(1)和(2)的结构式。
第四章12.写出下列化合物的系统名称:《有机化学》作业-4.2第四章13.用化学方法鉴别下列化合物:,,14.完成下列反应式:第五章15.请指出下列化合物之间的相互关系:16.指出以下化合物中手性碳的构型:第六章17.命名下列化合物:18.写出苯与溴在三溴化铁催化下的反应机制。
19.如何从苯合成下列化合物:;第七章20.某氯代物的分子离子峰与M+2峰的峰高之比接近1:1,该氯代物中含有几个氯原子?21.完成下列反应:22.溴代新戊烷是何种类型的卤代烷(伯仲叔)?在与乙醇反应时是进行S N1反应还是S N2反应?23.排列下列试剂在DMSO中亲核性的强弱:Br-、Cl-、CN-、I-《有机化学》作业-5.3第八章24.下列醇中哪些可以被高碘酸氧化?写出氧化产物:25.比较苯酚、对氯苯酚、对甲基苯酚与对硝基苯酚的酸性强弱;26.写出2-丁烯基苯基醚的克莱森重排产物。
27.完成下列反应:第九章28.下列化合物中哪些可以与亚硫酸氢钠反应?哪个反应的最快?苯乙酮、二苯酮、环己酮、丙醛29.下列化合物为降压药普萘洛尔的肟衍生物,在体内可代谢活化。
中国药科大学有机化学-题库合并

前言为了更好的配合课堂教学,有机化学组十余名课堂教学经验丰富的教师,根据教学大纲的要求和教材内容,编写了本套题库。
含盖了命名、名词解释、反应、机理、推结构以及合成这六大类型的千余道习题。
题库内容突出专业需要,覆盖面广而又不失重点,注重基础知识的演练而又有一定程度的拔高,紧密结合上课内容而又注意知识的扩展延伸,使同学们在做题的过程中能加深对相关章节知识的理解和掌握,更好的学习有机化学这门重要课程。
练习题是有机化学中的重要环节,是课堂和课本学习知识的初步运用与时间,通过思考和训练,不但能够考察对知识的理解和运用的程度,巩固书本知识,并且培养了科学的思维方法和分析,解决问题的能力。
如果仅仅是为了完成作业,应付考试,舍身于题海,则会劳多益少,趣味索然。
反之,如果能够直奔主题举一反三,可以收事半功倍之效,品其中之乐。
鉴于是首次组织编写网络题库,虽然经过了认真的校对和编排,但难免存在错误和不妥之处,还请各位专家和读者不吝赐教和指正,以便我们在今后的工作中加以改进,不胜感谢最后,向编写本套题库的广大专家同事表示感谢!有机化学教研组2006年7月10日第一大题:命名题 第二章1CH 3CH(C 2H 5)CH(CH 3)CH 2CH 32(CH 3)2CHCH 2CH(CH 3)23CH 3CH 2CHCH(CH 3)2CH(CH 3)24CH 3CH 2CH 2CHCH 2CH 2CHCH 35(C 2H 5)4C6CH 3CH 2CH 2CHCHCH 2CH 2CH 2CH 3CH(CH 3)2CH 2CH 2CH 2CH 2CH 37CH 3CH 3CH 2CCH 3CH 38910Cl第三章1CC(CH 3)2CHCH 3CH 2H 2CH 2CH 32C CHCH 3CH 3CH 2Cl 3CCCH 3CH 2HH2CH 2CH 34(CH 3)3CCHCH 2第四章1CH CH 2BrHC 2H 52HCl C 2H 5CH 3H CH 2Cl3CH 3ClHBrC 2H 5H 4CH 3H HHCl Br Br C 2H 51CH 3CHCHCH 2CH 2CH 3BrCH 2Cl2CH 2CH 2CHCHCHBr 2BrCH 3CH 33(CH 3)2CHCCH(CH 3)2CH 3Cl4CH 3Cl ClClCH 3H 5Br H36CH 3H HCl BrCH 2CH 2CH 3'第五章1C CH 2CH 2CH 2OH2CH 2CHCHCHCH 3CH 2CH 2CH 3OH3HHOH CH 2CH 34CH 3OH OH H HCH 2CH 3]5OCH 2CHCH 2CH 3CH 36OHCH 3CH 3OH HH 5C 27CH 3CH CHCHCHCH 2CH 3CH 2OHClCH 3CH 38CH 2CH 2CHCH 2CH 3OH CH 2OH1ClCH 3CH 32CH 3CH 33CH 3CH 34CH 3第六章1(CH 3)2CHCH 2CCH 2CH 3CH 22(CH 3)2CHCH CHCH 2CH 33CH 3CH 2C CHCH(CH 3)CH 2CH 3CH 2CH 34(CH 3)3CCHCHCH 2CH 35CH 3CH 2CCH(CH 3)2CHCH 36C CC 2H 5CH 3HCH 3789CCClHCH 3CH 2H10C CHCH 2CH 32CH 3第七章11(CH 3)2CHCH CH(CH 3)2CCH2CH 3CHCH 2CHCH 2CH 2CH 2CH 3CH(CH 3)2CCH3CH 2C(CH 3)C CCH 2CH CH 2CCC 2H 5CHCH 2(CH 3)2CHCCH45CCH HCH 3CH 2CH 2CCCH 2CH 3CH 3CH 36C CCH 3CH 321CH 3CH CHCH 2CH 2CH CH 22CH 3CH CHCH 2C CH3CH 3CH CHC(CH 3)CHCH 34(CH 3)2C CHC CCH 35CH 2CCCCH 3CH CH 3CH 2CH 36CH 3CCCHCHCH 2CH 3CH 2CH 3CH 3C CH CH 3第八章 11CH 2CH 2CCH2COOHNO 2Br3C C2CH 3H 3CH4SO 3H CH 35NO 26(CH 3)2CHCHCH(CH 3)27ClNO 2SO 3H8C 2H 5C 2H 521CH 3CH 3CH 32CH 3CH 3CH 3C H 33CH 34CH 2CHCH 3CH 25CH 2CH(CH 3)26CH 3CH 37CH 3Br8CH(CH 3)2C H 3第九章 羰基化合物第十章酚醌第十一章羧酸和取代羧酸第十二章羧酸衍生物第十三章含氮化合物第十四章杂环化合物第二章(1)3,4-二甲基己烷(2)2,4-二甲基戊烷(3)2,4-二甲基-3-乙基戊烷(4)2,6,6-三甲基-5-丙基辛烷(5)3,3-二乙基戊烷(6)4-异丙基-5-丁基癸烷(7)2-甲基双环[4.4.0]庚烷(8)1-甲基-4-氯螺[2.4]癸烷(9)2-氯双环[2.2.1]庚烷(10)环己基环己烷第三章(1)(Z)-2-甲基-3-乙基-3-庚烯(2)顺-1-氯-2-甲基-2-丁烯(3)3,3-二甲基-1-丁烯(4)Z-3-庚烯第四章1(1)(3R)-3-溴-1-戊烯(2)(2S,3R)-1,3-二氯-2-甲基戊烷(3) (2S,3S)-2-氯-3-溴戊烷(4) (2S,3S,4R)-2-氯-3,4-二溴己烷2(1)2-溴-3-氯甲基庚烷(2)1,1,5-三溴-2,3-二甲基戊烷(3)3-氯2,3,4-三甲基戊烷(4)(S)-2,2,3-三氯丁烷(5)(S)-1-氯-1-溴乙烷(6)(2R,3S)-2-氯-3-溴己烷第五章1(1)3-苯基-3-丁烯-1-醇(2)3-丙基-4-戊烯-2-醇(3)(1S,2R)-2-乙基环己醇(4)(2S,3R)-2,3-戊二醇(5)2,6-二甲苯基烯丙基醚(6)(3R)-2-甲基-2,3-戊二醇(7)3-氯-2,4,5-三甲基-1-庚醇(8)2-乙基1,4-丁二醇2 (1)1-氯-3,4-二甲基-双环[4. 4. 0]-3-癸烯(2)1,7-二甲基螺[4. 5]癸烷(3)顺-1,2-二甲基环己烷(4)3-甲基环己烯第六章1(1)4-甲基-2-乙基-1-戊烯(2)2-甲基-2-己烯(3)5-甲基-3-乙基- -3-庚烯(4)Z-2,2-二甲基-3-己烯(5)4-甲基-3-乙基-2-戊烯(6)顺(或E)-3-甲基-2-戊烯(7)5-甲基-3-乙基-3-庚烯(8)Z(或顺)-5-甲基-4-乙基-2-己烯(9)顺(或Z)-1-氯-1-丁烯(10)E-3-乙基-1,3-戊二烯第七章1(1)4-甲基-3-异丙基-1-戊炔(2)5,6-二甲基-3-正丁基-1-庚炔(3)1,6-庚二烯-3-炔(4)Z-3-乙基-4-异丙基-1,3-己二烯-5-炔(5)1-甲基-3-(1-丙炔基)环己烷(6)(2E,5Z)-6-甲基-2,5-壬二烯2(1)1,5-庚二烯(2)4-己稀-1-炔(3)3-甲基-2,4-己二烯(4)2-甲基-2-己稀-4-炔(5)2-仲丁基-1-戊稀-3-炔(6)4,7-二甲基-6-乙基-4-壬烯-2-炔第八章1(1)4-苯基-1-丁炔(2)3-硝基-4-溴苯甲酸(3)E-2-苯基-2-戊烯(4)2-甲基-1-萘磺酸(5)9-硝基蒽(6)2,4-二甲基-3-苯基戊烷(7)2-氯-3-硝基苯磺酸(8)2,2′-二乙基联苯2(1)1,3,5-三甲苯(2)1,2,4,5-四甲苯(3)1-甲基萘(4)1-甲基-4烯丙基苯(5)异丁基苯(6)2,6-二甲基萘(7)4-溴苯甲烷(8)对异丙基苯甲烷第九章(1)丙酮腙(2)笨甲醛(3)环己酮缩二乙醇(4)(4E)-4-甲基-5-苯基-4-己烯-3-酮(5) 二苯甲酮(6)苯乙酮(或乙酰苯)(7)丁酰苯(8)2-羟基环己酮(9)1-环己基-2-丁酮(10)环戊基甲醛(11)3-羟基丁醛(12)3-氯-3-甲基-2-戊酮(13)5-己烯醛(14)丙二醛(15)5-甲基-4-己烯醛(16)3-甲基环戊酮(17)3-乙基-2,4-戊二酮(18)3-(3,3-二甲基环己基)-丙醛(19)(3R)-3-氯-3-苯基-2-丁酮第十章(1)4,8-二甲基-1-萘酚(2)2,4,6-三硝基苯酚(3)2-萘酚或β-萘酚(4)5-甲基-2-异丙基苯酚(5)对-苯二酚或1,4-苯二酚(10)6-溴代-1,4-萘醌第十一章(1)(2S,3S)-2,3-二氯丁二酸(2) 2-氨基-3-(3,4-二羟基苯基)-丙酸(3)(2Z,4E)-5-甲基-4异丙基-6-羟基-2,4-己二烯酸(3)(2R)-2-乙烯基己酸(4) 3-羟基-环戊烷羧酸(5)4-溴丁酸(6)3-丁酮酸(7)4-甲基-4-苯基-3己酮酸(8)2-戊烯酸(9)2-甲基-2-丙烯酸(10)顺丁烯二酸(11)3-羟基-苯甲酸(12)3-甲基戊酸(13)(1R,3R)-1,3环己烷二羧酸(14)3-羟基-3羧基戊二酸(14)2-氨基4-甲硫基丁酸第十二章(1)邻氨甲酰基苯甲酸甲酯(2)1-氯代甲酸苄酯(3)(2R, 3S)-2, 3-二羟基丁二酸二乙酯(4) 丁酰氯(5)6-乙酰基-2-萘甲酰胺(6)戊二酰亚胺第十三章2-丙胺环己胺氯化三丙基苄铵1,4-丁二胺甲基乙基胺苯胺N-甲基苯胺1,2-乙二胺N,N-二甲基苯胺氯化四甲铵4-甲基-2-戊胺2-甲氨基-4-甲基戊烷乙基异丙基胺3-甲基N,N-二甲基苯胺二乙胺4-氨基苯甲酸乙酯2-(3,4-二羟基苯基)乙胺4-苯胺基苯胺溴化三甲基苄铵三乙胺2-乙酰氨基-3-硫基丙酸4,4’-二溴偶氮苯2,3-二甲氨基己烷2,4-二甲基-2-氨基-3-甲氨基戊烷第十四章4-溴-2-乙酰基呋喃N-甲基--乙基吡咯5-乙酰基噻唑2-甲基-7羟基-吲哚2-羟基-6硝基-8羟基嘌呤1-苄基-5,7-二甲氧基-异喹啉2,6-二羟基-9H-嘌呤4-氯甲基咪唑2-(2-噻吩基)乙醇2,4-二羟基-5甲基嘧啶1-甲基-6-氯异喹啉吡啶并嘧啶噻吩并吡咯吡唑并噁唑噻吩并[2,3-b]呋喃噻吩并[3,2-b] 噁唑咪唑并[2,1-b]噻唑吡唑并[4,5-d] 噁唑第二大题:名词解释(用结构式或反应式表示):第二章烷烃和环烷烃甲基乙基正丙基异丙基正丁基仲丁基异丁基叔丁基甲基游离基乙基游离基正丙基游离基异丙基游离基叔丁基游离基3-甲基戊烷2,3,4-三甲基癸烷异己烷4-异丙基十一烷新戊基反-1-甲基-4-叔丁基环己烷环戊基甲基二环[3.3.0]辛烷第三章立体化学基础对映体非对映体内消旋体外消旋体对称中心对称面手性碳原子手性分子第四章卤代烷甲基碳正离子乙基碳正离子二级碳正离子三级碳正离子叔丁基碳正离子格氏试剂瓦尔登(Walden)转化S N2反应中间体E2反应中间体扎衣采夫(Saytzeff)规则二碘二溴甲烷1-氯-2-苯基乙烷(S)-2-碘己烷新戊基氯乙基溴化镁第五章醇和醚氯化亚砜欧芬脑尔(Oppenauer)氧化卢卡斯(Lucas)试剂沙瑞特(Sarret)试剂琼斯(Jones)试剂(S)-1-苯基-2-丙烯醇(1S,2R)-2-氯环己醇2,3-二巯基丙醇丙烯基烯丙基醚3-甲氧基戊烷苯甲硫醚第六章烯烃丙烯基烯丙基烯丙基游离基烯丙基碳正离子NBS 2-丁烯基叔丁基碳正离子异丁烯亲电加成反应过氧化物效应马氏(Markovnikov’s) 规则2,4,4-三甲基-2-戊烯顺-3,4-二甲基-3-己烯E-3-甲基-4-异己基-3-癸烯(2-)反,(4-)顺-2,4-己二烯第七章炔烃和二烯烃林德拉(Lindlar)试剂狄尔斯-阿尔特(Diels-Alder)反应1,4-己二炔环丙基乙炔3,3-二甲基-2-己炔3-乙基-2-戊烯-4-炔互变异构第八章芳烃苯基苄基苄基游离基苄基碳正离子联苯傅瑞德尔-克拉夫茨(Friedel-Crafts)反应克来门森(Cemmensen)还原3,5-二硝基苯磺酸2,10-二甲基蒽2-氨基-5-溴-3-硝基苯甲酸Z-1-苯基-2-乙基-3-甲基-1-丁烯1,2-二苯乙烷2-氨基-5-羟基苯甲醛2,6-二甲基萘9-硝基菲第九章羰基化合物碘仿碘仿反应羟醛缩合反应(aldol condensation)西佛碱(Schiff’s base)杜伦(Tollens)试剂斐林Fecheling试剂克来门森(Cemmensen)还原乌尔夫-凯惜钠-黄鸣龙(Wolff- Kishner-Huang Minglong)还原法DMSO 麦尔外因-彭杜尔夫(Meerwein-Ponndorf)还原氢化锂铝硼氢化钠康尼查罗(Cannizzaro)反应交叉康尼查罗(Cannizzaro)反应魏悌希(Witting)反应磷叶立德(phosphorus ylide)达尔森(Darzen)反应盖特曼-柯赫(Gettermann-Koch)反应麦克尔加成(Michael addition)丙酮苯腙苯甲醛肟环己酮缩二乙醇乙烯酮(4E)-4-甲基-5-苯基-4-己烯-3-酮(2S,3S)-2,3-二溴丁醛(用Fisher投影式表示)第十章酚和醌苦味酸水杨酸β-萘酚克莱森(Claisen)重排傅瑞斯(Fries)重排柯尔柏一施密特(Kolbe-R.Schmitt)反应瑞穆尔—梯曼(Reimer-Timann )反应对苯醌邻苯醌第十一章羧酸和取代羧酸氯化亚砜酯化反应(esterification)赫尔-乌尔哈-泽林斯基(Hell-Volhard-Zelinsky)反应克脑文格尔(Knoevenagel)反应交酯雷福尔马茨基(Reformatsky)反应反-4-羟基环已烷羧酸(优势构象)(2S,3R)-2-羟基-3-苯基丁酸(Z,E,E)-9,11,13-十八碳三烯酸(R)-2-苯氧基丁酸第十二章羧酸衍生物罗森孟德(Rosenmund)反应克莱森缩合反应(Claisen condensation)交叉酯缩合(crossed ester condensation)狄克曼(Dieckmann)缩合霍夫曼重排(Hofmann rearrangement)光气脲硫脲胍胍基脒基3-甲基戊二腈邻乙酰氧基苯乙酸苯酯2-对羟基苯丙烯酸甲酯三乙酸甘油酯2.5-环已二烯基甲酰氯3-甲基邻苯二甲酸酐3-戊酮酸乙酯N-甲基-δ-戊内酰胺第十三章含氮化合物联苯胺重排(benzidine rearrangement)加布瑞尔(Gabriel)合成法霍夫曼(Hofmann)消除桑德迈尔(Sandmeyer)反应席曼(Schiemann)反应偶氮苯重氮甲烷卡宾(碳烯) (R)-仲丁胺二乙胺双-(2-氯乙基)-胺乙二胺N-甲基-N-乙基环已胺2-氨基乙醇1-萘甲胺4-联苯胺(S)-2-氨基-3-(3,4-二羟基苯基)丙酸第十四章杂环化合物“缺”芳杂环“多”芳杂环斯克劳普(Z.H.Shraup)合成-甲基噻吩5-甲基恶唑N-甲基四氢吡咯3-甲基吲哚5-硝基-8-羟基喹啉5, 6-苯并异喹啉2, 6-二甲基嘌呤吡啶并[2, 3-d]嘧啶3-吲哚乙酸8-溴异喹啉2-甲基-5-苯基吡嗪5-硝基-2-呋喃甲醛4,6-二甲基-2-吡喃酮第十六章氨基酸、多肽、蛋白质和酶的化学(简介)α-氨基酸内盐(偶极离子) 等电点二肽肽键第十七章糖类D-葡萄糖差向异构体D-吡喃葡萄糖端基异构体苷糖脎还原糖非还原糖第十九章类脂异戊二烯“异戊二烯规则”单萜二萜樟脑(-莰酮) 甾烷雌甾烷雄甾烷孕甾烷胆烷胆甾烷正系(5型) 别系(5型)第三大题:选择题(一)1.下面四个同分异构体中哪一种沸点最高?(A) 己烷 (B) 2-甲基戊烷(C) 2,3-二甲基丁烷 (D) 2,2-二甲基丁烷2. 下列环烷烃中加氢开环最容易的是:(A) 环丙烷 (B) 环丁烷(C) 环戊烷 (D) 环己烷3.光照下,烷烃卤代反应的机理是通过哪一种中间体进行的?(A) 碳正离子 (B) 自由基(C) 碳正离子 (D) 协同反应,无中间体4. 1-甲基-4-异丙基环己烷有几种异构体?(A) 2种 (B) 3种 (C) 4种 (D) 5种5.在下列哪种条件下能发生甲烷氯化反应?(A) 甲烷与氯气在室温下混合(B) 先将氯气用光照射再迅速与甲烷混合(C) 甲烷用光照射,在黑暗中与氯气混合(D) 甲烷与氯气均在黑暗中混合6. 下列一对化合物是什么异构体?(A) 非对映体 (B) 构型异构体(C) 对映体 (D) 构造异构体7.与相互关系是:(A) 对映体 (B) 非对映体(C) 构型异构体 (D) 构造异构体8.下列化合物中哪些可能有顺反异构体?(A) CHCl =CHCl (B) CH 2=CCl 2(C) 1-戊烯 (D) 2-甲基-2-丁烯9.构造式为CH 3CHClCH =CHCH 3的立体异构体数目是:(A) 2种 (B) 4种 (C) 3种 (D) 1种10.下列化合物中哪些可能有E ,Z 异构体?(A) 2-甲基-2-丁烯 (B) 2,3-二甲基-2-丁烯(C) 2-甲基-1-丁烯 (D) 2-戊烯HCH3CH 3HH H CH 3CH 3CH 3CH 3H CH 3H CH 311.实验室中常用Br 2的CCl 4溶液鉴定烯键,其反应历程是:(A) 亲电加成反应 (B) 自由基加成(C) 协同反应(D) 亲电取代反应12.(CH 3)2C =CH 2 产物主要是:(A) (CH 3)2CHCH 2Cl (B) (CH 3)2CClCH 3(C) CH 3CH 2CH 2CH 2Cl (D) CH 3CHClCH 2CH 313.CF 3CH =CH 2 + HCl :(A) CF 3CHClCH 3 (B) CF 3CH 2CH 2Cl(C) CF 3CHClCH 3与 CF 3CH 2CH 2Cl 相差不多 (D) 不能反应14.CH 3CH =CH 2 + Cl 2 + H 2O 主要产物为:(A) CH 3CHClCH 2Cl + CH 3CHClCH 2OH (B) CH 3CHOHCH 2Cl + CH 3CHClCH 2Cl(C) CH 3CHClCH 3 + CH 3CHClCH 2OH (D) CH 3CHClCH 2Cl15.某烯烃经臭氧化和还原水解后只得 CH 3COCH 3,该烯烃为:(A) (CH 3)2C =CHCH 3(B) CH 3CH =CH 2(C) (CH 3)2C =C(CH 3)2(D) (CH 3)2C =CH 216.CH 3CH =CHCH 2CH =CHCF 3 + Br 2 (1 mol) 主要产物为:(A) CH 3CHBrCHBrCH 2CH =CHCF 3 (B) CH 3CH =CHCH 2CHBrCHBrCF 3(C) CH 3CHBrCH =CHCH 2CHBrCF 3 (D) CH 3CHBrCH =CHCHBrCH 2CF 317.异戊二烯经臭氧化,在锌存在下水解,可得到哪一种产物?(A) HCHO + OHCCH 2CHO (B) HCHO + HOOCCH 2COOH(C) HCHO + CH 3COCHO (D) CH 3COCHO + CO 2 + H 2O18.下列化合物中哪一个能与顺丁烯二酸酐反应,生成固体产物?(A) 萘(B) CH 3CH 2CH =CH 2 (C) (D) 对二甲苯 19.二氯丙烷可能的异构体数目有多少?(A) 2 (B) 4 (C) 6 (D) 520.下列化合物进行S N 2反应时,哪个反应速率最快?21.下列化合物进行S N 1反应时,哪一个反应速率最快?CH 2C CH 3CH CH 2(A)I Br (C)Cl (B)F (D) (A) CH 3CH 2CH 2CH 2Br(B) CH 3CHCH 2CH Br CH 3222.在NaOH 水溶液中,(CH 3)3CX(I),(CH 3)2CHX(II),CH 3CH 2CH 2X(III),CH 2=CHX(IV)各卤代烃的反应活性次序为: (A) I>II>III>IV (B) I>II>IV>III (C) IV>I>II>III (D) III>II>I>IV23.(CH 3)3CBr 与乙醇钠在乙醇溶液中反应主要产物是: (A) (CH 3)3COCH 2CH 3 (B) (CH 3)2C =CH 2(C) CH 3CH =CHCH 3 (D) CH 3CH 2OCH 2CH 324.下列哪个化合物能生成稳定的格氏试剂?(A) CH 3CHClCH 2OH (B) CH 3CH 2CH 2Br (C) HC ≡CCH 2Cl (D) CH 3CONHCH 2CH 2Cl 25.合成格氏试剂一般在下列哪一溶剂中反应? (A) 醇 (B) 醚 (C) 酯 (D) 石油醚26.(CH 3)2CHCH 2Cl 与(CH 3)3CCl 是什么异构体? (A) 碳架异构 (B) 位置异构 (C) 官能团异构 (D) 互变异构27.(R )-2-氯丁烷与(S )-2-氯丁烷的哪种性质不同? (A) 熔点 (B) 沸点 (C) 折射率 (D) 比旋光度 28. 与一对化合物的相互关系是:(A) 对映异构体(B) 非对映异构体 (C) 相同化合物 (D) 不同的化合物 29. 主要产物是:30.C 2H 5CH 3Br H Br CH 3C 2H 5H CH 3CH 2C CH 3Cl CH 2CH 3+NaOH (A) CH 3CH 2C CH 3CHCH 3(B) CH 3CH 2C CH 2CH 3CH 2(C) CH 3CH 2C CH 2CH 3OH CH 3(D) CH 3CH 2( IV)( III )( II )( I )CHOCH 3CH 2OCH 3CHOCH 3CH 2OCH 3CH 2OHCHOH CH 2OCH 3CH 2OH CHOH CH 2OHCH 2OH沸点升高的顺序是: (A) I,II,III,IV (B) IV,III,II,I (C) I,II,IV,III (D) III,IV,II,I 31.环氧乙烷 + NH 3───> 产物是: (A) (B) NH(CH 2CH 2OH)2 (C) N(CH 2CH 2OH)3 (D) 全都有 32.ClCH 2CH 2CH 2OH + PBr 3──> 主要产物为: (A) BrCH 2CH 2CH 2OH (B) CH 2=CHCH 2OH (C) ClCH 2CH =CH 2(D) ClCH 2CH 2CH 2Br33.乙醇与二甲醚是什么异构体? (A) 碳干异构 (B) 位置异构 (C) 官能团异构 (D) 互变异构34.Williamson 合成法是合成哪一种化合物的主要方法? (A) 酮 (B) 卤代烃 (C) 混合醚 (D) 简单醚35.下列化合物HOH(I),CH 3OH(II),(CH 3)2CHOH(III),(CH 3)3COH(IV)的酸性大小顺序是: (A) I>II>III>IV (B) I>III>II>IV (C) I>II>IV>III (D) I>IV>II>III36.为了合成烯烃(CH 3)2C =CH 2,最好选用下列何种醇?37.为了合成烯烃CH 3CH 2CH 2CH =CH 2,应采用何种醇?38.下列反应应用何种试剂完成?(A) LiAlH 4 (B) NaBH 4 (C) Na + EtOH (D) Pt/H 239.用Grignard 试剂合成 ,不能使用的方法是什么?40.冠醚可以和金属正离子形成络合物,并随着环的大小不同而与不同的金属离子络合,18-冠CH 2CH 2OH NH 2CH 3CH 2CHCH 3OH (C)(CH 3)2CHCH 2OH(A)CH 3CH 2CH 2CH 2OH (D)(CH 3)3COH (B)CH 3CH 2CH 2CHCH 3OH(CH 3)2CHCHCH 3OH (C)(D)CH 3CH 2CH 2CH 2CH 2OH C OH CH 2CH 3(CH 3)2(A)(B)COOH CH 2OH (A) C 6H 5COCH 3CH 3CH 2MgBr (B) CH 3CH 2CCH 3O C 6H 5MgBr (C) C 6H 5CCH 2CH 3O CH 3MgI(D) C 6H 5MgBr CH 3CHO ++++C 6H5C CH 3OH CH 2CH 3-6最容易络合的离子是: (A) Li + (B) Na + (C) K + (D) Mg 2+41.分子式为C 5H 10的开链烯烃异构体数目应为: (A) 5种 (B) 4种 (C) 6种 (D) 7种 42.1,2- 二甲基环丁烷的立体异构体数目有:(A) 2种 (B) 4种 (C) 6种 (D) 3种43.下列化合物有对映异构的应是:(A) (1) (2) (B) (1) (3) (C) (2) (4) (D) (3)(4) 44.下列化合物有对映异构的应是:45.上述构型的正确命名是: (A )(1)R (2)R (3)S (B )(1)R (2)S (3)S (C )(1)S (2)S (3)S (D )(1)R (2)R (3)R 46.H O HM eC H 2O H H O H 化合物的构型正确命名是:(A) 2R , 3R (B) 2R , 3S (C) 2S , 3R (D) 2S , 3S47.用来表示下列药物假麻黄碱的投影式应是:CH 3COCH 3 CH 3CHOHCH 2CH 3CH 3CHOHCH 2CH 3CH 3CHOHCH 2CH 3(4)(3)(2)(1)C CC Me Me MeH O2O 2Br Br N N O2Br Br Br N CH 3CHDC 2H 5(1)(2)(3)(4)(A) (1),(2) (B) (1),(3) (C) (1),(4) (D) (2),(4)H NH 2CH 3Ph Br CH 2OH CH 3H Cl CH 2NH 2CH 2NHCH 3Br (1)(2)(3)PhMe H NHMe OHH Ph48.薄荷醇理论上所具有的立体异构体数目应为:(A) 8种 (B) 16种 (C) 2种 (D) 4种49.2,3-二甲基丁烷沿C2-C3旋转时最稳定的构象是:50.1,2-二甲基环丙烷有几个立体异构体? (A) 无立体异构体 (B) 二个,一对对映体 (C) 三个,一对对映体和一个内消旋体 (D) 四个,二对对映体51.判断下述四种联苯取代物中哪个是手性分子:52.BrCH 2CH 2Br 的优势构象是: (A) 全重叠构象 (B) 部分重叠构象 (C) 邻交叉构象 (D) 对交叉构象OH (D)(C)(B)(A)CH 3HH 3C CH 3HCH 3CH 3CH 3HH H CH 3CH 3CH 3CH 3H CH 3CH 3CH 3H H CH 3CH 3CH 3(D)(C)(B)(A)I I HO 2C CO 2H Br Br I ClI Br IIHO 2C CO 2H II53.下列构象的稳定性顺序为: _.54.在下列化合物中,属于手性分子的是:55.在下列化合物中, (R )-2-碘己烷的对映体是:(D )(C )(B )(A )___C H 3C C 4H 9n I H C 2H 5C n C 3H 7H IC 2H 5C C 3H 7 n I H _C H 3Cn C 4H 9HI 56.下列化合物中, 与(R )-2-甲基丁酸不相同的化合物是:(A) (a)>(b)>(c)>(d) (B) (b)>(a)>(d)>(c)(C) (c)>(b)>(a)>(d) (D) (d)>(a)>(b)>(c) (b)(d)(c)(a)H Br C 2H 5H 3C BrH Br Br H HCH 3C 2H 52H 5H 3CH 3C 2H 5BrH Br H (D)(C)(B)(A)6H 5C CH 3H 23C COOH Br 6H 5C HH CH 6H5CH 2C CH 3H 2(D)(C)(B)(A)C CH 3HOOC 2CH3C COOHCH 3CH 23C HCH 32CH 3C CH 3CH 3CH 257.下列各组投影式中, 两个投影式相同的组是:58.下列化合物中, 无光学活性的是:59. α, β-不饱和羰基化合物与共轭二烯反应得环己烯类化合物,这叫什么反应? (A) Hofmann 反应 (B) Sandmeyer 反应 (C) Diels-Alder 反应 (D) Perkin 反应60. 异戊二烯经臭氧化,在锌存在下水解,可得到哪一种产物? (A) HCHO + OHCCH 2CHO (B) HCHO + HOOCCH 2COOH (C) HCHO + CH 3COCHO(D) CH 3COCHO + CO 2 + H 2O61. 下列化合物中哪一个能与顺丁烯二酸酐反应,生成固体产物? (A) 萘(B) CH 3CH 2CH =CH 2 (C)(D) 对二甲苯62.丁二烯与溴化氢进行加成反应构成什么中间体?(C)(A)(D)(B)CHO CHO CH 3COOH H 2N H COOH H CH 3NH 2CH 2NH 2H OH H C 2H 5HOCH 2Br CH 3C 2H 5Br HCH 2OH OH H CH 2NH 2COOH C 6H 5Cl COOH C 6H 5Cl CH 3(D)(C)(B)(A)C C C CH 3C 2H 5BrBrC C C C H H Cl H C C C Cl Cl I BrC C C Cl Cl I I CH 2C CH 3CH CH 2CH 3CH CH CH 2(C)CH 2CH 2CH CH 2(D)CH 3CH CH CH 2(B)(A)CH 3CH CH CH 2+++_68.一个天然醇C 6H 12O 比旋光度[ ]25 = +69.5°,催化氢化后吸收一分子氢得到一个新的醇,比旋光度为0,则该天然醇结构是:64.下列试剂中,哪一个可用来区别顺和反-1,2-环戊二醇? (A) 丙酮 (B) 臭氧 (C) 异丙氧基铝 (D) 氢化铝锂 65.哪一种化合物不能用于干燥甲醇? (A) 无水氯化钙 (B) 氧化钙 (C) 甲醇镁 (D) 无水硫酸钠 66.为检查司机是否酒后驾车采用呼吸分析仪,其中装有K 2Cr 2O 7 +H 2SO 4,如果司机血液中含乙醇量超过标准,则该分析仪显示绿色,其原理是: (A) 乙醇被氧化 (B) 乙醇被吸收 (C) 乙醇被脱水 (D) 乙醇被还原 67.碳数相同的化合物乙醇(I),乙硫醇(II),二甲醚(III)的沸点次序是: (A) II>I>III (B) I>II>III (C) I>III>II (D) II>III>I 68.下列有机溶剂,具有最大火灾危险的是: (A)乙醇 (B)二乙醚 (C)四氯化碳 (D)煤油 69.下列化合物碱性大小的顺序为:① CH 3O -② (CH 3)2CHO -③ CH 3CH 2O -④ (CH 3)3CO -(A) ① > ③ > ② > ④ (B) ④ > ② > ③ > ① (C) ④ > ③ > ① > ② (D) ① > ② > ③ > ④ 70.氧化为的氧化剂应是:(A) ①② (B) ①③(C) ①④ (D) ②④71.(D)(B)OH CH 3CH 3CH 2CH CH 2OH CH CH 2(C)(A)CH 2CH CH 2CH 3CH 2CH OHOH OHO PhCO 3H KM n O 4/H +CrO 3/ MnO 2②③ ④吡啶新鲜 ①下列醇的酸性大小顺序为:① CH 3CH 2OH ② CH 3CHOHCH 3③ PhCH 2OH ④ (CH 3)3C ─OH (A) ③ > ① > ② > ④ (B) ① > ② > ③ > ④ (C) ③ > ② > ① > ④ (D) ① > ③ > ② > ④ 72.能使不饱和伯醇氧化成不饱和醛的氧化剂应是: ① KMnO 4/H +② CrO 3/H + ③ CrO 3/吡啶④新鲜 MnO 2(A) ③④ (B) ①④ (C) ①③ (D) ②③ 73.欲从制备, 应选用哪种反应条件?(A) CH 3OH/CH 3ONa(B) CH 3OH/H + (C) CH 3OH/H 2O(D) CH 3OCH 3 74.在碱性条件下, 可发生分子内S N 反应而生成环醚的是下列哪个卤代醇:75.乙醇和甲醚互为什么异构体?(A) 碳架异构体 (B) 互变异构体 (C) 官能团异构体 (D) 价键异构体 76.C 3H 6O 有几种稳定的同分异构体? (A) 3种 (B) 4种 (C) 5种 (D) 6种 77.下面反应的主要产物是:(A) (B)CH 2CH 3CH CH 3CHCH 2OCH 3 OH 22Br2Br 2(B)(A)2Br 2(D)(C)CH 3CH CCH 3CH 3CH 3CH 2C CH 3OSO 3H CH 3CH 3CH 2C CH 3O C CH 3CH 2CH 3CH 3CH 2CH 2CH 3CH 2C CH 3OH CH 350%H 2SO 4(C) (D)78. 下面反应的主要产物是:79.下述反应能用来制备伯醇的是: (A) 甲醛与格氏试剂加成, 然后水解 (B) 乙醛与格氏试剂加成, 然后水解 (C) 丙酮与格氏试剂加成, 然后水解 (D) 苯甲腈与格氏试剂加成, 然后水解 80.下面哪种试剂只能将烯丙位、苯甲位的伯醇、仲醇氧化成相应的醛和酮: (A) 过氧酸 (B) 琼斯试剂 (C) 新制的MnO 2 (D) 费兹纳-莫发特试剂 81.RMgX 与下列哪种化合物反应, 再水解, 可在碳链中增长两个碳: (A) (B)(C) (D)82.下列哪一种化合物不能用以制取醛酮的衍生物? (A) 羟胺盐酸盐 (B) 2,4-二硝基苯 (C) 氨基脲 (D) 苯肼 83.下列哪个化合物不能起卤仿反应? (A) CH 3CH(OH)CH 2CH 2CH 3 (B) C 6H 5COCH 3(C) CH 3CH 2CH 2OH (D) CH 3CHO 84.下列哪个化合物可以起卤仿反应?(A) CH 3CH 2CH 2OH (B) C 6H 5CH 2CH 2OHDMFRCl C 6H 5SO 2ClCH CH 2C 2H 5C OH CH 3CH 3C CH 2C Cl OH CH 3C 2H 5(D)C CH 2CH Cl C 2H 5CH 3(C)C 2H 5CCH 2CH Cl (B)(A)Cl CH 2CH C CH 3C 2H 5 吡啶CH 3CH 2OH CH 3CH 2XOC 2H 5COC 2H 5O(C) CH 3COCH 2CH 2COCH 3 (D) HCHO 85乙醛和过量甲醛在NaOH 作用下主要生成:86.用格氏试剂制备1-苯基-2-丙醇,最好采用哪种方案? (A) CH 3CHO + C 6H 5CH 2MgBr (B) C 6H 5CH 2CH 2MgBr + HCHO (C) C 6H 5MgBr + CH 3CH 2CHO (D) C 6H 5MgBr + CH 3COCH 3 87在稀碱作用下,下列哪组反应不能进行羟醛缩合反应? (A) HCHO + CH 3CHO (B) CH 3CH 2CHO + ArCHO (C) HCHO + (CH 3)3CCHO (D) ArCH 2CHO + (CH 3)3CCHO 88.下列四个反应,哪一个不能用来制备醛: (A) RMgX + (① HC(OEt)3,② H +/H 2O) (B) RCH 2OH + CrO 3/H 2SO 4蒸馏(C) RCH =CHR + (① O 3,②H 2O/Zn) (D) RCOCl + H 2/Pt 89.Clemmensen 还原是用Zn(Hg)/HCl 进行还原,其作用是使 : (A) 羰基成醇 (B) 羰基成亚甲基 (C) 酯成醇 (D) 酯成烃 90.Aldol(醛醇、醇醛、羟醛)缩合是用稀酸或稀碱催化,从反应活性中心看,它们是: (A) 一个羧酸酯出羰基,一个醛出α-C (B) 一个羧酸酯出羰基,一个酮出α-C (C) 两个羧酸酯,一个出羰基,一个α-C (D) 两个醛或酮,一个出羰基,一个α-C 91.黄鸣龙还原是指: (A) Na 或Li 还原苯环成为非共轭二烯 (B) Na + ROH 使羧酸酯还原成醇 (C) Na 使酮双分子还原(D) NH 2NH 2/KOH/高沸点溶剂,还原羰基成亚甲基 92下列四个反应,不能用于制备酮的是:93.下列四个试剂,不跟CH 3CH 2COCH 2CH 3反应的是: (A) RMgX (B) NaHSO 3饱和水溶液 (C) PCl 5 (D) LiAlH 4 94.完成下面的转变,需要哪组试剂?(A) (HOCH 2)3CCHO (B) C(CH 2OH)4 (C) CH 3CH CHCHO (D) CH 3CHCH 2CHO OH(A) R 2CHOH,CrO 3/H 2SO 4 (B) RCOCHR'CO 2C 2H 5,①OH -,(2)H 3O +/ (C) ArH,RCONH 2/AlCl 3 (D) R 2C =CR 2,①O 3,②H 3O +/Zn?CH3CH=CH(CH2)2CH=O ───→HOOCCH2CH2CH=O(A)KMnO4(B)(1)EtOH/干HCl (2)KMnO4 (3)H3O+(C)K2Cr2O7(D)HNO395.下面的氧化反应,用何种氧化剂较好?(A) K2Cr2O7/H+(B) CrO3·吡啶(C) Ag(NH3)2+(D) 稀、冷KMnO4CH O CO2H96.Tollens 试剂的组成是:(A) CrO3·吡啶(B) Cu(OH)2·酒石酸钾(C) Ag(NH3)2+·OH-(D) 新鲜MnO297.还原C=O 为CH2的试剂应是:(A) Na/EtOH (B) H2N-NH2/HCl(C) Sn/HCl (D) Zn-Hg/HCl98.下面化合物羰基活性最强的是:(A) ClCH2CH2CHO (B) CH3CH2CHO(C) CH3CHClCHO (D) CH3CHBrCHO99.Tollens 试剂的组成是:(A) CrO3·吡啶(B) Cu(OH)2·酒石酸钾(C) Ag(NH3)2+·OH-(D) 新鲜MnO2100.还原C=O 为CH2的试剂应是:(A) Na/EtOH (B) H2N-NH2/HCl(C) Sn/HCl (D) Zn-Hg/HCl101下面化合物羰基活性最差的是:(A) PhCHO (B) CH3CHO(C) PhCOCH3(D) CH3COCH3102下面化合物羰基活性最强的是:(A) ClCH2CH2CHO (B) CH3CH2CHO(C) CH 3CHClCHO (D) CH 3CHBrCHO 103.的产物是:104C 6H 5OCH 3(I),C 6H 5COCH 3(II),C 6H 6(III),C 6H 5Cl(IV)四种化合物硝化反应速率次序为: (A) I>III>II>IV (B) I>III>IV>II(C) IV>I>II>III (D) I>IV>II>III 105硝化反应的主要产物是:106苯乙烯用热KMnO 4氧化,得到什么产物?107苯乙烯用冷KMnO 4氧化,得到什么产物?(A) PhCHCH 2COCMe 3Et (B) PhCH CH C(OH)CMe 3Et (C) PhCHCH 2CHCMe 3OH Et (D) PhCH 2CH 2C(OH)CMe 3Et (2)H 3+(1)EtMgBrPhCH CHCOCMe 3NO 2(C)(D)(B)(A)O 2N NO 2NO 2NO 2NO 2NO 2NO 2NO 2(C)(D)(B)(A)CH 2COOH CH OH CH 2OH CO 2H CH 2CHO(C)(D)(B)(A)CH 2COOH CH OH CH 2OH CO 2H CH 2CHO108苯乙烯催化加氢,在室温低压下得到什么产物? (A) 无变化 (B) 乙苯 (C) 甲苯 (D) 乙基环己烷 109苯乙烯催化加氢,高温高压下得到什么产物? (A) 乙苯 (B) 甲苯 (C) 环己烷+乙烷 (D) 乙基环己烷 110C 6H 6 + (CH 3)2CHCH 2Cl ? (A) PhCH 2CH(CH 3)2 (B) PhC(CH 3)3 (C) PhCH(CH 3)CH 2CH 3 (D) Ph(CH 2)3CH 3111傅-克反应烷基易发生重排,为了得到正烷基苯,最可靠的方法是: (A) 使用AlCl 3作催化剂 (B) 使反应在较高温度下进行 (C) 通过酰基化反应,再还原 (D) 使用硝基苯作溶剂 112 用KMnO 4氧化的产物是:113 由───→最好的路线是:(A) 先硝化,再磺化,最后卤代 (B) 先磺化,再硝化,最后卤代 (C) 先卤代,再磺化,最后硝化 (D) 先卤代,再硝化,最后磺化 114.下列哪一种化合物不能用以制取醛酮的衍生物? (A) 羟胺盐酸盐 (B) 2,4-二硝基苯(C) 氨基脲 (D) 苯肼 115.下列哪个化合物不能起卤仿反应? (A) CH 3CH(OH)CH 2CH 2CH 3 (B) C 6H 5COCH 3(C) CH 3CH 2CH 2OH (D) CH 3CHO 116.下列哪个化合物可以起卤仿反应?(A) CH 3CH 2CH 2OH (B) C 6H 5CH 2CH 2OHAlCl 3CH 3C(CH 3)3COOH C(CH 3)3CH 3COOH COOH COOH CHOC(CH 3)3(D)(C)(B)(A)Cl O 2N NO 2SO 3H(C) CH 3COCH 2CH 2COCH 3 (D) HCHO 117.乙醛和过量甲醛在NaOH 作用下主要生成:主要产物是:(A)(B)118. (C) (D) 119用格氏试剂制备1-苯基-2-丙醇,最好采用哪种方案? (A) CH 3CHO + C 6H 5CH 2MgBr (B) C 6H 5CH 2CH 2MgBr + HCHO (C) C 6H 5MgBr + CH 3CH 2CHO (D) C 6H 5MgBr + CH 3COCH 3 120主要产物是:(A) C 6H 5CH 2OH C 6H 5COOH (B) C 6H 5CHOHCH 2COOCOCH 3 (C) C 6H 5CH =CHCOOCOCH 3(D) C 6H 5CH =CHCOOH121.在稀碱作用下,下列哪组反应不能进行羟醛缩合反应? (A) HCHO + CH 3CHO (B) CH 3CH 2CHO + ArCHO (C) HCHO + (CH 3)3CCHO (D) ArCH 2CHO + (CH 3)3CCHO 122三聚氰胺甲醛树脂常用于制造贴面板,合成原料是: (A) 三聚氰胺与甲醛 (B) 三聚异氰酸与甲胺 (C) 尿素与甲醛 (D) 尿素 + 丙二酸酯 123有些醛类化合物可被一些弱氧化剂氧化.Fehling 试剂指的是: (A) AgNO 3和NH 3(H 2O)生成的溶液(B) CuSO 4溶液与NaOH 和酒石酸钾钠生成的溶液 (C) CuSO 4溶液与NaOH 和柠檬酸生成的溶液 (D) CuSO 4与NH 3水的溶液 124.氢化铝锂和硼氢化钠都是常用的氢化金属络合物,当用它们还原醛或酮时,分子中的四个氢原子都能进行反应,这类反应的特点是: (A) 能产生氢正离子 (B) 能产生氢负离子 (C) 能产生氢自由基 (D) 铝或硼提供电子 125下列四个反应,哪一个不能用来制备醛:(A) (HOCH 2)3CCHO (B) C(CH 2OH)4 (C) CH 3CH CHCHO (D) CH 3CHCH 2CHO OH OH C O CH 3(C 6H 5)2C CH 3 C C 6H 5OC CH 3C 6H 5OH (CH 3)2C C 6H 5CH 3CC 6H 5(CH 3)2C C(C 6H 5)2OH OHC 6H 5CCH 3O C 6H 5CHO +(CH 3CO)2O(A) RMgX + (① HC(OEt)3,② H +/H 2O) (B) RCH 2OH + CrO 3/H 2SO 4蒸馏 (C) RCH =CHR + (① O 3,②H 2O/Zn) (D) RCOCl + H 2/Pt 126Clemmensen 还原是用Zn(Hg)/HCl 进行还原,其作用是使 : (A) 羰基成醇 (B) 羰基成亚甲基 (C) 酯成醇 (D) 酯成烃 127Aldol(醛醇、醇醛、羟醛)缩合是用稀酸或稀碱催化,从反应活性中心看,它们是: (A) 一个羧酸酯出羰基,一个醛出α-C (B) 一个羧酸酯出羰基,一个酮出α-C (C) 两个羧酸酯,一个出羰基,一个α-C (D) 两个醛或酮,一个出羰基,一个α-C 128黄鸣龙还原是指: (A) Na 或Li 还原苯环成为非共轭二烯 (B) Na + ROH 使羧酸酯还原成醇 (C) Na 使酮双分子还原(D) NH 2NH 2/KOH/高沸点溶剂,还原羰基成亚甲基 129下列四个反应,不能用于制备酮的是:130根据关键一步确定有机反应属于哪种类型: (A) 亲电反应 (B) 亲核反应 (C) 自由基反应 (D) 周环反应请用A ~D 字母代号判别下列反应:131CH 3(CH 2)5CHO CH 3(CH 2)5CH 2OH 应选用什么试剂: (A) Fe + HOAc (B) NH 2NH 2/KOH/二缩乙二醇/ (C) ①Mg(Hg) ②H 2O (D) Na + EtOH 132在下列化合物中,能被2,4-二硝基苯肼鉴别出的是: (A) 丁酮 (B) 丁醇 (C) 丁胺 (D) 丁腈 133下面反应属于何种缩合反应?(A) Claisen 缩合 (B) Perkin 缩合 (C) Dieckmann 缩合 (D) 半缩醛 134下面四个化合物中,能给出银镜反应的是:(A) R 2CHOH,CrO 3/H 2SO 4 (B) RCOCHR'CO 2C 2H 5,①OH -,(2)H 3O +/ (C) ArH,RCONH 2/AlCl 3 (D) R 2C =CR 2,①O 3,②H 3O +/Zn HCN(CH 3)2C CH 2COCH 3CN(CH 3)2C CHCOCH H+O OH H OH CH O(A)Ⅱ(B)Ⅱ,Ⅲ和Ⅳ(C)Ⅰ(D)Ⅱ和Ⅲ135完成下面的转变,需要哪组试剂??CH3CH=CH(CH2)2CH=O ───→HOOCCH2CH2CH=O(A)KMnO4(B)(1)EtOH/干HCl (2)KMnO4 (3)H3O+(C)K2Cr2O7(D)HNO3136下面的氧化反应,用何种氧化剂较好?(A) K2Cr2O7/H+(B) CrO3·吡啶(C) Ag(NH3)2+(D) 稀、冷KMnO4 137Tollens 试剂的组成是:(A) CrO3·吡啶(B) Cu(OH)2·酒石酸钾(C) Ag(NH3)2+·OH-(D) 新鲜MnO2138还原C=O 为CH2的试剂应是:(A) Na/EtOH (B) H2N-NH2/HCl(C) Sn/HCl (D) Zn-Hg/HCl139下面化合物羰基活性最差的是:(A) PhCHO (B) CH3CHO(C) PhCOCH3(D) CH3COCH3140下面化合物羰基活性最强的是:(A) ClCH2CH2CHO (B) CH3CH2CHO(C) CH3CHClCHO (D) CH3CHBrCHO141羟胺与醛酮发生亲核加成的产物是:(A) 腙(B) 西佛碱 (C) 肟(D) 缩氨脲142的产物是:CH O CO2H(A) PhCHCH2COCMe3Et (B) PhCH CH C(OH)CMe3Et(C) PhCHCH2CHCMe3OHEt(D) PhCH2CH2C(OH)CMe3Et(2)H3+(1)EtMgBrPhCH CHCOCMe3143.用Mg 将丙酮还原制备频哪醇时, 应选用哪个溶剂? (A) H 2O (B) C 2H 5OH (C)苯 (D)(CH 3)2CH ─OH 144下列化合物中, 哪个化合物有多于1组的等性原子? 145下列哪个化合物的红外光谱不可能出现羟基吸收峰。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
自由基取代反应、单分子消除反应、频哪醇的重排、Ferrier 重排反应、钯催化反应中的β-氢消除反应、Michael加成反应等简介摘要:本文通过查阅文献,简单介绍了环糊精对喹啉甲基自由基取代反应、单分子消除反应、频哪醇的重排、Ferrier 重排反应、钯催化反应中的β-氢消除反应、Michael加成反应等几个反应及其简单应用。
关键字:自由基取代,E1反应,频哪醇的重排,Ferrier 重排,钯催化反应,Michael加成一、环糊精对喹啉甲基自由基取代反应环糊精是由6、7或8个葡萄糖单元以1,4一糖苷键结合而成的环状化合物分别称为α,β或γ一环糊精,(简称为α、β或γ)。
它的分子形状略呈倒梯形。
环中各葡萄糖单元均处于椅式构象,每个葡萄糖单元的伯、仲羟基都处在空腔的外侧,因此呈亲水性;而空腔内侧呈疏水性,它像酶一样,提供了一个疏水结合部位,可以与许多分子形成包结物,被包结底物处在合适位置时,它可以使反应速率增加,否则可抑制反应的进行,因此表现出其特异的选择性。
据文献报导[1,2]。
喹啉在酸性条件下,银离子存在时,加入过二硫酸钱,可与叔丁醇或乙酸发生反应,生成2一甲基喹啉,4一甲基喹啉及2 ,4一二甲基喹啉。
反应是经过甲基自由基进行的。
喹啉甲基自由基取代反应的机理通常按以下方式进行:首先,在氧化还原体系中产生二价银离子,它与叔丁醇作用生成烷氧基自由基,烷氧基自由基再生成丙酮和甲基自由基,然后,甲基自由基与质子化的喹琳发生反应,生成2一甲基喹啉 ,4一甲基喹啉,和2 ,4一二甲基喹啉的混合产物。
若用乙酸代替叔丁醇时,则甲基自由基按如下方式产生。
当β-CD 存在时 ,关键在于β-CD 与喹啉形成包结物后才能起到保护作用而阻止反应进行。
喹啉与β-CD形成包结物,使喹啉中的氮原子深深嵌在β-CD 空腔内,因而使其质子化部分受阻,由于β-CD 空腔体已基本被体积较大的喹啉占满,尽管甲基自由基能进入空腔,但甲基自由基在其中的自由度大大受到影响,当喹啉进入β-CD空腔后,甲基自由基若要进入β-CD空腔与哇琳发生反应,所需时间则比直接与质子化的喹啉反应慢得多,因此使甲基自由基消耗较大,这样使得β-CD 存在时,反应得以抑制[3]。
二、单分子消除反应消除反应是指在一个有机分子中消去两个原子或基团的反应称为消除反应(elimination)。
可以根据两个消去基团的相对位置将其分类。
若两个消去基团连在同一个碳原子上,称为1,1-消除或α-消除;两个消去基团连在两个相邻的碳原子上,称为1,2-消除或β-消除;两个消去基团连在1,3位碳原子上,则称为1,3-消除或γ-消除[4]。
下面主要介绍一下E1消除反应:这类反应都是通过生成碳正离子进行的,其反应历程为在大多数情况下, E1反应没有立体选择性.但在有些情况下,E1反应是发生反式消除实验结果表明上式中主要产物是Hotmann烯烃应用构象分析我们对这一反应加以讨论,如果生成Saytzeff烯烃其反应物必须采取构象(I),而要生成Hotmann烯烃其反应物的构象应为(II)在构象中和在邻位交叉的位置上而互相排斥但在构象(II)中没有这种排斥,所以优先发生由构象(II)进行的消去,且是立体化学反式消去这时Hotmann消去比Saytzeff消去优先发生,其主要产物为Hotmann烯烃:上例反应中可得到(Z)型和(E)型两种异构体,从构象分析上看 ,生成(E)型时的构象比较稳定 ,因此(E)型生成的较多为主要产物 ,其结果与实验事实相吻合。
上述的E1反应是按极性的反应历程进行的。
有些单分子消除反应是按非极性的环形消除反应历程进行的,这些反应多是通过环状的过渡态进行热分解。
这样的反应历程要求消除的氢原于和离去基要处于顺位一顺式[5]。
例:Chugaev反应三、频哪醇的重排Pinacol重排反应是指1,2-二轻基化合物在质子酸或者路易斯酸存在条件下,脱去一份子水,然后发生一个1,2迁移,产生碳基化合物旳反应。
随着有机化学的发展,化合物2-6在温和条件下使离去基团X离去,然后发生一个1,2迁移,同样可以发生重排。
我们叫这种反应为Semipinacol重排反应[6]。
四、Ferrier 重排反应Ferrier 重排反应是一种类似于烯丙基重排的反应, 它可以广泛地用来合成2,3-不饱和糖苷. 1969 年, Ferrier等[7]。
使用 3,4,6-三-O-乙酰基-D-葡烯糖与醇或酚在路易斯酸的催化下, 合成了带有烷基或芳基的 2,3-不饱和糖苷。
五、钯催化反应中的β-氢消除反应自从 1958 年发现了Wacker 流程, 即乙烯在氯化钯和氯化铜催化下为空气氧化生成乙醛以来[8,9 ],现代钯化学得到了迅猛发展. 20世纪60年代后期, 钯催化下的烯烃芳基化或烯基化反应即Heck反应成为化学家手中的一个强有力的合成方法[10].第一个金属催化的交叉偶联反应——Kumada-Corriu 反应在 1972年作为一种合成手段得到应用[11,12],这是将两个有机基团形成一个碳—碳键的合成路线的开始[13,14].自从 Wilkinson 的先驱性工作以来,β-氢消除(以下称β-H 消除)被视为过渡金属化学中的一个最重要的基元反应.在Heck反应中, β-H消除是淬灭碳—钯键的关键步骤[15];在Wacker流程中,β-H消除虽然是淬灭碳—钯键的关键步骤, 但由此生成了零价钯, 必须再用氧化剂才能完成催化循环.Heck 反应的机理Wacker流程的简单机理六、Michael加成反应一个能提供碳负离子的化合物(称为给体)与一个能提供共轭体系的化合物,如α,β-不饱和醛、酮、腈、硝基化合物等(称为受体)在碱性催化剂作用下,发生亲核1,4-加成反应,称为Michael加成[4]。
Michael加成反应是有机合成化学中构筑碳-碳键以及碳-杂键最为重要的反应之一,自从1887年Michael首次报道了该反应以来[16],引起了世界各地化学工作者们极大的研究兴趣,成为有机化学中研究最为广泛的反应之一,一直是有机化学反应的研究热点。
手性是自然界的基本属性之一,许多重要的药物分子和天然产物都是有手性的,而且生命体内的物质大多数也是手性化合物,随着不对称Michael加成反应的研究发展和不断完善,为许多手性有机化合物的合成提供了一种有效途径。
因此不对称Michael加成反应的研究具有重要的现实意义[17]。
Michael加成反应的一般式如下:Michael加成反应反应机理:2003年Takemoto小组首次报道了手性双官能化硫脲催化剂49催化的丙二酸二乙酯对硝基苯乙稀的不对称Michael加成反应,产物的对映选择性可达93%。
实验结果表明,催化剂的活性与分子中的硫脲结构单元和叔胺基都有关系,分子中必须同时具有这两部分才能保持较高的催化活性和对映选择性,且叔胺基氮上的两个取代基大小会影响反应速率和对映选择性,如果单独采用硫脲或者叔胺类催化剂则不能有效催化该反应的进行,这说明此类催化剂是靠分子中的硫脲和叔胺基两部分来共同活化底物并控制反应的对映选择性,作者还提出了反应可能的过渡态,从下图可以看出,双官能团催化剂与丙二酸二乙酯和硝基烯都有相互作用,共同控制产物的立体选择性。
而且催化剂分子中三氟甲基的吸电子能力很强,可显著提高硫脲氮上氢的酸性,有利于与Lewis碱亲核试剂结合。
若将催化剂中苯环上的三氟甲基换成苯基,由于吸电子能力下降,改变了分子中电子云的分布,使得形成氢键的能力下降,会降低加成产物的对映选择性。
在之后的有机小分子催化中,该类催化剂具有重要应用,因此也被命名为Takemoto硫脲催化剂。
总之,有机反应种类较多,以上只是常见反应中的少数几个,又因为有机反应常常有新的反应被发现。
因此,我们在掌握常见有机反应的同时,更需要时常关注新的反应,用更完善的理论来指导我们的实践。
参考文献:[1].Minisci F.Nucleophilic character of alkyl-Vi.A new convenient selective alkyation of heteroaromatic bases.Tetrahedron1971.27:3575.[2].Minisci F,Galli R,Cecere m,Malatestu v,Caronna T, Nucleophilic character ofalkyl radicals: New syntheses by alkylradicals generated in redox processes. Tetrahedron Letters1968,5609〕[3]丁景范,刘博, 熊裕堂,金硕,夏炽中.β-环糊精对喹啉甲基自由基取代反应的抑制作用[J]. 山西大学学报1992,15(2)[4]邢其毅,裴伟伟,徐瑞秋,裴坚.第六章:脂肪族饱和碳原子的亲核取代反应β-消除反应,第十二章:醛和酮亲核加成共轭加成[M].基础有机化学(第三版),高等教育出版社,2005,06[5]梁丽华.消除消除反应的立体化学[J].山西师范大学,1997,11(02)[6]李辉. 对映选择性的溴代半频哪醇重排反应和Prins-Pinacol重排反应研究[D].甘肃:兰州大学有机合成,2013[7] Ferrier, R. J.; Prasad, N. J. Chem. Soc. (C) 1969, 570.[8] Tsuji, J. Organic Synthesis with Palladium Compounds, Springer-Veerlag, Berlin, 1980.[9]Tsuji, J. Palladium Reagents and Catalysts: Innovations in Organic Synthesis, Wiley, New York, 1995.[10] Heck, R. F. J. Am. Chem. Soc. 1968, 90, 5518.[11] Tamao, K.; Sumitani, K.; Kumada, M. J. Am Chem. Soc. 1972, 94, 4374.[12] Corriu, R. J. P.; Masse, J. P. J. Chem. Soc., Chem. Commun. 1972, 144.[13] Diederich, F.; Stang, P. J. Metal-Catalyzed Cross-Coupling Reactions,Wiley-VCH, Weinheim, 1998.[14] Tamao, K.; Hiyama, J.; Negishi, E. Special V olume of Thirty Years of the Cross-Coupling Reaction, J. Organomet. Chem. 2002, 653, pp. 1~160.[15]山本明夫,有机金属化学-基础与应用,陈惠麟,陆熙炎译,科学出版社,北京, 1997,p.361.[16] M ichael, A. J. Prakt. Chem. 1886, 35, 349.[17]刘耀宗.有机催化不对称Michael加成反应在手性吲哚-3-酮衍生物合成中的应用[D].甘肃:兰州大学有机化学,2012.。
