2019最新第三章 间歇反应器与理想反应器物理
合集下载
化学反应工程陈甘棠第三章课件

假设B间歇投料,A缓慢连续加料,则:
cB cB0
rAkcB0cA kcA
2019/9/23
对A进行物料衡算:
输入 = v0cA0
输出 = 0
积累 = dVR cA
dt
反应 = rAVRkcAVR
v0cA 0rAV RdV d R cA t
v0cA0kcA VRdV d RcA t
2019/9/23
第三节 全混流反应器
1 、物料衡算
输入 = v0cA0
积累 = 0
输出 = v0cA
A的反应量 = rAVR
v 0 c A 0 v 0 c A ( r A )V R 0
v0cA 0v0cArA V R
2019/9/23
VR
v0
cA0cA rA
例 3-1
用间歇反应器进行乙酸和乙醇的酯化反应,每天生 产乙酸乙酯12000kg,其化学反应式为:
k1
C3H CO O C2H H 5OH C3H CO2H O 5H C 2O k2
原料中反应组分的质量比为A:B:S=1:2:1.35, 反应液的 密度为1020kg/m3, 并假定在反应过程中不变,每批装 料,卸料及清洗等辅助操作时间为1h,反应在100℃ 下等温操作,其反应速率方程如下:
用直接迭代法或牛顿-拉夫森法求得满足上述关系的t值
2019/9/23
2.以生产费用最低为目标
AT
ata0t0aF VRCRMR
a 0 :辅助操作费用
a :单位时间内反应操作费用
a F :固定费用 AT :单位质量产品的总费用
2019/9/23
dA T dt
1
MRVR
acR
ata0t0
cB cB0
rAkcB0cA kcA
2019/9/23
对A进行物料衡算:
输入 = v0cA0
输出 = 0
积累 = dVR cA
dt
反应 = rAVRkcAVR
v0cA 0rAV RdV d R cA t
v0cA0kcA VRdV d RcA t
2019/9/23
第三节 全混流反应器
1 、物料衡算
输入 = v0cA0
积累 = 0
输出 = v0cA
A的反应量 = rAVR
v 0 c A 0 v 0 c A ( r A )V R 0
v0cA 0v0cArA V R
2019/9/23
VR
v0
cA0cA rA
例 3-1
用间歇反应器进行乙酸和乙醇的酯化反应,每天生 产乙酸乙酯12000kg,其化学反应式为:
k1
C3H CO O C2H H 5OH C3H CO2H O 5H C 2O k2
原料中反应组分的质量比为A:B:S=1:2:1.35, 反应液的 密度为1020kg/m3, 并假定在反应过程中不变,每批装 料,卸料及清洗等辅助操作时间为1h,反应在100℃ 下等温操作,其反应速率方程如下:
用直接迭代法或牛顿-拉夫森法求得满足上述关系的t值
2019/9/23
2.以生产费用最低为目标
AT
ata0t0aF VRCRMR
a 0 :辅助操作费用
a :单位时间内反应操作费用
a F :固定费用 AT :单位质量产品的总费用
2019/9/23
dA T dt
1
MRVR
acR
ata0t0
第三章理想间歇反应器与典型化学反应的基本特征

( − rA ) = k ′C A
反应转化为拟一级反应,从而遵守一级反应的规律,减 反应转化为拟一级反应,从而遵守一级反应的规律, 少了后期转化时间占总转化时间的分率。 少了后期转化时间占总转化时间的分率。
利用公式,解决反应时间、转化率,残余浓度之间的 关系的例题应用例题
蔗糖在稀水溶液中水解生成葡萄糖和果糖的, A(蔗糖)+B(水)→P(葡萄糖)+S(果糖) H当水大量时反应准寻一级反应动力学即 ( − rA )V = kcA , 当催化剂HCl浓度为0.01mol·L-1,反应温度为48℃时,反应的 速率常数为k=0.0193min-1。当蔗糖溶度为0.1mol·L-1和 0.5mol·L-1时计算: ⑴反应20min后,上述两初始浓度下的蔗糖、葡萄糖和果糖 的浓度分别为多少? ⑵计算两初始浓度下的蔗糖转化率? ⑶若蔗糖浓度降低到0.01mol·L-1,两种初始浓度下所需的反 应时间各位多少?
CA
代入数据求解:t1=0.0193-1ln0.1/0.01=120 t2=0.0193-1ln0.5/0.01=203 一般的解题方法是根据问题,找出应用公式,求出公 式中的已知项和未知项,应用化学计量关系和数学 公式导出未知项后,就可以代入公式求解了。
自催化反应
自催化反应的产物有催化剂的作用,一般自催化 反应式表示为
1 1 − xA 1 xA 2级反应 kt = 级反应: 级反应 cA0 1 − xA
1级反应 kt = ln 级反应: 级反应
,与cA0 无关 t ,与cA0 成反比 t
利用上述的反应特性,可以定性判别反应级数, 利用上述的反应特性,可以定性判别反应级数,例如确 的关系,判别反应级数 判别反应级数。 定 xA,然后测定 t与cA0 的关系 判别反应级数 然后测定
第3章理想间歇反应器与典型化学反应的基本特征
反应级数大于1的反应,后期的速度很小,高转化率或低残 余浓度的要求会使反应所需时间大幅度地增长。
例:试对一级和二级反应分别计算转化率 从90%提高到99%时,转化所需的时间是 其转化率为90%时所需时间的倍数。
解:(1)对一级反应
t 1 ln 1 k 1 x
t99%
1 k
ln 1 1 99%
反应器设计的基本内容
选择合适的反应器型式
反应动力学特性+反应器的流动特征+传递特 性
确定最佳的工艺条件
最大反应效果+反应器的操作稳定性
进口物料的配比、流量、反应温度、压力和最终转化率
计算所需反应器体积
规定任务+反应器结构和尺寸的优化
反应器设计的基本内容
操作型的计算:根据反应特征及反应器的体积,
决定最优化操作条件,使反应过程达到优化目标。 已知反应器的体积,求反应在该反应器内反应所 能达到的转化率?
(rA ) (rA )
k dnA
Vdt
k
dc cA
cA,0
A
k
t
dt
0
t
cA,0 cA k
cA,0 xA k
间歇反应器中的简单反应
反应速率
t CA dCA
CA0 (rA )
t CA0
xAf 0
dxA (rA )
(-rA)=k kt CA0 CA
解:由题条件: rA kCA2
t
CA0
xA 0
dxA rA
CA0
xA 0
dxA kCA20 1 xA
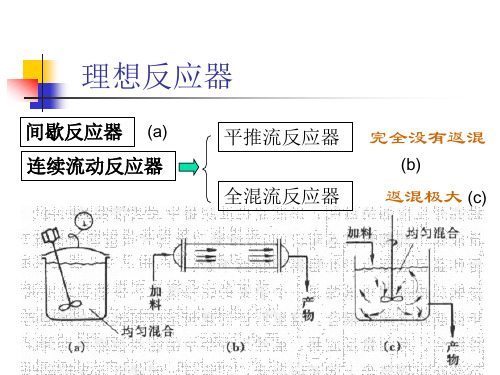
理想反应器
间歇反应器 (a) 连续流动反应器
平推流反应器 全混流反应器
完全没有返混
第三章 理想反应器

VR = V( t + t0 ) 而反应器的实际体积为
(3.3-6)
Vt = VR / f
(3.3-7)
式中f为填充系数或装料系数,是一个根据经验确定的参数,一般为0.4~0.85, 对不起泡不沸腾物料取0.7~0.85,对易起泡沸腾物料取0.4~0.6。
二、平推流反应器(PFR)反应体积的计算
单位时间A流入微元体的量为: V0CA0 (1 - x A ) 单位时间A流出微元体的量为: V0CA0(1 - xA - dxA ) 单位时间A在微元体内的反应量为: rA d V R 则定态下A的物料衡算式为:
∫ V R
= -V0
dC CAf
A
r CA0
A
dx A
=
-
dC A CA0
(3.3-12)
∫ ∫ τ
= CA0
dx xAf
A
0 rA
=-
dC CAf
A
r CA0
A
(3.3-13)
将式(3.3 -13)与间歇反应器反应时间的积分式 (3.3-5)比较,可以看出:
对恒容过程,为达到相同转化率,在间歇反应器中所需的反应时 间与在PFR中所需的接触时间相同。
第三章 理想反应器
本章讨论的主要内容: 1. 论述反应器内的流动模型,着重阐述混合与返混的异同
及理想流动模型的特征; 2. 以均相反应为背景,讨论理想反应器设计的基本方法; 3. 讨论理想流动反应器中复合反应的收率和选择率。
§3.1 概述
流动模型 是描述流体流经反应器时物料质点的流动与返混状况的模型,对各
2. 全混流模型
特征:
1)反应器内所有空间位置的温度、浓度、反应 速率等参数都相同,且等于出口处相应的值;
(3.3-6)
Vt = VR / f
(3.3-7)
式中f为填充系数或装料系数,是一个根据经验确定的参数,一般为0.4~0.85, 对不起泡不沸腾物料取0.7~0.85,对易起泡沸腾物料取0.4~0.6。
二、平推流反应器(PFR)反应体积的计算
单位时间A流入微元体的量为: V0CA0 (1 - x A ) 单位时间A流出微元体的量为: V0CA0(1 - xA - dxA ) 单位时间A在微元体内的反应量为: rA d V R 则定态下A的物料衡算式为:
∫ V R
= -V0
dC CAf
A
r CA0
A
dx A
=
-
dC A CA0
(3.3-12)
∫ ∫ τ
= CA0
dx xAf
A
0 rA
=-
dC CAf
A
r CA0
A
(3.3-13)
将式(3.3 -13)与间歇反应器反应时间的积分式 (3.3-5)比较,可以看出:
对恒容过程,为达到相同转化率,在间歇反应器中所需的反应时 间与在PFR中所需的接触时间相同。
第三章 理想反应器
本章讨论的主要内容: 1. 论述反应器内的流动模型,着重阐述混合与返混的异同
及理想流动模型的特征; 2. 以均相反应为背景,讨论理想反应器设计的基本方法; 3. 讨论理想流动反应器中复合反应的收率和选择率。
§3.1 概述
流动模型 是描述流体流经反应器时物料质点的流动与返混状况的模型,对各
2. 全混流模型
特征:
1)反应器内所有空间位置的温度、浓度、反应 速率等参数都相同,且等于出口处相应的值;
化学反应工程第三章

m 1c A0 c A 1 ln m x A 1 ln m 1 mc A m 1 m1 x A
m m xA ln m 1 m1 x A
cB 0 k t
3.3 反应温度
3.2 理想连续流动反应器(1)
一 平推流反应器
1.1. 平推流反应器的特点 流体在管内作平推流流动具有如下特征: (1) 在与流动方向呈垂直的截面上没有流速分布; (2) 而在流体流动的方向不存流体质点间的混合,即无返混现象; (3) 离开平推流反应器的所有流体质点均具有相同的平均停留时间, 而这个停留时间就等于反应时间。
k1 cQ k 2
cp
3.1.2 间歇反应器内复合反应的计算(4)
二 连串反应 等温间歇反应器进行一级不可逆连串反应
K1 K2 A P Q
dcA k1c A dt dc p k1c A k 2 cP dt
t 0, c A c A0 , cP 0, cQ 0, 积分第一式: c A c A0 e k1t 或 t 1 c A0 1 1 ln ln k1 c A k1 1 x A
B
A
O
D
E
t
间歇反应器最优化反应时间
3.1.3 间歇反应器优化操作(3)
(2) 以生产费用为目标
AT
at a0t0 a f VR cR
dcR ac at a t a 0 0 f R dt dA dcR cR 当 T =0, dt dt t a0t0 a f / a dAT 2 dt VR cR
产物P的浓度先增大,在降低,存在极大值。可对cp对时间求导, 得最优化时间
topt ln k1 / k 2 k1 k 2
工学第三章间歇反应器与理想反应器

代表反应器处理物料的能力
变小,处理能力变大
对于均相反应:
空
速
1 空时
(体积空速)
空速的意义:单位时间单位反应体积所处理的物料量。
空速越大,反应器的原料处理能力越大。
设计方程的应用
Vr cA0 cA cA0 X A
Q0
rA
rA
已知rA,可求得不同空时下的组成 已知rA,可求得不同转化率下的空时
dH2 HrrAVrdt (单一反应)
dH H1 dH2 H3
mt为反应物系的质量
mt c pt dT Hr rAVr dt cpt为反应物系的比热容
c pt为温度 T Tr间的平均比热容
变温间歇操作的热量衡算
又:dq UAh (TC T)dt
dT mt c pt dt UAh (Tc T ) HrVrrA
3.3 理想流动下的釜式反应器
• 连续搅拌槽式反应器,简 称 CSTR。流入反应器的 物料,在瞬间与反应器内 的物料混合均匀,即在反 应器中各处物料的温度、 浓度都是相同的。
• 全混流反应器,简称MFR。
3.3.1 全混流模型
基本假定: 反应器中的物料,包括刚进入的物料,都能立即 完全均匀地混合,即混合程度达到最大。
图解分析
正常动力学
A
1 rA
F
0
B
E
H X A1 XA
D
单釜
Vr
Q0cA0 X A2 rA ( X A2 )
K
X A2
两釜串联
Vr
Q0cA0 X A1 rA ( X A1)
对关键组分A有:
Vr
Q0cA0 X Af (k1 k2 )cA
对目的产物P有:
第三章 间歇反应器
( H ) N A0 1 T T0 = ( x A x A0 ) = ( x A x A0 ) mt c p λ
传热系数U由下式定义: 传热系数 由下式定义: 由下式定义
1 1 d Ak 1 Ak = + + U ak λ Am ar Ar
式中: αk、αr——分别为反应混合物一侧和热载体一侧 的给热系数,kcal/㎡hr℃; Ak、 Ar——分别为反应混合物一侧和热载体一侧的传 热面,㎡; Am——Ak和Ar的对数平均值; λ——器壁导热系数,kcal/mhr℃; d——壁厚,m。
(T ) ad (62.8 × 103 kJ/kmol)(0.156kg/kg)(227kg) = (227kg)(2.51kJ/kg K)(60kg/kmol)
= -65 K
T = 613 65xA
这一吸热反应,绝热操作将导致温度的激剧下降,因 这一吸热反应,绝热操作将导致温度的激剧下降, 此必须考虑加热。 此必须考虑加热。
N p NA (1 x A ) 1 xA = p t A0 = p A0 ( t ) Nt N t 0 (1 + ε A x A ) 1 + ε A x A pt 0
p A = pt
级反应为例, 以n级反应为例, 级反应为例
(1 + ε A x A ) θ= n 1 ∫x n A0 (1 x A ) kC A0 1
NS = NS0 + s N A0 x A0 a
N i = N i 0 (惰性组分) q + s a bL N t = N t 0 + N A0 xA a
总的摩尔数为 : N t = N t 0 + N A0δ A x A 由此得: 由此得:
Nt = 1 + ( y A0δ A ) x A ≡ 1 + ε A x A N t0
传热系数U由下式定义: 传热系数 由下式定义: 由下式定义
1 1 d Ak 1 Ak = + + U ak λ Am ar Ar
式中: αk、αr——分别为反应混合物一侧和热载体一侧 的给热系数,kcal/㎡hr℃; Ak、 Ar——分别为反应混合物一侧和热载体一侧的传 热面,㎡; Am——Ak和Ar的对数平均值; λ——器壁导热系数,kcal/mhr℃; d——壁厚,m。
(T ) ad (62.8 × 103 kJ/kmol)(0.156kg/kg)(227kg) = (227kg)(2.51kJ/kg K)(60kg/kmol)
= -65 K
T = 613 65xA
这一吸热反应,绝热操作将导致温度的激剧下降,因 这一吸热反应,绝热操作将导致温度的激剧下降, 此必须考虑加热。 此必须考虑加热。
N p NA (1 x A ) 1 xA = p t A0 = p A0 ( t ) Nt N t 0 (1 + ε A x A ) 1 + ε A x A pt 0
p A = pt
级反应为例, 以n级反应为例, 级反应为例
(1 + ε A x A ) θ= n 1 ∫x n A0 (1 x A ) kC A0 1
NS = NS0 + s N A0 x A0 a
N i = N i 0 (惰性组分) q + s a bL N t = N t 0 + N A0 xA a
总的摩尔数为 : N t = N t 0 + N A0δ A x A 由此得: 由此得:
Nt = 1 + ( y A0δ A ) x A ≡ 1 + ε A x A N t0
化学反应工程第三章
反应级数 反应速率
残余浓度式
转化率式
n=0
n=1
n=2 n级 n≠1
rA k
rA kCA
rA
kC
2 A
kt CA0 CA
kt CA0 xA
CA CA0 kt
xA
kt CA0
kt ln CA0 CA
CA CA0ekt
kt ln 1 1 xA
xA 1 ekt
kt 1 1
kt 1 xA
VR
V0CA0 xAf (rA ) f
式中 (rA) f 指按出口浓度计算的反应速率。
N A,CAf X Af
, 若 xA0 0 则物料衡算方程为:
[A流入量]-[A流出量]-[ A反应量]=累积量
NA '
NA
(rA ) f VR
0
N A ' N A0 (1 xA0 ) N A N A0 (1 xAf )
2级反应:CA
CA0 1 CA0kt
CA 随 t 缓慢下降。
对于一级或二级不可逆反应,在反应后期,CA的下降 速率,即xA的上升速率相当缓慢。若追求过低的残余 浓度,即过高的转化率,则在反应后期要花费大量的
反应时间。(见书上例3-1)
例 3-1 在间歇反应器中进行等温二级反应
A→B
反应速率
r
0.01C
应器中达到x=0.99,需要反应时间为10min,问:
(1)在全混流反应器中进行时, 应为多少?
(2)在两个串联全混流反应器中进行时, 又为多少?
第四节 多级全混流反应器的串联及优化
设有一反应,A的初始浓度为CA0,反应结束后最终浓度为 CAf,反应的平衡浓度为CA*,考察平推流反应器和全混流反应器 的浓度推动力。
间歇式反应器(专业教育)
转化率反映出原料通过反应器后产生化学变化的程度, 转化率增大说明产生化学变化的原料在总投料量中所占比例 增大。
②产率:一般是指单程收率。是指主产物的实际收得量与按 投入原料计算的理论产量之比值。用百分率或分率表示,并 用符号η表示产率。
目的产物实际得量
按投入原料计算的理论产量 100%
特备参考
23
特备参考
17
锅式反应器的特点及应用 1、特点:结构简单、加工方便、传质效率好、温度分布
均匀、便于控制和改变反应条件、操作上灵活性较大,适合 于多品种、小批量生产。
2、应用:
从反应物料看:它能够适应于各种不同相态组合的反 应物料。如:均液相、非均液相、液—固相、气—液相等
从反应类型看:它几乎适用于所有有机合成的单元操作。 如:氧化、还原、硝化、磺化、卤化、缩合、聚合、烷化、 酰化、重氮化、偶合等。
特备参考
8
②直接传热
特点:反应物直接与传热剂接触图 适用场合:反应物允许接触传热剂,要求快速升 温或降温。 控制温度的方法:传热剂的用量及温度。 如:直接蒸汽加热、直接加水冷却等。
特备参考
9
③蒸发传热
特点:靠蒸发性反应物或反应介质(如溶剂) 的蒸发移除热量。
适用场合:在沸腾下进行的化学反应。 控制温度的方法:沸点温度、气相压力。 如:通过回流冷凝器除热。
特备参考
14
4.间歇式反应器的类型
从几何形式上看:常用锅式(釜式)反应器,也有用管 式和塔式反应器的。
从所处理物料的相态上来看,有:
均 相 反 应 器 : 物 料 为 气相 或 均 液 相
对 反 应 器 要 求 较 低 , 一般 用 管 式 或 塔 式 反 应 器
液 相 物 料 有 时 还 装 搅 拌器 , 以 提 高 物 料 扩 散 和
化学反应工程原理-副本第三章 理想间歇反应器
第三章 理想间歇反应器1 理想间歇反应器的特征: ,因此理想间歇反应器的反应结果将 。
2 在BR 反应器中,反应物料达到一定转化率所需要的反应时间,只取决于 ,而与 无关。
反应器的大小只取决于 。
3 在BR 反应器中的简单反应的反应特性:(1)达到相同的转化率或残余浓度,k 值提高,都将减少 ,与 无关;(2)达到一定的转化率, 反应时间与初始浓度无关, 反应时间与初始浓度成反比, 反应时间与初始浓度成正比。
因此,对于一级反应和二级反应, 反应物初始浓度将 生产能力。
(3)反应级数越高,要求的残余浓度越低,反应时间 ;对于二级反应,提高转化率将大幅增加 。
4 自催化反应是 。
自催化反应的反应速率最大的C A 值为( 。
5 BR 反应器中的最优反应时间的条件是: ,单位时间产物生成量 。
6 简述反应器设计的步骤?7 简述可逆反应的重要特点、反应的浓度效应和温度效应?11.如果平行反应均为一级不可逆反应,若>,提高选择性应_______。
A. 提高浓度B. 提高温度C. 降低浓度D. 降低温度12. 如果平行反应均为一级不可逆反应,若>,提高收率应_______。
A. 提高浓度B. 降低浓度C. 提高温度D. 降低温度13 BR 反应器中的简单反应计算题:13.1 反应A B 为n 级不可逆反应。
已知在300K 时要使A 的转化率达到20%需要12.6分钟,而在304K 时达到同样的转化率仅需要3.20分钟,求该反应的活化能。
AP(主)S(副)主E 副E P S AP(主)S(副)主E 副E P。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
反应物料一次投入反应器内, 在反应过程中不再向反应器内 投料,也不向外排出,待反应 达到要求的转化率后,再全部 放出反应物料。反应器内的物 料在搅拌的作用下其参数(温 度及浓度)各处均一。
间歇反应器的特点:
①反应器内有效空间中各位置的物料温度、浓度都相同; ②所有物料在反应器中停留时间相同,不存在不同停留时间物料的 混合,即无返混现象; ③出料组成与反应器内物料的最终组成相同; ④为间歇操作,有辅助生产时间。一个生产周期应包括反应时间、 加料时间、出料时间、清洗时间、加热(或冷却)时间等。
0 0 rAVr
dnA dt
mol s1
整理得
rAVr
nA0
dxA dt
mol s1
当进口转化率为0时,分离变量并积分得
t
t
0 dt nA0
xA dxA 0 rAVr
为间歇反应器设计计算的通式。它表达了
在一定操作条件下,为达到所要求的转化
率xA所需的反应时间t。
①计算反应时间t;
tr
cA0
xA 0
dxA rA
②计算一批料所需时间tt;
tt=t+t’
t’为辅助生产时间
③计算每批投放物料总量F’A; F’A=FAtt
④计算反应器有效容积V’R;
Vr
FA CA0
或 Vr Q0 t t
⑤计算反应器总体积V。反应器总体积应包括有
效容积、分离空间、辅助部件占有体积。通常 有效容积占总体积分率为40%-85%,该分率 称为反应器装填系数f,由生产实际决定。
第三章 间歇反应器及理想流动反应器
3.1 概述
反应器的操作
间歇操作:不存在流动问题,物料浓度随时间变化。
连续操作: 存在流动问题 稳态流动:
稳态流动 非稳态流动
物料在同一空间位置各质点的流量、浓度和 温度等不随时间而变。
反应器的数学模型: 宏观模型:反应器内的浓度、温度等不随空间位置而变。 微观模型:反应器内的浓度、温度等随空间位置而变。
模型通常含有微分变量。
反应器设计的基础方程:“三传一反”
本征动力学:均相反应器 “一反”:反应动力学
宏观动力学: 非均相反应器
“三传”:质量传递、热量传递、动量传递
物料衡算方程(质量平衡)
物料衡算所针对的具体体系称体积元。 体积元有确定的边界,由这些边界围住的体积称为系统体积。 在这个体积元中,物料温度、浓度必须是均匀的。 在满足这个条件的前提下尽可能使这个体积元体积更大。 在这个体积元中对关键组分A进行物料衡算。
3.2.1 等温间歇反应器的设计计算
反应器有效容积中物料温度、浓度相同,故
选择整个有效容积Vr作为衡算体系。在单位时间
内,对组分A作物料衡算:
单位时间进入Vr 的物料A的量
单位时间排出Vr 的物料A的量
单位时间Vr内反应 消失的物料A的量
单位时间内Vr中 物料A的积累量
达到一定转化率所需的反应时间与反应器 大小无关,只取决于动力学因素。
温度越高,速率常数 k 越大,则达到相同 转化率所需的反应时间 t 越短。
区别
t 与cA0无关
t 与cA0有关
复合反应——平行反应 对各组分作物料衡算(恒容条件):
A k1 P rP k1cA A k2 Q rQ k2cA
对A作物 料衡算:
dcA dt
k1cA
cA
c ek1t A0
对P作物 料衡算:
dcP dt
k1cA
k2cP
cP
k1cA0 k1 k2
(ek2t
ek1t )
cQ cA0 (cA cP )
cQ
cA0[1
k2ek1t k1
k1ek2t k2
]
dcP 令: dt
Fin Fout Fr Fb
热量衡算方程(热量平衡)
单位时间随物料 单位时间随物料 单位时间内体积
流入体积元的热 流出体积元的热 元与周围环境交
量QinkJ s1
量QoutkJ s1 换的热量QukJ s1
nA0
dX A dt
rAVr
等温反应 UAh (Tc T ) H rVr rA
讨论
绝热反应
T
T0
nA0 (H r mt c pt
)
X
A
总结:通过热量衡算,找出T与XA的关系,代入设计基本方程积分, 即得反应时间t。
3.3 理想流动下的釜式反应器
• 连续搅拌槽式反应器,简 称 CSTR。流入反应器的 物料,在瞬间与反应器内 的物料混合均匀,即在反 应器中各处物料的温度、 浓度都是相同的。
0
得:
topt
n(k1 / k2 ) k1 k2
问题:假设k1=k2,topt=?
设计计算过程
对于给定的生产任务,即单位时间处理的 原料量FA[kmol·h-1]以及原料组成CA0[kmol·m-3]、 达到的产品要求xAf及辅助生产时间t’、动力 学方程等,均作为给定的条件,设计计算 出间歇反应器的体积。
dH2
根据热力学第一定律,反应器的热量衡算为:
q U 即:与环境交换的热=内能的变化
用焓变代替内能的变化
q H
间歇釜式反应器
dq dH
Tr为计算的基准温度
变温间歇操作的热量衡算
A B T C
H1 mt
Tr T
cpt dT
mt c pt (Tr
T)
H1
Vr
Q0cp , k1cA
设c p 0
0
对副产物Q有:
Vr
Q0cQ , k2cA
设cQ0
0
三式中有两式独立,可解Vr、XA、YP三者关系
复合反应-连串反应
A k1 P k2 Q
对关键组分A有
Vr
Q0cA0 X Af k1cA
对中间产物P:
Vr
Q0cp , k1cA k2cp
在恒容条件下, 上式可简化为:
cA cA0 1 xA
t
cA0
xA r cA0 A
间歇反应器内为达到一定转化率所需反应
时间 t,只是动力学方程式的直接积分,
与反应器大小及物料投入量无关。
1.反应体积
等温 BR 的计算
Vr Q0 (t t')
• 全混流反应器,简称MFR。
3.3.1 全混流模型
基本假定: 反应器中的物料,包括刚进入的物料,都能立即 完全均匀地混合,即混合程度达到最大。
全混流反应器的特性
①物料在反应器内充分返混; ②反应器内各处物料参数均一; ③反应器的出口组成与器内物料组成相同; ④连续、稳定流动,是一定态过程。
3.3.2 等温连续流动釜式反应器的设计计算
设c p 0
0
对最终产物Q:
Vr
Q0cQ , k2cP
设cQ0
0
三式中有两式独立,可解Vr、XA、YP三者关系
例: 对于一级不可逆串联反应:
c 求 p max
A k1 P k2 S
rA k1cA
rp k1cA k2cp
rs k2cp
对于着眼组分A有:
t 为反应时间:装料完毕开始反应算起到达到
操
一定转化率时所经历的时间。计算关键
作 时
t’ 为辅助时间:装料、卸料、清洗所需时间之和。 间
经验给定
2.反应器的体积 V Vr f
f : 装填系数,0.4-0.85 。一般由实验确定,也可根据反应物料
的性质不同而选择。 对于不起泡或不沸腾的液体,可取0.7-0.85 对于沸腾或起泡沫的液体物料,可取0.4-0.6
• 全混釜中各处物料均一,故选整个反应器 有效容积Vr为物料衡算体系,对组分A作物 料衡算。
输入的量=输出的量+反应消耗掉的量+累积量
FA0 FAf rAfVr FA0 FA0(1 X Af ) rAfVr
• 整理得到:
FA0 X Af rAfVr
Vr X Af FA0 rAf
Vr
Q0cA0 X Af rA ( X Af )
Vr Q0
cA0 X Af rA ( X Af )
复合反应-平行反应
A k1 P rP k1cA A k2 Q rQ k2cA
对关键组分A有:
Vr
Q0cA0 X Af (k1 k2 )cA
对目的产物P有:
V Vr f
3.2 变温间歇釜式反应器
间歇釜式反应器做到等温操作很困 难,当热效应小时,近似等温可以办到, 如果热效应大时,很难做到;
温度会影响到
X
A
,
Y p
,
r
和反应器的
生产强度等,很多时候变温的效果更好
变温间歇操作的热量衡算
A B T C
H1
H3
A B Tr C
1 e[(k1 k2 )t]
cQ
k 2 c A0 k1 k2
1 e[(k1k2 )t]
A P rP k1cA A Q rQ k2cA
t 1 n cA0 k1 k2 cA
设 t 0时,cA cA0,cP 0,cQ 0
cA0
A
c
AP AQ
c pt为温度 T Tr间的平均比热容
变温间歇操作的热量衡算
又:dq UAh (TC T )dt
间歇反应器的特点:
①反应器内有效空间中各位置的物料温度、浓度都相同; ②所有物料在反应器中停留时间相同,不存在不同停留时间物料的 混合,即无返混现象; ③出料组成与反应器内物料的最终组成相同; ④为间歇操作,有辅助生产时间。一个生产周期应包括反应时间、 加料时间、出料时间、清洗时间、加热(或冷却)时间等。
0 0 rAVr
dnA dt
mol s1
整理得
rAVr
nA0
dxA dt
mol s1
当进口转化率为0时,分离变量并积分得
t
t
0 dt nA0
xA dxA 0 rAVr
为间歇反应器设计计算的通式。它表达了
在一定操作条件下,为达到所要求的转化
率xA所需的反应时间t。
①计算反应时间t;
tr
cA0
xA 0
dxA rA
②计算一批料所需时间tt;
tt=t+t’
t’为辅助生产时间
③计算每批投放物料总量F’A; F’A=FAtt
④计算反应器有效容积V’R;
Vr
FA CA0
或 Vr Q0 t t
⑤计算反应器总体积V。反应器总体积应包括有
效容积、分离空间、辅助部件占有体积。通常 有效容积占总体积分率为40%-85%,该分率 称为反应器装填系数f,由生产实际决定。
第三章 间歇反应器及理想流动反应器
3.1 概述
反应器的操作
间歇操作:不存在流动问题,物料浓度随时间变化。
连续操作: 存在流动问题 稳态流动:
稳态流动 非稳态流动
物料在同一空间位置各质点的流量、浓度和 温度等不随时间而变。
反应器的数学模型: 宏观模型:反应器内的浓度、温度等不随空间位置而变。 微观模型:反应器内的浓度、温度等随空间位置而变。
模型通常含有微分变量。
反应器设计的基础方程:“三传一反”
本征动力学:均相反应器 “一反”:反应动力学
宏观动力学: 非均相反应器
“三传”:质量传递、热量传递、动量传递
物料衡算方程(质量平衡)
物料衡算所针对的具体体系称体积元。 体积元有确定的边界,由这些边界围住的体积称为系统体积。 在这个体积元中,物料温度、浓度必须是均匀的。 在满足这个条件的前提下尽可能使这个体积元体积更大。 在这个体积元中对关键组分A进行物料衡算。
3.2.1 等温间歇反应器的设计计算
反应器有效容积中物料温度、浓度相同,故
选择整个有效容积Vr作为衡算体系。在单位时间
内,对组分A作物料衡算:
单位时间进入Vr 的物料A的量
单位时间排出Vr 的物料A的量
单位时间Vr内反应 消失的物料A的量
单位时间内Vr中 物料A的积累量
达到一定转化率所需的反应时间与反应器 大小无关,只取决于动力学因素。
温度越高,速率常数 k 越大,则达到相同 转化率所需的反应时间 t 越短。
区别
t 与cA0无关
t 与cA0有关
复合反应——平行反应 对各组分作物料衡算(恒容条件):
A k1 P rP k1cA A k2 Q rQ k2cA
对A作物 料衡算:
dcA dt
k1cA
cA
c ek1t A0
对P作物 料衡算:
dcP dt
k1cA
k2cP
cP
k1cA0 k1 k2
(ek2t
ek1t )
cQ cA0 (cA cP )
cQ
cA0[1
k2ek1t k1
k1ek2t k2
]
dcP 令: dt
Fin Fout Fr Fb
热量衡算方程(热量平衡)
单位时间随物料 单位时间随物料 单位时间内体积
流入体积元的热 流出体积元的热 元与周围环境交
量QinkJ s1
量QoutkJ s1 换的热量QukJ s1
nA0
dX A dt
rAVr
等温反应 UAh (Tc T ) H rVr rA
讨论
绝热反应
T
T0
nA0 (H r mt c pt
)
X
A
总结:通过热量衡算,找出T与XA的关系,代入设计基本方程积分, 即得反应时间t。
3.3 理想流动下的釜式反应器
• 连续搅拌槽式反应器,简 称 CSTR。流入反应器的 物料,在瞬间与反应器内 的物料混合均匀,即在反 应器中各处物料的温度、 浓度都是相同的。
0
得:
topt
n(k1 / k2 ) k1 k2
问题:假设k1=k2,topt=?
设计计算过程
对于给定的生产任务,即单位时间处理的 原料量FA[kmol·h-1]以及原料组成CA0[kmol·m-3]、 达到的产品要求xAf及辅助生产时间t’、动力 学方程等,均作为给定的条件,设计计算 出间歇反应器的体积。
dH2
根据热力学第一定律,反应器的热量衡算为:
q U 即:与环境交换的热=内能的变化
用焓变代替内能的变化
q H
间歇釜式反应器
dq dH
Tr为计算的基准温度
变温间歇操作的热量衡算
A B T C
H1 mt
Tr T
cpt dT
mt c pt (Tr
T)
H1
Vr
Q0cp , k1cA
设c p 0
0
对副产物Q有:
Vr
Q0cQ , k2cA
设cQ0
0
三式中有两式独立,可解Vr、XA、YP三者关系
复合反应-连串反应
A k1 P k2 Q
对关键组分A有
Vr
Q0cA0 X Af k1cA
对中间产物P:
Vr
Q0cp , k1cA k2cp
在恒容条件下, 上式可简化为:
cA cA0 1 xA
t
cA0
xA r cA0 A
间歇反应器内为达到一定转化率所需反应
时间 t,只是动力学方程式的直接积分,
与反应器大小及物料投入量无关。
1.反应体积
等温 BR 的计算
Vr Q0 (t t')
• 全混流反应器,简称MFR。
3.3.1 全混流模型
基本假定: 反应器中的物料,包括刚进入的物料,都能立即 完全均匀地混合,即混合程度达到最大。
全混流反应器的特性
①物料在反应器内充分返混; ②反应器内各处物料参数均一; ③反应器的出口组成与器内物料组成相同; ④连续、稳定流动,是一定态过程。
3.3.2 等温连续流动釜式反应器的设计计算
设c p 0
0
对最终产物Q:
Vr
Q0cQ , k2cP
设cQ0
0
三式中有两式独立,可解Vr、XA、YP三者关系
例: 对于一级不可逆串联反应:
c 求 p max
A k1 P k2 S
rA k1cA
rp k1cA k2cp
rs k2cp
对于着眼组分A有:
t 为反应时间:装料完毕开始反应算起到达到
操
一定转化率时所经历的时间。计算关键
作 时
t’ 为辅助时间:装料、卸料、清洗所需时间之和。 间
经验给定
2.反应器的体积 V Vr f
f : 装填系数,0.4-0.85 。一般由实验确定,也可根据反应物料
的性质不同而选择。 对于不起泡或不沸腾的液体,可取0.7-0.85 对于沸腾或起泡沫的液体物料,可取0.4-0.6
• 全混釜中各处物料均一,故选整个反应器 有效容积Vr为物料衡算体系,对组分A作物 料衡算。
输入的量=输出的量+反应消耗掉的量+累积量
FA0 FAf rAfVr FA0 FA0(1 X Af ) rAfVr
• 整理得到:
FA0 X Af rAfVr
Vr X Af FA0 rAf
Vr
Q0cA0 X Af rA ( X Af )
Vr Q0
cA0 X Af rA ( X Af )
复合反应-平行反应
A k1 P rP k1cA A k2 Q rQ k2cA
对关键组分A有:
Vr
Q0cA0 X Af (k1 k2 )cA
对目的产物P有:
V Vr f
3.2 变温间歇釜式反应器
间歇釜式反应器做到等温操作很困 难,当热效应小时,近似等温可以办到, 如果热效应大时,很难做到;
温度会影响到
X
A
,
Y p
,
r
和反应器的
生产强度等,很多时候变温的效果更好
变温间歇操作的热量衡算
A B T C
H1
H3
A B Tr C
1 e[(k1 k2 )t]
cQ
k 2 c A0 k1 k2
1 e[(k1k2 )t]
A P rP k1cA A Q rQ k2cA
t 1 n cA0 k1 k2 cA
设 t 0时,cA cA0,cP 0,cQ 0
cA0
A
c
AP AQ
c pt为温度 T Tr间的平均比热容
变温间歇操作的热量衡算
又:dq UAh (TC T )dt
