新霉素液相检测(英国药典)
HPLC法测定复方硫酸新霉素滴眼液中肌苷的含量

r a n g e o f i n o s i n ew a s 0 . 2 2 3 2~ 0 . 6 6 9 4 g ( r =1 . 0 0 00) , t h e a v e r a g e r e c o v e r yw a s 1 0 0 . 4 % a n dt h e R S Dw a s 0 . 4 %. C o n -
( 4 . 6 m m x 2 5 0 m m, 5
在0 . 2 2 3 2~ 0 . 6 6 9 4 g范 围内, 线性 关 系良好( r =1 . 0 0 0 0 ) , 平均 回收率为 1 0 0 . 3 %, R S D为 0 . 4 % 。结论 便、 快速 、 重复性 好 , 可用于复方硫 酸新霉素滴 眼液 中肌苷 的质量控制。 关键 词 : 复方硫 酸新霉素滴眼液 ; 肌苷; 含量测 定; 高效液相 色谱 法 中图分类号 : R 9 2 7 . 2 文献标识码 : A 文章编号 : 2 0 9 5— 5 3 7 5( 2 0 1 3) 0 4— 0 2 1 3— 0 0 2
药学研究 ・  ̄u m a l o f P h a r m a c e u t i c a l Re s e a r c h 2 0 1 3 V o 1 . 3 2 , No . 4
HP L C法 测定 复 Байду номын сангаас硫 酸 新 霉 素滴 眼液 中肌 苷 的含量
吕光宇 , 吕立华 , 刘凤琴 , 李 秀珍 , 李 文
D r o p s . Me t h o d s G e n i p o s i d e w a s s e p a r a t e d o n X D B—C l 8 ( 4 . 6 m m x 2 5 0 mm, 5 I x m) c o l u mn , t h e m o b i l e p h a s e w a s me t h —
高效液相色谱法同时测定复方硫酸新霉素滴眼液中3种成分含量

•检验检测•/nspectos and Tesi221年5月20日 第3卷第10期VU 30, No. 17, May 27, 2721China PharmaceuticalsdU : D. 3969/j. imn. 1006 -4930 2020 10. 017高效液相色谱法同时测定复方硫酸新霉素滴眼液中3种成分含量赵猛,李玲(江苏省连云港市食品药品检验检测中心,江苏 连云港222000 )摘要:目的 建立同时测定复方硫酸新霉素滴眼液中肌苷、羟苯乙酯和地塞米松磷酸钠含量的高效液相色谱法。
方法 色谱柱为 Phenomenox Gemini C15柱(190 mm x 4. 6 mm , 5 im ),流动相为1%三乙胺溶液(用磷酸调pH 至3.0)-甲醇(梯度洗脱),流速为0 0 mL/min,检测波长为245 nm,柱温为25 C ,进样量为50 iL 结果 肌苷、羟苯乙酯和地塞米松磷酸钠进样量在2. 525〜7. 577 ig 、 0 055 ~31 120 ia 、2.510〜7.535 ig 范围內与峰面积线性关系良好(o > 0. 999 0),精密度、稳定性、重复性试验的RSD 均小于2.0% (p=6),平均加样回收率分别为98.80% ,99.59% ,98.33% , RSD 分别为0. 84% ,0 46% ,0 23% (p=6)。
结论 该方法简单、准确、稳定,可用于同时测定复方硫酸新霉素滴眼液中肌苷、羟苯乙酯和地塞米松磷酸钠3种成分的含量。
关键词:高效液相色谱法;复方硫酸新霉素滴眼液;肌苷;羟苯乙酯;地塞米松磷酸钠;含量测定中图分类号:R927, 2; R98& 1 文献标志码:A 文章编号:1006 - 4931 (2021)10 - 0065 - 03Simultanevue Determination of Three Constituente in Compound Nevmycin SulfateEye D ops by HPLCZHAO Meng , LA Ling(Liaoyungang Agt/utc for Ffd anO Drug Cggrcd ,Liaoyyngang , Jiangsu , China 222000)Abstract : Objective To estabUsh a high - pe/ormapce Uquid chromatoyranPy (HPLC ) methop for simu/aneons determination of inosine,ethylparabeU and d examethasone sofium pPospPato in Componud Neomycin Sulfate Eye Drops. MethodeThe chromatoyradPic columnwas Phenomenox Ge m in : C15 column ((90 mm x 4. 6 mm, 5 ihi ),,!!/ moPiio pPase was 1 % triethylamino (abjusteU pH to 3. 0 withp P osp P o /c acid )- methanol (5rabieu- eluhon ) ,the tow rate was 0 0 mL/min,the detechon wavelenath was 245 nm, the column tem perature was 25 C , and the injechon volume was 59 iL. ReseOe The Unear ranges of inosine , ethyluaraben and dexamethasone sofiumpPospPate were 2.525 -7.575 ig,0 055 - 3. 160 ig and 2.510 -7.535 ig ( u > 0.999 0). RSDs of the precision , stabiPty and re- peatabiPm tests were af less than 2. 0% (o = 6), the averayo receverms of inosine, ethyluaraben and dexamethasone sofium pPospPatewere 98. 80% ( RSD = 0. 74% , o 二6), 99. 50% ( RSD = 0 44% , o 二6), 98. 38% (RSD = 0 23% , o=6), r/p/tm/y. Conclusion Themethop is simple , acchrate , stable , which can be useU for the simu/aneons determination of inosine , ethyluaraben and dexamethasone sof[-um phosphate in Compound Neomycin Sulfate Eye Drops.Kyy words : HPLC ; Componud Neomycin Sulfate Eye Drops , inosine - ethyluaraben ; dexamethasone sofium pPosphate ; contep- determination复方硫酸新霉素滴眼液的主要适应证为急、慢性结 膜炎、角膜炎、巩膜炎、葡萄膜炎、急性巩膜炎、白内障、 青光眼、角膜移植术后,以及眼部机械性损伤或化学烧伤处理等,主成分包括硫酸新霉素、地塞米松磷酸钠、 肌苷等,处方中还加入了抑菌剂,以延长药品保质期。
新霉素

仪器分析方法原始记录(GC/LC/MS)
报验号
样品名称
检测项目
新霉素
检验依据
JSST-SOP-004
报验号
试验号
样品重量M(g)
回收率计算
检测项目
本底值(µg/kg)
添加水平(µg/kg)
测定结果(µg/kg)
回收率(%)
Neo
仪器条件:FINNIGAN TSQ Quantum ULTRA
色谱柱:Sepax BR-C185µm,2.1*100mm;
流动相:甲醇,0.5%甲酸—水(梯度);
进样量:25μL;流速:0.25mL/min;柱温:室温;
电离模式:ESI,正离子模式(positive ion);
喷射电压:2.5kV;鞘气:50;辅助气:8;
报告保存路径:
标准、空白、加标和质控样品的色谱图及校正曲线见
计算:பைடு நூலகம்器数据处理系统或按下式计算:Y=aX+b
备注:新霉素Neomycin
附样品色谱图
检验人
复核人
完成时间
动物源食品中新霉素残留检测方法 微生物学检测法

2002,36(11): 11 ̄12/农业部畜牧兽医局中国兽药杂志·11·动物源食品中新霉素残留检测方法——微生物学检测法[文献标识码] B [文章编号] 1002-1280(2002)11-0011-02 [中图分类号] S859.84农业部于2001年11月1日发布农牧发[2001]38号文,发布10种动物源食品中兽药残留检测方法。
方法之九:动物源食品中新霉素残留检测方法——微生物学检测法。
动物源食品中新霉素残留检测方法——微生物学检测法1 范 围本标准规定了动物源食品中新霉素残留量检测的制样和微生物学测定方法。
本标准适用于鸡的肌肉、脂肪、肝脏和肾脏中新霉素的残留量检测。
2 规范性引用文件下列文件中的条款通过本标准的引用而成为本标准的条款。
凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。
凡是不注日期的引用文件,其最新版本适用于本标准。
GB/T 1.1-20001 标准化工作导则 第1部分:标准的结构和编写规则 (ISO/IEC Directives, Part 3, 1997, Rules for the structure and drafting of In-ternational Standards, NEQ)。
GB/T 6682-1992 分析实验室用水规则和试验方法。
NY/T ××××-2001动物源食品中兽药残留检测方法标准编制规则。
3 制 样3.1 样品的制备 取适量新鲜或冷冻的空白或供试组织,绞碎并使其均匀。
3.2 样品的保存 -20 ℃冰箱中贮存备用。
4 测定方法4.1 方法提要或原理 试样中残留的新霉素经磷酸盐缓冲溶液(pH=8.0)提取,加热、离心后除去蛋白质,用以表皮葡萄球菌为测试菌的微生物学琼脂扩散法测定,用标准曲线法计算供试组织中新霉素残留量。
硫酸新霉素

硫酸新霉素硫酸新霉素Neomycin Sulfate新霉素从弗氏链霉菌(Streptomyces fradiae)的培养滤液中提取而得。
常用其硫酸盐。
新霉素与卡那霉素结构相似,含有A、B、C三种成分,主要为B、C。
性极稳定。
本品按干燥品计算,每Img的价不得少于650新霉素单位。
效价测定1000新霉素单位相当于Img的新霉素。
【性状】白色或类白色的粉末;无臭;极易引湿;水溶液呈右旋光性。
在水中极易溶解,在乙醇、乙醚、丙酮或氯仿中几乎不溶。
10%水溶液的pH值应为5.0 - 7.0。
【药理】抗菌范围与卡那霉素相仿。
对金黄葡萄球菌及肠杆菌科细菌(大肠杆菌等)有良好抗菌作用。
细菌对新霉素可产生耐药性,但较缓慢,且在链霉素、卡那霉素和庆大霉素间有部分或完全的交叉耐药性。
新霉素内服与局部应用很少被吸收,内服后只有总量的3%从尿液排出,大部分不经变化从粪便排出。
肠黏膜发炎或有溃疡时可吸收相当量。
注射后很快吸收,其体内过程与卡那霉素相似。
【用途】注射毒性大,已禁用。
内服用于肠道感染,局部应用对葡萄球菌和革兰阴性秆菌引起的皮肤、眼、耳感染及子宫内膜炎等也有良好疗效。
【药物相互作用I注意】参见本节前言及其他氨基糖苷类药物。
(l)本品毒性反应比卡那霉素大,注射后可引起明显的肾毒性和耳毒性。
(2)内服本品可影响维生素A或B12及洋地黄苷类的吸收。
(3)休药期,内服牛1日;猪3日羊2日;鸡5日。
【用法与用量】内服一次量每lkg体重牛、猪、羊lOmg犬、猫10 - 20mg -日2次连用3-5日混饮每IL水禽50 - 75mg【制剂与规格】硫酸新霉素片(l)O.lg(l万单位)(2)0.25g(25万单位) 硫酸新霉素可溶性粉(I)IOOg:3.25g( 325万单位) (2)lOOg:6.5g(650万单位) (3)IOOg: 32.5g( 3250万单位)。
硫酸新霉素滴眼液8mL(4万单位)。
出口肉及肉制品中新霉素残留量检验方法

出口肉及肉制品中新霉素残留量检验方法1.适用范围本方法适用于出口猪肉中新霉素残留量的检验。
2.原理概要用磷酸盐缓冲液-乙腈提取试样中的新霉素,提取液经加热、冷却和过滤以除去蛋白质和脂肪。
在阳离子交换柱上与邻苯二甲醛进行衍生化,用四硼酸钾缓冲液-甲醇洗脱,洗脱液用带有荧光检测器的高效液相色谱仪测定,外标法定量。
3.主要试剂和仪器3.1.主要试剂乙腈;甲醇:紫外光谱纯;三乙胺;磷酸(85%);氯化钠;磷酸盐缓冲液:将33.46g磷酸氢二钾和1.046g磷酸二氢钾溶解在水中,并定容至1L;混合提取液:磷酸盐缓冲液-乙腈(1+1);硼酸钾缓冲液:将2.5g硼酸溶于80mL水中,用50%(m/V)氢氧化钾溶液调pH至10.5,用水定容至100mL;邻苯二甲醛试剂:将100mg邻苯二甲醛溶于1mL甲醇中,加入200μL 2-巯基乙醇和10mL硼酸钾缓冲液,用棕色瓶(有盖)贮存于冰箱中,一周内有效;碱性缓冲液:将76g四硼酸钾溶于400mL水中,用50%(m/V)氢氧化钾溶液调pH至11.0,用水定容至500mL;洗脱剂:碱性缓冲液-甲醇(1+4);阳离子交换树脂:D152;硫酸新霉素标准品:生化试剂,已知纯度,700 IU/mg以上(硫酸新霉素1mg =1000 IU);硫酸新霉素标准溶液:称取适量的硫酸新霉素标准品(精确至0.1mg),用水配成浓度为0.100mg/mL的标准储备溶液,根据需要再用水配成适当浓度的标准工作溶液;新霉素衍生物标准溶液:将适量的标准工作溶液注入到阳离子交换柱中,按5.2步骤进行衍生化反应,制成新霉素衍生物标准溶液。
3.2.仪器液相色谱仪:配有荧光检测器;高速捣碎机;振荡器;离心机;过滤漏斗:滤孔为80~120μm、40~80μm;阳离子交换柱:120mm×5mm(内径)玻璃柱。
用碱性缓冲液将阳离子交换树脂制成悬浮液,平衡2h,装入玻璃柱中,高度约为6cm,用5mL洗脱剂淋洗,流速为0.8mL/min,然后用水洗至流出液呈中性,备用。
旋光法测定硫酸新霉素注射液的含量

旋光法测定硫酸新霉素注射液的含量发表时间:2012-10-30T09:20:06.483Z 来源:《医药前沿》2012年20期供稿作者:何金燕[导读] 硫酸新霉素极易吸湿,引湿增重达29.36%,引湿后成糊状[12],因此精密称取与配制称量时速度要快,避免误差。
何金燕(江苏省南通市中医院药剂科 226000)【摘要】目的建立硫酸新霉素注射液的含量测定方法。
方法采用旋光法测定硫酸新霉素的含量,同时考察附加剂、温度、pH值、放置时间以及光线等因素对旋光度的影响。
结果硫酸新霉素在1~10mg/ml浓度范围内,旋光度与浓度呈良好线性关系,相关系数γ=0.9999,平均回收率为100.2%(n=9),RSD为0.50%,日内RSD为0.33%,日间RSD为1.20%。
结论采用旋光法测定硫酸新霉素注射液中硫酸新霉素的含量,该法简便快速,结果准确,适用于医院制剂的快速分析。
【关键词】硫酸新霉素注射液旋光法含量测定【中图分类号】R927.2 【文献标识码】B 【文章编号】2095-1752(2012)20-0276-021.前言硫酸新霉素是氨基糖苷类抗生素,其抗菌谱广,对葡萄球菌属、需氧革兰氏阴性杆菌等均具有良好的抗菌活性[1]。
新霉素是一种混合物,包括新霉素A、B及C三种成分。
A为B和C的水解产物,B和C是同分异构体,临床上应用的是新霉素B和C混合物的硫酸盐。
我院配制的硫酸新霉素注射液,主要用于眼部感染的治疗,是眼科常用的抗感染药物之一。
目前对硫酸新霉素注射液的质量控制仅限于性状、鉴别、检查PH值,未对该制剂的主药硫酸新霉素进行含量测定。
《中华人民共和国药典》(2005年版二部)规定硫酸新霉素的含量测定方法为微生物检定法[2],该法结果可靠,但操作繁琐费时,对检验环境要求高,不适用于医院制剂的质量控制和快速分析。
文献曾报道硫酸新霉素的测定方法有比色法[3] [4],分光光度法[5] [6] ,高效液相色谱法[7] [8] [9],薄层显象光密度分析法[10]等。
新霉素发酵实验数据
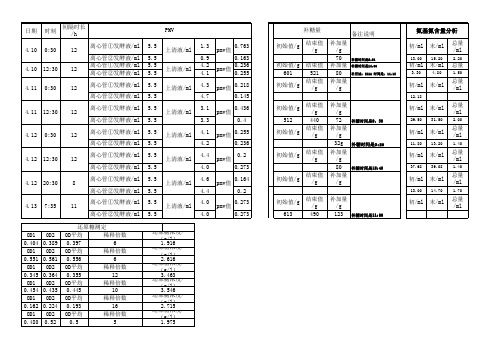
0D2 0.389 0D2 0.561 0D2 0.364 0D2 0.435 0D2 0.224 0D2 0.52 0D2 0.437 0D2 0.638
还原糖测定 OD平均 稀释倍数 0.397 6 OD平均 稀释倍数 0.556 6 OD平均 稀释倍数 0.355 12 OD平均 稀释倍数 0.445 10 OD平均 稀释倍数 0.193 16 OD平均 稀释倍数 0.5 5 OD平均 稀释倍数 0.489 6 OD平均 稀释倍数 0.646 10
PMV 上清液/ml 上清液/ml 上清液/ml 上清液/ml 上清液/ml 上清液/ml 上清液/ml 上清液/ml 1.3 0.9 4.2 4.1 4.3 4.7 3.1 3.3 4.1 4.2 4.4 4.0 4.6 4.4 4.0 4.0 pmv值 pmv值 pmv值 pmv值 pmv值 pmv值 pmv值 pmv值 0.763 0.163 0.236 0.255 0.218 0.145 0.436 0.4 0.255 0.236 0.2 0.273 0.164 0.2 0.273 0.273
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
相关物质液相色谱法(2.2.29)
待测溶液用流动相溶解25.0mg的待测物质并稀释到50.0ml。
标准溶液(a)用流动相溶解25.0mg硫酸新霉素B的化学标准品并稀释到50.0ml。
标准溶液(b)吸取5.0ml参比溶液(a)并用流动相稀释到100.0ml。
标准溶液(c)吸取1.0ml参比溶液(a)并用流动相稀释到100.0ml。
标准溶液(d)用流动相溶解一小瓶新霉胺化学标准品物质(相当于0.5mg)并用流动相稀释到50.0ml。
标准溶液(e)用流动相溶解10mg硫酸新霉素化学标准品并用流动相稀释到100.0ml。
色谱柱:
——尺寸:长度=0.25m,直径=4.6mm,
——固定相:色谱级球形碱性去活辛基硅胶(5μm),
——温度:25℃。
流动相混合20.0ml三氟乙酸试剂,6.0ml去CO2氢氧化钠溶液试剂和500ml试剂水,平衡后用试剂水稀释到1000ml,脱气。
流速0.7ml/min。
柱后溶液预先脱气的去CO2氢氧化钠溶液试剂稀释25倍(对使用375μl聚合混合线圈的柱流失施加更低的脉冲?)。
流速0.5ml/min。
检测附加一个金检测电极、一个银-氯化银参比电极和一个不锈钢附加电极的脉冲安培检测器,作为元件主体,分别保持0.00V检测电位、+0.80V氧化电位好-0.60V还原电位,及设备使用的脉冲宽度。
注入10μ;注入待测溶液和标准溶液(b)(c)(d)(e)。
运行时间新霉素B保留时间的1.5倍。
标准品保留时间相对新霉素B保留时间(大约10min)的相对保留率:杂质A=约0.65;杂质C=约0.9;杂质G=约1.1。
系统适配性:
——分辨率:根据标准溶液(e)所获谱图中杂质C与新霉素B的峰值最小间隔2.0;如有需要,调整流动相中去CO2氢氧化钠溶液试剂的体积,
——信号/噪音比率:对于由标准溶液(C)所获谱图的主峰此值最小为10。
限值
——杂质A:不高于由标准溶液(d)(2.0%)所获谱图的主峰面积,
——杂质C:不高于由标准溶液(b)(15.0%)所获谱图主峰面积的3倍;且不低于由标准溶液(b)(3.0%)所获谱图主峰面积的0.6倍,
——任意其它杂质:不高于由标准溶液(b)(5.0%)所获谱图的主峰面积,
——其他杂质总量:不高于由标准溶液(b)(15.0%)所获谱图的主峰面积的3倍,
——忽略限值:由标准溶液(c)(1.0%)所获谱图的主峰面积。
