反义寡核苷酸作用机理
aso反义寡核苷酸 可变剪接 -回复

aso反义寡核苷酸可变剪接-回复ASO反义寡核苷酸(Antisense oligonucleotide)是一种常用于基因治疗和基因调控的工具,其作用是通过与目标基因的RNA分子匹配形成双链结构,从而干扰或抑制目标基因的正常功能。
相比传统的药物靶向方法,ASO反义寡核苷酸具有更高的特异性和可调控性,因此被广泛应用于治疗多种疾病,尤其是一些遗传性疾病。
然而,除了ASO反义寡核苷酸用于基因治疗的传统应用外,近年来,科学家们还发现了ASO反义寡核苷酸在可变剪接中的重要作用。
可变剪接(Alternative Splicing)是指同一个基因在转录过程中可以产生多个不同的mRNA剪接变体,从而产生不同的蛋白质。
可变剪接是调控基因表达的重要机制之一,它可以增加基因功能的多样性和复杂性。
然而,由于可变剪接异常与多种疾病的发生和发展密切相关,如癌症、神经系统疾病等,因此对可变剪接的调控研究也日益引起科学家们的关注。
ASO反义寡核苷酸在可变剪接调控中的应用主要包括两个方面:调控剪接酶活性和调控剪接位点选择。
首先,ASO反义寡核苷酸可以通过与剪接酶相互作用,干扰或抑制其正常功能,从而调控可变剪接的发生。
剪接酶是调控剪接过程的关键酶,它可以选择性地切割mRNA前体,将其中的外显子连接起来,形成成熟的mRNA。
ASO反义寡核苷酸通过与剪接酶结合,阻断其结合到mRNA 前体上,或改变其构象,从而干扰剪接酶的活性,进而调控可变剪接的进行。
这种方法具有高度的特异性和可调控性,能够精确地调控某一特定的剪接酶活性,从而实现对特定剪接变体的调控。
其次,ASO反义寡核苷酸还可以通过调控剪接位点的选择,影响可变剪接的发生。
剪接位点是指mRNA前体上的两个外显子之间的连接点,它决定了哪些外显子会连接起来形成成熟的mRNA。
ASO反义寡核苷酸可以与mRNA前体中的剪接位点特异性地结合,从而改变剪接位点的选择,导致不同的mRNA剪接变体的产生。
反义寡核苷酸aso的递送系统_解释说明

反义寡核苷酸aso的递送系统解释说明1. 引言1.1 概述反义寡核苷酸(antisense oligonucleotide, ASO) 是一种具有广泛应用前景的基因治疗工具,它通过与特定mRNA分子序列互补结合,从而抑制或调控目标基因的表达。
ASO递送系统是将ASO有效地运送到靶位点的关键问题,它包括了手性寡核苷酸的设计、载体选择和优化策略,以及递送机制研究等方面。
1.2 文章结构本文将重点讨论反义寡核苷酸ASO的递送系统。
首先介绍反义寡核苷酸ASO 的概念和作用机制,明确其在基因治疗领域的重要性和应用前景。
接着,详细讨论目前存在的问题和挑战,如ASO递送效率低、稳定性差等。
然后,我们将介绍ASO递送系统的设计与原理,包括手性寡核苷酸设计原理、载体选择和优化策略以及递送机制研究进展。
接下来,在第四部分中探讨了ASO递送系统在遗传病治疗和肿瘤治疗中的应用前景,并探索了其他领域中的可能应用方向。
最后,通过总结和展望,提出未来关于ASO递送系统的研究方向。
1.3 目的本文的目的是全面介绍反义寡核苷酸ASO的递送系统。
通过对手性寡核苷酸设计原理、载体选择和优化策略以及递送机制研究进展的深入探讨,旨在提供关于ASO递送系统设计与优化的重要参考。
此外,本文还将预测ASO递送系统在遗传病治疗、肿瘤治疗以及其他领域中可能的应用前景,为相关领域的科学家和医生提供指导和启示。
最后,我们希望通过文章的撰写能够推动反义寡核苷酸ASO 递送系统领域的发展,并促进其在基因治疗中的应用成果。
2. 反义寡核苷酸ASO的递送系统2.1 反义寡核苷酸ASO简介反义寡核苷酸(Antisense oligonucleotide,ASO)是一种能够通过与靶标RNA 特异性杂交而调控基因表达的短链核酸分子。
ASO具有特异性、可调节性和高度选择性的特点,广泛应用于基因治疗、药物开发和生物学研究等领域。
ASO 的作用机理主要包括:阻断mRNA转录、刺激mRNA降解以及干扰蛋白质合成等。
乳腺癌反义寡核苷酸治疗的研究进展(一)

乳腺癌反义寡核苷酸治疗的研究进展(一)【关键词】乳腺癌反义寡核苷酸基因综述文献反义寡核苷酸技术(ASODN)作为一种新的分子生物学工具及新型药物受到医疗界越来越多的关注。
许多反义药物作为抗肿瘤药物已进入临床试验,并取得了令人欣喜的效果。
1反义寡核苷酸的作用机理简介1.1反义寡核苷酸是在体外人工合成的能与体内某RNA或DNA序列互补结合的短序列单链DNA。
它可以作为反义药物与细胞内特异的靶序列互补,从而抑制基因表达。
该技术的作用原理主要通过下列途径发挥作用:(1)ASODN与DNA结合,抑制DNA复制和转录,它通过在DNA 结合蛋白的识别点处与DNA双螺旋结合形成三螺旋,阻止基因的转录和复制。
(2)ASODN可影响真核生物mRNA核内加工的步骤,如5’端加帽结构、3’端加polyA及剪接的过程,从而抑制了mRNA的成熟过程。
(3)ASODN与目标mRNA特异性碱基互补结合,阻断RNA加工、成熟,阻止核糖体与起始因子的结合,影响核糖体沿mRNA移动,从而阻止翻译。
1.2天然的ASODN能够很快被在细胞内存有的大量的核酸外切酶和核酸内切酶降解。
因此,ASODN必须要经过修饰才能在体内发挥作用。
研究表明,硫代修饰之后的ASODN稳定,具有良好的水溶性,并容易大批量人工合成来应用于临床的研究。
所以,目前硫代磷酸型的ASODN 已应用于各个水平的研究领域中。
1.3反义寡核苷酸在乳腺癌的治疗研究中的应用主要通过抑制乳腺癌细胞生长、增殖、分化诱导凋亡,抑制乳腺癌细胞的转移和侵袭,降低乳腺癌的多药耐药性来实现。
1.4反义基因技术具有明显的优点,由于DNA序列在一般情况下是单拷贝,而mRNA是多拷贝,因此ASODN相比于反义RNA只需少量的ODN 与DNA靶序列结合,就可以具有很强的抑制效果。
它治疗乳腺癌特异性高,副作用少,与化疗、放疗和靶向药物结合有协同作用,并已逐步从实验室走向临床。
2针对主要的进入临床前试验的致乳腺癌基因的反义寡核苷酸的研究理论上认为任何致乳腺癌基因都可以成为ASODN的作用靶点,目前主要以细胞凋亡抑制基因、乳腺癌转移和血管生成基因、生长因子及受体、信号传导通路等作为常用的分子靶点。
ionis配体偶联反义(lica)技术的原理
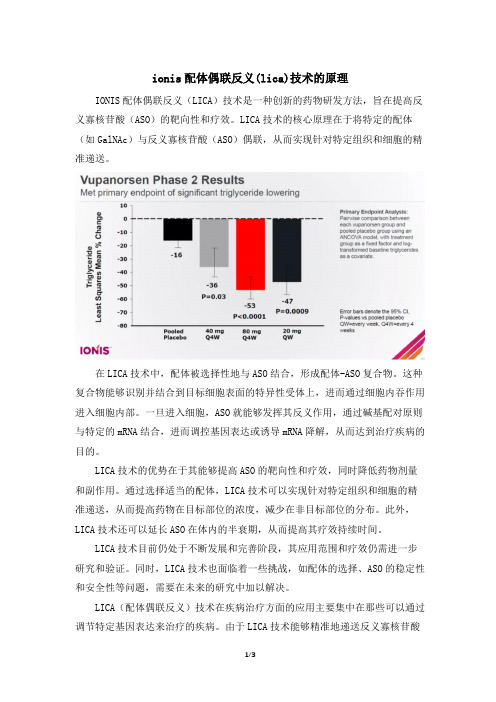
ionis配体偶联反义(lica)技术的原理IONIS配体偶联反义(LICA)技术是一种创新的药物研发方法,旨在提高反义寡核苷酸(ASO)的靶向性和疗效。
LICA技术的核心原理在于将特定的配体(如GalNAc)与反义寡核苷酸(ASO)偶联,从而实现针对特定组织和细胞的精准递送。
在LICA技术中,配体被选择性地与ASO结合,形成配体-ASO复合物。
这种复合物能够识别并结合到目标细胞表面的特异性受体上,进而通过细胞内吞作用进入细胞内部。
一旦进入细胞,ASO就能够发挥其反义作用,通过碱基配对原则与特定的mRNA结合,进而调控基因表达或诱导mRNA降解,从而达到治疗疾病的目的。
LICA技术的优势在于其能够提高ASO的靶向性和疗效,同时降低药物剂量和副作用。
通过选择适当的配体,LICA技术可以实现针对特定组织和细胞的精准递送,从而提高药物在目标部位的浓度,减少在非目标部位的分布。
此外,LICA技术还可以延长ASO在体内的半衰期,从而提高其疗效持续时间。
LICA技术目前仍处于不断发展和完善阶段,其应用范围和疗效仍需进一步研究和验证。
同时,LICA技术也面临着一些挑战,如配体的选择、ASO的稳定性和安全性等问题,需要在未来的研究中加以解决。
LICA(配体偶联反义)技术在疾病治疗方面的应用主要集中在那些可以通过调节特定基因表达来治疗的疾病。
由于LICA技术能够精准地递送反义寡核苷酸(ASO)到目标细胞,并调控特定基因的表达,因此它在多种疾病治疗中具有潜力。
具体来说,LICA技术可能适用于以下类型的疾病治疗:1.遗传性疾病:对于由基因突变引起的遗传性疾病,LICA技术可以通过调节突变基因的表达来减轻症状或治疗疾病。
2.代谢性疾病:LICA技术可以针对代谢通路中的关键基因进行调节,以纠正代谢紊乱,从而治疗代谢性疾病,如糖尿病、高脂血症等。
3.感染性疾病:LICA技术可以针对病原体的基因进行调节,以抑制病原体的生长和繁殖,从而治疗感染性疾病。
反义寡核苷酸序列

反义寡核苷酸序列反义寡核苷酸序列指的是一种与原始DNA或RNA序列有相反碱基配对的寡核苷酸序列。
在这种反义序列中,腺嘌呤(A)被胸腺嘧啶(T)取代,而胸腺嘧啶(T)则被腺嘌呤(A)取代;鸟嘌呤(G)被胞嘧啶(C)取代,而胞嘧啶(C)则被鸟嘌呤(G)取代。
反义寡核苷酸序列对于生物学和分子生物学领域具有重要意义。
其主要作用是在实验室中研究DNA和RNA的结构和功能,以及相关的分子机制。
在以下的几个方面我们可以看到反义寡核苷酸序列的应用。
1.基因工程:反义寡核苷酸序列可以通过DNA合成技术用于基因的修饰和重组。
通过引入反义寡核苷酸序列,可以修改目标基因的序列,并改变编码的蛋白质的氨基酸序列。
这种技术可以用来研究蛋白质的结构和功能。
2.基因表达调控:反义寡核苷酸序列可以用于基因表达的调控。
通过引入与目标基因相反的序列,可以抑制目标基因的表达。
这种技术被广泛应用于基因沉默(gene silencing),研究基因功能和调控机制。
3. RNA干扰:反义寡核苷酸序列也可以用于RNA干扰(RNA interference)。
这是一种通过引入小分子RNA序列来沉默目标基因的技术。
反义寡核苷酸序列可以与目标RNA序列互补配对,并引起RNA 降解或抑制翻译过程,从而抑制目标基因的表达。
4.抗病毒治疗:反义寡核苷酸序列可以用于抗病毒治疗。
病毒的基因组是RNA,通过设计与病毒基因组相反的寡核苷酸序列,可以特异性地结合病毒RNA,并阻断病毒蛋白质的合成和病毒复制过程,从而实现抗病毒治疗的效果。
总结起来,反义寡核苷酸序列在生物学和分子生物学领域具有广泛的应用。
通过对基因序列的修饰和调控,它们可以用来研究基因功能和调控机制。
在抗病毒治疗和基因沉默等方面,反义寡核苷酸序列也有着重要的应用潜力。
在未来的研究中,我们可以期待更多关于反义寡核苷酸序列的应用和发展。
反义寡聚核苷酸

首次应用合成的寡核苷酸成功的抑制基因的表达 ColE1 DNA复制研究中发现反义调节机制
Zamenick和Stephenson Itoh和Tomizawa
第二代反义核酸药物
Hybridon公司
首次提出反义核酸可用于下调原核生物与真核生物基因的表达 Coleman等
首次报道反义链下调一种细菌基因的表达
树枝状高聚物
转运带负电荷的ASODN,并形 成稳定的复合物
第一种ASODN药物---Vitravene
98年,第一种ASODN药物由FDA批准 使用 用于治疗一种由CMV(巨细胞病毒)引 起的眼部传染病---巨细胞病毒性视网 膜炎 流行于艾滋病人中
巨细胞病毒性视网膜炎
把药物注射到玻璃体中,然后被 视网膜中的受染细胞吸收,进入 细胞的ASODN与病毒的mRNA 结合
tat为HIV-l重要的调节基因,编码 反式激活因子 Tat蛋白 在逆转录病毒启动子LTR之后连接 反义tat与多聚TAR的构建物(LTR25TAR-AS-TAT) ,具有反义tat 及TAR诱饵的双重作用
发展史History时间/年1953 1957 1969 1978 1980 1981 1984 1987 1988 1988 1990 1997
事件
首次提出“反义”定义 三螺旋核酸概念的提出 第一代反义核酸药物(福米韦生,Fomivirsen)诞生
人或机构
Watson Davies Isis制药公司
24.1反义技术简介
反义技术(antisense technology)就是采用反义核
酸分子抑制、封闭或破坏靶基因的技术。
反义核酸是指与具有遗传信息的“正义”(positive sense)核酸链互补的核酸序列,与靶基因具有互补序列的 DNA或RNA片段,可通过碱基互补配对原则原理与特定靶基因 或mRNA形成杂交链,从而阻断基因转录和翻译。它包括反义 RNA、反义DNA及核酶(ribozyme),可通过人工合成和从生 物中提取获得它们。
反义核苷酸的研究

得到新型的化合物----多肽核酸(peptide
cle ic acid, PNA)。
nu
由于结构上 PNA 与 DNA 类似,其两相邻碱基间距 及碱基与类肽链骨架间的距离均相近, PNA 与 DNA 以 及RNA与PNA之间均可形成碱基配对。
第4条途径----偶联物
即综合应用多种化学修饰 ,效果很好,有“第二代
Cycle Diagram
是一种有高度原则性和 低毒性的基因药物,一般为寡核苷酸 类化合物。 反义寡聚核苷酸(antisense oligonucleotides):是一小段与mRNA 或DNA特异性结合并阻断其基因表达的人 工合成的短核酸片断。
反义RNA调节翻译的基本原理是:
1、反义 RNA与 mRNA 有互补序列,根据碱基互补原则,能
化学修饰方法
第1条途径-------磷酸二酯键的修饰:
磷原子是核酸酶的主要攻击位点 ,修饰后效果明显。 磷的修饰包括硫代、甲基化、氨化、酯化等,尤以硫代 磷酸寡核苷酸 (phosphoroth-ioteoligonucletide,PS-ODN) 最为常用,称为“第一代反义药物”。
PS-ODN 是至今研究最深入、应用最广泛的一类
反义药物”之称。它以 PS-ODN为核心,两翼序列上 的核糖的2’ 位被其它基团修饰。除了化学修饰,还可
以试作转基因表达反义核酸,在体细胞内以DNA为模
板转录产生 , 模拟天然RNA的形成过程 , 这样表达的 反义RNA可能在细胞内被天然修饰,从而稳定性得到 提高。
Hot Tip
国外已有反义药物应用于临床,Science杂志 1998年7月报道了第一个通过FDA认证的反义药物, 即用于治疗艾滋病人巨细胞病毒感染的视网膜炎的 ,这是ISIS公司的一大成果, 此外还有多种反 义药物包括核酶在内的新一代反义药物进入临床。
CTGF反义寡核苷酸对纤维结缔组织疾病的治疗作用与机制

结 缔 组 织 生 长 因 子 ( o n cie t s e g o h fc r c n e t i u r wt a t , v s o
调 节 细 胞 外 基 质 基 因 的表 达 : T F能 够 刺 激 成 纤 维 细 C G
在 病 理状 态 下 , 过 度 表 达 与 一 些 纤 维 增 生 性 疾 病 的 发 生 及 其
发 展 有 着 密 切关 系 。
1 C G T F的 促 纤 维 化 作 用
目前 , 们 已 经 知 道 C F 有 促 进 细 胞 增 殖 、 成 胶 人 TG 合
细 胞 外 基 质 来 源 的重 要 细胞 , 成 纤 维 细 胞 和 肾小 管 上皮 细 而
胞又是成肌纤 维细胞 的主 要来 源。C G T F可 明 显 上 调 人 肾
脉性 肝 硬 化 的发 生 。高 血 糖 及 高 胰 岛 素 通 过 上 调 非 酒 精 性
脂肪 肝 中 C GF mRN 的表 达 而 引 起 肝 脏 纤 维 化 [ 。C — T A 4 ] T
胡小 燕 综述 ) 汪 昌运 审校 ) ( , ( ( 昌大 学 a 研 究 生 院 医学部 2 0 南 . 0 5级 ; . b 第二 附属 医院眼科 , 南昌 3 0 0 ) 3 0 6
关 键 词 : T ; 义 寡 核 苷酸 ;基 因表 达 ;纤 维 化 ; 维 结 缔 组 织 ; 纤 维 细 胞 C GF 反 纤 成
原 、 节 细 胞 外 基 质 基 因 的表 达 、 导 细 胞 黏 附 、 调 介 刺激 细 胞 迁 移 、 速 新 生 血 管 的 形 成 、 进 软 骨 增 生 和 骨 骼 发 育 、 响 细 加 促 影 胞 凋 亡 过 程 等 多 种 生 物 作 用 。其 促 纤 维 化 的 作 用 已 成 为 近 年 来 研究 的 重 点 。 综 合 来 说 , T C GF主要 通 过 以 下 途 径 促 进
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
反义寡核苷酸作用机理
反义寡核苷酸(Antisense oligonucleotides,ASOs)是一种人工合成的核酸序列,其作用机理是通过碱基互补配对原则与特定的信使RNA(mRNA)结合,从而抑制基因的表达。
反义寡核苷酸的作用机理主要涉及以下几个方面:
抑制DNA复制和转录:反义寡核苷酸可与双链DNA通过Hoogsteen氢键结合形成三螺旋结合,以交联、切断等方式使之不能进一步复制和转录。
此外,反义寡核苷酸也可与复制和转录时解链的双链DNA的局部单链结合,抑制DNA的复制和转录。
抑制转录后加工:反义寡核苷酸可与mRNA靶序列通过Waston-Crick碱基配对结合,干扰mRNA的进一步加工成熟,发挥其抑制作用。
抑制翻译:经转录后加工成熟的mRNA必须从细胞核转至细胞质中,与核糖体和重要的启动因子结合,使蛋白质合成过程开始。
而反义寡核苷酸可与mRNA结合,由于直接的立体效应,影响核糖体和重要的启动因子结合,使蛋白质合成过程停止。
激活RNaseH:RNaseH是一种专一性降解DNA/RNA杂交链中RNA链的核酸酶。
反义寡核苷酸与靶RNA杂交后可被RNaseH识别并切割,从而加速RNA的降解。
总之,反义寡核苷酸的作用机理主要通过与特定基因或mRNA互补结合,抑制基因的表达。
其作用机制涉及多个环节,包括抑制DNA复制和转录、干扰mRNA加工成熟、抑制蛋白质合成以及激活RNaseH等。
反义寡核苷酸作为一类具有广泛应用前景的基因靶向治疗药物,对肿瘤、病毒感染等疾病的治疗具有重要意义。
