水质 碱度 酸碱指示剂滴定法
化验室酸碱滴定法测定水质碱度操作规程

化验室酸碱滴定法测定水质碱度操作规程一、引用标准GB/T15451-2006工业循环冷却水总碱及酚酞碱度的测定GBT1576-2018工业锅炉水质二、方法提要水的碱度是指水中含有能接受氢离子的物质的量,例如氢氧根、碳酸盐、重碳酸盐、磷酸盐、磷酸氢盐、硅酸盐、硅酸氢盐、亚硫酸盐、腐植酸盐和氯等,都是水中常见的碱性物质,它们都与酸进行反应。
因此选用适宜的指示剂,以标准酸溶液对它们进行滴定,便可测出水中碱度的含量。
碱度可分为酚酞碱度和全碱度两种,酚酞碱度是以酚酞作指示剂时所测出的量,其终点的pH值为8.3,全碱度是以甲基橙作指示剂时测出的终点pH值为4.2,若碱度很小时全碱度宜以甲基红—亚甲基蓝作指示剂,终点的pH值为5.0。
三、试剂及配制1、10g/L的酚酞酒精溶液:称取1g酚酞,溶于乙醇(95%),用乙醇(95%)稀释至100mL。
2、1g/L的甲基橙溶液:称取0.1g甲基橙,溶于70℃的水中,冷却,稀释至100mL。
3、甲基红-亚甲基蓝指示剂:准确称取0.125g甲基红和0.085g亚甲基蓝在研钵中研磨均匀后,溶于100mL95%乙醇中。
4、0.10moL/LHCl、0.050moL/LHCl、0.010moL/LHCl标准溶液。
四、操作步骤1、大碱度水样(如锅炉水、化学净水、冷却水、生水等)的测定取100mL透明水样注入锥形瓶中,加2~3滴酚酞指示剂,此时若显红色,则用0.100moL/L或0.0500moL/L盐酸标准溶液滴至红色刚消失,记录盐酸溶液的用量V1;然后再加入甲基橙指示剂2~3滴继续用盐酸标准溶液滴定至由淡黄色变为橙色,记录用量V2(不包括V1)。
2、小碱度水样(如凝结水、高纯水、给水等)的测定取100mL透明水样注入锥形瓶中,加2~3滴酚酞指示剂,此时若显红色。
则用微量滴定管以0.0100moL/L盐酸标准溶液滴至红色刚消失,记录盐酸溶液的用量V1;然后再加入甲基红—亚甲基蓝指示剂2~3滴继续用盐酸标准溶液滴定至由绿色变为紫色,记录用量V2(不包括V1)。
2017-1-14水质酸度、碱度的测定方法

酚酞碱度是以酚酞作指示剂测得的碱度,全碱度是 以甲基橙(或甲基红-亚甲基蓝) 作指示剂测得的碱 度。酚酞终点的pH约为8.3,甲基橙终点的pH约为 4.2,甲基红-亚甲基蓝终点的pH约为5.0。第一法 以酚酞(第一终点)和甲基橙(第二终点)作 指示剂; 第二法以酚酞(第一终点)和甲基红-亚甲基蓝(第二 终点)作指示剂。
分析步骤
注:水样中若含有游离氯,可加数滴 0.lmol/L硫代硫酸钠溶液,以消除游离氯 对测定的影响。
5 结果的表述
水样酸度SD(mmol/L)按下式计算:
c.v0
SD= 式中:
v
*1000
SD—酸度,mmol/L 。
C—氢氧化钠标准滴定溶液的浓度,mol/L。 V1—滴定消耗氢氧化钠标准滴定溶液体积,mL。 V—试样体积,mL。
H++OH-=H2O
Байду номын сангаас
3试剂
3.1 氢氧化钠标准滴定溶液[C=0.O5mol/L] :配制和 标定方法见 GB/T601 3.2 甲基橙指示剂(1g/L):称取 0.1g 甲基橙,溶于 70℃ 的水中,冷却,稀释至 100mL。 3.3 试剂纯 度应符合 GB/T6903 要求。
4 分析步骤
4.1 按DL/T502.2 规定方法采集样品。 4.2 取100mL水样(V)注入250mL锥形瓶中。 4.3 加2滴甲基橙指示剂,用0.05mol/L氢氧化钠标准 滴定溶液滴定至溶液呈橙黄色为止,记录所消耗氢氧 化钠标准滴定溶液的体积为V0。
水质中酸度、碱度的测定
陈丽春 2017-1-14
1 范围
1 范围 本规程规定了氢离子交换器出水中酸度的测定方
法。 本方法适用于氢离子交换器出水中酸度的测定。
水中碱度测定实验报告

一、实验目的1. 掌握水中碱度的测定方法。
2. 了解不同指示剂在不同pH值下的变色情况。
3. 熟悉酸碱滴定的原理和操作步骤。
二、实验原理水中碱度是指水中所含能与强酸发生中和作用的全部物质,即能接受质子H的物质的总量。
本实验采用酸碱滴定法测定水中碱度,以酚酞和甲基橙为指示剂,分别滴定水样中的OH-和CO32-。
三、实验仪器与试剂1. 仪器:酸式滴定管、锥形瓶、移液管、洗耳球、玻璃棒、烧杯、电子天平、pH 计、蒸馏水、标准HCl溶液(0.1000mol/L)、酚酞指示剂、甲基橙指示剂。
2. 试剂:酚酞指示剂(0.5g酚酞溶于50mL 95%乙醇中,用水稀释至100mL)、甲基橙指示剂(0.05g甲基橙溶于100mL蒸馏水中)、无CO2蒸馏水。
四、实验步骤1. 标准溶液的配制与标定(1)配制0.1000mol/L HCl标准溶液:称取3.65g HCl(分析纯),加入少量蒸馏水溶解,转移至1000mL容量瓶中,用水定容至刻度。
(2)标定HCl标准溶液:准确移取25.00mL HCl标准溶液于锥形瓶中,加入2滴酚酞指示剂,用0.1000mol/L NaOH标准溶液滴定至溶液呈微红色,记录消耗的NaOH体积。
2. 水样碱度的测定(1)取100mL水样于锥形瓶中,加入2滴酚酞指示剂,用HCl标准溶液滴定至溶液由红色变为无色,记录消耗的HCl体积P。
(2)继续加入2滴甲基橙指示剂,用HCl标准溶液滴定至溶液由橙黄色变为橙红色,记录消耗的HCl体积M。
五、实验结果与分析1. 计算水样碱度根据实验数据,计算水样碱度如下:OH-碱度= C(HCl) × P × 1000 / 1000CO32-碱度= C(HCl) × (M - P) × 1000 / 1000其中,C(HCl)为HCl标准溶液的浓度(mol/L),P和M分别为酚酞和甲基橙指示剂滴定所消耗的HCl体积(mL)。
1酸碱滴定法:碱度的测定
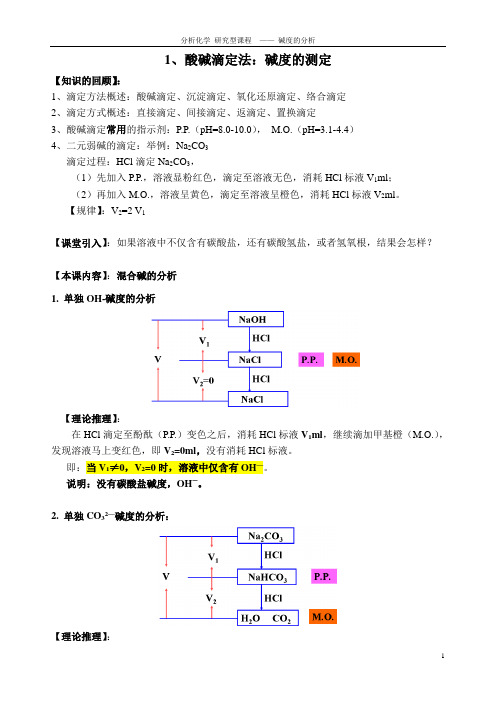
1、酸碱滴定法:碱度的测定【知识的回顾】:1、滴定方法概述:酸碱滴定、沉淀滴定、氧化还原滴定、络合滴定2、滴定方式概述:直接滴定、间接滴定、返滴定、置换滴定3、酸碱滴定常用的指示剂:P.P.(pH=8.0-10.0),M.O.(pH=3.1-4.4)4、二元弱碱的滴定:举例:Na2CO3滴定过程:HCl滴定Na2CO3,(1)先加入P.P.,溶液显粉红色,滴定至溶液无色,消耗HCl标液V1ml;(2)再加入M.O.,溶液呈黄色,滴定至溶液呈橙色,消耗HCl标液V2ml。
【规律】:V2=2 V1【课堂引入】:如果溶液中不仅含有碳酸盐,还有碳酸氢盐,或者氢氧根,结果会怎样?【本课内容】:混合碱的分析1. 单独OH-碱度的分析【理论推理】:在HCl滴定至酚酞(P.P.)变色之后,消耗HCl标液V1ml,继续滴加甲基橙(M.O.),发现溶液马上变红色,即V2=0ml,没有消耗HCl标液。
即:当V1≠0,V2=0时,溶液中仅含有OH—。
说明:没有碳酸盐碱度,OH—。
2. 单独CO32—碱度的分析:【理论推理】:在HCl滴定至酚酞(P.P.)变色之后,消耗HCl标液V1ml,继续滴加甲基橙(M.O.),滴定至溶液变红色,消耗HCl标液V2 ml,且V1=V2。
即:当V1=V2时,溶液中仅含有OH—。
说明:只有碳酸盐碱度,CO32—。
3. 单独HCO3—(重碳酸盐)碱度的分析:【理论推理】:向溶液中加入指示剂酚酞(P.P.),溶液不显粉红色,即消耗HCl标液V1=0ml,继续滴加甲基橙(M.O.),溶液呈现橙黄色,滴定至溶液变红色,消耗HCl标液V2 ml。
即:当V1=0,V2≠0时,溶液中仅含有HCO3—。
说明:只有碳酸盐碱度,HCO3—。
4. CO32—和HCO3—碱度的分析:【理论推理】:向溶液中加入指示剂酚酞(P.P.),溶液显粉红色,滴定至粉红色消失,消耗HCl标液V1ml,继续滴加甲基橙(M.O.),溶液呈现橙黄色,滴定至溶液变红色,消耗HCl标液V2 ml。
水中碱度的测定

⽔中碱度的测定⽔中碱度的测定(酸碱滴定法)⽔的碱度是指⽔中所含能够接受质⼦的物质总量⼀、实验⽬的通过实验掌握⽔中碱度的测定⽅法,进⼀步掌握滴定终点的判断⼆.实验原理酸碱滴定法1)适应范围本⽅法适⽤于天然⽔,循环⽔及炉⽔中碱度的测定⽅法。
2)测定原理采⽤连续滴定⽅法测定⽔中的碱度。
⾸先以酚酞为指⽰剂,⽤HNO3标准溶液滴定⾄终点溶液由红⾊变成⽆⾊,⽤量为P(mL);接着以甲基橙为指⽰剂,三、仪器与试剂1.C(HNO3)=0.1000mol/L标准滴定溶液。
(配制与标定在实验(⼀)中已讲过,这⾥就不在重述)2.甲基橙指⽰剂:称取0.05g甲基橙溶于100ml蒸馏⽔中3.酚酞指⽰剂:称取0.5g酚酞溶于50mL 95%⼄醇中,⽤⽔稀释⾄100mL4.酸式滴定管100mL ⼀⽀5.锥形瓶 250mL 三⽀6.移液管 100mL ⼀⽀7.⽆CO2蒸馏⽔四、实验步骤1、⽤移液管吸取两份⽔样和⼀份⽆CO2蒸馏⽔各100mL,分别放⼊250mL锥形瓶中,加⼊4滴酚酞指⽰剂,摇匀。
2、若溶液呈红⾊,⽤0.1000mol/L HNO3溶液滴定⾄刚好⽆⾊(可与⽆CO2蒸馏⽔的锥形瓶作颜⾊⽐较)。
记录滴加的⽤量(P)。
若加⼊酚酞指⽰剂后溶液⽆⾊,则不需要⽤HNO3溶液滴定。
按着下步骤操作。
3、再于每瓶中加3滴甲基橙指⽰剂,摇匀。
4、分两种情况:其⼀若⽔样变成橘黄⾊,则继续⽤C HNO3=0.1000mol/L标准液滴定⾄刚刚变成橙红⾊为⽌(可与⽆CO2蒸馏⽔的锥形瓶颜⾊作⽐较),记⽤量(M)。
其⼆如果加⼊甲基橙溶液后溶液变为橙红⾊,则不需要⽤HNO3溶液滴定。
6.计算:总碱度(CaO 计,mg/L)=1000*V 04.28*M P C )(+总碱度(CaCO 3计,mg/L)=1000*V05.50*M P C )(+式中V —⽔样的体积,mL ;C —硝酸标准滴定溶液的浓度,mol/L ;P —滴定酚酞碱度时,消耗硝酸标准滴定溶液的体积,mL ; M —滴定甲基橙碱度时,消耗硝酸标准滴定溶液的体积,mL ;28.04—氧化钙的摩尔质量(1/2CaO ,g/moL) 50.05—碳酸钙的摩尔质量(1/2CaCO 3 ,g/moL)表中T=P+M五、仪器整理六、写实验报告。
[精彩]水质酸碱度的测定1
![[精彩]水质酸碱度的测定1](https://img.taocdn.com/s3/m/fbbb01c727fff705cc1755270722192e453658fe.png)
水质酸碱度的测定一、实验目的水的酸碱度是判断水质和废水处理控制的重要指标,本实验的目的是掌握碱度的检测方法:指示剂滴定法。
二、实验原理酸/碱度是指水中所含能与强碱/强酸发生中和作用的物质的总和,酸碱度和pH值既有区别又有联系。
酸碱指示剂滴定法:用标准的氢氧化钠/硫酸溶液滴定水样至一定pH 值,根据其所消耗的试剂量计算酸度/碱度。
通常分为两种酸度/碱度:一是用酚酞作指示剂(其变色pH 为8.3)测得的酸度称为酚酞酸度(总酸度)/碱度;二是用甲基橙作指示剂(变色pH 约4.3)测得的酸度称甲基橙酸度/碱度(总碱度)。
三、实验仪器、药品试剂实验仪器:电子天平、50mL酸式滴定管、250mL锥形瓶、铁架台、烧杯、洗瓶;药品试剂:除盐水、C1/2H2SO4约0.05mol/L、无水碳酸钠、甲基橙指示剂(1g/L)、溴甲酚绿-甲基红指示剂。
四、实验步骤1.C1/2H2SO4的标定:准确称量已在250℃下干燥过的4h基准无水碳酸钠0.11±0.001g,置于250mL锥形瓶中,计下实际称量的无水碳酸钠的质量m,加50mL除盐水溶解,再加2滴溴甲酚绿-甲基红指示剂,用硫酸溶液滴定至刚出现红色,小心煮沸溶液至红色褪去,冷却至室温。
继续滴定、煮沸、冷却,直至刚出现的微红色在再加热时不褪色为止,计下消耗的硫酸体积V。
C(1/2H2SO4)=m/0.05299×V式中:C(1/2H2SO4) ──硫酸标准滴定溶液的物质的量浓度,mol/L;m ──称量无水碳酸钠质量,g;V ──滴定用去硫酸溶液实际体积,mL;0.05299 ──与1.00mL硫酸标准滴定溶液C(1/2H2SO4)=1.000mol/L〕相当的以克表示的无水碳酸钠的质量。
2.取地表水样100mL于锥形瓶内,滴入两滴甲基橙指示剂,以标定后的C1/2H2SO4滴定至由黄色变为橙色即为终点,计下消耗的C1/2H2SO4体积V1;3.重复第2步再测两次,计下体积V2、V3;4.取自来水样重复步骤2和3,测得自来水消耗的C1/2H2SO4体积;五、数据处理以mmol/L表示总碱度A T,其计算公式如下:A T=V1*c*1000/V o式中:V1——滴定时消耗的C1/2H2SO4体积(mL);c ——C1/2H2SO4浓度(mol/L);V o——水样取样体积,这里是100mL。
HZHJSZ00130 水质 碱度 总碱度 重碳酸盐和碳酸盐...

HZHJSZ00130 水质碱度总碱度重碳酸盐和碳酸盐的测定 酸碱指示剂滴定法 HZ-HJ-SZ-0130水质重碳酸盐和碳酸盐)的测定水中碱度的来源是多种多样的基本上是碳酸盐所以总碱度被当作这些成分浓度的总和磷酸盐或硅酸盐等时废水及其他复杂体系的水体中金属水解性盐类等在这些情况下代表能被强酸滴定的物质的总和只有当试样中的化学组成已知时对于天然水和未污染的地表水为酚酞碱度为甲基橙碱度重碳酸盐和氢氧根离子的含量污水这种计算无实际意义然后并作出解释是对水和废水处理过程的控制的判断性指标则碱度又是确定这种水是否适宜于灌溉的重要依据有两种常用的方法电位滴定法根据电位滴定曲线在终点时的突跃它不受水样浊度适用范围较广适用于控制性试验及例行分析样品采集后应在4·ÖÎöÇ°²»Ó¦´ò¿ªÆ¿ÈûÏ¡ÊÍ»òŨËõÌرðÊǵ±ÑùÆ·Öк¬ÓпÉË®½âÑÎÀà»òº¬ÓпÉÑõ»¯Ì¬ÑôÀë×Óʱ1 原理水样用标准酸溶液滴定至规定的pH值当滴定至酚酞指示剂由红色变为无色时指示水中氢氧根离子(OH-)已被中和反应如下 H2OCO32-+H+ÈÜÒºµÄpH值为4.4~4.5·´Ó¦ÈçÏÂH2O+CO2¿ÉÒÔ¼ÆËã³öË®ÖÐ̼ËáÑÎ上述计算方法不适用于污水及复杂体系中碳酸盐和重碳酸盐的计算有色均干扰测定可用电位滴定法测定例如水样中余氯可破坏指示剂(含余氯时3 方法的适用范围此法适用于不含有上述干扰的物质的水样4 试剂4.1 无二氧化碳水临用前煮沸15minpH 值应大于6.04.2 酚酞指示液用0.1mol/L 氢氧化钠溶液滴至出现淡红色为止称取0.1g 甲基橙溶于100mL 蒸馏水中0.0250mol/L) 烘干4h)的无水碳酸钠(Na 2CO 3)ÒÆÈë1000mL 容量瓶中摇匀保存时间不要超过一周用分度吸管吸取2.1mL 浓盐酸(ñ=1.19g/mL)此溶液浓度其准确浓度按下法标定加无二氧化碳水稀释至约100mL ÓÃÑÎËá±ê×¼ÈÜÒºµÎ¶¨ÖÁÓɽۻÆÉ«¸Õ±ä³É½ÛºìÉ«°´ÏÂʽ¼ÆËãÆä׼ȷŨ¶È0.0250 / V式中 V 盐酸标准溶液用量(mL)25mL250mL¼ÓÈë4滴酚酞指示液当溶液呈红色时记录盐酸标准溶液用量则不需用盐酸标准溶液滴定 6.2 向上述锥形瓶中加入3滴甲基橙指示液继续用盐酸标准溶液滴定至溶液由桔黄色刚刚变为桔红色为止 7 结果计算对于多数天然水样有五种情形令以酚酞作指示剂时所消耗盐酸标准溶液的量为P mL则盐酸标准溶液总消耗量为T PP 0时由于M Ò಻º¬ÖØ̼ËáÑÎP 氢氧化物P说明M 有碳酸盐存在2M 而且由于P说明尚有氢氧化物存在T -2(T -P ) 第三种情形21T M 时说明水中仅有碳酸盐2P TP此时P尚有水中原有的重碳酸盐2P T -2P P此时重碳酸盐=T =M以上五种情形的碱度表6-1 碱度的组成滴定的结果氢氧化物CO32-HCO 3-1/2T 2P -T2P -T 0 P 1/2T 0 2P T -2P P =0T按下述公式计算各种情况下总碱度重碳酸盐的含量mg/L) = c 1000 / V总碱度(以CaCO 3计P+M 50.05c ––––盐酸标准溶液浓度(mol/L)1/2CaO g/mol50.05––––碳酸钙摩尔质量T时0碳酸盐21T 时以CaO 计= c 1000 / V碳酸盐碱度mg/L T - P 50.051/2CO 32-, mol/L T - P 1000 / V重碳酸盐碱度= 0 (4) 当PPÒÔCaO 计= c28.04ÒÔCaCO 3计= c 50.051/2CO 32-, mol/L PHCO 3-21T 时P1000 / V 碳酸盐碱度(以CaCO 3计, mg/L) = c50.05PT - 2P 28.04T - 2P 50.05T - 2P 1000 / V(6) 当P =0时CO 32-M1000 /V重碳酸盐碱度(以CaCO 3计, mg/L) = c 50.05MÔÚHCO 3-含量为43.50mg/L时室间相对标准偏差为1.46%加标回收率为99.6取15个地表水水样进行测定相对标准偏差为0.1~1.4%注意事项1则不存在碳酸盐当水样中总碱度小于20mg/L时或改用10mL容量的微量滴定管9 参考文献±àί»á±àµÚÈý°æpp. 234~238±±¾©。
碱度和硬度的测定原理

碱度和硬度的测定原理
碱度和硬度是水质检测中常用的参数。
下面是碱度和硬度的测定原理。
碱度的测定原理:
碱度反映了水中碱性物质的含量,常用指标是水中的碳酸盐硬度。
常见的测定方法有酚酞法和酸碱滴定法。
酚酞法:该方法通过酚酞指示剂的变色反应来测定水中的碱度。
首先,将酚酞指示剂加入待测水样中,逐滴加入盐酸溶液直到溶液转为红色。
通过计算所使用的盐酸溶液的体积,可以确定水样中的碱度。
酸碱滴定法:该方法通过滴定剂和酸碱指示剂的反应来测定水中的碱度。
首先,将滴定剂(例如盐酸或硝酸)滴入待测水样中,滴定至溶液的pH值达到指示剂的变色点。
通过计算所使用的滴定剂的体积,可以确定水样中的碱度。
硬度的测定原理:
硬度是水中钙和镁离子的含量,可以分为总硬度和临时硬度两种。
常见的测定方法有EDTA滴定法和复合指示剂法。
EDTA滴定法:该方法通过EDTA (乙二胺四乙酸)与水样中的钙、镁离子生成络合物的滴定反应来测定水中的硬度。
首先,将专用指示剂(例如二甲基黄)加入水样中,直到溶液转为蓝色。
然后,滴定EDTA溶液直至溶液由蓝色转变为粉红
色。
通过计算所使用的EDTA溶液的体积,可以确定水样中的硬度。
复合指示剂法:该方法将复合的指示剂(例如酞菁T)与水样中的钙、镁离子生成络合物的反应来测定水中的硬度。
复合指示剂可在不同硬度的水样中产生颜色的变化,根据颜色的变化可以确定水样中的硬度。
总的来说,碱度和硬度的测定原理基于滴定反应或指示剂的变色反应,通过计算所使用的试剂体积,可以确定水样中的碱度和硬度。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
水质碱度(总碱度、重碳酸盐和碳酸盐)的测定酸碱指示剂滴定法水的碱度是指水中所含能与强酸定量作用的物质总量。
水中碱度的来源是多种多样的。
地表水的碱度,基本上是碳酸盐、重碳酸盐及氢氧化物含量的函数,所以总碱度被当作这些成分浓度的总和。
当水中含有硼酸盐、磷酸盐或硅酸盐等时,则总碱度的测定值也包含它们所起的作用。
废水及其他复杂体系的水体中,还含有有机碱类、金属水解性盐类等,均为碱度组成部分。
在这些情况下,碱度就成为一种水的综合性特征指标,代表能被强酸滴定的物质的总和。
碱度的测定值因使用的终点pH值不同而有很大的差异,只有当试样中的化学组成已知时,才能解释为具体的物质。
对于天然水和未污染的地表水,可直接用酸滴定至pH8.3时消耗的量,为酚酞碱度。
以酸滴定至pH为4.4~4.5时消耗的量,为甲基橙碱度。
通过计算可求出相应的碳酸盐、重碳酸盐和氢氧根离子的含量;对于废水、污水,则由于组分复杂,这种计算无实际意义,往往需耍根据水中物质的组分确定其与酸作用达终点时的pH值。
然后,用酸滴定以便获得分析者感兴趣的参数,并作出解释。
碱度指标常用于评价水体的缓冲能力及金属在其中的溶解性和毒性,是对水和废水处理过程的控制的判断性指标。
若碱度是由过量的碱金属盐类所形成,则碱度又是确定这种水是否适宜于灌溉的重要依据。
用标准酸滴定水中碱度是各种方法的基础。
有两种常用的方法,即酸碱指示剂滴定法和电位滴定法。
电位滴定法根据电位滴定曲线在终点时的突跃,确定特定pH值下的碱度,它不受水样浊度、色度的影响,适用范围较广。
用指示剂判断滴定终点的方法简便快速、适用于控制性试验及例行分析。
二法均可根据需要和条件选用。
样品采集后应在4℃保存,分析前不应打开瓶塞,不能过滤、稀释或浓缩。
样品应于采集后的当天进行分析,特别是当样品中含有可水解盐类或含有可氧化态阳离子时,应及时分析。
1.原理水样用标准酸溶液滴定至规定的pH值,其终点可由加入的酸碱指示剂在该pH值时颜色的变化来判断。
当滴定至酚酞指示剂由红色变为无色时,溶液pH值即为8.3,指示水中氢氧根离子(OH-)已被中和,碳酸盐(CO32-)均被转为重碳酸盐(HCO3-),反应如下:OH-+H+―H2OCO32-+H+―HCO3–当滴定至甲基橙指示剂由桔黄色变成桔红色时,溶液的pH值为4.4~4.5,指示水中的重碳酸盐(包括原有的和由碳酸盐转化成的)已被中和,反应如下:HCO3+H+―H2O+CO2根据上述两个终点到达时所消耗的盐酸标准滴定溶液的量,可以计算出水中碳酸盐、重碳酸盐及总碱度。
上述计算方法不适用于污水及复杂体系中碳酸盐和重碳酸盐的计算。
2.干扰及消除水样浑浊,有色均干扰测定,遇此情况,可用电位滴定法测定。
能使指示剂褪色的氧化还原性物质也干扰测定。
例如水样中余氯可破坏指示剂(含余氯时,可加入1~2滴0.1mol/L硫代硫酸钠溶液消除)。
3.方法的适用范围此法适用于不含有上述干扰的物质的水样。
4.试剂4.1无二氧化碳水。
用于制备标准溶液及稀释用的蒸馏水或去离子水,临用前煮沸15min,冷却至室温。
pH值应大于6.0,电导率小于2μS/cm。
4.2酚酞指示液。
称取1g酚酞溶于100mL 95%乙醇中,用0.1mol/L氢氧化钠溶液滴至出现淡红色为止。
4.3甲基橙指示剂。
称取0.1g甲基橙溶于100mL蒸馏水中。
4.4碳酸钠标准溶液(1/2Na2CO3 0.0250mol/L)。
称取 1.3249g(于250烘干4h) 的无水碳酸钠(Na2CO3),溶于少量无二氧化碳水中,移入1000mL容量瓶中,用水稀释至标线,摇匀,贮于聚乙烯瓶中。
保存时间不要超过一周。
4.5盐酸标准溶液(0.0250mol/L)。
用分度吸管吸取2.1 mL浓盐酸(ñ=1.19g/mL),并用蒸馏水稀释至1000mL,此溶液浓度≈0.025mol/L,其准确浓度按下法标定:用无分度吸管吸取25.00mL碳酸钠标准溶液于250mL锥形瓶中,加无二氧化碳水稀释至约100mL,加入3滴甲基橙指示液,用盐酸标准溶液滴定至由桔黄色刚变成桔红色,记录盐酸标准溶液用量,按下式计算其准确浓度:c=25.00×0.0250/V式中:c----盐酸标准溶液浓度(mol/L);V----盐酸标准溶液用量(mL)。
5.仪器5.1酸式滴定管,25mL。
5.2锥形瓶,250mL。
6.操作步骤6.1分取100mL水样于250mL锥形瓶中,加入4滴酚酞指示液摇匀,当溶液呈红色时,用盐酸标准溶液滴定至刚刚褪至无色,记录盐酸标准溶液用量。
若加酚酞指示剂后溶液无色,则不需用盐酸标准溶液滴定,并接着进行下项操作。
6.2向上述锥形瓶中加入3滴甲基橙指示液,摇匀,继续用盐酸标准溶液滴定至溶液由桔黄色刚刚变为桔红色为止。
记录盐酸标准溶液用量。
7.结果计算对于多数天然水样,碱性化合物在水中所产生的碱度,有五种情形。
为说明方便,令以酚酞作指示剂时,滴定至颜色变化。
所消耗盐酸标准溶液的量为P mL,以甲基橙作指示剂时盐酸标准溶液用量为MmL,则盐酸标准溶液总消耗量为T=M+P。
第一种情形,P=T或M=0时:P代表全部氢氧化物及碳酸盐的一半,由于M=0表示不含有碳酸盐,亦不含重碳酸盐。
因此P=T=氢氧化物。
第二种情形,P>1/2T时;说明M>O,有碳酸盐存在,且碳酸盐=2M=2(T-P)。
而且由于P>M,说明尚有氢氧化物存在,氢氧化物=T-2(T-P)=2P-T。
第三种情形,P=1/2T,即P=M时;M代表碳酸盐的一半,说明水中仅有碳酸盐。
碳酸盐=2P=2M=T。
第四种情形,P<1/2T时;此时M>P,因此M除代表由碳酸盐生成的重碳酸盐外,尚有水中原有的重碳酸盐。
碳酸盐=2P,重碳酸盐=T-2P。
第五种情形,P=0时;此时,水中只有重碳酸盐存在。
重碳酸盐=T=M。
以上五种情形的碱度示于表1中:表6-1 碱度的组成按下述公式计算各种情况下总碱度、碳酸盐、重碳酸盐的含量。
(1)总碱度(以CaO计,mg/L) =c(P+M)× 28.04×1000/V计,mg/L) =c(P+M)×50.05×1000/V总碱度(以CaCO3式中:c----盐酸标准溶液浓度(mol/L);28.04----氧化钙(1/2CaO)摩尔质量(g/mol)50.05----碳酸钙(1/2CaCO3)摩尔质量(g/mol)(2)当P=T时,M=02-)=0碳酸盐(CO3-)=0重碳酸盐(HCO3(3)当 P>1/2T 时碳酸盐碱度(以CaO计,mg/L)=c(T-P)×28.04×1000/ V计,mg/L)=c(T-P)×50.05×1000/ V 碳酸盐碱度(以CaCO32-,mol/L)=c(T-P)×1000/ V碳酸盐碱度(1/2CO3-)=0重碳酸盐碱度(HCO3(4)当P=1/2T时,P=M碳酸盐碱度(以CaO计,mg/L)=c·P×28.04×1000/V计,mg/L)=c·P×50.05×1000/V碳酸盐碱度(以CaCO32-,mol/L)=c·P×1000 / V重碳酸盐碱度(1/2CO3-)=0重碳酸盐碱度(HCO3(5)当P<1/2T时:碳酸盐碱度(以CaO计,mg/L)=c·P×28.04×1000/V碳酸盐碱度(以CaCO计,mg/L)=c·P×50.05×1000/V32-,mol/L)=c·P×1000/V碳酸盐碱度(1/2CO3重碳酸盐碱度(以CaO计,mg/L)=c·(T-2P)×28.04×1000/V计,mg/L)=c·(T-2P)×50.05×1000/V 重碳酸盐碱度(以CaCO3-,mol/L)=c·(T-2P)×1000/V重碳酸盐碱度(HCO3(6)当 P=0时2-)=0碳酸盐(CO3重碳酸盐碱度(以CaO计,mg/L)=c·M×28.04×1000/V重碳酸盐碱度(以CaCO计,mg/L)=c·M×50.05×1000/V3-,mol/L)=c·M×1000/V重碳酸盐碱度(HCO38.精密度和准确度-含量五个实验室对人工配制的统一标准进行方法验证的结果如下:在HCO3为43.50mg/L时,总碱度的室内相对标准偏差为0.71%;室间相对标准偏差为1.46%;相对误差为0.75%;加标回收率为99.6±7.5%。
取15个地表水水样进行测定,浓度范围在14.0~88.50mg/L时,相对标准偏差为0.1~1.4%,加标回收率为96.0~102%。
注意事项:(1)若水样中含有游离二氧化碳,则不存在碳酸盐,可直接以甲基橙作指示剂进行滴定。
(2)当水样中总碱度小于20mg/L时,可改用0.01mol/L盐酸标准溶液滴定,或改用 10mL 容量的微量滴定管,以提高测定精度。
9.参考文献《水和废水监测分析方法》编委会编,水和废水监测分析方法(第三版),pp.234~238,中国环境科学出版社,北京,1997。
