(完整版)高考化学燃料电池练习及答案.doc
高考化学一轮复习电化学专题03燃料电池练习(2021年整理)

2019年高考化学一轮复习电化学专题03 燃料电池练习编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(2019年高考化学一轮复习电化学专题03 燃料电池练习)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为2019年高考化学一轮复习电化学专题03 燃料电池练习的全部内容。
专题03 燃料电池1.在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(NO3−)以达到消除污染的目的。
其工作原理的示意图如下:下列说法不正确...的是A. Ir的表面发生反应:H2 + N2O == N2 + H2OB. 导电基体上的负极反应:H2-2e− == 2H+C. 若导电基体上只有单原子铜,也能消除含氮污染物D。
若导电基体上的Pt颗粒增多,不利于降低溶液中的含氮量【答案】C2.微生物燃料电池( MPC)处理技术是通过微生物的作用去除污染物,该技术可广泛应用于去除土壤中有机污染物。
一种土壤微生物燃料电池的纵截面如图所示,下列说法不正确的是A。
电流从活性炭电极经工作站流向碳纤维布电极B. 有机污染物在电池负极上氧化为对环境无害的物质C。
活性炭能有效吸附空气,提高电池的工作效率D。
该电池的正极反应式为O2+4e -↓+2H2O==4OH—【答案】D【解析】根据图示,活性炭电极通入空气,所以活性炭电极是正极,电流从活性炭电极经工作站流向碳纤维布电极,故A正确;电池负极失电子发生氧化反应,故B正确;活性炭的表面积大,能有效吸附空气,提高电池的工作效率,故C正确;微生物燃料电池含有质子交换膜燃,该电池的正极反应式为O2+4e -↓+4H+==2H2O,故D错误.3.某新型电池,以NaBH4(B的化合价为+3价)和H2O2作原料,负极材料采用Pt,正极材料采用MnO2(既作电极材料又对该极的电极反应具有催化作用),该电池可用作卫星、深水勘探等无空气环境电源,其工作原理如图所示。
高考化学原电池题型专项训练题(附答案)

高考化学原电池题型专项训练题(附答案)2017高考化学原电池题型专项训练题(附答案)在高考化学原电池题型训练中,大家首先要把基本概念理解到位,然后配合题型训练更好地掌握模块精髓。
以下是店铺搜索整理的一份高考化学原电池题型专项训练题(附答案),供参考练习,希望对大家有所帮助!想了解更多相关信息请持续关注我们店铺!高考化学原电池题型训练真题及答案例1.(江苏卷,T9)Mg-H2O2电池可用于驱动无人驾驶的潜航器。
该电池以海水为电解质溶液,示意图如下。
该电池工作时,下列说法正确的是A.Mg电极是该电池的正极B.H2O2在石墨电极上发生氧化反应C.石墨电极附近溶液的pH增大D.溶液中Cl-向正极移动【解析】:原电池的负极被氧化,镁为负极,而非正极,A选项错误;双氧水作为氧化剂,在正极(石墨)上发生还原反应,B选项错误;石墨电极上发生反应:H2O2+2e—+2H+=2H2O,消耗了H+,溶液PH值增大,C选项正确;溶液中Cl-向负极方向移动,D选项错误。
【答案】:C迁移训练1:(2013海南卷,T4)Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为:2AgCl+Mg=Mg2++2Ag+2Cl-。
有关该电池的说法正确的是A.Mg为电池的正极B.负极反应为AgCl+e-=Ag+Cl-C.不能被KCl溶液激活D.可用于海上应急照明供电例2.(全国理综II化学卷,T12)2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系。
下列叙述错误的是A.a为电池的正极B.电池充电反应为LiMn2O4=Li1-xMn2O4+xLiC.放电时,a极锂的化合价发生变化D.放电时,溶液中的Li+从b向a迁移【解析】由电池的结构知b为电池的负极,发生反应:Li-e-=Li+,a为电池的正极,A选项正确,a极发生反应:Li1-xMn2O4+Li++e-=LiMn2O4,电解质溶液中的Li+得到电子生成单质Li嵌入Li1-xMn2O4中生成LiMn2O4,所以,a极锂的价态没有改变,C选项错误;放电时,总反应为:Li1-xMn2O4+xLi=LiMn2O4,所以,电池充电反应为LiMn2O4=Li1-xMn2O4+xLi;B选项正确;LiMn2O4中的`Mn 元素化合价发生变化,放电时,Li+向正极移动,D选项正确§。
2019届高考化学最有效的解题方法难点【23】燃料电池(含答案)

2018高考化学最有效的解题方法难点23 燃料电池燃料电池两电极都不参加反应,反应的是通到电极上的燃料和氧气,电极反应式的书写有难度。
●难点磁场请试做下列题目,然后自我界定学习本篇是否需要。
熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为阳极燃气,空气与CO2的混合气为阴极助燃气,制得在650 ℃下工作的燃料电池,完成有关的电池反应式:负极反应式:2CO+2CO-23−→−4CO2+4e-正极反应式:。
总电池反应式:。
●案例探究[例题]某原电池中盛有KOH浓溶液,若分别向________(填“正”或“负”,下同)极通入可燃性气体,向________极通入O2,则电路中就有电流通过,试完成下列问题:(6)知识依托:原电池原理和氧化还原反应原理。
错解分析:忽视电解质溶液是KOH溶液,误以为负极能放出酸性气体。
解题思路:燃料电池中,负极通入的气体具有可燃性,在反应中失去电子,被氧化到较高价态:氢元素将被氧化到最高价:+1价,在碱性溶液中产物不是H+,而是H2O——H+与OH-结合的产物。
H2S中硫元素,含碳物质中的碳元素将被氧化到+4价,而+4价的硫(或+4价的碳)又不能单独存在,在其常见形式SO2和SO-23 (或CO2和CO-23)中,因周围环境显碱性生成酸性氧化物是不可能的,产物应为SO-23(或CO-23),O2-由谁来提供?显然是OH-,提供O2-后裸离的H+怎么办?与别的OH-结合生成H2O。
若燃料中含有+1价的氢元素,则它反应前后的价态不变(都是+1价),氢元素反应前在含碳燃料中,反应后在生成物水中。
负极电极反应式可根据电荷守恒而配平。
燃料电池中,正极通入的O2得电子被还原,成为O2-。
O2-4e-====2O2-O2-被H2O分子俘获变为OH-:H2O+O2-====2OH-将正、负两极电极反应式叠加,可得电池总反应。
根据电池总反应可判定电解质溶液pH的变化。
2019高考化学难点剖析专题43燃料电池练习

专题43燃料电池1. (2017-2018学年浙江省温州六校协作体第一学期期末联考)甲醇燃料电池由于结构简单、能量转化率高、 对环境无污染,可作为常规能源的替代品而越来越受到关注,其工作示意图如下,其总反应为 2CH 30H+ 302===2C02+4H2°。
下列说法不正确的是()质子交换膜A.电极A 是负极,物质a 为甲醇B.电池工作时,电解液中的H+通过质子交换膜向B 电极迁移C.放电前后电解质溶液的pH 增大D. b 物质在电极上发生的电极反应式为:O 2+4e-+2H 2O = 4OH- 【答案】D【解析】甲醇的燃料电池,甲醇在负极被氧化,氧气在正极被还原S 电子由A 流出经过导线流入E,电极A 是负极,物质a 为甲酯,A 正确」H-应该向正极(B 电极)移动,B 正确s 负极反应:2CHQH-1%-+2H2O2coJ+12H+,正极反应3<^-12e--12H-=6H 2O,反应前后H 卡总量没变,但是反应后生 成了水,造成了 H+的浓度减小,电解质溶淹的pH 增大,C 正确A 酸性环境下,氧气在B 电极上发生的电 极反应式为:Or4-MH+=2H?O , D 错误口2. (2018届湖南省衡阳市高三下学期第三次联考)微生物燃料电池(MPC )处理技术是通过微生物的作用去 除污染物,该技术可广泛应用于去除土壤中有机污染物。
一种土壤微生物燃料电池的纵截面如图所示,下 列说法不正确的是A.电流从活性炭电极经工作站流向碳纤维布电极催化剂 用电器 |c ,催化剂B.有机污染物在电池负极上氧化为对环境无害的物质C.活性炭能有效吸附空气,提高电池的工作效率D.该电池的正极反应式为02+4e - ;+2H20==40H-【答案】D【解析】根据图示,活性炭电极通入空气,所以活性炭电极是正极,电流从活性炭电极经工作站流向碳纤维布电极,A正确/电池负极失电子发生氧化反应,E正确s活性炭的表面积大,能有效吸附空气,提高电池的工作效率,C正确?微生物燃料电池含有质子交换膜燃,该电池的正极反应式为g血-1MH+—2HQ, D错误。
高考化学全国卷Ⅰ专题———燃料电池
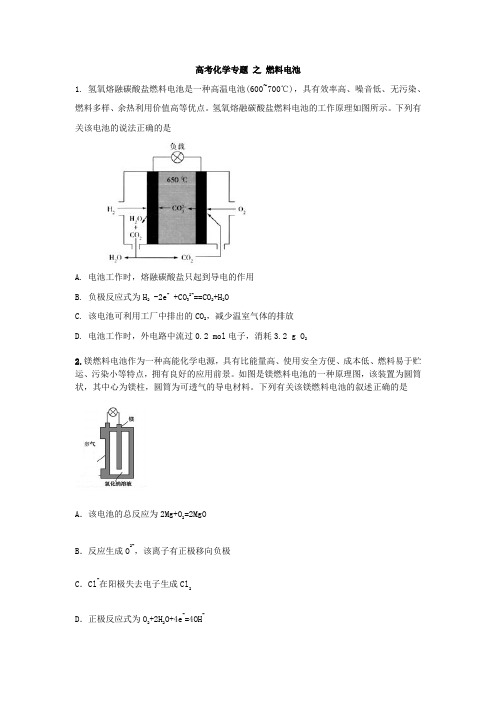
高考化学专题之燃料电池1. 氢氧熔融碳酸盐燃料电池是一种高温电池(600~700℃),具有效率高、噪音低、无污染、燃料多样、余热利用价值高等优点。
氢氧熔融碳酸盐燃料电池的工作原理如图所示。
下列有关该电池的说法正确的是A. 电池工作时,熔融碳酸盐只起到导电的作用B. 负极反应式为H2 -2e- +CO32-==CO2+H2OC. 该电池可利用工厂中排出的CO2,减少温室气体的排放D. 电池工作时,外电路中流过0.2 mol电子,消耗3.2 g O22.镁燃料电池作为一种高能化学电源,具有比能量高、使用安全方便、成本低、燃料易于贮运、污染小等特点,拥有良好的应用前景。
如图是镁燃料电池的一种原理图,该装置为圆筒状,其中心为镁柱,圆筒为可透气的导电材料。
下列有关该镁燃料电池的叙述正确的是A.该电池的总反应为2Mg+O2=2MgOB.反应生成O2-,该离子有正极移向负极C.Cl-在阳极失去电子生成Cl2D.正极反应式为O2+2H2O+4e-=4OH-3.一种新型燃料电池,是用两根金属铂做电极插入KOH溶液中,然后向两极上分别通入CH3OH和O2,下解说法不正确的是A.通入CH3OH的电极为负极B.随着放电的进行,负极附近pH上升C.每消耗1molCH3OH可以向外电路提供6mol e-D.通入O2的一极电极反应为 4H2O+2O2-8e-=8OH-4.微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。
下列有关微生物电池的说法错误的是A.正极反应中有CO2生成B.微生物促进了反应中电子的转移C.质子通过交换膜从负极区移向正极区D.电池总反应为C6H12O6+6O26CO2+6H2O5.如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面图.下列说法正确的是()A.该电化腐蚀为析氢腐蚀.B.C.D.7.太阳能光电池由于具有可靠性好、寿命长等特点,适于很多特蛛环境和场合,现已得到广泛应用。
燃料电池(高考真题高考试题)

燃料电池1.氢氧燃料电池的突出优点是把化学能直接转变为电能,而不经过热能这一中间形式,已用于宇宙飞船及潜艇中,其电极反应为:负极:2H2+4OH--4e-4H2O正极:O2+2H2O+4e-4OH-所产生的水还可作为饮用水,今欲得常温下1 L水,则电池内电子转移的物质的量约为()-3 mol-2 mol2 mol2.质子交换膜燃料电池(PEMFC)常作为电动汽车的动力源。
该燃料电池以氢气为燃料,空气为氧化剂,铂作催化剂,导电离子是H+。
下列对该燃料电池的描述中正确的是()①正极反应为:O2+4H++4e-2H2O②负极反应为:2H2-4e-4H+③总的化学反应为:2H2+O22H2O④氢离子通过电解质向正极移动A.①②③B.②③④C.①②④D.①②③④3.美国加州Miramar海军航空站安装了一台250 kW的MCFC型燃料电池,该电池可同时供应电和水蒸气,其工作温度为600~700 ℃,所用燃料为H2,电解质为熔融的K2CO3。
该电池的总反应为2H2+O22H2O,负极反应为H2+C-2e-H2O+CO2。
则下列推断中正确的是()A.正极反应:4OH--4e-2H2O+O2↑B.当电池生成1 mol H2O时,转移4 mol电子C.放电时C向负极移动D.放电时C向正极移动4.有四种燃料电池:A.固体氧化物燃料电池 B.碱性氢氧化物燃料电池 C.质子交换膜燃料电池 D.熔融盐燃料电池,下面是工作原理示意图,其中正极反应生成水的是()5.固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。
它以固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。
该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。
下列判断正确的是()A.有O2放电的a极为电池的负极B.有H2放电的b极为电池的正极C.a极对应的电极反应为O2+2H2O+4e-4OH-D.该电池的总反应方程式为2H2+O22H2O6.一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CH3CH2OH-4e-+H2O CH3COOH+4H+。
2020届高三化学一轮复习——各种各样的“燃料电池”专题训练(有答案和详细解析)

2020届高三化学一轮复习——各种各样的“燃料电池”专题训练(有答案和详细解析)一、选择题1.某航空站安装了一台燃料电池,该电池可同时提供电和水蒸气。
所用燃料为氢气,电解质为熔融的碳酸钾。
已知该电池的总反应为2H 2+O 2===2H 2O ,正极反应为O 2+2CO 2+4e -===2CO 2-3,则下列推断正确的是( )A .负极反应为H 2+2OH --2e -===2H 2OB .该电池可在常温或高温时进行工作,对环境具有较强的适应性C .该电池供应2 mol 水蒸气,同时转移2 mol 电子D .放电时负极有CO 2生成 答案 D解析 由总反应式减去正极反应式得到负极反应式:2H 2+2CO 2-3-4e -===2H 2O +2CO 2,则可判断负极有CO 2生成,A 项错误,D 项正确;该电池使用的电解质是熔融的碳酸钾,在常温下无法工作,B 错误;该电池供应2 mol 水蒸气时,转移的电子为4 mol ,C 错误。
2.一种新型燃料电池,以镍板为电极插入KOH 溶液中,分别向两极通入乙烷(C 2H 6)和氧气,其中某一电极反应式为C 2H 6+18OH --14e -===2CO 2-3+12H 2O 。
有关此电池的推断不正确的是( ) A .通入氧气的电极为正极B .参加反应的O 2与C 2H 6的物质的量之比为7∶2 C .放电一段时间后,KOH 的物质的量浓度将下降D .放电一段时间后,正极区附近溶液的pH 减小 答案 D解析 A 项,通入乙烷的一极为负极,通入氧气的一极为正极,正确;B 项,1 mol 乙烷参与反应时转移14 mol 电子,则参与反应的氧气的量为14 mol 4=72 mol ,正确;C 项,根据电极反应式或总反应方程式可知,氢氧化钾被消耗,正确;D 项,放电时正极产生OH -,则pH 增大,错误。
3.关于如图微生物燃料电池结构示意图的说法:①微生物促进了电子的转移 ②微生物所在电极区放电时发生还原反应 ③放电过程中,H +从正极区移向负极区 ④正极反应式为:MnO 2+4H ++2e -===Mn 2++2H 2O ,正确的是( )A.④B.①③C.①④D.②③答案C解析①在微生物作用下C m(H2O)n转化为CO2促进电子的转移,正确;②微生物在右侧,右侧电极为电源的负极,所以微生物所在电极区放电时发生氧化反应,错误;③根据电流的方向,放电过程中,H+从负极区移向正极区,错误;④电池左侧为电池的正极区,MnO2在H+条件下发生得电子反应,所以正极反应式为:MnO2+4H++2e-===Mn2++2H2O,正确。
高二化学上学期原电池燃料电池精选习题(附答案)

2020年03月17日高二化学上学期原电池燃料电池精选习题学校:___________注意事项: 2、请将答案正确填写在答题卡上第1卷一、单选题Zn+2NH Cl+2MnO=Zn(NH)Cl+2MnO(OH)。
下列说法不正确的其电池反应方程式为42322是( )A.石墨作正极B.锌发生氧化反应C.电池工作时,电子从石墨经导线流向锌NH+MnO+e=MnO(OH)+NHD.正极的电极反应为+-4232、锌锰干电池在放电时,电池总反应方程式可以表示为:Zn + 2MnO 2 + 2NH 4+= Zn 2++ Mn 2O 3 + 2NH 3 + H 2O在此电池放电时,正极(碳棒)上发生反应的物质是A.Zn B.碳棒C.MnO2和NH4+D.Zn2+和NH4+3、锌锰干电池在放电时,电池总反应方程式可以表示为Zn+2MnO 2+2NH 4+=Zn 2++Mn 2O 3+2NH 3+H 2O。
在此电池放电时,正极(碳棒)上发生反应的物质是( )A.MnO2和NH4+B.Zn2+和NH4+C.Zn D.碳棒4.据报道,美国正在研究用锌电池取代目前广泛使用的蓄电池,它具有容量大、污染小的特点,其电池反应为:2Zn+O2=2ZnO ,其原料为锌、空气和碱性电解质溶液,则下列叙述正确的是()A.锌为正极,空气在负极反应B.负极还原反应,正极氧化反应C.负极的电极反应为:Zn + 2OH- -2e-=ZnO + H2OD.电池工作时溶液的pH 升高5.A、B、C、D分别为固体氧化物燃料电池、碱性氢氧燃料电池、质子交换膜燃料电池、熔融盐燃料电池,其中正极的反应产物为水的是( )A.B.C.D.6.某固体酸燃料电池以4NaHSO 固体为电解质传递+H ,其基本结构见图,电池总反应可表示为: 222H +O 22H O ,下列有关说法正确的是( )A.电子通过外电路从b 极流向a 极B. +H 由a 极通过固体酸电解质传递到b 极C.b 极上的电极反应式为: 22O +2H O+4e -4OH -D.每转移0.1mol 电子,消耗1.12L 的2H7.某原电池装置如图所示,阳离子交换膜电池总反应为22Ag+Cl =2AgCl 。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高考化学燃料电池1.“直接煤燃料电池”能够将煤中的化学能高效、清洁地转化为电能,下图是用固体氧化物作“直接煤燃料电池”的电解质。
有关说法正确的是A. 电极 b 为电池的负极B.电池反应为: C + CO2 = 2COC.电子由电极 a 沿导线流向 bD.煤燃料电池比煤直接燃烧发电能量利用率低2.如图所示是一种以液态肼(N 2H4)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。
该固体氧化物电解质的工作温度高达700 -900℃时,O2 -可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。
下列说法正确的是A. 电池内的O2 -由电极乙移向电极甲B. 电池总反应为N2H4+2O2= 2NO+2H 2OC. 当甲电极上有lmol N 2 H4消耗时,乙电极上有22.4LO 2参与反应D.电池外电路的电子由电极乙移向电极甲3.硼化钒( VB2) -空气电池是目前储电能力最高的电池,电池示意图如下。
该电池工作时的反应为 4VB 2+ 11O 2=4B 2O3+2V 2O5。
下列说法正确的是A. 电极 a 为电池负极B. 反应过程中溶液的pH 升高C.电池连续反应过程中,选择性透过膜采用阳离子选择性膜D.VB2极的电极反应式为: 2VB 2 + 22OH - -22e - =V 2O5+ 2B2 O3+ 11H 2O4.以 NaBH4和 H2 O2作原料的燃料电池,可用作空军通信卫星。
电池负极材料采用Pt/C ,正极材料采用MnO 2,其工作原理如下图所示。
下列说法错误..的是A.电池放电时 Na+从 a 极区移向 b 极区B.电极 b 采用 Pt/C ,该极溶液的 pH 增大C.该电池 a 极的反应为 BH 4- +8OH--8e-===BO 2-+6H 2OD.电池总反应: BH4- + 4H 2 O2 === BO2- + 6H2O5.科学家设想以N2和 H2为反应物,以溶有 A 的稀盐酸为电解质溶液,可制造出既能提供电能又能固氮的新型电池,其装置如图所示,下列说法不正确的是A. 电路中转移3mol 电子时,有11.2LN 2参加反应B. A 为 NH4 ClC. 该电池外电路中的电流从 a 电极流向 b 电极D. b 电汲为负极6.一种基于酸性燃料电池原理设计的酒精检测仪,电池反应的化学方程式为:CH3CH2OH+O2=CH3 COOH+H2 O.下列有关说法不正确的是()A. 检测时,电解质溶液中的H+向正极移动B. 若有0.4 mol 电子转移,则消耗 2.24 L 氧气C.正极上发生还原反应,负极上发生氧化反应﹣D. 负极上的反应为:CH3CH2 OH﹣ 4e +H 2O℃ CH3COOH+4H+7.乙烯直接氧化法制乙醛的总反应方程式为2CH2 =CH2+O22CH3CHO。
现有人将该反应设计成如图所示的燃料电池,下列有关说法正确的A. a 为负极,发生还原反应B. 电子移动方向:电极a→磷酸溶液→电极 bC. 放电时,电路中每转移0.4mol 电子,溶液中就有0.4molH +向负极迁移D. 该电池负极反应式为CH2=CH2 +H2O℃ 2e ˉ =CH3CHO+2H +8.氢氧燃料电池已用于航天飞机,以30%KOH溶液为电解质溶液的这种电池在使用时的电极反应如下: 2H 2+4OH --4e-=4H 2 O, O2+2H 2O+4e -= 4OH -。
下列叙述不正确的是A. 氢氧燃料电池能量转化率可达100%B.是一种不需要将还原剂和氧化剂全部贮存在电池内的新型发电装置C.供电时的总反应为: 2H 2+O2=2H 2 O,产物为无污染的水,属于环境友好电池D.氧气在正极反生还原反应9.一种新型熔融碳酸盐燃料电池原理示意如图。
下列有关该电池的说法正确的是()A. 催化重整中 CH +H O=3H2 +CO℃ 1 mol CH 参加反应转移 2 mol 电子4 2 4B. 电极 A 上 H2参与的电极反应为:H2+2OH --2e-=2H 2OC. 电池工作时, CO32 -向电极 B 移动D. 电极 B 上的电极反应:O2 +2CO2+4e - =2CO32 -10 .℃ Nature》期刊曾报道一例CH3OH-O2原电池,其工作示意图如下℃下列说法不正确的是A. 电极 A 是负极,发生氧化反应B. 电解质溶液中H+由 A 极流向 B 极C.电极 B 的电极反应为 : O2 +2e -+H+=HO2-D.外电路中通过 6mol 电子,生成 CO2的体积为 22.4L11 .熔融碳酸盐燃料电池(Molen Cathomale Fuel Cell)简称MCFC,具有高发电效率。
工作原理示意图如图。
下列说法正确的是A. 电极 M 为负极, K+、 Na+移向 MB. 电池工作时,熔融盐中CO32 -物质的量增大C. A 为 CO2,正极的电极反应为:O2 +4e- +2CO2 = 2CO32-D. 若用 MCFC 给铅蓄电池充电,电极N 接 Pb 极12.下图是某碱性氢氧燃料电池的工作原理示意图,下列说法错误的是A. 气体 2是氧气B. C1极为电源负极C.负极上的电极反应式为 H2 -2e- ==2H +D.装置中能量转化形式有 :化学能→电能、电能→光能13.液体燃料电池相对于气体燃料电池具有体积小,无需气体存储装置等优点。
一种以肼(N2 H4) 为燃料的电池装置如图所示。
该电池用空气中的氧气作为氧化剂,H2SO4作为电解质。
下列关于该燃料电池的叙述正确的是()A.电流从左侧电极经过负载后流向右侧电极B. 该燃料电池正极发生的电极反应式为N H -4e - N ↑+4H2 4 2C. 利用该燃料电池工业上可以电解熔融MgCl2 制备 MgD. 该燃料电池持续放电时,右侧电池区中因电极反应消耗H+,故 c(H + )逐渐减小14 .已知: 2H 2S(g)+O2 (g) = S 2 (s)+2H 2 O(l) ℃ H=- 632 kJ?mol -1,如图为质子膜H2S 燃料电池的示意图。
下列说法正确的是A. 电极 a 上发生的电极反应式为:H2S - 2e- = S+2H+B. 电池工作时,电流从电极 b 经过负载流向电极 aC. 电路中每流过 1 mol 电子,电池内部释放158 kJ 的热能D.每 11.2 LH 2S 参与反应,有 1 mol H +经固体电解质膜进入正极区15 .在固态金属氧化物燃料电解池中,以H2— CO 混合气体为燃料,基本原理如右图所示。
下列说法不正确的是A. Y 极是原电池的正极,发生还原反应B. 负极的电极反应式是:2 2H2℃ 2e ˉ℃Oˉ℃H2O CO℃ 2e ˉ℃O2COC.总反应可表示为: H2℃ CO℃O2℃H2 O℃ CO2D.同温同压下两极消耗的气体的体积之比是1℃116 .二甲醚( CH3OCH3)燃料电池的工作原理如右图,有关叙述正确的是A. 该装置能实现化学能100% 转化为电能B. 电子移动方向为: a 极→b极→质子交换膜→a极C. a电极的电极反应式为:CH3 OCH3+3H 2 O=2CO2+12e -+12H +D. 当 b 电极消耗 22.4LO 2时,质子交換膜有4moIH +通过17 .某种熔融碳酸盐燃料电池以Li 2CO3和 K2CO3为电解质、以CH4为燃料,该电池的工作原理如下图所示,下列说法正确的是A. 电极 a 为负极,发生氧化反应B. CO32-向正极移动C. 正极电极反应式为 O2+2H 2 O+4e- =4OH-D. 此电池在常温下也能工作18 .在固态金属氧化物燃料电池中,以H2-CO混合气体为燃料 ,基本原理如图所示。
下列说法不正确的是A. X 极是原电池的负极,发生氧化反应B. 负极的电极反应式为H 2-- 2e -===H 2--2e -===CO+O O℃CO+O2 2 2C. Y 极每消耗16gO2,电路中有 2mol 电子通过D. 同温同压下两极消耗的气体体积之比是1:119.燃料电池是目前电池研究的热点之一。
现有某课外小组自制的氢氧燃料电池,如图所示, a、 b 均为惰性电极。
下列叙述错误的是A.a 电极是负极,该电极上发生氧化反应B.b 极反应是 O2+2H 2O-4e-=4OH-C.总反应方程式为 2H2 +O2 =2H 2OD.使用过程中电解质溶液的 pH 逐渐减小20 .甲醇 -空气燃料电池(DMFC)是一种高效能、轻污染电动汽车的车载电池,该燃料电池的电池反应式为:2CH3OH(l) + 3O2 (g)→ 2CO(g) + 4H2O(l),其工作原理示意图如图,下列说法正确的是()A.甲为电池的负极,发生还原反应B.负极的电极反应式为: CH3OH + H2 O- 6e-= CO2+ 6H +C.b 口通入的气体为 O2D. 用该电池进行电解水,当电路中转移0.2N A个电子时,生成 2.24L 氢气21 .肼 (N 2H4 )-空气燃料电池是一种环保型碱性燃料电池,电解质溶液是20%~30% 的 KOH 溶液。
电池总反应为N2H4+O 2=N 2+2H 2O。
下列关于该燃料电池工作时的说法正确的是()A. 负极的电极反应式是N2 H4+4OH --4e- =4H 2O+N2↑B. 正极的电极反应式是O2+4H ++4e -=2H 2 OC.溶液中阴离子向正极移动D.放电后电解质溶液的碱性增强22.燃料电池型呼气酒精测试仪具有稳定性好,精度高,抗干扰性好等优点,是专门为警察设计的一款执法的检测工具,如图所示是一种酸性燃料电池酒精检测仪的示意图。
下列说法错误的是(℃A. 该电池的负极反应式为:CH3CH2OH-4e-+H2O=CH3COOH+4H+B. 当电路中有0.4mol 电子转移时,消耗 3.2gO2C.电池工作时 H+从右向左通过质子交换膜D.微处理器通过检测电流大小可计算出被测气体中酒精的含量23.酒精检测仪可帮助执法交警测试驾驶员饮酒的多少,其工作原理示意图如图所示。
反应原理为: CH3CH2 OH+O2=CH3 COOH+H2O,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量。
下列说法不正确的是...A. b 为正极,电极反应式为:O2+2H 2 O+4e-=4OH-B. 电解质溶液中的H+移向 b 电极C. 若有 0.4mol 电子转移,则在标准状况下消耗 2.24L 氧气D.呼出气体中酒精含量越高,微处理器中通过的电流越大24.℃℃℃℃℃℃℃℃℃℃℃℃2CO3℃K2CO3Li℃℃℃℃℃℃4℃℃℃℃℃℃℃℃℃℃℃℃℃℃℃℃℃℃℃℃℃℃℃℃CHA.℃℃℃℃℃℃℃℃O2+2C2+4e-=2CO32-B. CO32-℃℃℃℃℃C.℃℃℃℃℃℃℃℃℃℃℃D.a ℃ CH4℃ b℃ CO225 .新型 NaBH /H O 燃料电池 (DBFC) 的结构如图所示,该电池总反应方程式:NaBH4 2 24+4H 2 O2=NaBO2 +6H 2O,有关的说法不正确的是A.纳米 MnO 2层的作用是提高原电池的工作效率B.放电过程中, Na+从 B 极区移向 A 极区C. 电池负极的电极反应为:一BH4 +8OH - - 8e =BO2-+6H 2OD. 在电池反应中,每消耗1L 1mol / L H2O2溶液,理论上流过电路中的电子为2 mol1.C2.A4.B5.A6.B7.D8.A9.D10. D11. C12. C13. C14. B15. D16. C17. A18. D19. B20. B21. A22. C23. A24. A25. B11。
