2017届高三化学有机化学专题复习
2017届高三化学总复习课件九

反应制取(CH3)3CCl
在镍作催化剂的条件下,苯与 氢气反应生成环己烷 在银作催化剂的条件下,乙醇 与空气中的氧气反应生成乙醛 乙酸乙酯在酸作催化剂条件下 与水反应生成乙醇和乙酸
B
C
D
解析:A项中反应Ⅰ为取代反应,反应Ⅱ为加成反应。B项中均为
加成反应。C项中反应 Ⅰ为氧化反应,反应Ⅱ为加聚反应。D项中反应 Ⅰ为取代反应,反应Ⅱ为加成反应。
解析: (1) 已知 A 是乙醇分子的比例模型,然后比较观察得出 B 是乙 酸,D是水。然后就应想到 C是乙酸乙酯。(2)酯化反应的反应条件为加浓
硫酸和加热。 (3) 在这样的酯化反应中,醇分子里断裂的化学键是 O—H
键,则 18O 应在乙酸乙酯分子中。 (4) 乙酸分子里的 2 个碳原子和 2 个氧原 子,都是最外层电子数为8的原子。
(4)气态烃完全燃烧时,若温度低于 100 ℃,则反应后的气体体积一定 y 减少 1+4 体积,若温度高于 100 ℃时,则有:y=4 时,完全燃烧前后气体 的体积不变;y<4 时,完全燃烧后气体的体积减小;y>4 时,完全燃烧后气 体的体积增大。
现有 CH4 、 C3H4 、 C2H4 、 C2H6 、 C3H6 五种有机物。同质 CH4 量的以上物质中,在相同状况下体积最大的是________ ;同质量的以上物 CH4 质完全燃烧时耗去O2的量最多的是________ ;同状况、同体积的以上五种 C 物质完全燃烧时耗去O 的量最多的是 ________ ;同质量的以上五种物质燃 3 H6
4.氧化反应 有机物得氧或去氢的反应。
如有机物在空气中燃烧,乙醇转化为乙醛,葡萄糖与新制氢氧化铜
悬浊液的反应,乙烯使酸性高锰酸钾溶液褪色等都属于氧化反应。 5.还原反应
(完整word版)2017届高三化学有机化学专题复习

2017届高三化学有机化学专题复习考点1:通过计算推出分子式或结构式例题1:A 的蒸气密度为相同状况下氢气密度的77倍,有机物A 中氧的质量分数约为41。
6%,则A 的分子式为_________。
例题2:某烃A 的相对分子质量在90到100之间,1molA 完全燃烧可以产生4molH 2O ,则A 的分子式为。
例题3:某羧酸酯的分子式为C 18H 26O 5,1mol 该酯完全水解可得到1mol 羧酸和2mol 乙醇,该羧酸的分子式为____________。
方法小结:1。
看清组成元素2、先确定原子量较大的原子数目 3.分子式中:C :H>=n:2n+2 强化训练1:1、已知有机物B 中含有C ,H ,O 元素,其与H 2的相对密度为23,分子中碳、氢原子个数比为1:3有机物B 的分子式为。
2、 A 的相对分子质量是104,1molA 与足量NaHCO 3反应生成2mol 气体,其结构式为________。
3、 1mol 丁二酸和1mol 丙二醇反应生成环酯类的分子式为_____________.考点2:分子式和耗氧量、核磁共振氢谱、官能团名称和性质判断 例题1:化合物I ()的分子式为,1mol 该物质完全燃烧最少需要消耗molO 2. 例题2:的分子式为__________,含有的官能团有_____________________,1mol 该有机物可以消耗______molBr 2,________molNaOH 。
例题3:化合物I()的分子式为,其核磁共振氢谱有组峰,分子中官能团的名称为。
强化训练:1、 化合物A 结构如下图所示,该化合物的分子式为______,1mol 该有机物燃烧需要消耗______molO 2,最多可以消耗______molH 2和_________molBr 2。
2、香兰素()除了醚键之外,还含有的官能团名称..是 ,1mol 香兰素最多可与molH 2发生加成反应。
2017届高考化学第一轮知识点总复习课件36(第十一章_有机化学基础(选修)_烃的含氧衍生物)

• (3)醇的分类。
本ppt来自:千教网()
• 2.醇类 • (1)概念:
• 羟基与烃C基nH或2n+2苯O(n环≥1侧) 链上碳原子相连的化合 物称为醇,饱和一元醇的分子通式为 _____________________。
• ③毒性。
本ppt来自:千教网()
(3)化学性质。 ①羟基上氢原子的性质。 a.弱酸性: 电离方程式:___C_6_H_5_O__H____C__6H__5_O_-_+__H__+_____,俗称_石__炭___酸__,酸性 很弱,不能使石蕊试液变红; b.与活泼金属反应: 与 Na 反应的化学方程式为: __2_C_6_H_5_O__H_+__2_N__a_―_→__2_C__6H__5_O_N__a_+__H_2_↑_; c.与碱的反应: 苯酚的浑浊液中加入N―a―O→H溶液现象为:__溶__液__变__澄__清__再通入――CO→2气体 现象为:_溶__液__又__变__浑__浊___。
互影响。 • 3.结合实际了解某些有机化合物对环境和健
康可能产生的影响,关注有机化合物的安全 使用问题。
本ppt来自:千教网()
•考点一 醇和酚
知识梳理
1.醇、酚的概念 (1)醇是羟基与_烃__基___或_苯__环__侧__链___上的碳原子相连的化合物,饱和一 元醇的分子通式为___C_n_H__2n_+_1_O__H_(_n_≥_1_)___。 (2)酚是羟基与苯环__直__接__相连而形成的化合物,最简单的酚为苯酚 (________________)。
本ppt来自:千教网()
该过程中发生反应的化学方程式分别为: __________________________________________________________, _________________________________________________________。
【五年高考三年模拟】2017届高三化学新课标一轮复习练习:专题二十五 有机化学基础 Word版含解析

专题二十五有机化学基础考点一烃及烃的衍生物的结构与性质12.(2015海南单科,18-Ⅰ,6分)下列有机物的命名错误..的是( )答案BC按照系统命名法的命名原则,A、D正确;B项,应为3-甲基-1-戊烯;C项,应为2-丁醇。
13.(2013山东理综,10,4分)莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是( )A.分子式为C7H6O5B.分子中含有2种官能团C.可发生加成和取代反应D.在水溶液中羧基和羟基均能电离出H+答案C由莽草酸的结构简式可推出其分子式为C7H10O5,A项错误;其含有的官能团是碳碳双键、羧基、羟基,碳碳双键可发生加成反应,羟基和羧基可发生取代反应,B项错误,C项正确;在水溶液中羧基能电离出H+,羟基不能电离出H+,D项错误。
14.(2013江苏单科,12,4分)药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:+乙酰水杨酸对乙酰氨基酚+H2O贝诺酯下列有关叙述正确的是( )A.贝诺酯分子中有三种含氧官能团B.可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚C.乙酰水杨酸和对乙酰氨基酚均能与NaHCO3溶液反应D.贝诺酯与足量NaOH溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠答案B贝诺酯分子中只有酯基和肽键两种含氧官能团,A项错误;乙酰水杨酸中不含酚羟基,对乙酰氨基酚中含酚羟基,B项正确;对乙酰氨基酚不能与NaHCO3溶液反应,C项错误;贝诺酯与足量NaOH溶液共热,最终生成、、CH3COONa三种物质,D项错误。
15.(2012北京理综,11,6分,★★)下列说法正确的是( )A.天然植物油常温下一般呈液态,难溶于水,有恒定的熔点、沸点B.麦芽糖与蔗糖的水解产物均含葡萄糖,故二者均为还原型二糖C.若两种二肽互为同分异构体,则二者的水解产物不一致D.乙醛、氯乙烯和乙二醇均可作为合成聚合物的单体答案D A项,天然植物油的主要成分为高级脂肪酸甘油酯,有单甘油酯、混甘油酯等,属混合物,故无恒定的熔点、沸点;B项,麦芽糖是还原型二糖,蔗糖不是还原型二糖;C项,H2N—R1—CONH—R2—COOH与H2N—R2—CONH—R1—COOH互为同分异构体,水解产物相同;D项,乙醛能与酚类发生类似甲醛与苯酚的缩聚反应。
江苏省建湖县第二中学2017届高三化学复习:有机化合物

专题2第一单元有机化合物的结构课时11.二氟甲烷是性能优异的环保产品,它可替代某些会破坏臭氧层的“氟里昂”产品,用作空调、冰箱和冷冻库等中的致冷剂。
试判断二氟甲烷的核磁共振氢谱共有多少个峰( )A.4 B.3C.2 D.12.Fe(C5H5)2的结构如右图,其中氢原子的化学环境完全相同。
但早期人们却错误地认为它的结构为:。
核磁共振法能够区分这两种结构。
在核磁共振氢谱中,正确的结构与错误的结构核磁共振氢谱的峰分别为 ( )A.5,5 B.3,5C.5,1 D.1,33.下列各化合物中有无手性碳原子?(若有,用*标记手性碳原子)4.某有机化合物结构如下,分析其结构并完成下列问题。
(1)写出其分子式________。
(2)其中含有________个不饱和碳原子。
(3)分子中不同原子间形成的共价键有_____ __。
(4)分子中的饱和碳原子有________个;一定与苯环处于同一平面的碳原子有________个(不包括苯环碳原子)。
5.如下图所示,乙酸跟乙醇在浓硫酸存在并加热的条件下发生酯化反应(反应A),其逆反应是水解反应(反应B)。
反应可能经历了生成中间体(Ⅰ)这一步。
(1)A ~F 六个反应中(将字母代号填入下列横线上),属于取代反应的是________;属于加成反应的是________。
(2)中间体(Ⅰ)属于有机物的________类。
(3)如果将原料C 2H 5OH 中的氧原子用18O 标记,则生成物乙酸乙酯中是否有18O ?如果将原料中羧羟基中的氧原子用18O 标记,则生成物H 2O 中的氧原子是否有18O ?试简述你作此判断的理由 。
6.为测定一种气态烃的化学式,取一定量的A 置于密闭容器中燃烧,定性实验表明产物是CO 2、CO 和水蒸气。
学生甲、乙设计了如下两个方案,均认为根据自己的方案能求出A 的最简式。
他们测得的有关数据如下(图中的箭头表示气体的流向,实验前系统内的空气已排除):甲方案:燃烧产物――→浓硫酸增重――→碱石灰增重――→点燃生成CO 22.52 g 1.32 g 1. 76 g乙方案:燃烧产物――→碱石灰增重――――→灼热CuO 减轻――→石灰水增重5.6 g 0.64 g 4 g试回答:(1)根据两方案,你认为能否求出A 的最简式(填“能”或“不能”)?甲方案:________;乙方案:________。
有机化学Ⅰ复习题(给教师2017)
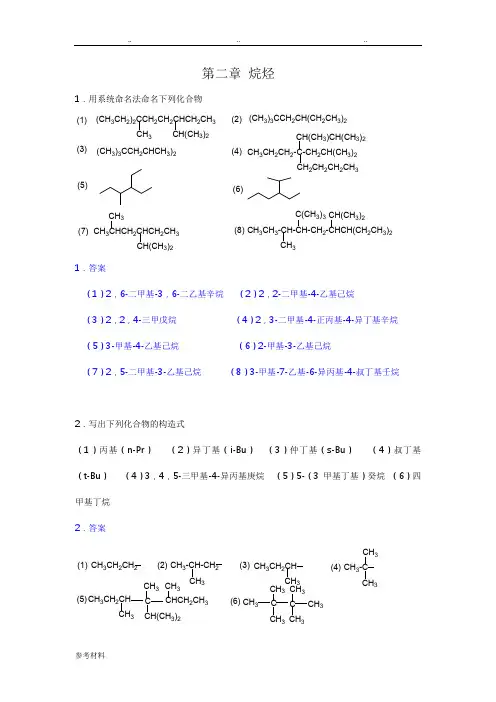
第二章烷烃1.用系统命名法命名下列化合物(CH3CH2)2CCH2CH2CHCH2CH333)2(CH3)3CCH2CH(CH2CH3)2CH3CH2CH2-C-CH2CH(CH3)2CH(CH3)CH(CH3)2CH2CH2CH2CH3(1)(2) (3)(4)(5)(6)(CH3)3CCH2CHCH3)2CH32CHCH2CH3CH3CH(CH3)2CH3CH3-CH-CH-CH22CH3)2C(CH3)3CH(CH3)2CH3(7)(8)1.答案(1)2,6-二甲基-3,6-二乙基辛烷(2)2,2-二甲基-4-乙基己烷(3)2,2,4-三甲戊烷(4)2,3-二甲基-4-正丙基-4-异丁基辛烷(5)3-甲基-4-乙基己烷(6)2-甲基-3-乙基己烷(7)2,5-二甲基-3-乙基己烷(8)3-甲基-7-乙基-6-异丙基-4-叔丁基壬烷2.写出下列化合物的构造式(1)丙基(n-Pr)(2)异丁基(i-Bu)(3)仲丁基(s-Bu)(4)叔丁基(t-Bu)(4)3,4,5-三甲基-4-异丙基庚烷(5)5-(3甲基丁基)癸烷(6)四甲基丁烷2.答案CH3CH2CH2CH3-CH-CH2CH3CH3CH2CH CH3-CCH3CH3CH33 CH3CH33CH(CH3)2CH3CH2CH C CHCH2CH3CH3C C CH33CH3CH3(1)(2)(3)(4) (5)(6)3.某烷烃的相对分子质量为86,写出符合下列要求的烷烃的构造式(1)二种一溴取代物(2)三种一溴取代物(3)四种一溴取代物(4)五种一溴取代物3.答案(1) CH3-CH-CH-CH3CH33(2) CH3CH2CH2CH2CH2CH3 CH3-C-CH2CH3CH33(3) CH3CH2CHCH2CH3CH3(4)CH3CHCH2CH2CH3CH34.用Newman投影式和锯架式(透视式)表示下列化合物的最稳定构象(1)正丁烷沿C2-C3旋转(2)BrCH2-CH2Br4.答案3HCH3HHCH3HHBrClHBrCl(1)(2)5.比较下列化合物指定性质的高低(1)熔点:A正戊烷;B异戊烷;C新戊烷(2)沸点:A 3,3-二甲基戊烷;B正庚烷;C 2-甲基庚烷;D正戊烷;E 2-甲基己烷;F 2,3-二甲基戊烷(3)自由基稳定性:A正丁基;B仲丁基;C叔丁基;D甲基5,答案(1)C>A>B(2)C>B>E>F>A>D (3)C>B>A>D6.假烷烃溴化时,相应氢原子被溴代的活性比为伯氢∶仲氢∶叔氢=1∶80∶1600。
高三有机化学总复习
高三有机化学总复习::::高三化学复习材料第三部分有机化学有机化学给学生的印象通常是比较复杂,没有什么头绪,对看似纷繁复杂的反应有一种摸不着头脑的感觉,而这部分知识无论是在高考中的分娄比例还是个人的化学素养的体现上都有着极重析理论及现实意义,而且有机化学在如今的化学发展中居于较活跃的地位。
以官能团为核心,根据官能团的性质来掌握该物质的化学性质,并掌握此一类物质的化学性质,这是学好有机化学知识的前提条件。
定点迷宫牢牢地抓住一些基本的有机概念,基本官能团的反应,由此扩展到整个有机系统的知识是有机知识体系的基本要求。
这部分知识可分为以下三部分:碳氢化合物;碳氢化合物衍生物;糖和蛋白质。
在“烃”一章中,主要目的是学习一些有机化学中的基本概念,属有机化学启蒙章节,主要包括:有机物烷、烯、炔的及苯性质,同系物,同分异构体及加成、消除反应等。
无论从考试中的题目含量上,还是知识本身的灵活变通性上,“烃的衍生物”都是有机化学中的核心,也是我们在学习有机化学中应着重花费功夫的地方。
包括“醇”、“酚”、“醛”、“羧酸”、“酯”等几大知识块。
在中学阶段,“糖类、蛋白质”知识只能达到初步涉猎的层次,一些基本的概念及知识在本章显得尤为重要。
有机计算和有机推理中经常使用一种强大的工具——不饱和度的应用,这将在以下知识中描述。
有机物燃烧前后,掌握压强的变化也是比较重要的能力。
有机实验很有代表性。
根据一些基本原则设计新的实验也是我们应该掌握的。
二、学海导航思维基础(一)知识基础1.列出有机碳键之间连接的可能形式和性质。
答复:① 单键;② 苯环上的碳-碳键;③ 双键;④ 三键键长度① > ② > ③ > ④ 关键能源① > ② > ①2.甲烷的空间结构为正四面体型结构.h―c―h键角为109?28’,应将这个规律推广――凡是一个碳原子周围以4个单键与其它原子相结合,无论这些原子是否相同,所形成的以该碳原子为顶点的键角均约为109?28’,这在判断有机分子中各碳原子是否在同一平面上有着积极的意义。
17年高考化学一轮复习有机化学备考策略
17年高考化学一轮复习有机化学备考策略有机化学知识是历年高考必考内容之一,例如有机物的分类、结构与组成、有机反应类型、有机物的相互转化、有机物的制取和合成以及石油化工、煤化工等,以下是有机化学备考策略,请考生和老师认真阅读。
依据有机物的结构特点和性质递变规律,可以采用“立体交叉法”来复习各类有机物的有关性质和有机反应类型等相关知识点。
首先,根据饱和烃、不饱和烃、芳香烃、烃的衍生物的顺序,依次整理其结构特征、物理性质的变化规律、化学性质中的反应类型和化学方程式的书写以及各种有机物的制取方法。
这些资料各种参考书都有,但学生却不太重视,大多数同学仅仅看看而已,却不知根据“全息记忆法”,只有自已动手在纸上边理解边书写,才能深刻印入脑海,记在心中。
其次,按照有机化学反应的七大类型(取代、加成、消去、氧化、还原、加聚、缩聚),归纳出何种有机物能发生相关反应,并且写出化学方程式。
第三,依照官能团的顺序,列出某种官能团所具有的化学性质和反应,这样交叉复习,足以达到基础知识熟练的目的。
熟练的标准为:一提到某一有机物,立刻能反应出它的各项性质;一提到某类有机特征反应,立即能反应出是哪些有机物所具备的特性;一提到某一官能团,便知道相应的化学性质。
物质的一般性质必定伴有其特殊性。
例如烷烃取代反应的连续性、乙烯的平面分子结构、二烯烃的1-4加成与加聚反应形成新的双健、苯的环状共轭大丌键的特征、甲苯的氧化反应、卤代烃的水解和消去反应、l-位醇和2-位醇氧化反应的区别、醛基既可被氧化又可被还原、苯酚与甲醛的缩聚反应、羧基中的碳氧双键不会断裂发生加氢反应、有机物燃烧的规律、碳原子共线共面问题、官能团相互影响引起该物质化学性质的改变等,这些矛盾的特殊性往往是考题的重要源泉,必须足够重视。
例题一:该题为2019年上海高考第29题。
这是一道典型的基础型应用题,其有机基础知识为:1-3丁二烯的加聚原理、卤代烃的水解、烯烃的加成反应、l-位醇的氧化、羧酸与醇的酯化反应以及反应类型的判断等。
2017版高考化学一轮总复习 第13章 有机化学基础 第2讲 烃和卤代烃
第2讲烃和卤代烃课时规范训练[单独成册]1.某有机物的结构简式为,其名称是( )A.5乙基2己烯B.3甲基庚烯C.3甲基5庚烯D.5甲基2庚烯解析:选D。
该有机物的结构简式展开为:,从离双键最近的一端编号,故其名称为5甲基2庚烯。
2.下列关于常见有机物的说法中正确的是( )A.等质量的乙烯和苯完全燃烧时,苯消耗的氧气多B.苯不能使酸性KMnO4溶液褪色,因此苯不能发生氧化反应C.用苯萃取溴水中的溴,分液时有机层从分液漏斗下端放出D.乙烯和甲烷可用酸性高锰酸钾溶液和溴水鉴别解析:选D。
分子中氢的含量越高,等质量的烃完全燃烧消耗的氧气越多,根据最简式,C6H6→CH、C2H4→CH2,知乙烯耗氧多,A项错;苯可以燃烧,是氧化反应,B项错;苯的密度比水小,浮在水面上,故有机层应从上端倒出,C项错;D项中乙烯可以使酸性KMnO4溶液和溴水褪色,而甲烷不反应,D正确。
3.(多选)下列有关有机物结构和性质的说法中正确的是( )D.合成药物盐酸沙格雷酯的重要中间体为,该有机物能发生加成、水解、酯化、中和等反应解析:选BC。
中无碳碳双键,其中的碳碳键是一种介于碳碳单键和碳碳双键之间的特殊的键,A错;醋酸与硬脂酸均为饱和羧酸,通式为C n H2n O2,一定互为同系物,C6H14和C9H20均属于烷烃,相差3个CH2,且通式均为C n H2n+2,故一定互为同系物,B正确;根据酚与醛的反应原理,酚醛树脂的结构简式是,C正确;该有机物中含有苯环,能发生加成反应,含有—OH,能发生酯化反应,但不能发生水解和中和反应,D错误。
4.某化学式为C3H6O2的有机物的核磁共振氢谱有三个峰,且峰面积比为3∶2∶1,则该有机物的结构简式不可能是( )A.CH3CH2COOH B.CH3COOCH3C.HCOOCH2CH3D.CH3COCH2OH解析:选B。
高考化学有机化学重点知识点总结
高考化学有机化学重点知识点总结
一、有机化学基本概念
1. 有机物的定义和特点
2. 有机化合物的分类和命名方法
3. 有机化学中常见的官能团和官能团转化反应
二、碳链的构建和环状化合物
1. 碳链的构建:饱和和不饱和碳链的区别和构建方法
2. 碳链上的取代反应和它们的主要特点
3. 环状化合物的构建和命名方法
4. 环状化合物的稳定性和活性
三、烷烃和烯烃类化合物
1. 烷烃的命名和性质
2. 烯烃的构建和命名方法
3. 烯烃的立体化学和环状烯烃的特性
四、卤代烃和醇类化合物
1. 卤代烃的命名和性质
2. 卤代烃的取代反应和消除反应
3. 醇类化合物的命名、分类和性质
4. 醇类的酸碱性和醇酸酯的制备方法
五、醛类和酮类化合物
1. 醛类和酮类化合物的命名和性质
2. 醛类和酮类的氧化还原反应
3. 醛类和酮类的加成反应和缩合反应
六、羧酸和酯类化合物
1. 羧酸的命名和性质
2. 酯类化合物的命名和性质
3. 羧酸的还原反应和酯的酸碱性
七、胺类化合物
1. 胺类化合物的命名和性质
2. 胺的亲核取代反应和亲电取代反应
3. 氨在生物体中的重要作用
八、重要的生物大分子
1. 碳水化合物的分类和结构特点
2. 蛋白质的结构和功能
3. 脂类的结构和功能
4. 核酸的结构和功能
九、化学实验中的有机化学技术
1. 有机合成实验中的常用反应和技术方法
2. 有机化合物的分离和纯化方法
3. 有机化合物的鉴定和定量分析方法
本总结仅列举了高考有机化学的一些重点知识点,希望能对你的复习有所帮助。
如果还有其他问题,可以继续询问。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2017届高三化学有机化学专题复习考点1:通过计算推出分子式或结构式例题1:A的蒸气密度为相同状况下氢气密度的77倍,有机物A中氧的质量分数约为41.6%,则A的分子式为_________。
例题2:某烃A的相对分子质量在90到100之间,1molA完全燃烧可以产生4molH2O,则A的分子式为。
例题3:某羧酸酯的分子式为C18H26O5,1mol该酯完全水解可得到1mol羧酸和2mol乙醇,该羧酸的分子式为____________。
方法小结:1.看清组成元素2、先确定原子量较大的原子数目 3.分子式中:C:H>=n:2n+2强化训练1:1、已知有机物B中含有C,H,O元素,其与H2的相对密度为23,分子中碳、氢原子个数比为1:3 有机物B的分子式为。
2、A的相对分子质量是104,1 mol A与足量NaHCO3反应生成2 mol气体,其结构式为________。
3、1mol丁二酸和1mol丙二醇反应生成环酯类的分子式为_____________。
考点2:分子式和耗氧量、核磁共振氢谱、官能团名称和性质判断例题1:化合物I()的分子式为,1mol该物质完全燃烧最少需要消耗molO2。
例题2:的分子式为__________,含有的官能团有_____________________,1mol该有机物可以消耗______molBr2,________mol NaOH。
例题3:化合物I()的分子式为,其核磁共振氢谱有组峰,分子中官能团的名称为。
强化训练:1、化合物A结构如下图所示,该化合物的分子式为______,1mol该有机物燃烧需要消耗______molO2, 最多可以消耗______mol H2和_________mol Br2。
2、香兰素()除了醚键之外,还含有的官能团名称..是,1mol香兰素最多可与molH2发生加成反应。
3、化合物含有的官能团名称为__________,1mol该有机物最多消耗_____molNaOH,_____mol Ag(NH3)2OH, ______mol H2.考点3:反应类型的判断例1:CH3Cl C7H5Cl3反应的化学方程为,该反应类型为。
若该反应在Fe作为催化剂的条件下,有机产物的结构式为。
例2:CH2ClCH2COOH与NaOH水溶液反应类型为,化学方程式为__________________________________________________________________。
若该有机物与NaOH醇溶液反应时,反应类型为__________________,化学方程式为__________________________________________________________________。
例3:该反应类型是_____________反应,写出苯甲醛与丙醛反应的产物。
例4:在碱性条件下,由Ⅳ(HOCH(CH3)CH=CH2)与反应合成Ⅱ(),其反应类型为。
强化训练:1、 由化合物IV (N CH CH 2[]n)转化为克矽平()的反应类型是 。
2、反应的反应类型是 _________。
3 的反应类型: 。
4、的反应类型是 ,则写出苯乙炔和丙酮在该条件下的反应产物: 。
考点4:有机方程式的书写例1: 化合物II (H CHCH 2OHCH 2OH)①写出该物质与足量浓氢溴酸反应的化学方程式为(注明条件),②写出该物质与乙二酸生成七元环酯的方程式为(注明条件)。
③写出该物质发生聚合反应的方程式:_ 。
例2:丙二醛与足量的银氨溶液反应的方程式:___________________________________________________________________________________。
)发生加聚反应的化学方程式为例3:化合物III(N CH CH2。
例4:苯酚与甲醛合成酚醛树脂:。
例5:香豆素()在过量NaOH溶液中完全水解的化学方程式为。
强化训练:1、由CH2CH2Br通过消去反应制备Ⅰ()的化学方程式为(注明反应条件)。
2、在浓硫酸存在和加热条件下,化合物Ⅳ()易发生消去反应生成不含甲基的产物,该反应方程式为(注明反应条件)。
3、化合物Ⅲ(分子式为C10H11C1)可与NaOH水溶液共热生成化合物Ⅱ(),相应的化学方程式为。
化合物Ⅲ与NaOH乙醇溶液共热生成化合物Ⅳ,Ⅳ的核磁共振氢谱除苯环峰外还有四组峰,峰面积之比为1 : 1 : 1 : 2,反应的化学方程式为。
4、Ⅱ()与过量C2H5OH在酸催化下发生酯化反应,化学方程式为。
5、 已知:,M 中含氧官能团的名称为 。
M 与足量醋酸完全反应的方程式为 。
反应②的化学方程式 ;考点5:有机推断1、PC 是一种可降解的聚碳酸酯类高分子材料,由于其具有优良的耐冲击性和韧性,因而得到了广泛的应用。
以下是某研究小组开发的生产PC 的合成路线:++ 2C + D+ H 2O n E + n CO 2O H C O C OHCH 3CH 3O[]n ( PC )+ (n -1)H 2O已知以下信息:①A可使溴的CCl4溶液褪色;②B中有五种不同化学环境的氢;③C可与FeCl3溶液发生显色反应;④D不能使溴的CCl4褪色,其核磁共振氢谱为单峰。
写出各有机物的结构简式:A:B:C:D:E:2、香豆素是一种天然香料,存在于黑香豆、兰花等植物中。
工业上常用水杨醛与乙酸酐在催化剂存在下加热反应制得:以下是由甲苯为原料生产香豆素的一种合成路线(部分反应条件及副产物已略去)CH3AC7H7ClBC7H8O已知以下信息:①A中有五种不同化学环境的氢;②B可与FeCl3溶液发生显色反应;③同一个碳原子上连有两个羟基通常不稳定,易脱水形成羰基。
写出各有机物的结构简式:A:B:C:D:3、对羟基甲苯甲酸丁酯(俗称尼泊金丁酯)可用作防腐剂,对酵母和霉菌有很强的抑制作用,工业上常用对羟基苯甲酸与丁醇在浓硫酸催化下进行酯化反应而制得。
以下是某课题组开发的廉价、易得的化工原料出发制备对羟基苯甲酸丁酯的合成路线:已知以下信息:①通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基;②D可与银氨溶液反应生成银镜;③F的核磁共振氢谱表明其有两种不同化学环境的氢,且峰面积比为1:1。
写出各有机物的结构简式:A:B:C:D:E:F:G:4、査尔酮类化合物G是黄酮类药物的主要合成中间体,其中一种合成路线如下:已知以下信息:①芳香烃A的相对分子质量在100~110之间,1mol A充分燃烧可生成72g水。
②C不能发生银镜反应。
③D能发生银镜反应、可溶于饱和Na2CO3溶液、核磁共振氢谱显示有4种氢。
④ONa+RCH2I OCH2R;⑤RCOCH3+R′CHO RCOCH=CHR′。
写出各有机物的结构简式:A:B:C:D:E:F:G:5、席夫碱类化合物G在催化、药物、新材料等方面有广泛应用。
合成G的一种路线如下:已知以下信息:①②1mol B经上述反应可生成2mol C,且C不能发生银镜反应。
③D属于单取代芳烃,其相对分子质量为106。
④核磁共振氢谱显示F苯环上有两种化学环境的氢。
⑤写出各有机物的结构简式:A:B:C:D:E:F:G:6、A(C2H2)是基本有机化工原料。
由A制备聚乙烯醇缩丁醛和顺式聚异戊二烯的合成路线(部分反应条件略去)如下所示:写出各有机物的结构简式:A:B:C:D:考点6:有机合成路线设计例题1:参照下述异戊二烯的合成路线,设计一条由A和乙醛为起始原料制备1,3﹣丁二烯的合成路线。
例题2:已知:CH2=CH-CH3CH CH3 CH3CH3CH CH3OHCH 3C CH 3O CH 3C CH 3OH COOHCH 3C CH 3OH COOCH 3CH 2C 3CH 3[]n (有机玻璃)聚乳酸()是一种生物可降解材料,参考上述信息设计由乙醇制备聚乳酸的合成路线:。
强化训练:1、已知:根据上述合成路线,设计一条由乙烯为原料合成H2NCH2CH2CH2CH2NH2的合成路线。
,合成阿斯巴甜的一种合成路线如下:参照上述合成路线,设计一条由甲醛为起始原料制备氨基乙酸的合成路线3、非诺洛芬可通过以下方法合成:根据已有知识并结合相关信息,写出以为原料制备的合成路线。
考点7:同分异构体例题1:CH3OH的同分异构体中含有苯环的还有种,其中在核磁共振氢谱中只出现四组峰的有种。
例题2:CH2CH3H2N的同分异构体中含有苯环的还有种(不考虑立体异构)。
其中核磁共振氢谱中有4组峰,且面积比为6:2:2:1的是。
(写出其中的一种的结构简式)。
强化训练:实用文案标准文档 1、CH CH 33的同分异构体中含有苯环的还有 种,其中在核磁共振氢谱中出现两组峰,且峰面积之比为3:1的是 (写出结构简式)。
2、CH 3C CH 3O有多种同分异构体,其中能发生银镜反应的是 (写出结构简式) 3、CHO OH 的同分异构体中含有苯环的还有 种,其中:①既能发生银境反应,又能发生水解反应的是 (写结构简式);②能够与饱和碳酸氢钠溶液反应放出CO 2的是 (写结构简式)。
4、COOH Cl 的同分异构体中含有苯环且能发生银镜反应的共有 种,其中核磁共振氢谱三种不同化学环境的氢,且峰面积比为2:2:1的是 (写结构简式)。
