第七章 有机波谱分析
有机化学:有机化合物的波谱分析(6H)

第一节 电磁波与分子吸收光谱
第二节 红外光谱
第三节 核磁共振谱
第一页,共92页。
测定有机化合物的方法有两种,即化学方法和物 理方法。随着科学技术的不断发展,近三、四十年来 研究有机化合物的结构,主要采用以各种新型精密仪 器为手段的物理方法,该法的优点有:
样品用量少(一般在3~5mg,有的在微克级); 测定时间短;
Eh hc
第八页,共92页。
所以,对某一分子来说,它只能吸收某一特定 频率的辐射能量。
如吸收的能量引起分子中价电子跃迁而产生的 吸收光谱叫做紫外光谱。
如吸收的能量引起分子中成键原子振动能级的跃迁 而产生的光谱,叫做红外光谱。
如吸收的能量引起分子中核自旋能级跃迁而产生的 光谱叫做核磁共振谱。
第九页,共92页。
操作方法简便;
测定结果准确性高(质谱法误差10-9 )。
第二页,共92页。
四谱:
紫外光谱(简称UV) (Ultraviolet Spectroscopy)
红外光谱(简称IR)
(Infrared Spectroscopy)
核磁共振谱(简称NMR)
(Nuclear Magnetic Resonance Spectroscopy)
IR:3430, 3360, 3200, 3050, 1620, 1600, 1500, 1460, 1310, 1280, 760, 690cm-1
第三十七页,共92页。
Br OH
图7-9 2-溴苯酚的红外光谱图 IR:3500, 3080, 1600, 1480, 1350, 1300, 840, 750, 6602 C NH2
图7-22 丙酰胺的红外光谱图
IR:3360, 3200, 2920, 2860, 1660, 1470, 1420, 1300,
有机化学课件浙江大学第7章有机波谱分析基础

3.红外光谱的分区 按吸收的特征,通常将4000-400 cm-1范围的红外光谱分为官
能团吸收区和指纹区。 (1)官能团吸收区 在1250-3700cm-1区域,称为高频区,有机化合物各种官能团
的吸收峰都在此区,可用来鉴定官能团。
(2)指纹区 所谓指纹区是指频率小于1250 cm-1的低频区,主要代表某些 分子骨架的特征振动以及C—C、C—O、C—N等单键的伸缩 振动和各种弯曲振动的吸收。只有结构完全相同的化合物,其 指纹区才相同。
红外光谱波长范围 波长范围为780-5×105 nm. 三个区域:
近红外(λ=780-2500 nm,υ=12820-4000 cm-1); 中红外(λ=2500-25000nm,υ=4000-400cm-1); 远红外(25000-5×105 nm,υ=400-20 cm-1)。
一般红外光谱仪使用的波数为4000-400cm-1,属中红外区,相 当于分子的振动能量,红外光谱也称为振动光谱。
7.2.1 分子的振动形式和红外光谱
红外光谱的基本原理
• 分子是由各种原子通过化学键互相连接而成的。 • 分子的振动是键合的原子通过化学键而引起的伸缩或弯曲运
动。
• 物质吸收红外光的能量大小与原子振动能级能量相当,就产
生振动能级跃迁,产生红外吸收光谱,振动能级的大小与化学 键的类型和其振动方式有关。
C-H键伸缩振动
C-H键伸缩振动所产生的吸收峰在高频区 CSP3—H :2800-3000cm-1, CSP2—H :3000-3100cm-1处, CSP—H :3300cm-1
(2)芳烃的红外光谱
芳烃的红外吸收主要为苯环上的C—H键及环骨架中 的C=C键振动所引起。芳烃主要有三种特征吸收。
第七章 有机波谱分析
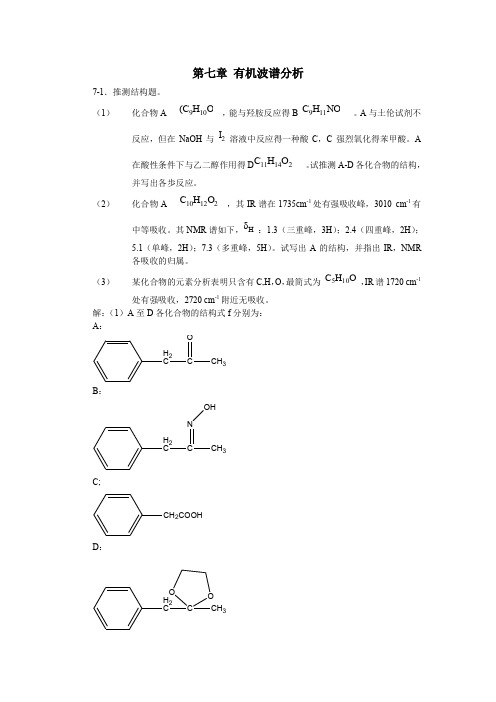
第七章 有机波谱分析7-1.推测结构题。
(1)化合物A (C 9H 10O ,能与羟胺反应得B C 9H 11NO 。
A 与土伦试剂不反应,但在NaOH 与 I 2 溶液中反应得一种酸C ,C 强烈氧化得苯甲酸。
A 在酸性条件下与乙二醇作用得D C 11H 14O 2 。
试推测A-D 各化合物的结构,并写出各歩反应。
(2)化合物A C 10H 12O 2 ,其IR 谱在1735cm -1处有强吸收峰,3010 cm -1有中等吸收。
其NMR 谱如下,δH :1.3(三重峰,3H );2.4(四重峰,2H );5.1(单峰,2H );7.3(多重峰,5H )。
试写出A 的结构,并指出IR ,NMR 各吸收的归属。
(3)某化合物的元素分析表明只含有C,H ,O ,最简式为 C 5H 10O ,IR 谱1720 cm -1处有强吸收,2720 cm -1附近无吸收。
解:(1)A 至D 各化合物的结构式f 分别为: A :H 2CCH 3OB :H 2CCNCH 3OHC;CH 2COOHD :H 2CCCH 3O O各步反应如下:H 2CCCH 3OH 2CCCH 3NOHNH 2OHH 2CCCH 3O H 2CCCH3O O 22+CH 3IH 2CCH 3O H 2CCCH3O O 22+CH 3ICH 2COOHCOOH[O](2)A 的结构式为:H 2COCOH 2CCH 3A 的IR ,NMR 各吸收归属为:H 2COCOH 2CCH 3dcbaIR :1735 cm -1(强)酯的 v Ar-H ;3010 cm -1(中强) v c=O 。
NMR :δH :1.3(三重峰,3H )a ;2.4(四重峰,2H )b ;5.1(单峰,2H )c ;7.3(多重峰,5H )d 。
(3)IR 的谱1720 cm -1处有强吸收,2720 cm -1附近处无吸收,表明有酮羰基 RCOR '。
有机化学-第七章有机化合物的波谱分析

分子化学键的振动和红外光谱
1.振动方程式
式中:μ为折合质量;ml和m2分别为化学键所连的两个原子的质量,单位为g, 是为化学键的力常数,单位为N·cm-1(牛顿·厘米-1),其含义是两个原子由平衡位置伸长0.1 nm后的恢复力。
可把双原子分子的振动近似地看成用弹簧连接着的两个小球的简谐振动。根据Hooke定律可得其振动频率为:
本章讨论的红外光谱和核磁共振谱为吸收光谱。质谱是化合物分子经电子流轰击形成正电荷离子,在电场、磁场的作用下按质量大小排列而成的图谱,不是吸收光谱。
7.2红外吸收光谱
用红外光照射试样分子,引起分子中化学键振动能级的跃迁所测得的吸收光谱为红外吸收光谱,简称红外光谱(Infrared Spectroscopy,缩写为IR)。红外光谱是以波长λ或波数σ为横坐标,表示吸收峰的峰位;以透射比T(以百分数表示)为纵坐标,表示吸收强度。
1H的自旋量子数I为1/2,它在磁场中有两种取向,与磁场方向相同的,用+1/2表示,为低能级;与磁场方向相反的,用-1/2表示,为高能级。两个能级之差为△E,见图7–4。
有机化学经常研究的是1H和13C的核磁共振谱,下面主要介绍1H核磁共振谱(质子核磁共振谱)。
式中:γ 称为磁旋比,是物质的特征常数,对于质子其量值为2.675×108A·m2·J-1·s-1; h为Plank常量; ν为无线电波的频率。
测量核磁共振谱时,可以固定磁场改变频率,也可以固定频率改变磁场,一般常用后者。 若以通过电流所表现的吸收能量为纵坐标,磁场强度为横坐标,则可得到如图7–6所示的NMR谱。
一张核磁共振谱图,通常可以给出四种重要的结构信息:化学位移、自旋裂分、偶合常数和峰面积(积分线)。如图7–7所示。
峰面积大小与质子数成正比,可由阶梯式积分曲线求出。峰面积(积分线高度)之比为质子个数之比,图中积分线高度比为1:2:3,等于质子个数之比(OH:CH2:CH3)。
有机化学 12 第七章 波谱分析 (三) 核磁共振

H 实 = H 0 H 0σ = H 0 (1 σ )
在真实分子中,发生核磁共振的条件是:
ν RF
γ = H 0 (1 σ ) 2π
这里σ是屏蔽常数. 不同化学环境的质子,因其周围电子云密度不同,裸 露程度不同,其σ值也不同,从而发生核磁共振的H0 不 同.这就是化学位移的来源. 所以,化学位移也可定义为由于屏蔽程度不同 由于屏蔽程度不同而引起 由于屏蔽程度不同 的NMR吸收峰位置的变化.
OCH3
的NMR?
与氧原子相 连的甲基氢
δ3.9(单峰 单峰) 单峰 -OCH3 δ6.7~7.3 苯环氢
苯氢
所以,该图是2,3,4-三氯苯甲醚的NMR.
例3:下图与A,B,C哪个化合物的结构符合?
ClCH2C(OCH2CH3)2 Cl A Cl2CHCH(OCH2CH3)2 B CH3CH2OCH-CHOCH2CH3 Cl Cl C
例1:CH3CH2CH2NO2的NMR谱.
例2:CH3CH2OH的NMR谱.
通常,只有相邻碳 1H才相互偶合. 相邻碳上 相邻碳
1,1,2-三溴乙烷
(4) 积分曲线与质子的数目
积分曲线的高度与其相对应的一组吸收峰的峰面积成正 比,而峰面积与一组磁等价质子的数目成正比. 以乙醇 乙醇的NMR为例. 乙醇
(三) 核磁共振
(1) 1H-NMR的基本原理 (2) 1H-NMR的化学位移 (3) 1H-NMR的自旋偶合与自旋裂分 (4) 积分曲线与质子的数目 (5) 1H-NMR的谱图解析 (6) 13C-NMR谱简介(自学)
(三) 核磁共振
(Nuclear Magnetic Resonance Spectroscopy)
C Ha C Hb Ha C C Ha Hb C C Hb
有机波谱分析的应用

有机波谱分析的应用有机波谱分析是一种常用的分析技术,广泛应用于化学、生物、医学等领域。
通过对有机化合物的谱图进行解析和研究,可以揭示有机化合物的结构、性质和反应特性,为相关研究和应用提供关键信息。
本文将介绍有机波谱分析的基本原理和常见的应用。
一、有机波谱分析的基本原理有机波谱分析主要包括红外光谱、质谱和核磁共振三种常见技术。
这些技术基于有机分子在不同电磁波频段的吸收、发射或散射特性,从而获取有机分子结构和性质的相关信息。
1. 红外光谱红外光谱是利用有机分子在红外光区(波长范围为0.78-1000微米)的吸收特性来分析有机物的结构和功能基团的一种方法。
红外光谱通过检测样品吸收红外辐射的能量,得到红外光谱图,从而确定化合物中的主要化学键和它们的相对位置。
2. 质谱质谱是通过对化合物分子中的正离子进行分析,获得化合物的分子量和结构信息的一种技术。
在质谱中,分子或分子片段在电离源中被电离,形成正离子,然后通过分析正离子的质量/电荷比,确定化合物的分子量和结构。
3. 核磁共振核磁共振是一种利用核自旋在外磁场作用下的共振现象来分析有机物结构和环境的技术。
核磁共振通过测量有机分子中核自旋的共振频率和相对强度,可以确定有机分子的化学环境,分析其分子结构和相互作用。
二、有机波谱分析的应用有机波谱分析技术广泛应用于化学、生物、医学等领域。
以下将介绍几个常见的应用案例。
1. 有机合成的结构确定有机合成是化学领域的一项重要研究。
有机波谱分析技术可以帮助确定有机合成产物的结构。
例如,通过红外光谱可以确定化合物中特定官能团的存在与否,通过质谱可以测定化合物的分子量,通过核磁共振可以确定化合物的结构和官能团的相对位置。
2. 药物分析与药效评价有机波谱分析在药物研究和开发中起着重要作用。
通过红外光谱,可以分析药物中的官能团,从而了解其化学性质和稳定性。
质谱可以用于分析药物的结构、分子量和组成成分。
核磁共振则可以揭示药物的分子结构和化学环境,为药效评价提供重要信息。
有机波谱第七章谱图综合解析

•3. 活泼氢的识别 OH, NH2, NH, COOH, CHO 等活泼氢的存
在可由IR谱、1H NMR谱的特征吸收来识别, 1H NMR 重水交换谱可进一步证实。对于某 些存在互变异构(如β-二酮的烯醇结构)的活泼 氢也可由此识别。除此之外,由分子中氢原 子的数目减去由偏共振去偶13C NMR谱计算 的与碳原子直接相连的氢原子的数目,剩余 氢亦为活泼氢。
复习题
1.在质谱分析中,试以分子中由双电子构成的σ键断裂过程说明均裂、异 裂和半异裂的含义。 2.在红外光谱分析中,习惯上把红外光谱图按波数范围分为四大峰区,每 个峰区都对应于某些特征的振动吸收。请简述各峰区的波数范围及对应的 特征振动吸收,并在每一峰区列举至少三种属于该类特征振动吸收的具体 化学键。 3.有机分子电子跃迁类型主要有哪些?请简要回答并画出简图进行说明。 4. 影响化学位移的因素有哪些?
• 13C NMR δ 114~117 范围的共振吸收峰为sp2杂化 碳的共振吸收,其中有 ,C=C, C=O基存在。
• 1H NMR δ 6~8的多组多重峰为烯烃和苯氢的共振 吸收峰。
以上推导的不饱和基在不同光谱中均有其特征吸收 峰,且与不饱和度相符。故分子中含有 ,C=C, C=O。
• 活泼氢的确定:
CH3 H3C C CH2 OH
CH3
4、 化合物的分子式为C4H6O2,其1H NMR 谱图(300MHz)如图所 示,谱图中δ12.5ppm峰重水交换后消失,推导其结构。
由以上分析可知,当N=0时,O=4,可能分子式 为C14H18O4。当N=2时,O=2.5,不合理应舍去。 故该化合物的分子式为C14H18O4 ,因UN=6
10有机化学 第七章 有机化合物的波谱分析

分子运动能级
用电磁波照射有机分 子时,分子便会吸收 那些与分子内的能级 差相当的电磁波,引 起分子振动、转动或 电子运动能级跃迁, 即分子可选择性地吸 收电磁波使分子内能 提高。用仪器记录分 子对不同波长的电磁 波的吸收情况,就可 得到光谱。
E³ ª E³ ª E³ ª EÕ ñ EÕ ñ EÕ ñ Eµ ³Ô Ç ç Ó ½ ¨
(丁) 解析实例:
例1:C8H16O的IR谱图 例2:C5H10O的IR谱图 例3:C7H8的IR谱图 例4:C7H8O的IR谱图 例5:C8H8O2的IR谱图 例6:C3H7NO的IR谱图
(1) IR的基本原理
(甲) 分子振动与红外光谱 (乙) 分子振动的类型 (丙) 红外吸收峰产生的条件
(1) IR的基本原理
(甲) 分子振动与红外光谱
分子的近似机械模型——弹簧连接小球。 分子的振动可用Hooke’s rule来描述:
1 1 1 n k( ) 2 m1 m2
红外光谱中,频率常用波数表示。
(3) 不饱和度(U)
当一个化合物衍变为相应的烃后,与其同碳的饱和 开链烃比较,每缺少2个氢为1个不饱和度。 所以: 一个双键的不饱和度为1,一个叁键的不饱和度为2, 一个环的不饱和度为1,一个苯环的不饱和度为4。 例如: CH2£CH£COOH U£2 £ CH2£CH£CN £ U£3 £ £
红外谱图一般以1300cm-1为界:
4000~1300cm-1:官能团区,用于官能团鉴定; 1300~650cm-1:指纹区,用于鉴别两化合物是否相同。
官能团区吸收峰大多由成键原子的伸缩振动而产生,与 整个分子的关系不大,不同化合物中的相同官能团的 出峰位置相对固定,可用于确定分子中含有哪些官能 团。 指纹区吸收峰大多与整个分子的结构密切相关,不同分 子的指纹区吸收不同,就象不同的人有不同的指纹, 可鉴别两个化合物是否相同。指纹区内的吸收峰不可 能一一指认。 例:庚酸和正癸酸的红外光谱。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第七章 有机波谱分析7-1.推测结构题。
(1)化合物A (C 9H 10O ,能与羟胺反应得B C 9H 11NO 。
A 与土伦试剂不反应,但在NaOH 与 I 2 溶液中反应得一种酸C ,C 强烈氧化得苯甲酸。
A 在酸性条件下与乙二醇作用得D C 11H 14O 2 。
试推测A-D 各化合物的结构,并写出各歩反应。
(2)化合物A C 10H 12O 2 ,其IR 谱在1735cm -1处有强吸收峰,3010 cm -1有中等吸收。
其NMR 谱如下,δH :1.3(三重峰,3H );2.4(四重峰,2H );5.1(单峰,2H );7.3(多重峰,5H )。
试写出A 的结构,并指出IR ,NMR 各吸收的归属。
(3)某化合物的元素分析表明只含有C,H ,O ,最简式为 C 5H 10O ,IR 谱1720 cm -1处有强吸收,2720 cm -1附近无吸收。
解:(1)A 至D 各化合物的结构式f 分别为: A :H 2CCH 3OB :H 2CCNCH 3OHC;CH 2COOHD :H 2CCCH 3O O各步反应如下:H 2CCCH 3OH 2CCCH 3NOHNH 2OHH 2CCCH 3O H 2CCCH3O O 22+CH 3IH 2CCH 3O H 2CCCH3O O 22+CH 3ICH 2COOHCOOH[O](2)A 的结构式为:H 2COCOH 2CCH 3A 的IR ,NMR 各吸收归属为:H 2COCOH 2CCH 3dcbaIR :1735 cm -1(强)酯的 v Ar-H ;3010 cm -1(中强) v c=O 。
NMR :δH :1.3(三重峰,3H )a ;2.4(四重峰,2H )b ;5.1(单峰,2H )c ;7.3(多重峰,5H )d 。
(3)IR 的谱1720 cm -1处有强吸收,2720 cm -1附近处无吸收,表明有酮羰基 RCOR '。
7-2.化合物 C 6H 12O 2 在1740 cm -1,1250 cm -1,1060 cm -1处有强的红外吸收峰。
在2950cm-1以上无红外吸收峰。
核磁共振谱图上有两个单峰δ=3.4(3H),δ=1.0(9H),请写出该化合物的结构式。
解:1740 cm-1为羰基-CO-吸收峰,1250 cm-1,1060 cm-1印证其为酯羰基,在2950 cm-1无红外吸收峰,说明无不饱和键。
核磁共振谱图上有两个单峰,说明有两个氢原子。
综上,化合物的结构式为:(CH3)3OOCH37-3.(1)化合物D C7H14O,IR显示1710 cm-1处有强吸收峰,HNMR由三个单峰构成,其峰面积比为9:3:2 ,δ=1.0,2.1,2.3,推出化合物D的结构式。
(2)某化合物A,分子式为C10H18O2,可使Br2/CCl4褪色,但不发生银镜反应;A经O3氧化后水解可得到丙酮及某酸性物质B,B可以发生碘仿反应生成另一酸性物质C;C经加热后得到环戊酮,请写出A,B,C的可能结构。
解:(1)1710 cm-1为羰基吸收峰,HNMR由三个单峰构成,其峰面积比为9:3:2,所以该化合物有三种氢,并且个数比为9:3:2.化合物D的结构式为:O(2)A可使Br2/CCl4褪色,但不发生银镜反应,所以A有双键,并且不是醛。
经臭氧氧化后得到羧酸可确定双键的位置,所以A,B,C的可能结构为:A:OB:OOHOC:OOHOOH7-4.某无色有机液体化合物,具有类似茉莉清甜的香气,在新鲜草莓中微量存在,在一些口香糖中也使用。
MS 分析得到离子峰m/z=164,基峰m/z=91;元素分析结果如下:C (73.15%),H(7.37%),O(19.48%);其IR 谱中在-3080cm 有中强度的吸收,在-1740cm -1及-1230cm -1有强的吸收;HNMR 数据如下: (ppm )-7.20(5H ,m ),5.34(2H,s),2.29(5H,q,J7.1Hz),1.14(3H,t,J7.1Hz).该化合物水解产物与水溶液不显色。
请根据上述有关数据推到该有机物的结构。
并对IR 的主要吸收峰及HNMR 的化学位移进行归属。
解:由m/z 及元素分析数据求分子式:根据离子峰164,C,H,O 原子数目只比为可求的:C:H:O=73.15%*164/12.01:7.37%*164/1.008:19.48%*164/16.00=10:12:12 所以化合物的分子式为 C 10H 12O 2不饱和度为: W =5 IR 的主要吸收峰归属:O H 2CO(v C -o)vC=O OO-3080cm-1v C (苯环)HNMR 的化学位移归属:-7.20,5H2.29(2H,q,J7.1)1.14(3H,t,J7.1)OCH 2CH 3H 2COCO5.34(2H,s)m/z=91的基峰可归属于C 6H 5CH 2+因此,未知物的结构为:OCH2CH3δ-7.205.34 2.29 1.1412301740因化合物的水解产物不能使三氯化铁溶液褪色,所以排除OH2C COCH2CH37-5.化合物A C6H12O3,其红外光谱在1710 cm-1处有强吸收峰。
A与I2/NaOH溶液作用得到黄色沉淀,与Tollens试剂作用无银镜反应。
但A用稀H2SO4处理后,所生成化合物与Tollens试剂作用有银镜反应。
A的HNMR数据如下:δ=2.1(单峰,3H),δ=2.6(双峰,2H),δ=3.2(单峰,6H),δ=4.7(三重峰,1H);写出A 的构造式及相关反应式.解:A能发生碘仿反应但不能发生银镜反应,所以A无醛基,可能有羰基,A的红外光谱在1710cm处有强吸收峰,说明A中有羟基。
由IR和HNMR数据可得到A的构造式为:CH3COCH2CH(OCH3)2A发生相关的反应为:H3COCH2CH(OCH3)22CH3I3+NaOOCCH2CH(OCH3)2H3COCH2CH(OCH3)224CH32CHOOAg(NH)OH CH3CCH2COONH2O+Ag7-6.某光学活性化合物A C12H16O红外光谱图中在3000-3500cm-1有一个强吸收峰,在1580和1500cm-1处分别有中等强度的吸收峰,该化合物不与2,4-二硝基苯肼反应,但用I2/NaOH 处理,A被氧化,发生碘仿反应。
A经臭氧氧化反应还原水解得到B C9H10和C C3H6O2。
B ,C 和2,4-二硝基苯反应均生成沉淀,但用Tollens 试剂处理只有C 呈正结果。
B 经硝化HNO 3/H 2SO 4 可得到两个一硝化合物D 和E 。
但实际上却只有得到D 。
将C 和Tollens 实际反应的产物酸化后加热,得到F C 6H 8O 4。
该化合物的红外光谱图中在3100 cm -1以上不出现吸收峰。
试写出A ,B ,C ,D ,E ,F 的结构化学式.解:根据A 的红外吸收光谱,在3000-3500 cm -1有一个强吸收峰,可知A 有一个苯环;在1580和1500 cm -1处分别有中等强度的吸收峰,可知A 有双键。
F 红外吸收光谱中在3100 cm -1以上不出现吸收峰,推断F 中没有苯环。
A 能发生碘仿反应推知A 结构中有CH 3CH 3OH ,所以A ,B ,C ,D ,E ,F 的化学结构式分别为:A:H 3CC CH 3C HH C OHCH 3B:H 3CC OCH 3CCH 3CHCHO OH:D:C NO 2CH 3OH 3CE:CH 3NO 2COH 3CFOO OH3CCH3O7-7.某同学用萘钾处理β-丁内酯,再与碘乙烷处理,得到分子式为C6H10O2的液体化合物A。
O OCH(1)K(2)CH3CH2IA请根据下列测试结果确定A的结构,并对所有的谱学数据进行归属。
1H NMR(CDCl3/TMS):δ:1.31(τ,ϑ=7H z,3H),1.88(d,J=6Hz,3H),4.20(q,J=7Hz,2H) 5.85(d,J=14Hz,1H),6.9-7.2(m,1H);IR(capiliary cell,cm-1):3040(w),1740(s),1660(cm),1185(s);MS m/z (relative intensity) 69(100), 99(30),114(2,M ).解:C sp2-H 3040C=C C=O C-O 1660174011851H NMR:CH3HH OH2C CH31.88 5.856.9-7.2 4.20 1.31MS:CH3HHO CH3HHOO CH2m/z=69(基峰)m/z=99所以,A的结构式为:CH3HHO OH2C CH37-8.某化合物A(C6H8O3),催化氢化吸收一摩尔氢生成化合物B(C6H10O),,B与NaOH/D2O 反应生成化合物C6H7OD3,与过氧乙酸反应生成化合物C(C6H10O2),A,B,C具有如下一些波谱特征:IR:(cm-1) NMR:( )A B C1720(S)1.74(3H,二重峰)1745(S)1.06(3H,二重峰)1735(S)1.90(3H,二重峰)试推出A,B,C的结构式。
解:根据化合物的IR和NMR数据可得出A,B,C,均有羰基。
A催化氢化吸收一摩尔氢生成化合物B,可知A为有一双键的化合物。
A,B,C,的结构式分别为:A:3或OCH3;B:OCH3:C:OOCH37-9.某研究生合成得到了一化合物,其可能结构如下所示,请根据下列测试数据确定具体是哪一个,并对所有核磁数据进行归属。
A:OO OOB:OOOOC:O OOD:OO OO1HNMR(270Hz,CDCl 3/TMS):δ 1.21(τ,ϑ 7.8H z,3H),1.29(t,J 7.0Hz,3H),2.50(q,J7.8Hz,2H),4.20(q,J 7.0Hz,2H),5.70(d,J 12.6Hz,1H),8.30(d,J 12.6Hz,1H);13CNMR(67.5Hz,CDCl 3TMS)δ 8.60,14.3,27.2,60.4,105.6,149.3,166.0,170.2;HPM∑(EI) Calcd FOR C 8H 12O 4][M ]170.0736,found 172.0747.解;化合物为D ,其核磁共振归属如下:1HNMRH2CH 3COOOC H 2CH 313CNMRO OHH1.212.508.305.704.201.298.6027.2170.2149.3106.6166.060.414.37-10.根据所给分子式IR , 1HN M R 主要数据,推测相应化合物的结构,并指出各吸收峰的归属。
