电镀基本原理
电镀的生产原理及应用技术

电镀的生产原理及应用技术电镀是利用电解作用将金属沉积在工件表面的一种表面处理技术。
其原理是利用电力将带正电荷的金属离子在电解质溶液中还原成金属沉积在工件表面。
电镀技术广泛应用于制造业,具有美观、防腐蚀、提高硬度等优点。
电镀的原理可简单概括为三个基本要素:工件、阳极和电解液。
工件是待镀件,通常是金属,而阳极则是用来提供金属离子的金属板。
电解液是含有金属离子的溶液。
在电极两极加上电压后,阳极上的金属板逐渐溶解产生金属离子,而工件上的金属离子则通过电解液中的电子还原成金属沉积在工件表面。
电镀的应用技术根据金属的不同有很多种类。
最常见的是镀金、镀银、镀铜等等。
这些金属镀层使普通金属具有金属镀层的特性,如耐腐蚀、耐磨擦、不易氧化等,同时也增加了产品的美观度。
电镀还可以通过调节电镀条件来改变金属镀层的性能,达到不同要求。
例如,增加电流密度可以获得较厚的金属镀层,提高镀层的硬度。
此外,电镀还可以通过改变电镀液的成分来获得不同的色彩效果,如红铜、黄铜等。
因此,电镀技术在制造业中有广泛的应用。
电镀在制造业中有着重要的地位。
除了美观外,电镀还可以增加产品的耐磨擦性、耐腐蚀性和导电性能。
例如,在汽车制造中,电镀可以保护零件不受氧化和腐蚀,同时还能提高导电性,提高电子设备的性能。
在电子工业中,电镀可以制造电路板,增加导电性。
在首饰制造中,电镀可以提供不同的金属色彩,增加首饰的美观度。
此外,电镀还广泛应用于制造硬币、钟表、眼镜等。
然而,电镀也存在一些问题和挑战。
首先,电镀过程需要大量的电能和水资源,因此对环境造成一定的影响。
其次,电镀过程中产生的废水和废液中含有复杂的化学物质,需要进行合理的处理和回收。
此外,电镀涂层也容易出现开裂、脱落等问题,影响使用寿命和性能。
为了解决上述问题,电镀技术在不断发展。
如今,已经出现了无铬电镀、无氰电镀等环保电镀技术。
无铬电镀是一种不使用有害的六价铬盐的电镀技术,有效地减少了对人体和环境的危害。
电镀是什么原理

电镀是什么原理电镀是一种常见的表面处理工艺,它通过在金属表面涂覆一层金属或合金来改善其表面性能。
电镀的原理是利用电化学原理,在电解液中利用外加电流的作用,在被镀件表面沉积金属或合金,从而使被镀件表面获得一定的性能和外观。
电镀的原理主要包括电解液、阳极、阴极和外加电源等几个方面。
首先,电镀的原理与电解液密切相关。
电解液是电镀过程中的重要介质,它能够提供金属离子和保持电解质平衡。
在电镀过程中,电解液中的金属离子会在外加电流的作用下在被镀件表面沉积,从而形成一层金属或合金镀层。
不同的电解液适用于不同的金属或合金,选择合适的电解液对于获得理想的电镀效果至关重要。
其次,电镀的原理还涉及到阳极和阴极的作用。
在电镀过程中,被镀件作为阴极,而金属板或其他材料作为阳极。
在外加电流的作用下,金属离子从阳极释放,并在阴极表面沉积形成金属镀层。
阳极和阴极的选择和处理对于电镀的效果和成本都有很大的影响,因此在实际生产中需要进行合理的设计和选择。
另外,外加电源也是电镀原理中不可或缺的一部分。
外加电源提供了必要的电流,使得金属离子在电解液中移动并在被镀件表面沉积。
外加电源的稳定性和电流密度的控制对于电镀过程中镀层的厚度、均匀性和结合力都有着重要的影响,因此在电镀过程中需要进行严格的控制和监测。
总的来说,电镀的原理是利用电化学原理,在特定的电解液和外加电流的作用下,在被镀件表面沉积金属或合金,从而改善其表面性能。
在实际生产中,需要充分考虑电解液、阳极、阴极、外加电源等因素,合理设计和控制电镀工艺参数,以获得理想的电镀效果。
电镀作为一种重要的表面处理工艺,在汽车、家电、建筑等领域有着广泛的应用,对于提高产品的外观质量和耐腐蚀性能都起着至关重要的作用。
电镀原理是什么

电镀原理是什么电镀原理是指利用电化学原理将金属离子沉积在导电基材表面形成金属膜的工艺过程。
电镀是一种常见的表面处理技术,通过电解槽中的阳极和阴极之间的电流传导,在阴极上沉积金属离子,从而实现对基材表面的镀层覆盖。
电镀原理的核心是电化学反应,下面将详细介绍电镀的原理及其相关知识。
首先,电镀原理的基础是电化学原理。
在电解槽中,阳极和阴极之间的电流传导导致金属离子在阴极上还原成金属原子,从而形成金属膜。
同时,阳极上的金属原子被氧化成金属离子,并溶解在电解液中。
这一过程是通过电化学反应实现的,包括氧化反应和还原反应。
在电解槽中,电解液中的金属离子通过电流传导在阴极上沉积成金属层,而阳极上的金属则被氧化成离子并溶解在电解液中,这一过程就是电镀原理的基本原理。
其次,电镀原理还涉及到电解液的选择。
电解液是电镀过程中至关重要的一环,它不仅可以提供金属离子,还能影响电镀层的质量和性能。
通常情况下,电解液是由金属盐和相应的酸碱盐组成的。
选择合适的电解液可以提高电镀层的均匀性、结晶度和附着力,从而得到高质量的电镀层。
同时,电解液的温度、浓度和PH值等参数也会对电镀过程产生影响,需要进行精确控制。
另外,电镀原理还与电镀设备和工艺参数有关。
电镀设备包括电解槽、电源、搅拌装置等,其设计和性能会直接影响到电镀层的质量和生产效率。
而工艺参数如电流密度、温度、时间等也会对电镀层的厚度、结构和性能产生影响。
因此,在实际的电镀生产中,需要根据不同的基材和要求,合理选择电解液和工艺参数,以确保获得理想的电镀效果。
总的来说,电镀原理是利用电化学原理实现金属离子沉积在基材表面形成金属膜的工艺过程。
通过电解槽中的阳极和阴极之间的电流传导,金属离子在阴极上还原成金属原子,形成金属膜。
电解液的选择、电镀设备和工艺参数的控制都是影响电镀效果的重要因素。
只有全面理解电镀原理,并合理控制各项参数,才能获得高质量的电镀层,满足不同工业领域的需求。
综上所述,电镀原理是一项复杂而又精密的工艺,它的实现需要深厚的电化学知识和丰富的生产经验。
关于电镀的知识点总结

关于电镀的知识点总结一、电镀的原理电镀是利用电解质中的金属离子在电场作用下沉积在导电基材上形成金属镀层的表面处理方法。
其主要原理是在外加电压的作用下,金属阳离子在阴极处接受电子并还原成金属原子,然后随着电流的通过沉积在导电基材表面,形成金属镀层。
同时,阴极处的氧化物或者其它不溶于水的物质在电场作用下会向阳极迁移,使阳极被腐蚀掉。
二、电镀的工艺流程电镀工艺流程包括前处理、电镀、后处理等步骤。
其中前处理是为了去除基材表面的油污、氧化膜等杂质,以便金属镀层的附着力和质量。
常见的前处理方法包括除油、脱脂、去氧化等。
电镀是将经过前处理的基材浸泡在电解液中,通过外加电压使金属离子沉积在基材表面形成金属镀层。
后处理主要是清洗,以去除电解液残留和电镀产生的杂质,提高镀层的质量。
三、电镀常见问题及解决方法1. 镀层不结合:可能的原因包括基材表面处理不当、电解液浓度不足、电流密度过大等。
解决方法是加强前处理工艺、根据实际情况调整电解液的浓度和电流密度。
2. 镀层孔洞:可能的原因包括电解液中含有杂质、电流密度不均匀等。
解决方法是加强后处理工艺,定期更换电解液,调整电流密度。
3. 镀层粗糙:可能的原因包括电解液中有悬浮颗粒、电流密度过大等。
解决方法是过滤电解液,均匀分布电流密度。
4. 镀层起泡:可能的原因包括电解液中有气体、电流密度过大等。
解决方法是排除电解液中的气泡,调整电流密度。
四、电镀的应用电镀广泛应用于汽车零部件、家用电器、建筑材料等领域。
其中汽车零部件包括车身、底盘、发动机等部件的表面处理。
家用电器包括厨房用具、浴室用具等的表面处理。
建筑材料包括门窗、护栏等的表面处理。
电镀能够提高材料的耐腐蚀性、导电性和外观质量,使其更耐用、美观。
五、电镀的发展趋势随着环保意识的增强,传统的化学镀铬已经被禁止使用。
因此,发展环保型电镀技术是电镀行业的发展趋势之一。
这包括采用无铬镀层、无镍镀层等新型电镀方法。
同时,随着电子、汽车、航空等行业的快速发展,对高耐蚀、高导电、高强度的金属表面处理要求也在不断提高,因此电镀行业需要不断研发新的电镀工艺和技术,以满足不同材料和工艺的需求。
电镀的基本原理

电镀设备
挂具:方形挂具与方形镀槽配合使用,圆形挂具与圆形镀槽配合使用.圆形镀 槽和挂具更有利于保证电流分布均匀,方形挂具则需在挂具周围加设诸如铁丝网之 类的分散电流装置或缩短两侧阳极板的长度,使用如图所示的椭圆形阳极排布.
★电镀基本工艺及各工序的作用
基本工序
(磨光-抛光)-上挂-脱脂除油-水洗-(电解抛光或化学抛光
-(预镀)-电镀-水洗-(后处理)-水洗-乾燥-下挂-检验包装 各工序的作用 前处理:施镀前的所有工序称为前处理,其目的是修整工件表面,除掉工件 表面的油脂,锈皮,氧化膜等,为后续镀层的沉积提供所需的电镀表面.前处理主
搅拌装置:促进溶液流动,使溶液状态分布均匀,消除气泡在工件表面的停留 电源: 直流,稳定性好,波纹系数小.
后处理 电镀后对镀层进行各种处理以增强镀层的各种性能,如耐蚀性,抗变色能力, 可焊性等.
脱水处理: 水中添加脱水剂,如镀亮镍后处理
钝化处理: 提高镀层耐蚀性,如镀锌
防变色处理:水中添加防变色药剂,如镀银,镀锡,镀仿金等 提高可焊性处理:如镀锡 因此后处理工艺的优劣直接影响到镀层这些功能的 好坏.
3.电镀的分类
按镀层组成分
单金属电镀(应用较广的镀层有锌、镉、铜、铬、锡、镍、金、银等)
二元合金电镀(常用的有锡-铅合金,锌-镍,锌-钴
,铜-锡等)
合金电镀 三元合金电镀(常用的有铜-
锡-锌,锌-镍-铁等)
多元合金电镀(基本处于研究阶段)
复合电沉积(电镀层中嵌入固体颗粒形成复合镀层)
按获取镀层方式分
热浸镀(常用的有热浸锌、锡、铝、铅)火焰喷涂
电镀基本原理
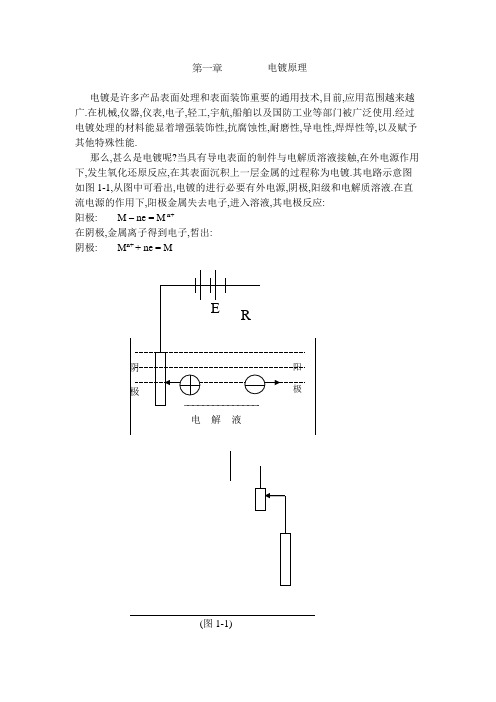
第一章电镀原理电镀是许多产品表面处理和表面装饰重要的通用技术,目前,应用范围越来越广.在机械,仪器,仪表,电子,轻工,宇航,船舶以及国防工业等部门被广泛使用.经过电镀处理的材料能显着增强装饰性,抗腐蚀性,耐磨性,导电性,焊焊性等,以及赋予其他特殊性能.那么,甚么是电镀呢?当具有导电表面的制件与电解质溶液接触,在外电源作用下,发生氧化还原反应,在其表面沉积上一层金属的过程称为电镀.其电路示意图如图1-1,从图中可看出,电镀的进行必要有外电源,阴极,阳级和电解质溶液.在直流电源的作用下,阳极金属失去电子,进入溶液,其电极反应:阳极: M – ne = M n+在阴极,金属离子得到电子,皙出:阴极: M n+ + ne = M(图1-1)阴极电解液在通常情况下,接通电源后,在电性作用下,阳离子向阴极移动,并在阴极上结合电子进行还原反应,阴离子向阳极移动并在电极上失去电子发生氧化反应.因而,阴阳极分别产生新物质.由金属活动性顺序表可知:K Ca Na Mg Al Zn Fe Ni Sn Pb(H) Cu Hg Ag Pt Au金属活动性逐步减小电极电位逐步升高在阴极上发生还原反应的能力逐步增强一.电镀层的作用:(1).提高金属零件在使用环境中的抗蚀性能;(2).装饰零件的外表,使其光亮美观;(3).提高零件的工作性能,如:提高零件表面硬度,耐磨性;增加金属表面的反光和防反光能力,提高导电性,电磁性,耐热性,焊焊性等.二.对镀层的要求:不同的产品,对镀层的要求也不同.但就其共性来说,对镀层的要求如下:(1).镀层与基体,镀层与镀层之间,应有良好的结合力;(2).镀层在零件的表面,应有均匀的厚度和细致的结构;(3).镀层应达到规定的厚度和尽可能少的孔隙;(4).镀层应具有符合规定的各项指标.第二章预处理第一节脱脂一.脱脂原理:油脂分为皂化性油脂和非皂化性油脂两类.动植物油属于皂化性油脂,能与碱性发生皂化反应生成可溶于水的肥皂;不能与碱发生皂化反应的矿物油属非皂化性油脂.除油方法一般有机械除油,化学除油,电化学除油三种.我们所使用的脱脂为电化学除油方式.在碱性电解液中金属工件受直流电的作用发生极化作用,使金属—溶液界面张力降低,溶液易于润湿并渗入油膜下的工件表面.同时,析出大量氢或氧对油膜猛烈地撞击和撕裂,对溶液产生强烈搅拌,加强油膜表面溶液的更新,油膜被分散成细小油珠脱离工件表面而进入溶液中形成乳浊液.电化学除油分为阴极除油和阳极除油两种.在相同的电流下,阴极除油产生的氢气比阳极除油产生的氧气多一倍,气泡小而密,乳化能力大,除油效果.但容易造成工件渗氢,引起氢脆和杂质在阴极析出的现象.阳极除油虽没有这些缺点,但可能会造成工件表面氧化和溶解.因而,应根据材料的不同,选择使用或结合使用.二.槽液成份及工艺条件:CP-100(g/L) 50- ~ 90 (自来水配制)温度(℃) 65- ~ 75电流密度(A/dm2) 1- ~ 5除油时间(min) 0.2- ~ 3PH值三.各组分作用:1.NaOH 有很强的皂化能力,其含量提高可加强皂化作用,但过高的含量会使皂化反应形成的肥皂溶解困难,对除油不利.2.Na2CO3呈弱碱性,水解生成碳酸氢钠,有一定皂化能力和对溶液PH值起缓冲作用(PH<8.5皂化反应不能进行,PH>10.2肥皂发生水解)3.磷酸盐有一定皂化能力和缓冲PH值的作用,同时又是一种乳化剂,溶解度大,洗去性好.四.常见故障分析及排除方法:第二节酸洗一.酸洗原理:酸洗指在酸液中除去金属工件表面上的氧化皮,不良表层组织的处理过程.CuO + H2SO4 = CuSO4 + H2O二.槽液成份及工作条件:30% H2SO40.6L/L (自来水配制)玻美度18 ~ -23时间0.2- ~ 2min三.组分作用:H2SO4主要是去掉来料的氧化皮,同时中和脱脂中带出的少量碱.反应为: H+ + OH- = H2O四.常见故障分析及排除方法:第三节 后处理一.冷热水洗:通过热水洗,冷水洗,使镀层表面附着异物彻底去除,将镀层清洗干凈. 二.风干,烘干.:主要为防止镀层附着水,使镀层发生斑渍,变色等,影响镀层的质量,最终导致不良品产生.第三章 镀镍第一节 镀镍层的性质和用途镍是白色微黄的金属,具有铁磁性.通常在其表面存在一层钝化膜,因而具有较高的化学稳定性.在常温下,对水和空气都是稳定的.易溶于稀酸,在稀H 2SO 4和稀盐酸中比在稀硝酸中溶解得慢,遇到发烟硝酸,则呈钝态.镍与强碱不发生作用. 镍的标准电极电位为-0.25V ,铜的标准电极电位为+0.34V .其元素符号为Ni,原子量为58.7,一般显示化合价为+2价.密度为8.90×103Kg/m 3(20℃).镍镀层的性质与采用的镀镍工艺有密切关系,工艺不同,获得的镍镀层的性能也不同.数据表明,采用氨基磺酸盐镀镍时,其镀层的物理性质如下表: 镍镀层的用途一般分为防护装饰性镀层和功能性镀层.我们在铜底材上镀镍属于防护装饰性镀层.以保护基体材料不受腐蚀.第二节 氨基磺酸盐镀镍一.原理:阴极反应: Ni 2+ + 2e = Ni 副反应: 2H + + 2e = H 2↑阳极反应: Ni - 2e = Ni2+ 副反应: 4OH- - 4e→2H2O+ O2↑析氧时,还发生镍被氧化成氧化膜的反应: 2Ni + 3[o] = Ni2O3 (禢色)严重时会产氯气: 2Cl- - 2e = Cl2↑因此,为了防止镍阳极氧化,常需加入阳极活化剂.二.槽液成份及工艺条件:氨基磺酸镍Ni(SO3NH2)2•4H2O 95 ~ 110 g/L氯化镍NiCl210.8 ~ 15 g/L硼酸H3BO330 ~ 50 g/LMP-200 适量PH值 3.5 ~ 4.2温度(℃) 55 ~ 65电流密度(A/dm2) < 25A/dm2.三.各组分作用:1.氨基磺酸镍: 主盐,提供电镀过程中不断消耗的Ni2+.2.氯化镍: 阳极活化剂,由于金属镍有很强钝化力,为了防止镍阳极钝化,加入NiCl2.它能促进阳极溶解,保证Ni2+正常补充,且可增加溶液的导电性,使镀层表面平滑,结晶细致,覆盖能力及分散能力改善.氯化物含量过低,阳极易钝化;过高会造成阳极过蚀,产生大量阳极泥渣,造成镀层起毛刺,且会增加镀层内应力,影响镀层质量.3.硼酸: 缓冲剂,该镀液镀Ni的合适PH为3.5 ~4.2. PH过低H+易放电,降低镀镍的电流效率,镀层易产生针孔.PH过高时,镀液混浊,阳极周围的金属离子会以金属氢氧化物夹入镀层中,使镀层机械性能恶化,外观粗糙.4.MP-200: 光亮剂,可增加阴极极化,降低镀层晶粒尺寸,使镀层细致,光亮,均匀.5.NiCO3: 导电盐,增加槽液的导电性,且可调升PH值.6.氨基磺酸盐: 调低槽液PH值.第四章镀钯镍第一节钯的基本特性钯为银白色贵金属,具有延展性.易受硝酸浸蚀,色泽较暗,在空气中还会变色.为了改善这些缺点,一般采用电镀白色光亮性钯镍合金.钯的密度为12g/cm3,元素符号Pd,原子量为106.4,一呈现+2价,电极电位为+0.8IV.电镀钯镍在电子工业中应用很广,用作硬金镀层的底层可以节约大量黄金,降低了电镀成本.第二节镀钯镍一.原理:电镀钯镍合金是一种光亮,银白色,硬度较高的镀层.可用于装饰性方面,如眼镜架,工艺品上,又可用于功能性方面,如电子工业上,一般采用不溶性阳极,用刷镀或浸镀或喷镀等方式.阳极反应: 40H- - 4E→O2↑+ 2H2O阴极反应: Pd2+ + 2e = Pd Ni2+ + 2e = Ni 其析为Pd/Ni合金二.槽液成份及工艺条件:Pd2+20g/LNi2+15 g/LNH3•H2O 适量湿润剂(Wetting) 适量光亮剂(Additive) 适量玻美度10 ~ 30PH 8.0 ~ 8.2温度45 ~ 55℃电流密度< 25 A/dm2三.各组分作用:1.P d2+主盐一般以氯化氨钯的形式存在,由于采用不溶性阳极,镀液中钯离子逐渐消耗,必须定时补充.2.N i2+主盐一般以氨基磺酸镍形式存在.可获得色泽较白的镀层,韧性也较好.3.N H3•H2O 稳定剂,并调整镀液的PH值,以保证在最佳范围.氨水的存在可使氯化钯以氯化铵钯形式存在于镀液中.氨水易挥发,须根据实际补充.一般低氨时槽液呈绿色,高氨为紫色,合适时为蓝绿色.4.光亮剂: 光亮剂可改善镀层性质,使光亮范围变宽,且镀层光亮细致,电流密度范围宽,分散性能良好.5.湿润剂: 辅助结合.四.常见故障分析及排除方法:第五章镀金金是一种色泽为金黄色的黄金属.元素符号为Au,原子量为197,一般呈+1价态,标准电极电位为+1.44V.电镀金层的性能优越,化学稳定性好,易于抛光延展性好.它的耐腐蚀性好,导电性良好,易焊接,耐高温,空气中不变色,被广泛应用于线路,板接插件等方面.一.原理:镀金溶液一般分为无氰化物溶液,低氰化物溶液和氰化物溶液.我们采用的是低氰化物溶液,以金氰化钾(K[Au(CN)2])为主盐.一般采用刷镀和喷镀.二.槽液成分及工艺条件:KAu(CN)2 (g/L) 3 ~ 13 g/L柠檬酸(g/L) 6 ~ 10 g/LCo2+750ppm平衡盐20 g/L导电盐玻美度<12 添加PH 4.5左右温度(℃) 55 ~ 65电流密度(A/dm2) < 25 A/dm2三.各组分作用:1.金的含量: 提高其含量可相应提高电流密度上限和镀层的光泽,加快沉积速率,但过高则镀层结晶较粗,颜变红,金含量低时,电流密度范围变窄,镀层呈暗红色.2.钴的含量: 钴的含量升高时,则阴极电流效率下降,内应力提高,沉积速率下降,镀层变得光亮.3.有机添加剂: 由于有机添加剂在电极表面吸附,增大了电化学反应的阻力,使金属离子还原的反应变得困难,有利于晶核的形成,可获得细小的晶粒.另外,加入添加剂后,它可优先吸附在某些活性较高,生长速度较快的晶面,使金属原子进入这些位置遇到困难,即将各个晶面的生长速度拉匀,构成致密的镀层.4.柠檬酸: 调节PH值,作为络合剂,络合金离子.]第六章镀Sn/Pb锡是银白色金属,具有较高的化学稳定性,在大气中不易变色,在硫酸,硝酸,盐酸的稀溶液中几乎不溶解,特别是在有机酸中很稳定.元素符号为Sn,原子量为118.7,一般呈+2价,电极电位为-0.14V.铅是软的,强度不高的金属,很易被空气氧化成致密的碱式碳酸盐保护层.无素符号为Pb,原子量为207.2,一般+2价,电极电位-0.26V.一.原理:锡铅合金的熔点比纯锡和纯铅还低,它的孔隙率,可焊性比单金属好.由于锡和铅都属碳族元素,且标准电位只相差10mv,两者的超电压都很小,很容易形成锡铅合金镀层.二.槽液成分及工艺条件:Sn2+45 ~ 69g/LPb2+ 3.8 ~ 8 g/L锡铅酸15 ~ 25%BT-----–64 Additive 适量BTD Additive 适量Carrier (辅助剂) 适量抗氧化剂RD 适量温度(℃) 15 ~ 30℃电流密度(A/dm2) < 25 A/dm2三.各组分作用:1.Sn2+ Pb2+ 主盐提供镀层金属2.锡铅酸: 提供介质环境3.光亮剂: 促进镀层表面光亮,改善镀层的外观效果,过少,镀层易烧焦,过多,容易造成槽液老化.附录:附录一.常见电镀术语1.电镀: 在外电源作用下,被迫发生氧化还原反应,从而使金属或非金属工件表面上沉积一层金属的方法.2.电解: 在外电源作用下,发生氧化还原反应的过程.3.化学镀: 发生氧化还原反应,从而使金属或非金属工件表面再沉积一层金属的方法.4.电极: 金属和电解质溶液(离子导电相)直接接触所构成的体系称为电化学电极,简称电极.5.氧化还原反应: 有氧化数变化或电子转移的化学反应.6.电极电量: 产生在金属和它的盐溶液之间的电量叫金属的电极电量.7.电导率: 指长1m,截面积为1m2的导体的电导.单位为数n-1,m-1).8.电导: 电阻的倒数单位为(n-1).9.内应力: 由于种种原因引起镀层晶体结构的变化,常会使其被伸长或缩短,但因镀层被固定基体金属上,遂使镀层处于受力状态,这种作用于镀层单位面积上的内力.就称为内应力.10.刷镀: 使用不溶性阳极,阳极表面覆有吸附材料,这些吸附材料浸在电解液中,在完全浸润的情况下,将阳极与阴极(镀件)相接触,电沉积便发生了.这种电镀方式称为刷镀.11.浸镀: 将阴极全浸(或部分)浸在槽液中,以得到镀层的方式,称为浸镀.12.喷镀: 使用不溶性阳极,用控制电解液与待镀工件接触部位的工具具(如刻孔皮带),使工件通过时,电解液只沿规定方向与工件接触,在接触部位生成镀层的方法.13.氢脆: 氢离子在阴极被还原后,一部分以H2↑逸,出一部分以原子氢的状态渗入基体金属及镀层的韧性下降而变脆.这称为氢脆.14.针孔: 氢在阴极析出后,若在电镀过程中,氢气泡总是滞留在一个地方,就会在镀层中形成空洞或缝隙,亦称针孔.15.麻点: 若氢气泡在阴极上附着得不牢固,发生周期性的滞留与脱落,就会出现麻点.16.白针: 镀金部位未镀到金,称为白针.17.烧焦: 指镀层发黑.,发暗等现象.18.Sn/Pb白雾: Sn/Pb槽液附着在镀层上形成的雾状物.19.脱皮: 镀层与其体金属或镀层与镀层之间接触不好,或附着性差,使镀层松散脱落,称为脱皮.20.阴极: 电化学上析出金属或氢气的电极→发生还原.21.阳极: 金属发生电化学溶解,或不溶性的场合,发生阴离子氧化的电极,→发生氧化22.电流密度: 电极的单位面积上通过的电流.23.Hull槽试验: 观察在各种电流密度或不同条件下,电极表面镀层变化的一种特殊形状电解槽的试验.24.酸洗: 将工件浸入酸溶液中,以去除表面氧化皮的过程.25.脱脂: 将工件表面油污去除的过程.26.带出: 槽内溶液附着于被镀表面上而被带出槽子.27.表面活性剂: 减少表面张力,使其湿润良好或乳化分散的物质.28.光亮剂: 让电镀膜光泽性改善的物质.29.阳极袋: 为了防止阳极泥渣影响被镀工件质量而用的袋子.30.密着性:电镀层与其下层金属之间附着力之强弱.。
电镀生产 原理

电镀生产原理
电镀生产是一种将金属涂覆在物体表面的工艺,通过电解液中的金属离子在电流作用下,被还原为金属原子并沉积在物体表面的过程。
电镀生产的主要原理是基于电解现象。
当直流电流通过电解液时,正极(阳极)上的金属离子会被还原成金属原子,而负极(阴极)上的物体表面则接收并沉积这些金属原子。
这样一来,物体表面就形成了一层金属覆盖层,实现了电镀。
为了进行电镀,在电解槽中需要加入一种称为电解液的溶液。
电解液通常由金属盐和其他添加剂组成,以提供金属离子和调节电解液性质的功能。
金属离子在电解液中的浓度决定了电镀效果的好坏。
在电镀生产中,除了使用适当的电解液,还需要控制电镀过程中的参数,如电流强度、电镀时间、电极间距等。
这些参数的调整可以影响金属离子在物体表面沉积的速度和均匀性,进而影响电镀层的质量。
电镀生产具有重要的应用价值。
通过电镀,可以有效地改善物体的外观和性能,例如增加金属的亮度和耐腐蚀性。
此外,电镀还可以在产品制造过程中实现精密加工,提高产品质量和精度,因此广泛应用于电子、汽车、家居等领域。
总之,电镀生产是一种利用电解现象将金属涂覆在物体表面的工艺。
通过控制电流、电解液和工艺参数,可以实现金属离子
在物体表面的沉积,形成金属覆盖层,从而改善物体的外观和性能。
电镀的基本原理

电镀的基本原理电镀是指在金属表面电解沉积一层金属或非金属的薄膜,以改善金属表面性质或美观性。
其基本原理是利用电解质中的离子,通过电场的作用,将金属离子沉积在工件表面,形成均匀、致密的金属膜。
下面就来详细介绍一下电镀的基本原理。
1. 电解质电解质是电镀过程中的重要组成部分,它既可以提供金属的离子,也可以在电解过程中起到保护和调节电解质pH值的作用。
电解质的种类和组成因不同的金属和不同的电镀工艺而异,一般包括金属盐、酸和碱等。
2. 电源电源是电镀过程中的另一个重要组成部分,它提供电能使电镀过程得以进行。
电源的种类包括直流电源和交流电源,其中直流电源是电镀的主要电源。
在电镀过程中,电源的电压和电流密度是影响电镀质量的重要因素。
3. 电极电极是电镀过程中的一个关键部分,它是连接电源和工件的桥梁。
电极分为阴极和阳极两种,阴极是工件,阳极是电解质中提供金属离子的金属条。
在电极反应中,阴极上的金属离子被还原,生成金属膜,阳极上的金属被氧化,形成离子进入电解质中。
4. 电镀过程电镀过程是通过电解质中的离子,通过电场的作用,将金属离子沉积在工件表面的过程。
在电镀过程中,阴极上的金属离子被还原为金属膜,而阳极上的金属被氧化成离子进入电解质中。
因此,电镀过程中,阴极的电流密度要比阳极小得多,以保证金属离子能够沉积在工件表面。
5. 电镀质量电镀质量是评价电镀产品好坏的重要指标。
电镀质量受到多种因素的影响,如电解质的种类和浓度、电源的电压和电流密度、电镀时间、温度和搅拌等。
在电镀过程中,要保证各种因素的协调和平衡,以获得良好的电镀质量。
电镀是一种重要的表面处理方法,其基本原理是利用电解质中的离子,在电场的作用下,将金属离子沉积在工件表面,形成均匀、致密的金属膜。
电解质、电源、电极和电镀过程是电镀过程中的基本组成部分,它们的协调和平衡是保证电镀质量的关键。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
电镀基本原理电镀工艺基础理论一、电镀概述简单来说,电镀指借助外界直流电的作用,在溶液中进行电解反应,使导电体例如金属的表面沉积一金属或合金层。
我们以硫酸铜的电镀作例子:硫酸铜镀液主要有硫酸铜、硫酸和水,甚至也有其它添加剂。
硫酸铜是铜离子(Cu2+)的来源,当溶解于水中会离解出铜离子,铜离子会在阴极(工件)还原(得到电子)沈积成金属铜。
这个沉积过程会受镀浴的状况如铜离子浓度、酸碱度(pH)、温度、搅拌、电流、添加剂等影响。
阴极主要反应: Cu2+(aq) + 2e-→Cu (s)电镀过程中的铜离子浓度因消耗而下降,影响沉积过程。
面对这个问题,可以两个方法解决:1.在浴中添加硫酸铜;2.用铜作阳极。
添加硫酸铜方法比较麻烦,又要分析又要计算。
用铜作阳极比较简单。
阳极的作用主要是导体,将电路回路接通。
但铜作阳极还有另一功能,是氧化(失去电子)溶解成铜离子,补充铜离子的消耗。
阳极主要反应: Cu (s) →Cu2+(aq) + 2e-由于整个镀液主要有水,也会发生水电解产生氢气(在阴极)和氧气(在阳极)的副反应阴极副反应: 2H3O+(aq) + 2e-→H2(g) + 2H2O(l)阳极副反应: 6H2O(l) →O2(g) + 4H3O+(aq) + 4e-结果,工件的表面上覆盖了一层金属铜。
这是一个典型的电镀机理,但实际的情况十分复杂。
电镀为一种电解过程,提供镀层金属的金属片作用有如阳极,电解液通常为镀着金属的离子溶液,被镀物作用则有如阴极。
阳极与阴极间输入电压后,吸引电解液中的金属离子游至阴极,还原后即镀着其上。
同时阳极的金属再溶解,提供电解液更多的金属离子。
某些情况下使用不溶性阳极,电镀时需添加新群电解液补充镀着金属离子。
电镀一般泛指以电解还原反应在物体上镀一层膜。
其目前使用种类有:一般电镀法(electroplating)、复合电镀(composite plating)、合金电镀(alloy plating)、局部电镀(selective plating)、笔镀(pen plating)等等。
由于电镀表面具有保护兼装饰效用;故广被应用。
也有少部分的电镀提供其它特性,诸如高导电性、高度光反射性或降低毒性,最常使用的电镀金属为镍、铬、锡、铜、银及金。
点击观看电沉积原理Flash图二、电镀的原理和概念2.1 电镀的定义和目的电镀(electroplating)被定义为一种电沉积过程(electrode-position process),是利用电极(electrode)通过电流,使金属附着于物体表面上,其目的是在改变物体表面之特性或尺寸。
电镀的目的是在基材上镀上金属镀层(deposit),改变基材表面性质或尺寸。
例如赋予金属光泽美观、物品的防锈、防止磨耗、提高导电度、润滑性、强度、耐热性、耐候性、热处理之防止渗碳、氮化、尺寸错误或磨耗之另件之修补。
2.2电镀基础知识电镀大部份在液体(solution)下进行,又绝大部份是由水溶液(aqueous solution)中电镀,约有30种的金属可由水溶液进行电镀,由水溶液电镀的金属有:铜Cu、镍Ni、铬Cr、锌Zn、镉Cd、铅Pb、金Au、银Ag、铂Pt、钴Co、锰Mn、锑Sb、铋Bi、汞Hg 、镓Ga、铟In、铊、As、Se、Te、Pd、Mn、Re、Rh、Os、Ir、Nb、W 等;有些必须由非水溶液电镀如锂、钠、钾、铍、镁、钙、锶、钡、铝、La、Ti、Zr、Ge、Mo等;既可由水溶液又可由非水溶液电镀的有铜、银、锌、镉、锑、铋、锰、钴、镍等金属。
电镀的基本知识包括:溶液性质;物质反应;电化学;化学反应方程式;界面物理化学;材料性质等。
电镀与其它镀覆方法电沉积过程的比较2.2.1 溶液(solution)被溶解之物质称为溶质(solute),使溶质溶解之液体称之溶剂(solute)。
溶剂为水的溶液称之水溶液(aqueous solution)。
表示溶质溶解于溶液中的量为浓度(concentration)。
在一定量溶剂中,溶质能溶解之最大量值称为溶解度(solubility)。
达到溶解度值的溶液称为饱和溶液(saturated solution),反之为非饱和溶液(unsaturated solution)。
溶液浓度,在工厂及作业现场,使用易了解及便利的重量百分率浓度(weight percentage)。
另外常用的莫耳浓度(molal concentration)。
2.2.2 物质反应(reaction of matter)在电镀处理过程中,有物理变化及化学变化,例如研磨、干燥等为物理反应,电解过程有化学反应,我们必须充份了解在处里过程中各种物理及化学反应及其相互间关系与影响。
2.2.3 电镀常用之方程式(chemical formular)见附录一。
2.2.4 电化学(electrochemistry)电镀是一种电沉积( electrodeposition )过程,利用电解体electrolysis)在电极(electrode)沉积金属,它是属于电化学应用的一类。
电化学是研究有关电能与化学能交互变化作用及转换过程。
电解质(electrolyte)例子NaCl,也就是其溶液具有电解性质的溶液(electrolytic solution)它含有部份离子(ions),经由这些离子移动(movement)而能导电。
带负电荷朝向阳极(anode)移动称为阴离子(anion),带正电荷朝向阴极(cathode)移动(migrate)者称为阳离子cations)。
这些带电荷粒子(particles)称之为离子(ions)。
放出电子产生氧化反应的电极称为阳极(anode),得到电子产生还原反应的电极称为阴极(cathode)。
整个反应过程称为电解(electrolysis)。
2.2.4.1 电极电位(electrode potentials)电位(electrode potential)为在电解池(electrolytic)中的导电体,电流经由它流入或流出。
电极电位(electrode potential)是电极与电解液之间的电动势差,单独电极电位不能测定需参考一些标准电极(standard electrode)。
2.2.4.2 标准电极电位(standard electrode potential)标准电极电位(standard electrode potential)是指金属电极活度为1(纯金属)及在金属离子活度为1时的电极电位。
氢的标准电位在任何温度下都定为0,作为其它电极的参考电极(REFERENCE ELECTRODE),以氢标准电极为基准0,各种金属的标准电位不同。
排列在前头的金属如Li较易失去电子,易被氧化、溶解、腐蚀,可称为溅金属或金属(basic metal)。
相反如Au金属不易失去电子,不易氧化,不易溶解,容易被还原称为贵金属(noble/precious metal)。
2.2.4.3 Nernst 电位学说金属含有该金属离子的溶液相接触,则在金属与溶液界面会产生电荷移动现象。
这种电荷移动,仍是由于金属与溶液的界面有电位势差即电位差所引起,此现象Nernst解释如下: 设驱使金属失去电子变为阳离子溶入溶液中的电离溶解液解压(electrolatic solution pressure)为Ps,而使溶液中的阳离子得到电子还元成金属渗透压(osmotic pressure)为Po,则有三种情况发生:(1) Ps>Po时,金属被氧化,失去电子,溶解成金属离子于溶液中,因此金属电极本体接收电子而带负电;(2) Ps<Po时,金属阳离子得到电子被还原并沉积于金属电极表面上,金属电极本身供给电子,因此金属电极带正电;(3) Ps=Po时,没有产生任何变化。
2.2.4.4电极电位在热力学的表示法电极反应是由氧化反应及还原反应所组成。
例如Cu ? Cu+++2e-还原状态氧化状态可用下列二式表示:Cu??? Cu+++2e-氧化反应Cu? Cu+++2e-还原反应例1: 氧电极反应的电位1/2O2+H2O+2e-? 2OH-例2: 氯化汞电极反应的电位Hg2+2+2e-? 2 Hg E=E0- RT/nF ln aHg(s) /aHg2+2例3: 氢电极反应的电位1/2H2(g) ? H++e- E=E0-RT/F ln aH+/aH21/2(g)2.2.4.5 电极电位的意义(1)电解电位分类为三种:M/M+n即金属含有该金属离子的相接触有二种形式:(1)金属与溶液间水的结合力大于金属阳离子M+n与电子的结合力,则金属会溶解失去电子形式金属阳离子与水结合成为M+n?xH2O,此时金属电极获得额外电子,故带负电。
这类金属电极称为阴电性,如Mg、Zn及Fe等浸入酸、盐类的水溶液时,就会产生这种电极电位。
即Mt M(aq)+n+ ne-。
金属与溶液的水结合力小于金属离子M+n与电子结合力时,金属离子会游向金属电极得到电子而沉积在金属电极上,于是金属电极带正电,溶液带负电。
(2)金属M与难溶性的盐MX相接触,同时MX又与阴离子KX相接触,即(M x MX,KX) 如氯化汞电极(Hg2Cl2)。
(3)不溶性金属如Pt,与含有氧化或还原系离子的溶液相接触,例如Pt x Fe++ 、FE++或Pt x Cr+2、Cr+3等。
2.2.4.6 界面电性二重层在金属与溶液的界面处带电粒子与表面电荷形成的吸附层,偶极子的排列层以及扩散层等三层所组合的区域称为界面性二重层。
2.2.4.7液间电位差(liquid junction potential)又称为扩散电位差(diffusion potential),系由阴离子与阳离子的移动度不同而形成电位差,通常溶液浓度差愈大,阴阳离子移动度差愈大,则液间电位差愈大。
2.2.4.8过电压(overvoltage)当电流通过时,由于电极的溶解、离子化、放电、及扩散等过程中有一些阻碍,必须加额外的电压来克服,这些阻碍使电流通过,这种额外电压消除阻碍者称为过电压。
此种现象称之为极化(polarization)。
此时阴极、阳极实际电位与平衡电位之差即为阴极过电压、阳极过电压。
过电压可分下列四种:1.活化能过电压(activiation overvoltage)任何反应,不论吸热或放热反应皆需克服最低能量障,该能障称为活化能,在电解反应需要额外电压来克服活化能阻碍,这个额外电压的活化能过电压,其电流i愈大,g act愈大,电镀中gact 占很小一部份,几乎可以忽略,除非电流密度很大。
氢过电压(hydrogen overvoltage),在酸性水溶液中阴极反应产生H2气体,这个额外电压称为氢的过电压,即gH2=Ei-Eeq 式中gH2=氢过电压Ei=实际电压,Eeq=平衡电压。
