药品稳定性试验标准操作规程
注射用重组人生长激素稳定性试验方案

注射用重组人生长激素稳定性试验方案一、研究目的本试验旨在评估注射用重组人生长激素的稳定性,以确定其在一定条件下的质量保持期限。
二、试验方法1.试验样品-收集符合规定的注射用重组人生长激素样品,确保其符合药品质量标准。
-样品应避免暴露在光线和高温等有害因素下,同时在试验过程中避免反复冻融。
2.试验条件-温度:在25°C±2°C的条件下进行试验。
-湿度:相对湿度控制在60%±5%。
-光照条件:采用黑暗遮光的环境,避免光照影响。
-储存容器:试验样品储存在由玻璃或塑料制成的密封容器中。
3.试验项目-化学稳定性:包括药物活性、纯度、杂质含量、溶解度等方面的评估内容。
-物理稳定性:包括药物的颜色、外观、稠度等方面的评估内容。
-微生物稳定性:包括细菌、真菌等微生物污染的评估。
4.试验过程-样品储存在不同时间点下,在试验结束时进行检测。
-化学稳定性:使用适当的化学分析方法,对样品进行相关化学指标的测定。
-物理稳定性:通过观察样品的外观、颜色、气味等特征判断其稳定性。
-微生物稳定性:使用适当的微生物检测方法,对样品进行微生物污染的评估。
5.数据分析-根据试验结果,综合分析药物在不同条件下的稳定性表现。
-结合药物质量标准,确定药物的质量保持期限。
三、质量控制2.试验操作:试验过程中严格按照标准操作规程进行,保证数据的准确性和可靠性。
3.试剂和仪器设备:选择合适的试剂和仪器设备,保证试验结果的准确性和可靠性。
4.数据分析:对试验结果进行统计分析和合理解释。
四、安全防范措施1.安全操作:试验过程中保持良好的个人卫生,严格遵循实验室的操作规程。
2.废弃物处理:将试验所产生的废弃物进行分类和正确处理,遵循相关的废弃物处理规范。
通过以上试验方案,可以对注射用重组人生长激素的稳定性进行评估,并确定其质量保持期限,以保证药物在使用过程中的有效性和安全性。
同时,该方案还包括了质量控制和安全防范措施,以确保试验过程的可靠性和安全性。
稳定性试验操作规程

稳定性试验操作规程一、目的:保健食品稳定性试验是指保健食品通过一定程序和方法的试验,考察样品的感官、化学、物理及生物学的变化情况。
通过稳定性试验,考察样品在不同环境条件下(如温度、相对湿度等)的感官、化学、物理及生物学随时间增加其变化程度和规律,从而判断样品包装、贮存条件和保质期内的稳定性。
二、适用范围:所有市售批次产品。
二、稳定性试验的要求:1.稳定性试验包括长期试验和加速试验。
长期试验和加速试验考察产品质量稳定性的样品,总体考察时间应涵盖所预期的保质期,长期试验和加速试验的数据应以与0月数据相比无明显改变。
2.长期试验和加速试验适用于软硬胶囊及固体制剂的保健品, 供试品取样量是全检量的两倍。
供试品应是市售包装一致的产品。
3.长期试验和加速试验供试品的质量标准应与市售产品质量标准一致。
4.加速试验所用设备:应能控制温度±2℃,相对湿度±5%,并能对真实温度和湿度进行监控。
4.研究保健品稳定性,要采用专属性强、准确、精密、灵活的分析方法,并对方法进行验证以保证供试品稳定性试验结果的可靠性。
三、保健品的稳定性试验:1.加速试验:加速试验是在超常的条件下进行的。
其目的是通过加速供试品的化学或物理变化,探讨供试品的稳定性,为供试品审评、包装、运输及储存提供必要的资料。
要求供试品,在温度37℃±2℃、相对湿度75%±5% 的条件下放置3个月,避免光线直射。
在试验期间第0个月、1个月、2个月、3个月末各取样一次,按稳定性重点考察项目进行检测。
将结果与0月的数据比较,以确定样品的有效期。
2.长期试验:长期试验是在接近供试品的实际储存条件下进行,其目的为制订样品的有效期提供数据。
要求供试品,在温度25℃±2℃、相对湿度60%±10% 的条件下放置至保质期,避免光线直射。
第一年每 3 个月取样一次,分别于0个月、3个月、6个月、9个月、12个月,按稳定性重点考察项目进行检测。
药品稳定性试验标准操作规程

目的:考核药品质量稳定性,为确定药品的合理有效期提供科学依据。
范围:原料、中间产品、成品的稳定性试验1.药物稳定性试验的目的是考察药物在规定的条件下随时间变化的规律,为药品的生产、包装、贮存、运输条件提供科学依据,同时通过试验建立药品的有效期。
2.稳定性试验的基本要求2.1稳定性试验包括影响因素试验、加速试验和长期试验。
其中影响因素试验适用于原料药,而加速试验和长期试验适用于原料药和制剂。
2.2 加速试验和长期试验样品所用容器、包装材料和包装方式应与上市产品一致。
2.3 应重视有关物质的检查。
3.影响因素试验影响因素试验是在比加速试验更强烈的条件下进行,其目的是探讨药物的固有稳定性,了解影响其稳定性的因素及可能的降解途径与降解产物,为制剂生产工艺、包装、贮存条件与建立降解产物的分析方法提供科学依据。
试验时,将样品置于适宜的容器中,摊成≤5mm厚的薄层,疏松原料药可摊成≤10mm厚的薄层,进行以下试验:3.1高温试验3.1.1将供试品置于适宜的容器中(如称量瓶或培养皿中)摊成≤5mm厚的薄层,疏松原料药可摊成≤10mm厚的薄层,在60℃下放置10天,于第5天和第10天取样,按照稳定性重点考察项目进行检测,即:性状、熔点、含量、有关物质、吸湿性、以及根据药品性质选定的考察项目。
3.1.2 若检测结果与0天结果比较,有明显变化(如含量下降5%),则40℃下按同法进行试验。
如60℃的结果无明显变化,不再进行40℃试验。
3.2 高湿度试验在25℃将供试品开口置于相对湿度90±5%的恒湿密闭容器中(在密闭容器中放置硝酸钾饱和溶液),放置10天,于第5天和第10天取样,检验上述项目,重点考察供试品的吸湿性。
如吸湿增重5%以上,则在相对湿度75±5%条件下(在密闭容器中放置氯化钠饱和溶液),同法进行试验。
如吸湿增重5%以下,而且其他项目符合要求,则不再进行此项试验。
3.3 强光照射试验将供试品开口置于装有日光灯的光照箱或适宜的光照箱中,照度为4500±500lx,放置10天,于第5天和第10天取样,检验上述项目,特别要注意外观的变化。
稳定性考察操作规程

一、目的:建立稳定性考察操作规程,规范稳定性考察方法。
二、范围:本规程规定了稳定性考察方法和操作要求;适用于物料及产品的稳定性考察。
三、职责:质量控制科负责人、质量控制科技术员、质量控制科检验员对实施本标准负责。
四、内容:1 制定年度持续稳定性考察计划1.1 质量控制科负责人于每年12月份根据下一年度的生产计划制订第二年的《年度持续稳定性考察计划》,确定第二年度持续稳定性考察程序的品种。
并交质量管理负责人审核批准。
2 各品种持续稳定性考察方案的制定2.1 质量控制科技术员应在收到持续稳定性考察的申请单后1周内完成该品种持续稳定性考察方案的编写工作,并交质量控制科负责人审核,质量管理负责人批准。
2.2 持续稳定性考察方案的内容2.2.1 需进行考察产品的名称、规格、考察批次数。
2.2.2 相关的物理、化学、微生物和生物学检验方法,或采用持续稳定性考察专属的检验方法。
2.2.3 检验方法依据。
2.2.4 合格标准。
2.2.5 容器密封系统的描述。
2.2.6 试验间隔时间。
2.2.7 贮存条件或试验条件采用《中国药典》规定的稳定性试验标准条件。
2.2.8 检验项目,为产品质量标准所包含的全部项目,如检验项目少于产品质量标准所包含的项目,应当说明理由。
2 各品种持续稳定性考察样品量2.1 影响因素试验需1个批次,加速试验和长期试验需3个批次(或至少每年应当考察一个批次,除非当年没有生产。
)。
3 各品种持续稳定性考察项目3.1 产品持续稳定性考察项目:产品持续稳定性考察项目表3.2 中间产品、待包装产品持续稳定性考察项目除装量外均按3.1项执行。
4 持续稳定性考察方法4.1 影响因素试验4.1.1 高温试验:供试品开口置密封洁净容器中,在60℃温度下放置10天,于第5天和第10天取样检测有关指标。
如供试品发生显著变化,则应在40℃下同法进行试验。
如60℃无明显变化,则不必进行40℃试验。
4.1.2 高湿度试验:供试品开口置恒湿密闭容器中,于温度25℃,相对湿度 90%±5%条件下放置10天,在第5天和第10天取样检测有关指标。
稳定性试验规定,稳定性指导原则,稳定性试验方法

FDA药物稳定性试验指导原则药品稳定性试验规定每年底制定下年度原料和制剂成品稳定性试验书面计划,内容包括:规格标准、检验方法、检验周期、每批数量、考查项目、考查频次、时间等。
经批准后执行,新开发的制剂品种在开发阶段应制定稳定性计划。
3 公司药品生产用原料稳定性试验可采用影响因素试验法:3.1 将一批供试品除去包装以后,平放在平皿中,在以下条件下按规定贮存,检测重点考查项目各项质量指标的变化情况。
重点考查项目包括:性状、熔点、含量、有关物质、吸湿性及根据药品性质选定的考查项目。
影响因素试验条件:3.1.1 暴露在常温空气中;3.1.2 高温试验,温度分别为60℃、40℃两个温度水平;3.1.3 高湿试验,湿度分别为90%±5%、75%±5%两个湿度水平;3.1.4 强光照射试验,照度为4500LX±500LX4 制剂稳定性试验:4.1 加速试验:取供试品三批,按市售包装,在温度40℃±2℃,相对温度75%±5%的条件下放置6个月,在第一个月、第二个月、第三个月、第六个月末取样检测各剂型规定的重点考查项目的质量指标变化情况。
片剂的重点考察项目为:性状、含量、有关物质、崩解时限或溶出度。
硬胶囊剂的重点考查项目为:外观、内容物色泽、含量、有关物质、崩解时限或溶出度、水份。
液体制剂的重点考察项目为:性状、相对密度、含量、pH值、微生物限度检查。
3个月后测试符合要求,有效期暂定为2年,6个月后测试符合要求有效期暂定为3年。
4.2 长期试验:取供试品三批,按市售包装,在规定保存条件下贮存,每年检测一次,重点考查项目的质量指标变化情况,观察3年的检验结果,以确定产品的贮存期或有效期。
5 严格按照批准的书面稳定性计划,做好试验记录,如发现异常情况,采取措施及时调整。
6 试验结束后,对试验结果进行数理统计后处理,评定并作出结论。
写出稳定性试验报告,所有资料归档保存。
稳定性试验标准操作规程

--------------------------------------------------------------------------------------------------------------------------------------------稳定性实验标准操作规程1、目的:考察药品在温度、湿度、光线的影响下随时间变化的规律,为药品的生产、包装、储存、运输条件提供科学依据,同时通过试验建立药品的有效期。
2、仪器设备恒温恒湿培养箱、光照箱4、实验主体内容4。
1 稳定性试验的内容:4.1。
1加速破坏试验,预测样品的有效期4.1。
2样品在规定的保存条件下观察若干年限的检测结果。
4。
2稳定性试验的基本要求:4.2.1稳定性试验包括影响因素试验、加速试验和长期试验4。
2。
1。
1 影响因素试验适用于原料药的考察,用1 批原料药进行4。
2。
1。
2加速试验和长期试验适用于原料药与药物制剂,要求用3 批供试品进行4。
2。
2原料药供试品是一定规模生产的,供试品量相当于制剂稳定性实验所要求的批量,原料药合成工艺路线、方法、步骤应与大生产一致。
药物制剂的供试品应是放大试验的产品,其处方与生产工艺应与大生产一致4。
2。
3供试品的质量标准应与各项基础研究及临床验证所使用的供试品质量标准一致4。
2.4加速试验与长期试验所用供试品的容器和包装材料及包装方式应与上市产品一致4。
2。
5研究药物稳定性,要采用专属性强、准确、精密、灵活的药物分析方法和有关物质的检查方法,并对方法进行验证以保证药物稳定性试验结果的可靠---------------------------------------------------------精品文档-----------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------性。
原料药与稳定性试验标准操作规程

目的:为考察产品的性质在温度、湿度、光线等条件的影响下随时间变化的规律,为产品在生产、包装、贮存、运输条件和有效期的确定提供科学依据,以保障产品安全有效。
应用范围:适用于本公司产品的稳定性考察。
负责人:QC、QA、质量部负责人内容:1 质量部负责稳定性试验的全面工作,化验室负责稳定性的检验工作。
2 质量部每年年底制定下年度稳定性考察计划,内容包括:产品名称、检验方法依据、检验方法、检验项目、贮存条件、每批数量、测试时间等,经质量负责人批准后方可执行。
新开发的产品在开发阶段应制定稳定性计划。
3 基本要求。
3.1 稳定性试验包括影响因素试验、加速试验与长期试验。
影响因素试验用1批原料药或1批制剂进行。
加速试验与长期试验用3批供试品进行。
3.2 原料药供试品应是一定规模生产的,供试品量相当于制剂稳定性实验所要求的批量,原料合成工艺路线、方法、步骤应与大生产一致。
药物制剂的供试品应是放大试验的产品其处方与生产工艺应与大生产一致。
药物制剂如片剂、胶囊剂、每批放大试验的规模,片剂或胶囊剂在10000片或10000粒。
大体积包装的制剂如静脉输液等,每批放大规模的数量至少应为各项实验所需总量的10倍。
特殊品种、特殊剂型所需数量,根据情况另定。
3.3 供试品的质量标准应与临床前研究及临床实验和规模生产所使用的供试品质量标准一致。
3.4 加速试验与长期试验所用供试品的包装应与上市产品一致。
3.5 研究药物稳定性,要采用专属性强、准确、精密、灵敏的药物分析方法与有关物质(含降解产物及其他变化所生成的产物)的检查方法,并对方法进行验证,以保证药物稳定性结果的可靠性。
在稳定性试验中,应重视降解产物的检查。
3.6 由于放大试验比规模生产的数量要小,故申报者应承诺在获得批准后,从放大试验转入规模生产时,对最初通过生产验证的3批规模生产的产品仍需进行加速试验与长期稳定性试验。
4 操作流程4.1 稳定性试验计划4.1.1 计划内容应包括:产品名称、产品考察批次、检验方法依据、检验方法、检验项目、合格标准、考察时间、贮存条件、4.1.2 产品考察批次应选择具有代表性,能反映出研究目的。
SHH-SD型药品稳定性试验箱标准操作规程
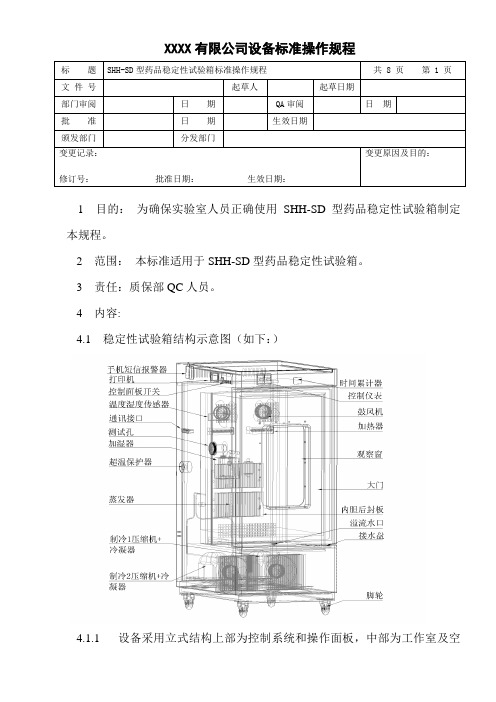
XXXX有限公司设备标准操作规程标题SHH-SD型药品稳定性试验箱标准操作规程共 8 页第 1 页文件号起草人起草日期部门审阅日期QA审阅日期批准日期生效日期颁发部门分发部门变更原因及目的:变更记录:修订号:批准日期:生效日期:1 目的:为确保实验室人员正确使用SHH-SD型药品稳定性试验箱制定本规程。
2 范围:本标准适用于SHH-SD型药品稳定性试验箱。
3 责任:质保部QC人员。
4 内容:4.1 稳定性试验箱结构示意图(如下:)4.1.1 设备采用立式结构上部为控制系统和操作面板,中部为工作室及空调室,下部为制冷系统。
4.1.2 箱壳采用优质冷轧钢板拼块结构。
4.1.3 内胆采用镜面不锈钢钢板。
4.1.4 保温材料为超细玻璃棉或泡沫板。
4.1.5 矩形中空玻璃观察窗。
4.2 供水系统连接:4.2.1 供水系统示意图如下:4.2.2 接上进水连接管(另一头和水泵出水口相接);4.2.3 接上出水连接管和溢流连接管(另一头通过水桶盖插入水桶);4.2.4 将水桶按供水要求加满水后,盖上桶盖;4.2.5 插上抽水泵电源。
5 操作使用:5.1 控制面板操作说明5.1.1 控制面板示意图如下:5.1.2 插上电源连线后打开电源开关。
5.1.3 超温保护设定:设定在试验温度以上10~20℃。
其作用是如果出现温度高于超温保护器时,设备将自动断电保护。
5.1.4 温湿度超差报警:当试验箱温度出现±2℃、湿度出现±5%R.H的超差时会报警,此时设备本身自带蜂鸣器会发出“滴滴”报警声,并向所设置的手机号码发送报警短信。
此时控制仪表上“EV1”灯亮,开启“报警消声”开关,即可消除蜂鸣器报警声。
5.1.5 制冷机组:打开面板制冷开关,并通过观察仪表温度显示屏一段时间后,温度开始下降,这表明制冷机开始工作。
5.1.6 使用该设备做下述对应试验条件时,参照执行下表规定的开关设置要求:面板开关试验温湿度条件制冷1 制冷2 照明报警消声备注40℃,75%R.H 关开需要时开启1.刚试机时温湿度不稳定可打开.2.试验温湿度稳定后关闭1.400SD,500SD和1000SD在室温30℃左右时可同时打开制冷1和制冷2;2.当制冷1系统被确认有故障时,关闭制冷1系统,启用制冷2系统;3.当春夏季环境气温较高时,可启动制冷2系统。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
目的:考核药品质量稳定性,为确定药品的合理有效期提供科学依据。
范围:原料、中间产品、成品的稳定性试验
1 .药物稳定性试验的目的是考察药物在规定的条件下随时间变化的规律,为药品的生产、包装、贮存、运输条件提供科学依据,同时通过试验建立药品的有效期。
2. 稳定性试验的基本要求
2.1稳定性试验包括影响因素试验、加速试验和长期试验。
其中影响因素试
验适用于原料药,而加速试验和长期试验适用于原料药和制剂。
2.2加速试验和长期试验样品所用容器、包装材料和包装方式应与上市产品一致。
2.3应重视有关物质的检查。
3. 影响因素试验
影响因素试验是在比加速试验更强烈的条件下进行,其目的是探讨药物的固
有稳定性,了解影响其稳定性的因素及可能的降解途径与降解产物,为制剂生产
工艺、包装、贮存条件与建立降解产物的分析方法提供科学依据。
试验时,将样品置于适宜的容器中,摊成w 5mm厚的薄层,疏松原料药可摊成w 10mm厚的薄层,进行以下试验:
3.1咼温试验
3.1.1将供试品置于适宜的容器中(如称量瓶或培养皿中)摊成w 5mm厚的
薄层,疏松原料药可摊成w 10mm厚的薄层,在60C下放置10天,于第5天和
第 10 天取样,按照稳定性重点考察项目进行检测,即:性状、熔点、含量、有
关物质、吸湿性、以及根据药品性质选定的考察项目。
3.1.2若检测结果与0天结果比较,有明显变化(如含量下降 5%),则40C 下按同法进行试验。
如60 °C的结果无明显变化,不再进行 40 °C试验。
3.2 高湿度试验
在25C将供试品开口置于相对湿度 90±5%的恒湿密闭容器中(在密闭容器中放置硝酸钾饱和溶液),放置 10 天,于第 5 天和第 10 天取样,检验上述项目,重点考察供试品的吸湿性。
如吸湿增重 5%以上,则在相对湿度 75± 5%条件下(在密闭容器中放置氯化钠饱和溶液),同法进行试验。
如吸湿增重 5%以下,而且其他项目符合要求,则不再进行此项试验。
3.3 强光照射试验
将供试品开口置于装有日光灯的光照箱或适宜的光照箱中,照度为4500±
500IX,放置10天,于第5天和第10天取样,检验上述项目,特别要注意外观的变化。
光照箱要有恒定的照度,要注意防尘。
4.加速试验
4.1 加速试验是在超常的条件下进行,其目的是通过加速药物的化学或物理变化,探讨药物的稳定性,为药品评审、包装、运输及贮存提供必要的资料。
具体试验方法为:取供试品三批,按市售包装,在温度 40 ± 2 C,相对湿度75 ± 5% (在密闭容器中放置氯化钠饱和溶液)条件下,放置六个月。
分别在第 1 个月、 2 个月、 3 个月、 6 个月末取样检测。
按稳定性重点考察项目检测。
如在 6 个月内供试品经检测不符合质量标准,则应在30 ± 2C,相对湿度60 ± 5% (在密闭容器中放置亚硝酸钠饱和溶液)条件下,同法
进行加速试验,时间仍为 6 个月。
4.2对温度特别敏感的药物,预计只能在冰箱中(4〜8C)保存的药物,其加速试验,可在25± 2C、相对湿度60± 5% (在密闭容器中放置亚硝酸钠饱和溶液)条件下进行,时间为 6 个月。
4.3 对于包装在半透性容器的制剂,如塑料袋装溶液、塑料瓶装滴眼剂和滴鼻剂等,
应在相对湿度 20± 2% (在密闭容器中放置 CH3C00K • 1.5H2O饱和溶液)条件下,同法进行加速试验 6 个月。
4.4加速试验使用的恒温设备应能控制温度在土 2C,设备内各部分温度应均匀,
并适合长期使用。
4.5 液体制剂可不要求控制相对湿度。
5.长期试验
按照《中国药典》 2000 年版二部附录“药物稳定性试验指导原则”中的长期试验方法进行考察,目的是通过长期试验建立药品的有效期。
5.1 试验要求
5.1.1要求供试品三批,市售包装。
在接近 25±2C、相对湿度60± 10%的条件下放置,分别于 0 个月、 3 个月、 6 个月、 9 个月、 12 个月、 18个月、 24 个月、 36 个月取样,按照《中国药典》 2000年版二部附录“药物稳定性试验指导原则”中稳定性重点考察项目进行检测。
将检测结果与 0月比较,以确定有效期。
5.1.2对温度特别敏感的药物,可在温度 6± 2 C的条件下放置,按上述时间要求进行检测,制订低温条件下的有效期。
5.1.3 原料药包装应采用模拟小包装,但所用材料与封装条件应与大包装相同。
5.1.4 在稳定性考察期间,应详细放置样品的环境条件(温度和相对湿度)。
5.2 有效期的确定
5.2.1 将实测数据进行统计分析,得出合理的有效期。
如三批统计分析结果差别较小,
则取最短的时间为有效期。
5.2.2 如果数据变化很小,说明药物很稳定,可不作统计分析,直接确定有效期。
