有机化学第三章环烷烃读书笔记
有机化学环烷烃

有机化学环烷烃在有机化学的广袤领域中,环烷烃是一类具有独特结构和性质的化合物。
它们就像是化学世界里的“小圈圈”,有着自己独特的魅力和价值。
环烷烃,简单来说,就是碳原子通过单键连接形成环状结构的烃类化合物。
与我们熟悉的直链烷烃相比,环烷烃的环状结构赋予了它们一些与众不同的特点。
从结构上看,环烷烃的碳原子排列成环。
环的大小可以不同,常见的有三元环、四元环、五元环等等。
环的大小对环烷烃的稳定性有着重要的影响。
比如,三元环和四元环由于环张力较大,相对来说不太稳定,容易发生开环反应。
而五元环和六元环则相对稳定得多。
稳定性的差异导致了它们在化学反应中的表现各不相同。
以开环反应为例,小环烷烃在一定条件下能够与氢气、卤素等发生开环加成反应。
这是因为小环烷烃的环张力使得它们的化学键相对更容易被打开,从而与其他物质发生反应。
而大环烷烃则相对较难发生这样的反应。
环烷烃的物理性质也有其特点。
一般来说,环烷烃的沸点和熔点比相同碳原子数的直链烷烃要高。
这是因为环状结构使得分子间的接触更为紧密,相互作用增强,从而需要更高的温度来打破这种相互作用。
在实际应用中,环烷烃有着广泛的用途。
在石油化工领域,环烷烃是重要的原料。
通过一系列的化学反应,可以将它们转化为各种有用的化学品,如溶剂、润滑油等。
在医药领域,一些含有环烷烃结构的化合物具有特定的生物活性,被用于药物的研发和制造。
让我们更深入地了解一下环烷烃的命名规则。
对于简单的环烷烃,通常以“环”字开头,然后根据环上碳原子的数目称为“环某烷”。
如果环上有取代基,则要按照一定的顺序为取代基编号,以表明它们在环上的位置。
再来看看环烷烃的同分异构体。
由于环的结构可以有多种变化,所以相同碳原子数的环烷烃可能存在多种同分异构体。
比如,C₅H₁₀就有环戊烷和甲基环丁烷等多种同分异构体。
环烷烃的存在和性质对于我们理解有机化学的整体框架有着重要的意义。
它们不仅丰富了有机化合物的种类,也为我们研究和应用有机化学提供了更多的可能性。
有机化学第三章环烷烃
2、加成反应 、
小环烷烃,特别是环丙烷,和一些试剂作用时易发生开环。 小环烷烃,特别是环丙烷,和一些试剂作用时易发生开环。 A: 加氢(随碳原子数增加,环的稳定性增加;加氢反应条 加氢(随碳原子数增加,环的稳定性增加; 件也愈苛刻) 件也愈苛刻)
Ni + H2 40 C Ni 110 C Pt 330 C以 上 以
互为构象异构体。 互为构象异构体。
重叠式构象
交叉式构象
一、环己烷的构象
1918年 Mohr提出非平面无张力环学说,提出环已烷 年 提出非平面无张力环学说, 提出非平面无张力环学说 的六个碳原子都保持正常键角109o28’的椅式和船式构象。 构象。 的六个碳原子都保持正常键角 的椅式和船式构象
1、椅式构象(稳定的极限构象) 椅式构象(稳定的极限构象)
环 丁烷 环 丙烷 cyclopropane cyclobutane
环戊烷 cyclopentane
CH3 CH3 A: Isopropylcyclopentane
CH2CH2CH2CH2CH3 B: 1-Cyclobutylpentane
C3
2
4
D
1
5 4 3 2
E
CH3 CH3 CH CH3
F
CH3 CH3 CH3CCH CH3 Br
+ HBr
3、氧化反应 、
a)小环不被高锰酸钾,臭氧所氧化 )小环不被高锰酸钾,
+ KMnO4 + O3 H+ × H+ ×
应用:鉴别小环与不饱和烃类化合物 应用:
CH3 CH=C H 3C H3C CH3 KMnO4 H3C H
+
COOH +
第3章 环烷烃(武汉大学化学与分子科学学院)

饱和脂环烃— 饱和脂环烃—环烷烃 脂环烃 不饱和脂环烃—环烯烃、 不饱和脂环烃—环烯烃、环炔烃
环丙烷
环丁烷
环戊烷
环己烷
环戊二烯
环己烯
环辛炔
2
目录
3-1 3-2 3-3 3-4 3-5 小结 环烷烃的结构、分类、 环烷烃的结构、分类、异构和命名 环烷烃的稳定性与环大小的关系 环己环及其衍生物的构象 环烷烃的物理性质 环烷烃的化学性质 环烷烃的
5
环烷烃的分类 环烷烃的分类
单环 1. 按环数 二环 多环
小环( 小环(C3-C4) ) 普通环( 普通环(C5-C7) ) 中环( 中环(C8-C11) ) 大环( 大环(> C12) )
螺环:两环共用1 螺环:两环共用1个碳 2. 按环的 连接方式 螺[4.5]癸烷 癸烷 桥环: 桥环:共有两个或三个 以上的碳原子
22
环戊烷的构象:环戊烷具有信封式的构象,键角 戊烷的构象 环戊烷具有信封式的构象,
6
环烷烃的异构: 环烷烃的异构:构造异构和立体异构
构造异构: 1. 构造异构:由于环的大小及取代基位置的不同而有各 种构造异构体。 种构造异构体。 三元环最简单,无构造异构体。 ① 三元环最简单,无构造异构体。 含四个碳原子的单环烃( ),仅有 构造异构体: 仅有2个 ② 含四个碳原子的单环烃(C4H8),仅有 个构造异构体:
命名时,从桥头碳原子开始编号,从最长桥编到另一桥头碳; 命名时,从桥头碳原子开始编号,从最长桥编到另一桥头碳; 然后沿次长桥回到第一个桥头碳; 然后沿次长桥回到第一个桥头碳;再按桥渐短的次序将其余的桥 编号;按所含碳原子的总数,称为某烷。还要标明取代基的位置, 编号;按所含碳原子的总数,称为某烷。还要标明取代基的位置, 数目,名称,所含环的数目,桥的长短。 数目,名称,所含环的数目,桥的长短。
大学有机化学第三章 环 烃
a e
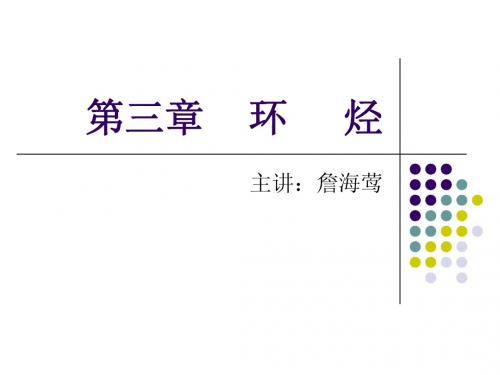
怎样画椅式环己烷的构象式?
H H H H H H H H H H H H
a e
e a
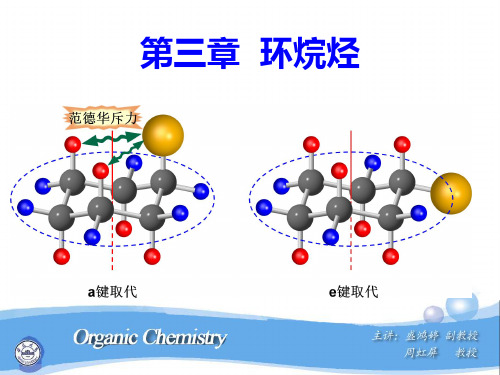
(四) 取代环己烷的构象分析
空间张力
H 5 4 H H 6 1 3 2 H H
1,3-二竖键相互作用力
H
-7.5kJ/mol
4 3 H
5 H 2
6 1
H H H H
弱的引力
甲基在a键 5%
甲基在e键
95%
亲电取代反应(卤代、硝化、磺化、烷基化反应); 侧链上的氧化反应 ; 侧链上的取代反应
掌握判断芳香性的的4n+2规则 掌握定位规律的应用
第一节 脂 环 烃
环烃又称闭链烃,为碳骨架成环状结构的一类 碳氢化合物。根据结构和性质,又可分为:
脂环烃(alicyclic hydrocarbon) 单脂环烃 多脂环烃
三、环烷烃的性质
脂环烃的物理性质和化学性质与相应的脂肪烃 相似。环烷烃性质似烷烃。 但小环的环烷烃不稳定, 容易发生开环加成反应。 (一) 自由基取代反应:
300℃
+ Br2 ——>
Br + H—Br
(二) 加成反应:
1. 催化加氢
CH2 + H2 H2C CH2 Ni 80℃ CH3—CH2—CH3
(1,2,3-trimethylbenzene)
若苯环上连接不同的烷基时,烷基名称的排列 顺序按“优先基团”后列出的原则,其位置的编号 应将简单的烷基所连的碳原子定为1-位,并以位号 总和最小为原则来命名。
CH2CH3
1 2 3
CH(CH3)2
CH3CH2CH2
5
1-乙基-5-丙基-2-异丙基苯 (1-ethyl-2-isopropyl-5-propylbenzene)
第三章有机化合物知识点总结

第三章有机化合物本章包括最简单的有机化合物——甲烷、来自石油和煤的两种基本化工原料、生活中两种常见的有机物、基本营养物质四节内容,就其主要题型有:(1)甲烷的组成与结构; (2)甲烷的物理与化学性质;(3)同分异构体 同系物 ; 确定未知气态烃分子结构 (4)乙烯的分子结构; (5)乙烯的性质; (6)苯的化学性质;(7)苯的分子结构 ;(8)乙醇的性质; (9)酯化反应;(10)乙酸的化学性质; (11)酯、油脂的性质; (12)糖类的性质;(13)蛋白质的性质等等。
本章从日常生活中我们熟悉的物质开始,介绍了它们的来源、性质、用途等若干知识,有助于我们常识性、基础性地了解这些物质。
同时有机化学是高考内容的重要组成部分,学好本章内容会对以后进一步学习有机化学打下坚实的基础。
第一节最简单的有机物——甲烷甲烷:CH4 正四面体结构 1.氧化反应CH 4(g)+2O 2(g) → CO 2(g)+2H 2O(l) 2.取代反应CH 4+Cl 2(g) → CH 3Cl (g )+HCl 反应条件为光照生成的一氯甲烷与氯气进一步反应依次生成难溶于水的油状液体:二氯甲烷、三氯甲烷、四氯化碳;3.烷烃的通式:C n H 2n+2 n ≤4为气体 、所有1-4个碳内的烃为气体,都难溶于水,比水轻;4.命名:碳原子数在十以下的,依次用甲、乙、丙、丁、戊、己、庚、辛、壬、癸,其后加“烷”字;碳原子数在十以上的以汉字数字代表;5.同系物:结构相似,在分子组成上相差一个或若干个CH 2原子团的物质互称为同系物;6.同分异构体:具有同分异构现象的化合物互称为同分异构;7.同素异形体:同种元素形成不同的单质;特点在理解同分异构现象和同分异构体时应注意以下几点:(1)同分异构现象、同分异构体概念的内涵包括缺一不可的两点:一是分子式相同,分子式相同必然相对分子质量相同,但相对分子质量相同分子式不一定相同,如H3PO4与H2SO4、C2H6与NO均是相对分子质量相同,但分子式不同。
《有机化学(第二版)》第3章:环烷烃

1-甲基-3-乙基环戊烷
CH2 CH3
1-甲基-4-异丙基环己烷 含双键的脂环烃称为环烯
4 5 6 1 3
1-甲基-4-异丙烯基环己烯 苧烯 4-甲基-1-环己烯
2
如取代基为较长的碳链,将环作为取代基: 3-环己基己烷
19:46
环烷烃的异构
环的大小、侧链的长短及位置不同而产生构造异构体 4C
椅式(chair form)
H H H H H
H H H H
19:46
H H H 透视式
相邻两个碳原子 的C-H键都处在 交叉式的位置
1、3、5碳在同一平面上 2、4、6碳在另一平面上 两个平面相互平行 C3轴对称
纽曼式
丁烷的邻位交叉式
(2)船式构象
H H H
3
19:46
H
1
4
H
5
2
6
H
H
H H
★ 环己烷多元取代物中,体积大的取代基在e位的构象较稳定
H
19:46
两个规则
Hassel规则
带有相同基团的多取代环己烷,如果没有其它因素 的参与,那末在两个构象异构体之间,总是有较多取代基 取e键向位的构象为优势构象。
Barton规则
带有不同基团的多取代环己烷,如果没有其它因素的 参与,那末其优势构象总是趋向于使作用最强的和较强的 基团尽可能多地取e键的向位。
2-溴丁烷
(键断裂的位置是在含氢最多和含氢最少的碳原子之间)
4 氧化反应:
+ KMnO4 不反应
19:46
可与烯烃或炔烃区别开来。
+
O2
++ Co , P
HOOC(CH2)4COOH
第三章 环烷烃

环戊烯
环辛炔
1,3-环己二烯
带有侧链的环烯烃命名:
a. 若只有一个不饱和碳上有侧链,该不饱和碳编号为1; b. 若两个不饱和碳都有侧链或都没有侧链,则碳原子编号顺序除双 键所在位置号码最小外,还要同时以侧链位置号码的加和数为最 小。
第三章 环烃
第一节 脂环烃
脂环族化合物:结构上具有环状碳骨架,性质与开链化合物相似的
一类化合物。脂环烃:只有C、H两种元素组成的脂环化合物。
一、脂环烃的分类
1、按碳环数分:单环脂环烃;二环脂环烃和多环脂环烃等
CH3
十氢化萘
降冰片烷
螺[2,4]庚烷
立方烷
棱烷
蓝烷
金刚烷
2、按成环碳原子数分:三元环、四元环、五元环脂环烃等
环己烷不是平面结构,较为稳定的构象 为折叠的船型构象和椅型构象。
1
(Ⅰ)
6 1
2
3 5 3 2 5
4
(Ⅱ)
6
4
Ⅰ
Ⅱ
在(Ⅰ)和(Ⅱ)中,C2、C3 、C5 、C6都在一个平面内,但在(Ⅱ)
中,C1和C4在平面的同一侧,这种构象叫船式构象;而在(Ⅰ)
中,C1和C4在平面的上下两侧,这种构象叫椅式构象
HH3C 3C
11
1 C1-C2 1 C1-C2
C5-C4 6 C5-C4 6 C1-C2 C1-C2 C5-C4 C5-C4
4
HH HH3C 2 3C HH HH
2
H H
6 6 44 55
胡宏纹第四版有机化学-第三章 环烷烃(上下)(完整版)
1,5-二甲基螺 [3,5]壬烷
7
6
12
2
54
3
2,7,7-三甲基二环[2,2,1]庚烷
CH3
1
56
4
3
9
7 8
2,8-二甲基-1-乙基二环[3,2,1]辛烷
1,8-二甲基-2-乙基-6-氯-双环[3,2,1]辛烷
8
1
7
2
8
71
6
2
1 8
2 10
97
3
Cl 6 5 4
3
5
43
65 4
三环[3,3,11,5 ,13,7 ]癸烷
Br
Br + HBr
CH2CH2Br
+ Br2
rt
Br
FeBr3
C: 与卤化氢加成
+ HBr
CH3CH2CH2Br
+ HBr
CH3CHCH2CH3
Br
规律:环丙烷衍生物与HX加成时,环的破裂处发生在
连接烷基最多的和最少的碳原子间,加成时产
物符合马氏规则,卤素加在含H较少的C上,H
加
在含H较多的C上。
7
6
1
5
32
4
9 10 1
2 8
5
3
7
64
CH3
螺[2, 4]庚烷
7-甲基螺[4, 5]癸烷
9 10 1
5 8
母体为:螺[3,4]辛烷
65 3
5-甲基螺[3,4]辛烷
7 8
4 2
1 9
CH3
2
1-甲基螺[3,5]-5-壬烯
螺[4,5]-1,6-癸二烯
3
76 4
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
读书笔记有机化学
第三章碳环烃
第一节环烷烃
1、环烷烃简介
分子通式为C n H2n
环烷烃是具有链烃性质的环烃,环烷烃及其衍生物广泛存在于自然界中,石油中含多种环烷烃,一些植物中所含精油其成分大多是环烯烃及其含氧衍生物。
精油是中草药中重要的有效成分,有的可做香料。
在自然界广泛存在的甾族化合物都是环烷烃的衍生物,在人体起重要作用。
环烷烃是由碳和氢构成的环状化合物,并且分子中不含双键或三键结构2、环烷烃的物理性质
环烷烃的物理性质及其变化规律与烷烃相似,沸点和熔点随着成环的碳原子数的增加而升高。
在室温和常压下,环丙烷和环丁烷为气体,环戊烷至环十一烷为液体,环十二烷以上为固体。
环烷的熔点、沸点和相对密度都比含同数碳原子的直链烷高。
环戊烷、环己烷及其烷基取代物存在于某些石油中。
环己烷是重要的化工原料。
溶解性:微溶于乙醇,溶于丙酮、氯仿、苯。
3、环烷烃的化学性质
(1)加成:环烷烃发生加成反应,碳环会被打开,转变为开链烃及其衍生物。
(2)氧化:环烷烃在通常情况下不易发生氧化反应,在室温下它不与高锰酸钾水溶液反应。
因此这可作为环烷烃与炔烃的鉴别反应。
(3)卤化:在高温与紫外线的作用下,环烷烃上的氢原子可被卤素取代而生成卤代环烃。
