第9章-氧化反应
化学氧化还原

化学氧化还原化学氧化还原是化学中非常重要的一个概念,它描述了化学反应中的电子转移过程。
化学氧化还原反应可以说是化学世界中最具活力和独特性质的一种反应类型。
它们在自然界中广泛存在,包括生物体的新陈代谢、各种能源的释放与转化等。
本文将从氧化还原反应的基本概念、反应类型、电位和应用等方面进行介绍。
首先,我们来了解氧化还原反应的基本概念。
氧化是指物质失去电子或氢原子,而还原是指物质获得电子或氢原子。
换言之,氧化是指电子从一个物质或原子转移到另一个物质或原子,而还原则是电子从另一个物质或原子转移到一个物质或原子。
例如,当金属与非金属离子结合形成化合物时,金属丧失了电子,即发生了氧化反应;而非金属离子则获得了金属丧失的电子,发生了还原反应。
氧化还原反应可以分为两种类型:直接氧化还原反应和间接氧化还原反应。
直接氧化还原反应是指直接发生电子转移的反应,例如金属与非金属之间的反应;而间接氧化还原反应是指通过中间体(如氧气)来传递电子的反应,例如金属与酸反应产生的氢气可以被氧气氧化。
间接氧化还原反应中,氧化剂被还原,而还原剂被氧化。
在氧化还原反应中,经常会涉及到电位的概念。
电位是描述物质的氧化还原性质的一个重要参数,它表示一个物质氧化还原反应的趋势。
具有较高电位的物质具有较强的氧化性,即它们容易被还原;而具有较低电位的物质具有较强的还原性,即它们容易被氧化。
通过比较不同物质的电位,我们可以推测氧化还原反应中电子的流动方向。
化学氧化还原反应在生活和工业中有广泛的应用。
其中最为常见的应用是电池和蓄电池。
电池是一种将化学能转化为电能的装置,它是通过氧化还原反应来实现的。
正极发生氧化反应,负极发生还原反应,从而产生电子流动,产生电能。
电池在现代社会中无处不在,为我们的生活提供了便利。
此外,化学氧化还原反应还应用于金属腐蚀、光合作用、水处理等领域。
金属腐蚀是指金属与氧气或其他氧化剂反应导致金属表面出现氧化层的现象,它是一种氧化还原反应。
第九章 氧化还原反应 答案2022

第九章氧化还原反应9.1(1) Cr2O72-+14H+ +6e-= 2Cr3++ 7H2O (酸性介质);(2) MnO4-+8H++5e-= Mn2++4H2O6H+ + 5e-(3) MnO4-+4H++3e-= MnO2+2H2O(中性介质);(4) 1/2I2 + 6 OH-= IO3-+3H2O+ 5e-(碱性介质);(5) H2C2O4 = 2CO2 + 2H+ + 2e-(酸性介质);(6) H2O2 = O2 + 2H+ + 2e-(酸性介质);(7) H2O2 +2OH-= O2 + 2H2O + 2e-(碱性介质);(8) H2O2 +2H+ + 2e- = 2H2O(酸性介质);(9) H2O2 +2e- = 2OH-(碱性介质);(10) Ag + Cl- = Ag Cl + e-9.2(1) 3As2O3 +4NO3-+7H2O + 4H+ = 6H3AsO4 +4NO(酸性介质);(2) Cr2O72-+3H2S + 8H+ = 2Cr3++ 3S + 3H2O (酸性介质);(3) 2MnO4-+5H2C2O4 + 6H+ = 2Mn2++10CO2 +8H2O (酸性介质);(4) 2Cr3++3S2O82-+7H2O = Cr2O72-+6SO42-+ 14H+ (酸性介质);(5) 2Mn2++5NaBiO3 + 14H+ = 2MnO4-+5Bi3++5Na+ + 7H2O (酸性介质);(6) 4Co(NH3)62++O2 +2H2O =4Co(NH3)63++4OH-;(7) 2Cr(OH)4-+3HO2-=2CrO42-+OH-+ 5H2O;(8) H3AsO4 +2I-=HAsO2 +I2 + 2H2O (酸性介质);(9) 2Cu2++2I-=2CuI +I2;(10) Hg2Cl2 +NH3 = HgNH2Cl +Hg+ HCl;(11) 3MnO42-+ 4H+ = 2MnO4-+MnO2 +2H2O 。
第9章---第1节

课 时 · 知 能 · 训 练
高考新课标大一轮总复习 · 配人教版 · 化学 2.(2010·宁德模拟 关于如图所示的原电池,下列说法正确的 . 宁德模拟)关于如图所示的原电池 宁德模拟 关于如图所示的原电池, ) 是(
基 础 · 回 扣 · 检 验
随 堂 · 分 类 · 练 习
考 点 · 突 破 · 方 法
课 时 · 知 能 · 训 练
菜
单
高考新课标大一轮总复习 · 配人教版 · 化学
基 础 · 回 扣 · 检 验
二、常见的化学电源 1.一次电池(以碱性锌锰电池为例 .一次电池 以碱性锌锰电池为例 以碱性锌锰电池为例) 总反应为: + 总反应为:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2 = + 负极: 负极: Zn+2OH--2e-===Zn(OH)2 。 +
随 堂 · 分 类 · 练 习
考 点 · 突 破 · 方 法
中两电极相同; 【解析】 依据构成原电池的三个条件分析:A中两电极相同;C 解析】 依据构成原电池的三个条件分析: 中两电极相同 中没有构成闭合回路; 中酒精是非电解质 只有B符合条件 中酒精是非电解质; 符合条件。 中没有构成闭合回路;D中酒精是非电解质;只有 符合条件。 答案】 【答案】 B
【解析】 解析】 A 项中电池放电时正极应发生还原反应,电极反应为:
考 点 · 突 破 · 方 法
PbO2+4H++SO2-+2e-===PbSO4+2H2O;C 项中电池充电时硫酸的 4 浓度应不断增大,D 项充电时阳极应发生氧化反应:PbSO4 -2e - + 2H2O===PbO2+SO2-+4H+。 4
考 点 · 突 破 · 方 法 随 堂 · 分 类 · 练 习
09第九章氧化反应

常用共氧化试剂——催化量OsO4与H2O2或氯酸盐等 氧化试剂共同使用:
OsO4首先进攻位阻小的碳中心,随后其他氧化剂将生成 的Os2+离子氧化为OsO4 ,反应循环进行
原因:毒性和价格因素
三、碳碳双键臭氧化反应:
臭氧能氧化碳碳双键得臭氧化产物,产物加入 锌粉还原可得醛或酮,强还原剂则得醇
9.1 醇的氧化
负载下的氧化剂氧化:
负载氧化是工业上最常用的氧化方法,好处有:
操作简单,反应快速、完全,环境友好 相对于普通氧化,氧化活性和选择性更高
负载氧化一般将氧化剂(常用高价金属阳离子) 附着于具有大表面积的支撑物(如硅胶和树脂 等)上,实现氧化和再生
9.2 碳碳双键的氧化
9.1 醇的氧化
针对铬酸缺陷的解决方案:
换用溶剂体系:
Jones(琼斯)试剂(铬酐-硫酸-丙酮),使用时将 醇的丙酮溶液滴入配好的铬酐-硫酸中
PCC(吡啶-氯铬酸盐,Corey氧化法),铬酐的盐 酸溶液中加吡啶得到的结晶。该试剂仍具有一定酸 性,使用范围小
Sarett(萨雷特)试剂(铬酐-双吡啶配合物),将 铬酐加入吡啶中,是最常使用的铬酸氧化剂
PDC(吡啶-双铬酸盐),将吡啶加入中性的铬酐水 溶液得到的吡啶双铬酸盐(Sarett试剂区别?), 中性试剂,可替代PCC。
9.1 醇的氧化
改善氧化条件:
在醛刚生成时利用蒸馏等手段加以分离,使其脱离 氧化剂的接触,从而避免进一步氧化
Sarett(萨雷特)试剂:
特别适用于分子中含有对酸敏感的基团(如缩 醛)或易氧化基团(如碳碳双键)的醇类
无水条件得到反式,有水条件得到顺式
五、双键的催化氧化:
09 第九章 氧化还原反应

化学与材料科学学院
殷焕顺
2.离子--电子法(ion-electron method)
配平原则:整个反应中氧化剂和还原剂得失电子 数相等;反应前后各元素的原子总数相等。
例如:酸性条件下 K2Cr2O7 与KI反应 (1) 写出基本离子反应 (氧化还原产物) Cr2O72- + I- → Cr3+ + I2 (2) 把离子方程式分成氧化和还原两个半反应 氧化半反应:2I- →I2 还原半反应:Cr2O72- → 2Cr3+
化学与材料科学学院
殷焕顺
练习:写出电池符号。 Cu(s)+Cl2(105Pa) = Cu2+(1mol· -1)+Cl-(1mol· -1) L L (-) Cu | Cu2+(1mol/L) || Cl-(1mol/L) | Cl2(105Pa) | Pt (+) 写出原电池的电极反应和电池反应 (-) Pt| H2 (105Pa)| H+(1.0M)||Ag+(1.0 M)|Ag(+) 正极: Ag++e ⇌ Ag(还原反应) 负极: H2 ⇌ 2H+ +2e (氧化反应) 电池反应: 2Ag++H2 ⇌ 2H++2Ag
化学与材料科学学院
殷焕顺
三、氧化还原反应式的配平 (balancing of oxidation-reduction equation ) 两种方法:
氧化数法
(the oxidation number method)
离子——电子法
(ion-electron method)
化学与材料科学学院
殷焕顺
化学与材料科学学院
殷焕顺
从电势看金属活性顺序
电对
K+/ K Ca 2+/Ca Na+/Na Mg2+/Mg Al3+/Al Zn2+/Zn Fe2+/Fe Sn2+/Sn
第九章氧化还原反应

Tollens试剂氧化
Tollens试剂氧化醛生成酸和银镜。
托伦斯试剂(Tollens) :硝酸银的氨溶液
CH=CHCHO
托伦试剂
CH=CHCOOH
CH2CHO Ag(NH3)2OH
CH2COOH
次氯(溴)酸氧化甲基酮—卤仿反应
甲基酮用次氯(溴)酸氧化得到少一个碳的羧酸。
O R C CH3 + NaOH + X2 (H) (NaOX) O R C CX3 (H) OH CHX3 + RCOONa 卤仿
Birch还原——钠把电子转移给芳香环 溶剂化电子
自由基负离子
环己二烯自由基 环己二烯负离子
1.4-环己二烯
4.形成脂的中间体历程
很少有机物的氧化作用生产了酯的中间体,再由酯中间体进一步裂解生成 氧化产物。这种酯中间体一般为无机酸酯。
例:伯醇被铬酸氧化成铜
5.加成—消除反应历程
氧化剂与底物加成,氧化剂的一部分发生离去。 二氧化硒氧化酮
氧化范围:烃(烯烃、炔烃、芳烃侧链)、醇。
例 1:
℃ 油酸(9-十八碳烯酸)
( KMnO4、H2O,碱性,低温得邻二醇) 加入冠醚(相转移催化剂)氧化活性增强,断碳链得羧酸。
例 2:
℃
例3:
仲醇得混合物
b. MnO2
MnO2/60% H2SO4:温和氧化剂
活性MnO2:温和高选择性氧化剂 例:
℃
℃
(二)有机氧化剂:
1、有机过氧酸:C6H5COOOH,CH3COOOH,CF3COOOH等。 2、CrO3—吡啶络合物。
3、Pb(OCOCH3)4,CH3SOCH3
1、有机过氧酸:
1)
3)
第九章 氧化-还原反应

2020/11/22
第28张共79张
例5:根据电池符号写出电池反应式
(-) Pt | H2(1kPa) | H+(0.1mol·dm-3)|| Fe3+(0.1mol·dm-3), Fe2+(1mol·dm-3) Pt(+)
解:
2 Fe3+ (1mol.dm-3) + H2(1kPa)
2Fe2+(1mol·dm-3) + 2H+(0.1mol·dm-3)
2020/11/22
第32张共79张
请分析以下两个电极的金属板上 带什么电荷?
2020/11/22
第33张共79张
三、标准(参比)电极电势( θ)
• 热力学标准态是如何规定的?
–所有离子、分子a=1 ( c1mol/L) –所有气体为pө ( =100 kPa) –纯液体、纯固体组分。
2020/11/22
2020/11/22
第29张共79张
• 为什么两个合适电极相连,回路上有 电流产生?
二、电极电势(electrode potential)
1. 电极电势的产生:
Zn
Nernst双电层理论
溶解(氧化)
M
Mn+ + ne
沉积(还原)
2020/11/22
第30张共79张
ZnSO4溶液
活泼金属
绝对电极电势
第34张共79张
1.标准氢电极
2H+ + 2e
H2
规定:在任何温度下
θ(H+/H2)= 0.0000V
2020/11/22
第35张共79张
2020/11/22
第9章 生物氧化与氧化磷酸化
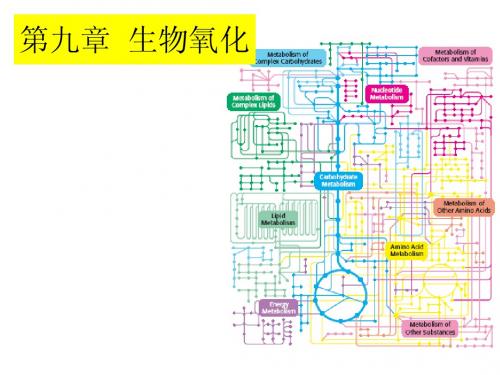
2GSH
DHA
2Cu+
2e
1/2 O2
2H+
S
脱氢酶
+ NADPH+H
GSSG
AA
2Cu2+
2e 抗坏血酸氧化酶
O
H2O
谷胱甘肽还原酶 脱氢抗坏血酸还原酶
黄素蛋白氧化酶
一切以FMN或FAD为辅基的酶或传递体都可称为黄酶, 它的作用是不经过细胞色素或其他传递体而将氢直接交 给分子氧,生成过氧化氢。作用模式如下:
- - - ++++
H+ H+
1. 在呼吸链上传氢体和传电子体交替排列, 在线粒体的内膜上具有特定的位置,催化的 反应是定向的。 2. 传氢体具有氢泵的作用, 当传氢体由线粒 体内膜的内侧接受从底物传来的2H后, 将电 子(2e)传给其后的电子传递体, 而将质子泵出 内膜。
3. 质子不能自由通过内膜。泵出的质子不能 返回,从而形成了跨膜的质子浓度梯度,即: ∆pH,外正内负。此电位差包含着电子传递 过程中所释放的能量,象电池两极的离子浓 度差造成电位差而含有电能一样。 4. 质子通过特殊的通道返回内膜的途中, 驱动ATP合酶,合成ATP。由质子浓度 梯度所释放的自由能偶联ADP和Pi形成 ATP,质子的化学势梯度也随之消失。
过氧化氢酶催化 过氧化物酶催化
或
2H2O22H2OΒιβλιοθήκη + O2抗氰呼吸途径
I、Ⅱ、Ⅲ、Ⅳ为正常呼吸链的四个复合物; FPma 为一种具有 中等氧化还原电位的黄素蛋白; CRO 为抗氰氧化酶
本章重点:
磷酸化的类型,电子传递链(体)、 化学渗透学说的要点。
第九章 生物氧化
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
氧化反应是自然界普遍存在的一类重要反应。在有机合成 中,多数有机化学家认为,它应包括下列几个方面:
(1)氧对底物的加成,如乙烯转化为环氧乙烷的反应;
(2)脱氢,如乙醇氧化为乙醛的反应;
(3)从分子中除去一个电子,如酚氧负离子转化为酚氧自 由基的反应。
•醇羟基和酚羟基的氧化反应; •烯烃双键的氧化反应; •芳烃侧链烯丙位的氧化反应; •酮的氧化反应
O
R R' 78%~98%
9.1 醇羟基和酚羟基的氧化反应
9. 1. 1 醇羟基的氧化反应
1.氧化剂直接氧化法
IBX =
BF4-
NO Re PPh3 R
R HO
IBX, DMSO, 20 oC, 3-4h
BF4NO Re PPh3 R
R O
65%~76%
RCH2OH + Ph3P CHCO2Et
IBX, DMSO, r.t., 1-48h
2h
77% CH3
CH3CH=CCHO
OH OH
CH2OH OH
HO
HO
H OH
OH H
CH2
O2,Pt
HO
COOH OH
HO
HO
H OH
OH H
CH2
t-BuO
CH3(CH2)10COOH 96%
O
O2/Pt, 57 oC
HO
t-BuO 80%~85%
C6H5CH=CHCH2OH
C6H5CH=CHCHO 91%
9.1 醇羟基和酚羟基的氧化反应
9. 1. 1 醇羟基的氧化反应 1.氧化剂直接氧化法
6) 其他氧化法
CH3(CH2)10CH2OH
O2,Pt C7H16,0.5h
CH3 CH3CH=CCH2OH
O2,Pt C7H16
CH3(CH2)10CHO
H3C OH H3C
Ag2CO3 C6H6
H3C O H3C
H3C CH3 OH
H3C CH3 OH
OH H3C
OH H3C
H3C
Ag2CO3 CH3COCH3
H3C
HO
O
9.1 醇羟基和酚羟基的氧化反应
9. 1. 1 醇羟基的氧化反应 1.氧化剂直接氧化法
3) 碳酸银氧化法
O H CH2OH O H CH2OH
H O MeO
OH
OH
MnO2 丙酮
MeO
H
HO
O
OH
O H 97%
O 82%
9.1 醇羟基和酚羟基的氧化反应
9. 1. 1 醇羟基的氧化反应 1.氧化剂直接氧化法
3) 碳酸银氧化法
沉淀在硅藻土上的碳酸银是一种能将伯醇和仲醇以很高的产率氧化成醛和酮 的极好试剂,反应在温和的近中性条件下进行,一般其他官能团不起反应。
_ O
+
(
N )2 Cr O
_
O
O
O 92%
9.1 醇羟基和酚羟基的氧化反应
9. 1. 1 醇羟基的氧化反应 1.氧化剂直接氧化法
2) 二氧化锰氧化法
二氧化锰是一种能将伯醇和仲醇氧化成羰基化合物的常用的温和
试剂,它特别适合于烯丙醇和苄醇羟基的氧化,反应在室温下,中性
溶剂(水、苯、石油醚、氯仿)中即可进行。常用的方法是将醇与
R CO2Et
69%~98%
HO O I O
O
OH ( )n
IBX, DMSO, 2-24h
OH (n=1, 2, 6)
( )n
9.1 醇羟基和酚羟基的氧化反应
9. 1. 1 醇羟基的氧化反应 1.氧化剂直接氧化法
6) 其他氧化法
CH3 CH3CHOHCH=CHCH=CCH=CH2
Al(OC4H9-n)3 沸苯,丙酮
9. 1. 1 醇羟基的氧化反应
1.氧化剂直接氧化法
4) 亚硝酸钠、醋酸酐氧化法
RCH2OH
NaNO2-AC2O 25 ℃,<1min
RCHO
①反应快—在所有情况下完成反应不超 过1min;
②没有过氧化物羧酸生成;
③伯脂肪醇,伯脂肪二醇,烯丙醇和苄 醇均被选择性氧化生成相应的醛类化 合物;
④α,β-不饱和醇的氧化没有双键异构现 象;
Ag2CO3-硅 藻 土 C6H6
O H O
O O
H
CH2
OH OH
A g2CO3-硅 藻 土 C6H6
CH2 OO
OH
O OH OH
OH
Ag2CO3, 硅藻土
O
HO O
80%
OH
Ag2CO3-硅藻土
OH
C6H6
HO
OH Ag2CO3-Celite HO
O
O
OH 80%
9.1 醇羟基和酚羟基的氧化反应
MnO2在溶剂中搅拌几个小时即可完成。二氧化锰要经特殊方法制备才
能具有最高活性,最好的方法是让硫酸锰与KMnO4在碱性溶液中反应
来制备。烯键和炔键不与该试剂发生反应。
OH
OH
HC C
CH3 CH C CH2OH
MCHO
HO
HO
MnO2,CHCl3 室温
⑤分子中存在伯醇羟基和仲醇羟基(包 括仲苄基醇)时,伯醇羟基发生选择 性氧化;
⑥在杂环醇分子中,发生选择性氧化, 杂原子如N,S不受影响。
9.1 醇羟基和酚羟基的氧化反应
9. 1. 1 醇羟基的氧化反应
1.氧化剂直接氧化法
IBX =
HO O I O
5)有机五价碘氧化剂
O
1-羟基碘酰苯(简称IBX)及其衍生物—高价碘化物作为一种性能温和、选择性 高及环境友好的醇氧化剂在有机合成中得到了广泛的应用。它不同于其它类型氧化 剂的显著特点在于对底物的化学选择性极高,即一般仅氧化醇羟基为羰基,而不会 氧化其它一些易被氧化的官能团如氨基、巯基等,所以它在合成一些药物和天然产 物方面具有独特的优势。
HO R R'
R R' OH
IBX DMSO, r. t.
O R
R O
O 或
R
R R'
OH
RO OO
NH2 O
CH2OH O O
NHAC
75%~100%
Ph
IBX, DMSO, r.t.
RO OO
NH2 O
O CH O O
NHAC
AcO
OAc OAc
AcO
OAc OAc
OH R R'
Ph
IBX DMSO, r.t.
CH3 HO
Al(OC4H9-n)3 CH3COCH3
O
CH3
CH3 CH3COCH=CHCH=CCH=CH2
80%
Oppenauer 氧化法
CH3(CH2)3CH2OH
Pb(OCOCH3)4 吡啶
CH3(CH2)3CHO 70%
CH3CHOHCH2CH2CHOHCH3
CH3COCH2CH2COCH3 89%
9.1 醇羟基和酚羟基的氧化反应
9. 1. 1 醇羟基的氧化反应 1.氧化剂直接氧化法
1) 三氧化铬——吡啶络合物氧化法
HO
HO HO
CH3CHO,H+
H CH3
HO
CH3
O O CH 3 ① CrO3, 吡啶,CH2Cl2
② H3O+
HO O
HO
HO
O O
O
O O O
2
N + CrO3
O O
HO
