实验室纯水制备及检验记录表
实验室用水标准和制备要求的简介说明

实验室用水标准和制备要求的简介说明水是实验室常用的良好溶剂,溶解能力强,作各种溶剂和用于洗涤仪器等。
随着分析仪器的新发展和广泛应用,对水的质量的要求已成为关键性问题之一,尤其是在食品中药物残留和有害元素的检测方面以及减低实验空白都直接与水的纯净度有密切关系,超纯水就是经过水处理装置进行提炼的纯水。
鉴于目前检验检疫实验室用水的概念不强、制备的纯度低、贮存期间细菌污染严重等情况,本文详细阐述了实验室用水的纯度要求,贮存注意事项等,有利于确保实验数据的科学性和公证性。
1 纯水的技术指标1.1 实验室用水外观看,实验室用水目视观察应为无色透明的液体;从级别看,实验室用水的原水一般应为饮用水或适当纯度的水。
国际标准化组织(ISO)于1983年制定纯水的纯水标准,将纯水分为三个级别。
国内参照ISO纯水标准(1987)制定我国的纯水标准,将适用于化学分析和无机痕量分析等试验用水,其中三级水适用于一般化学分析实验。
注:1 由于在一级水、二级水的纯度下,难于测定其真实的pH 值,因此,对一级水、二级水的pH值范围不做规定。
2一级水、二级水的电导率需用新制备的水“在线”测定。
3由于在一级水的纯度下,难于测定可氧化物质和蒸发残渣,对其限量不做规定。
可用其他条件和制备方法来保证一级水的质量。
1.2 蒸馏水蒸馏水系指《中华人民共和国药典》(1995年版)所收载的蒸馏水,在该版的凡例二十五条中明确指出,试验用的水,除令有规定外,均系指蒸馏水或去离子水。
由上所知,一般实验室用水不外乎三级水和蒸馏水这两种规格,但计量认证时则要求实验室用水必需按GB6682-92执行。
可以看出,三级水与蒸馏水在外观、性状方面基本相同,控制的成分是一致的。
只是药典中所载的蒸馏水其检验项目较GB6682-92中三级水的项目多而全,这可能是因为蒸馏水除做实验用水外,还因药用的缘故。
1.3 去离子水用离子交换法制得的化验用水,常称去离子水或离子交换水。
纯化水理化检测原始记录表
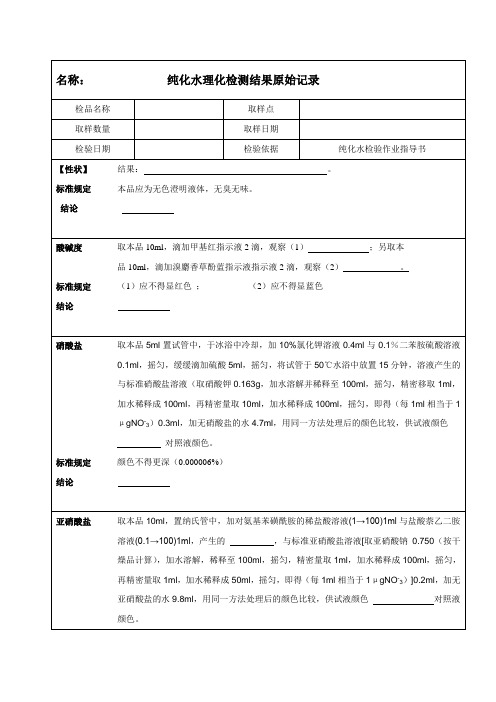
硝酸盐取本品5ml置试管中,于冰浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的与标准硝酸盐溶液(取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密移取1ml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1μgNO-3)0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较,供试液颜色
标准规定颜色不得更深(0.000002%)
结论
电导率使用在线或离线电导率仪完成。电导率µS/cm。
标准规定不超过4.3µS/cm
结论
氨取本品50ml,加碱性碘化汞钾试液2ml,放置15分钟;如显色,与氯化铵溶液1.5ml,加无氨水48ml与碱性碘化汞钾试液2ml制成对照液比较,供试液颜色对照液颜色。
名称:纯化水理化检测结果原始记录
检品名称
取样点
取样数量
取样日期
检验日期
检验依据
纯化水检验作业指导书
【性状】结果:。
标准规定本品应为无色澄明液体,无臭无味。
结论
酸碱度取本品10ml,滴加甲基红指示液2滴,观察(1);另取本
品10பைடு நூலகம்l,滴加溴麝香草酚蓝指示液指示液2滴,观察(2)。
标准规定(1)应不得显红色;(2)应不得显蓝色
标准规定颜色不得更深(0.00001%)
结论
记录人:审核人:
日期:日期:
对照液颜色。
标准规定颜色不得更深(0.000006%)
结论
亚硝酸盐取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液(1→100)1ml与盐酸萘乙二胺溶液(0.1→100)1ml,产生的,与标准亚硝酸盐溶液[取亚硝酸钠0.750(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,摇匀,再精密量取1ml,加水稀释成50ml,摇匀,即得(每1ml相当于1μgNO-3)]0.2ml,加无亚硝酸盐的水9.8ml,用同一方法处理后的颜色比较,供试液颜色对照液颜色。
(完整版)纯化水原始记录

纯化水(全检)取水点:批号:共页第1页【性状】实验室环境:温度;湿度。
本品为(标准:无色澄清)液体;(标准:无臭),(标准:无味)。
本项结论规定检验者日期. 【检查】实验室环境:温度;湿度。
酸碱度取本品(标准:10ml),加甲基红指示液(标准:2滴)(标准:不得显红色);另取(标准:10ml),加溴麝香草酚蓝指示液(标准:5滴)(标准:不得显蓝色)。
本项结论规定检验者日期. 硝酸盐实验室环境:温度;湿度。
取本品(标准:5m1)置试管中,于冷浴中冷却,加10%氯化钾溶液(标准:0.4ml)与0.1%二苯胺硫酸溶液(标准:0.1ml),摇匀,缓缓滴加(标准:硫酸5ml),将试管于(标准:50℃)水浴中放置(标准:l5分钟),溶液产生的(标准:蓝色)与标准硝酸盐溶液[取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1μg NO3)]0.3ml,加无硝酸盐的水(标准:4.7ml),同一方法处理后的颜色比较(标准:不得更深)(0.000006%)。
本项结论规定检验者日期. 亚硝酸盐实验室环境:温度;湿度。
取本品(标准:l0ml),置比色管中,加对氨基苯磺酰胺的稀盐酸溶液(1→100)(标准:1ml)与盐酸萘乙二胺溶液(0.1→100)(标准:1ml),产生的(标准:粉红色)与标准亚硝酸盐溶液[取亚硝酸钠0.750g(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,摇匀,再精密量取1ml,加水稀释成50ml,摇匀,即得(每1ml相当于1μg NO2)]0.2ml,加无亚硝酸盐的水(标准:9.8ml),用同一方法处理后的颜色比较(标准:不得更深)(0.000002%)。
本项结论规定检验者日期. 氨实验室环境:温度;湿度。
纯化水(全检)取水点:批号:共页第2页取本品(标准:50ml),加碱性碘化汞钾试液(标准:2ml),放置(标准:15分钟),溶液(标准:不显色);如显色,与氯化铵溶液(取氯化铵31.5mg,加无氨水适量使溶解并稀释成1000ml)1.5ml,加无氨水(标准:48ml)与碱性碘化汞钾试液(标准:2ml)制成的对照液比较(标准:不得更深)(0.00003%)。
纯化水检验作业指导书

纯化水检验作业指导书1. 目的规范我司生产用水的检验要求,确保原水、生产用水和实验用纯水符合质量标准,特此制定本检验标准。
2. 适用范围适用于原水、车间生产用水、器具清洗用水、实验室检验用水。
3. 职责检验员:负责按照作业指导书执行操作。
实验室主管:负责作业指导书的修订。
质量部门负责人:负责作业指导书的审核。
质量负责人:负责作业指导书的批准。
4. 检验依据及标准4.1 依据检验根据《中国药典》现行版、GB 5749《生活饮用水卫生标准》现行版编写。
4.2 检验标准及频率4.2.1 理化检测4.2.2 微生物检测进行检测。
5. 内容5.1 感官指标5.1.1 外观、色泽取试样置于比色管中,在非阳光直射条件下进行目测:为无色、无杂质的澄清液体。
5.1.2 气味打开装纯化水的PE瓶盖子,在瓶口上方轻轻扇动,纯化水应无臭、无味。
5.2 理化指标5.2.1 pH值(25℃)取样时,将样品盛装充满容器,减少和空气接触面,取样后及时加盖。
用经校正的pH计直接测定。
若检测过程中遇不稳定时,可以在100mL检测样中加入0.3mL饱和氯化钾溶液依法测定。
5.2.1.1 pH计预热及校正测定前将pH计预热约5min后进行校正,具体校正方法参考pH计操作规程。
校正结束后,将电极清洗干净,用滤纸吸干水,用待测水样冲洗电极,再将电极浸入试样中,按“READ”键开始测量。
测量的过程中,不要摇动和搅拌水样,以减少CO2的吸收。
同时pH计小数点会闪烁,当测定结果稳定后,测量停止,小数点不再闪烁,同时结果显示图标上出现A时可读数。
5.2.1.2 实验结束用纯水冲洗干净电极,将电极插入装有足量填充液(3mol/L KCL溶液)的电极保护帽内。
5.3电导率(25℃)5.3.1测定前将电导率仪预热约5min后进行校正,具体校正方法参考:电导率检验作业指导书。
5.3.2仪器校正后,把电导电极插进待测溶液中。
按“Read”开始测量,终点图标不再闪烁,同时结果显示图标上会出现A,测量完毕,可以读数。
实验室用水质量记录表(优.选)

≤0.4
≤2.0
试验依据:GB/T6682-2008分析实验室用水规格和试验方法
pH计编号:
电导率仪编号:
电子天平编号:
纯水用途
检验依据
检验环境条件
℃%RH
检验日期
检验项目、数据和结果
项目
检验记录
检验结果
1外观
无色透明液体(是□、否□)
满足□;不满足□
2 pH值
一级□;二级□;三级□
3电导率
实验室用水水质测量记录表
记录编号:纯水机编号:
日期
pH(25℃)
(无量纲)
电导率(25℃)
(μS/cm)
可氧化物质含量(以O计)
(mg/L)
蒸发残渣(105℃±2℃)含量
(mg/L)
是否满足三级用水要求
检测人员
测量值
达标值(三级)
测量值
达标值(三级)
测量值
达标值(三级)
测量值
达标值(三级)
5.0~7.5
≤5.0
≤0.4
≤2.0
5.0~7.5
≤5.0
≤0.4
≤2.0
5.0~7.5
≤5.0
≤0.4
≤2.0
5.0~7.5
≤5.0
≤0.4
≤2.0
5.0~7.5
≤.0
≤0.4
≤2.0
5.0~7.5
≤5.0
≤0.4
≤2.0
5.0~7.5
≤5.0
≤0.4
≤2.0
5.0~7.5
≤5.0
≤0.4
≤2.0
5.0~7.5
一级□;二级□;三级□
附录
依据《分析实验室用水国家标准》(GB/T6682-2008),不同级别纯水的相关参数、制取方法和用途列表如下:
【化学探究实验报告】纯净水的制备及其纯度检测

西安电子科技大学化学探究实验课程实验报告实验名称纯净水的制备及其纯度检测学院班Array姓名学号同作者实验序号实验日期2020 年7 月9日一、实验目的1、学习离子交换法制备纯净水的原理和方法。
2、熟悉用阴、阳离子交换树脂制备纯净水的过程。
3、了解纯净水水样质量的简单检测方法。
4、掌握原子吸收光谱法测定水中钙、镁离子的含量。
二、实验原理当自来水通过阳离子交换柱时,水中Na +、Mg 2+、Ca 2+等阳离子与树脂上的H +发生如下交换反应:223322RSO H Mg (RSO )Mg 2H -++-++++ (1-1)当水通过阴离子交换柱时,水中的Cl -、SO 42-、CO 32-等阴离子与树脂上的OH -发生交换,反应如下:3333RN(CH )OH Cl RN(CH )Cl OH --++ (1-2)经阴、阳离子交换后产生的H + 与OH - 结合又生成水。
2H OH H O+-+=(1-3)经过阴、阳离子交换柱以后的水,杂质阴、阳离子均已除去,故称为纯净水。
为进一步提高水质,可在阴离子交换柱后再串接一个阴、阳离子交换树脂混合柱,其作用相当于多级交换,可进一步提高水质纯度。
纯净水中离子的鉴定方法:AgNO 3、BaCl 2溶液可分别用以检验水样中的Cl - 和SO 42- 离子的存在。
而铬黑T 、钙指示剂可分别用以检验Mg 2+、Ca 2+ 离子的存在。
在pH = 8~11的溶液中,铬黑T 能与Mg 2+离子作用而显红色;在pH > 12的溶液中,钙指示剂能与Ca 2+ 离子作用而显红色,在此pH 值下,Mg 2+离子的存在不干涉Ca 2+ 离子的检验,因为这时Mg 2+离子以Mg(OH)2沉淀析出。
纯净水的纯度可通过原子吸收光谱法测定水样中钙、镁含量来检测,此方法绝对分析灵敏度可高达10-9,其基本原理简述如下:1.原子吸收光谱分析基本原理原子吸收光谱法(AAS )是基于:由待测元素空心阴极灯发射出一定强度和波长的特征谱线的光,当它通过含有待测元素的基态原子蒸汽时,原子蒸汽对这一波长的光产生吸收,未被吸收的特征谱线的光经单色器分光后,照射到光电检测器上被检测,根据该特征谱线光强度被吸收的程度,即可测得试样中待测元素的含量。
化验室用水的制备与检验方法
化验室用水的制备与检验方法摘要:化验室经常要用到纯水,由于分析任务,分析方法的不同,对纯水的质量要求也就不同。
因此对实验室用水规格必须有一定的了解。
化学分析和仪器分析,常量分析和微量分析,各种实验项目对水质的要求不同,则要求使用不同级别的”分析实验室用水”。
关键词:化验室用水的规格;指标;制备方法一、化验室用水的规格1化验室用水的外观:化验室用水应为无色透明的液体,不得有肉眼可辨的颜色和纤絮杂质。
2化验室用水的级别:化验室用水分三个级别:一级水二级水和三级水。
一级水为超纯水,用于严格要求的分析实验,一级水可由二级水处理制得。
二级水用于无机痕量分析等实验,可用蒸馏、电渗析或离子交换法制的的水进行再蒸馏的方法制得。
三级水用于一般化学分析实验,可用蒸馏.电渗析或离子交换等方法制取。
3化验室用水质量指标化验室用水质量指标二、化验室用水制备方法1 净化水质的一般工艺方法和流程常用净化水质的工艺方法有蒸馏法. 离子交换法. 电渗析法. 反渗透法. 过滤法. 吸附法. 紫外氧化法等。
实验室常用的纯水制备方法是:蒸馏法. 离子交换法等。
由于制备方法不同,水中带有少量杂质种类大小也不同,如用铜蒸馏器蒸馏的水,则会含有微量的铜离子;而用玻璃蒸馏器蒸馏的水则会含有钠离子和硅酸根离子;用离子交换法制得的纯水,将会含有少量的有机物质.微生物等。
一般制得的纯水由于空气中CO2的影响,水的PH值均小于7,约为5~6。
高纯水的纯化工艺流程大致分为三个部分:预处理.脱盐和后处理。
每一个部分都要除去一定种类的杂质。
预处理过程采用砂滤,膜过滤,活性炭吸附法除去悬浮物,有机物。
通过砂芯滤板和纤维柱滤除机械杂质。
活性炭是光谱吸附剂,可吸附气体成分,吸附细菌和某些过渡金属等。
脱盐过程采用电渗析,反渗透,离子交换方法,除去盐类物质。
后处理过程采用紫外线杀菌,臭氧杀菌,超过滤,微孔过滤方法,除去细菌,颗粒。
高纯水纯化的一般流程原水→过滤器→活性炭过滤器→反渗透器(或电渗析器)→阳离子交换柱→阴离子交换柱→混合阴.阳离子交换柱→有机物吸附物→紫外灯杀菌器→精密过滤器→高纯水2 蒸馏法制备纯水水经过加热沸腾便气化成蒸汽,蒸汽经冷凝液化得到的水叫蒸馏水。
纯水制备仪器校验规程
纯水制备仪器校验规程1目的确保实验室用水符合各项实验要求。
2范围新购置、使用中、检修后的纯水制备仪器。
3校准用设备电阻表、酸度计、分光光度计、电子天平4校准方法4.1取制好的各级纯水按实验室用水标准进行检测。
4.2制备的水不符合标准的仪器按仪器操作说明清洗或更换滤柱。
4.3检修后仪器制备的纯水重新检测,仍不合格的联系生产厂进行检修。
5.校验周期一年。
6.参考文件JJF 1071国家计量校准规范编写规则JJF 1001 通用计量术语及定义GBT/T 8170 数值修约规则与极限数值的表示和判定7.记录表格《测试设备校验记录表》附录:实验室用水标准(中国国家实验室用水标准G B 6 6 8 2–9 2)一级PH 值范围( 25 ℃):——电导率(μs/cm.25 ℃):≤0.1比电阻( MΩ.cm. 25℃):≥10可氧化物质 [ 以( 0 )计上 ] , mg/L :——吸光度( 254nm , 1cm 光程):≤0.001蒸发残渣( 105±2 ℃), mg/L :——可溶性硅 [ 以( SIo2] 计, mg/L :<0.01二级PH 值范围( 25 ℃):——电导率(μs/cm.25 ℃):≤1比电阻( MΩ.cm. 25℃):≥1可氧化物质 [ 以( 0 )计上 ] , mg/L :< 0.08吸光度( 254nm , 1cm 光程):≤0.01蒸发残渣( 105±2 ℃), mg/L :≤1.0可溶性硅 [ 以( SIo2] 计, mg/L :< 0.02三级PH 值范围( 25 ℃): 5.0-7.5。
纯化水检测原始记录
纯化水检测原始记录文件编号:样品编号检测依据药典2015二部纯化水检测日期取样地点检测项目名称检测方法及判定依据检验结果备注性状无色的澄清液体;无臭不挥发物取样品100ml,105℃水浴蒸干后遗留残渣不得超过1mg硝酸盐a实验组:样品5ml,冰浴冷却。
b对照组:1μg/ml标准硝酸盐溶液0.3ml加无硝酸盐水4.7ml,冰浴冷却。
步骤:分别加10%氯化钾0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓慢滴加浓硫酸5ml,摇匀,50℃水浴15分钟。
蓝色比较,不得比对照更深≤0.000006%重金属a实验组:样品100ml,加水19ml,蒸发至20ml,放冷。
b对照组:10μg/ml标准铅溶液1.0ml加水19ml。
步骤:加ph3.5醋酸盐缓冲溶液2ml,加水定容至25ml,加硫代乙酰胺试液2ml(取5ml混合液(1mol/L氢氧化钠溶液15ml,加甘油20ml,加水5ml)加1ml4%硫代乙酰胺溶液,沸水浴加热20秒,冷却即用)颜色比较,不得比对照更深≤0.00001%氨a实验组:样品50ml,b对照组:31.5mg/L氯化铵溶液1.5ml加无氨水48ml 步骤:加碱性碘化汞钾试液2ml,放置15分钟。
颜色比较,不得比对照更深≤0.00003%易氧化物取本品100ml,加稀硫酸10ml,煮沸后,加高锰酸钾滴定液(0.002mol/L)0.10ml,再煮沸10分钟,粉红色不得完全消失。
亚硝酸盐a实验组:样品10ml,b对照组:1μg/ml标准亚硝酸盐溶液0.2ml加无亚硝酸盐水9.8ml步骤:加对氨基苯磺酰胺稀盐酸溶液1ml与盐酸萘乙二胺溶液1ml,产生粉红色。
颜色比较,不得比对照更深≤0.000002%酸碱度取本品10ml,加甲基红指示液2滴,不得显红色,另取10ml,加溴麝香草酚蓝指示液5滴,不得显蓝色。
电导率≤5.1μs/cm微生物限度≤100CFU/ml检测人员:复核:审核:日期:日期:日期:。
实验室用水质量记录表
5.0~7.5
≤5.0
≤0.4
≤2.0
试验依据:GB/T6682-2008 分析实验室用水规格和试验方法
pH 计编号:
电导率仪编号:
电子天平编号:
D/0 检测人员
TR-08-03
纯水用途 检验依据 检验环境条件 检验日期
项目 1 外观 2 pH 值 3 电导率
D/0
℃
%RH
检验项目、数据和结果 检验记录 无色透明液体(是□、否□)
检验结果 满足□ ;不满足□ 一级□ ;二级□ ;三级□ 一级□ ;二级□ ;三级□
TR-08-03
D/0
依据《分析实验室用水国家标准》(GB/T6682-2008),不同级别纯水
的相关参数、制取方法和用途列表如下:
附录
纯水 级别
一级
相关参数
pH 值
电导率
(25℃) (S/cm,25℃)
—
≤0.1
TR-08-03
实验室用水水质测量记录表
记录编量纲)
电导率(25℃) (μS/cm)
蒸发残渣(105℃±2℃) 可氧化物质含量(以 O 计)
含量 (mg/L)
(mg/L)
是否满足三 级用水要求
测量值 达标值(三级) 测量值 达标值(三级) 测量值 达标值(三级) 测量值 达标值(三级)
5.0~7.5
≤5.0
≤0.4
≤2.0
5.0~7.5
≤5.0
≤0.4
≤2.0
5.0~7.5
≤5.0
≤0.4
≤2.0
5.0~7.5
≤5.0
≤0.4
≤2.0
5.0~7.5
≤5.0
≤0.4
