化学反应工程基本概念
化学反应工程(第三版)第二章

得
dnA Vdt
12.34cA2
[mol/L h]
14
2.2 单一反应速率式的解析
反应速率的定义式是微分式,将其与动力学方程关联并积分,可
得到反应物浓度随时间变化的关系。该过程称为反应速率式的解析。
本节介绍等温、恒容、间歇操作条件下单一反应速率式的解析。
2.2-1 不可逆反应
一、一级不可逆反应
A
5
2.1 基本概念及术语
二、膨胀因子(气相反应)
物理意义:每消耗1mol反应物K,引起整个物系总物质的量的变化。
(1)由化学计量式计算
K
i K
(2-1-16)
(2)由总物料衡算计算
K
n n0 nK 0 xK
n n0 n0 yK 0 xK
(2-1-17)
整理得
n n0 (1 K yK 0 xK )
行分析的基本依据。
9
2.1.2 均相反应动力学方程
解:将Arrhenius式取对数,则有
E ln k RT ln k0
由式可见,lnk与1/T之间为线性关系。整理表2.1-1中数据可得
10
lnk
B
-7.2
-7.4
-7.6
-7.8
-8.0
-8.2
-8.4
2.30
2.32
2.34
2.36
2.38
nk nk0 (1 xk )
则组分A的反应速率可用转化率表示为:
(rA )
dnA Vdt
nA0 V
dxA dt
恒容条件下
(rA )
cA0
dxA dt
讨论:转化率是衡量反应物转化程度的量,若存在多种反应物
化学反应工程

化学反应工程一、化学反应工程的定义及意义化学反应工程是一门研究在化学反应过程中如何设计,建造,操作,监测和控制化学反应过程的学科。
在化学反应工程中,我们致力于优化反应条件,提高反应产率,降低反应副产品的生成率,并同时考虑了成本、环保和安全等因素。
化学反应工程的意义在于,它可以将实验室研究的成果转换为大规模生产的实际应用,满足人类社会的各种需求。
无论是医药、材料、化妆品、能源等领域,都需要化学反应工程的支持。
二、化学反应工程的步骤化学反应工程的一个标准流程包括以下步骤:1.设计化学反应过程:首先需要确定需要反应的物质,反应类型,反应条件等。
2.化学反应实验:在实验室中对已设计好的化学反应过程进行实验,获得反应的产物及产率、减少产物的副产物等数据,为后续的生产提供重要的数据支持。
3. 确定反应动力学:用数学模型定量描述反应速率、浓度和温度之间的关系。
4.数据分析:对实验数据进行分析,确定化学反应满足产品质量要求、成本和安全要求。
5.装备设计:选择适合规模化生产的反应器类型和形式,并开发相应的仪表控制系统。
6.生产过程操作:根据设计好的化学反应过程,通过正确的操作,监测和控制,达到预期的产品质量要求和工业安全要求。
7.成本评估:评估生产过程和装备设计的成本,调整成本结构,使之达到最低成本。
8.项目管理:建立生产计划,制定管理程序,开具生产报表。
9.产品营销:成功的化学反应工程管理不仅要满足客户的品质要求,还需要推销产品市场。
三、化学反应工程的关键问题1. 反应机理:通过对反应物的结构和反应条件之间的关系进行深入研究,掌握化学反应的本质规律,揭示反应机制及过程。
了解反应机理可以提供反应过程改革的线索。
2. 反应体系的热力学分析:化学反应工程涉及到多种多样的反应情况,可能伴随着放热、吸热、化学平衡等等。
反应体系的热力学分析可以指导反应过程的控制及优化。
3. 反应条件控制:化学反应过程容易受到外界环境影响,如温度、压力、光、氧化还原状态和组分间的质量传递等一系列因素。
化学反应工程学及其现代应用

化学反应工程学及其现代应用化学反应工程学是一门研究化学反应过程在工业生产中的应用和优化的学科。
反应工程学不仅涉及到化学、物理、数学等多个学科,也与工程技术密切相关。
随着化学工业快速发展,反应工程学的研究日趋深入,其在实际应用中也发挥了越来越重要的作用。
本文将从反应工程学的定义、研究领域、应用现状以及发展趋势几个方面,进行简单探讨。
一、反应工程学的定义反应工程学是一门跨学科的学科,它研究的是化学反应在工业生产中的应用和优化。
它主要关注的是从热力学、动力学、传质等角度,对反应体系进行全面和系统的分析。
通过分析反应体系的物理化学特性,并探究其反应动力学规律,从而制定出最佳的工业反应工艺,提高反应过程的效率和产值,降低生产成本。
二、反应工程学的研究领域1. 反应体系的热力学特性研究在反应工程学中,热力学研究是非常重要的一项工作。
热力学主要是对反应体系中化学反应的各种热力学参数进行研究,比如反应焓、反应熵、反应自由能等。
这些参数的研究对于反应工艺设计和工艺优化具有十分重要的价值。
2. 反应动力学研究反应动力学是反应工程学的核心内容之一,其研究反应体系在动力学上的特性。
通过对反应速率、活化能、反应机理等动力学参数的研究,可以为反应工艺的设计和优化提供理论基础和实验数据。
3. 反应器设计反应器是工业生产中最常使用的化学反应设备之一。
而反应器的设计则是反应器生产中最具有挑战性的问题之一。
反应器设计需要考虑的因素包括反应器的材料、反应器形状、反应器搅拌方式等多个问题。
反应器设计的合理与否直接影响到反应工艺的效果和经济效益。
4. 工艺控制工艺控制是反应工程学的重要组成部分之一。
在反应工艺从实验室向生产规模转移的过程中,工艺控制扮演了至关重要的角色。
通过工艺控制,可以保证反应工艺为高效的、稳定的生产。
化学反应过程中,各种因素都会对反应过程产生影响,工艺控制的目的是尽量消除不利因素,保证反应过程正常进行。
三、反应工程学的应用现状反应工程学已经在很多领域得到了广泛应用,如化工、医药、材料、农业等。
化学反应工程知识点梳理
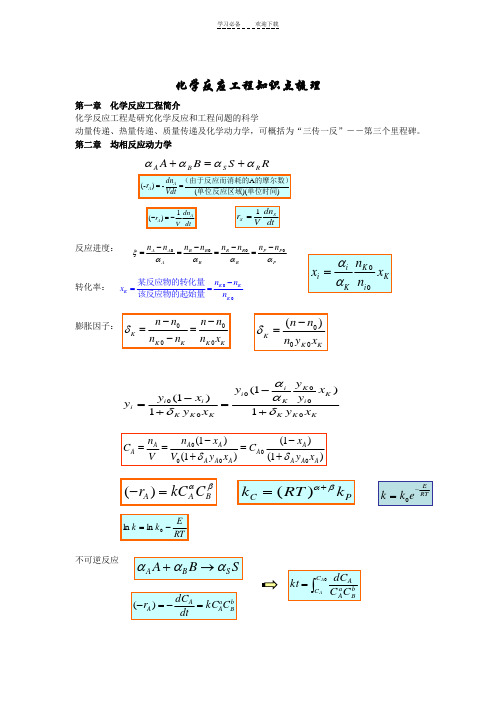
化学反应工程知识点梳理第一章化学反应工程简介化学反应工程是研究化学反应和工程问题的科学动量传递、热量传递、质量传递及化学动力学,可概括为“三传一反”--第三个里程碑。
第二章均相反应动力学反应进度:转化率:膨胀因子:不可逆反应A(-)-()()AAdnrVdt==(由于反应而消耗的的摩尔数)单位反应区域单位时间RSBARSBAαααα+=+1()AAdnrV dt-=-dtdnVr SS1=PPPRRRBBBAAAnnnnnnnnααααξ0-=-=-=-=K KKKn nxn-==某反应物的转化量该反应物的起始量KiKKiixnnxαα=0000KK K K Kn n n nn n n xδ--==-00()KK Kn nn y xδ-=KKKKiKKiiKKKiii xyxyyyxyxyy1)1(1)1(δααδ+-=+-=000(1)(1)(1)(1)A AA AA AA A A A A An xn xC CV V y x y xδδ--===++()A A Br kC Cαβ-=()C Pk RT kαβ+=ERTk k e-=RTEkk-=lnlnSBASBAααα→+bBaAAACkCdtdCr=-=-)(⎰=0AACC bBaAACCdCkt均相催化反应 CC 为催化剂浓度自催化反应A + C → 2C + R …串联反应总收率瞬时收率得率yield总选择性 目的产物P 所生成的摩尔数与副产物S 生成的摩尔数之比,用S0表示:平行反应串联反应()()AA C A dC r kC C dt-=-=CA A A C kCdt dCr =-=-)(A + B P R+S 00PP P A A n n n n -Φ=-/()/p P P A A A r dC dt dC P A r dC dt dC φ====---单位时间内生成的摩尔数单位时间内消耗的摩尔数00/)(A P P P n n n X -=000PP S S n n S n n -=-αA2A αS S (副)αA1A αP P (主),11A A r k C -=(),22A A r k C -=(),1,212()()AA A A A dC r r r k k C dt-=-+-=+=()()A A P A A p P P C k r dt dC r 11,1,1,)(αααα-=--==AA S S S C k dt dC r 22,αα-==tk k A A eC C )(021+-=A P S (均为一级反应)k 1k 2P A P P C k C k dt dC r 21-==PSS C k dt dC r 2==第三章 理想均相反应器 间歇反应器(BSTR)反应时间实际操作时间(operating time)= 反应时间(t) + 辅助时间auxiliary time (t') 反应体积V 是指反应物料在反应器中所占的体积 V = v0 (t + t')为装料系数(the volume charge coefficient),通常在0.4~0.85平推流反应器PFR 空时全混流反应器(CSTR)绝热操作恒容间歇反应器的设计式为:变温平推流反应器⎰⎰--=-=A A A C C A Ax A A A r dC r dx C t 0)()(00等容过程,液相反应 VV ϕ=实际实际的反应器体积为:0V v τ==反应器的容积进料的体积流量0R V dV t v ==⎰反应器中物料反应期的容积的体积流量000()()A A A AA A C C C x V v r r τ-===--0()A A A x V F r =-005000024R R R F v C M ==⨯00000000()(1)A A A A A A x x x A AA A A A E nx x x n n A ART A A dx dx dx t C C C r kC k e C x -===--⎰⎰⎰1001()A A x A A n xA t I x dx k C -=⎰20()()4A A A P A F dx r dV r D dl π=-=-20()4A A A dx D r dl F π-=00000()A x A A A A A dx V V F r v C C τ===-⎰化学反应工程研究的目的是实现工业化学反应过程的优化 全混流平推流多级CSTR 串联的优化对于一级不可逆反应应有PFR: 同间歇釜CSTR:全混流反应器的热衡算方程第四章 非理想流动 停留时间分布()⎰-==A x AAA B A B r dx C t F V 000BR : ()⎰-==Ax A AA P A P r dxCF V 000τPF R: ()000m m A A A A V x F C r τ-==-CST R: 112100010200...(1)(1)(1)Am Am A A A R A A A A A A Am x x x x x V v C kC x kC x kC x -⎛⎫---=+++ ⎪---⎝⎭0121110(1,2,.....1)(1)1Ai RAi Ai Ai v x V i m x k x x -+⎡⎤-∂=-==-⎢⎥∂--⎣⎦11111Ai Ai Ai Ai Ai Ai x xx x x x -++--=--221max 1max 02()k k k P P A C k X C k -==max max 1202211[(/)1]P P A C X C k k ==+1212ln(/)opt k k k k τ=-121opt k k τ=)()1())((0000Pm P P r A c v UAT T c v UA T c v H r V ρρρ+-+=∆--)()1(000P m P r c v UAT T c v UAT Q ρρ+-+= (){}E t P t residence time t t ∆=<<+停留时间分布函数 (){}=<F t P residence time t方差PFRCSTR最大层流流动 轴向扩散模型 0()()d t F t E t t=⎰22222()()()()()()t t t E t dtt t E t dt t E t dt tE t dtσ∞∞∞∞-==-=-⎰⎰⎰⎰0 t t () t t 0 t t E t <⎧⎪=∞=⎨⎪>⎩2220()()()0t t t E t dt t t σ∞=-=-=⎰0 t t () 1 t tF t <⎧=⎨≥⎩()11()t tt tF t e E t et---=-=222 1.0ttθσσ==22()()[2()]r r F t R R =-222/222()2()(1)212()(1)Z t uL E z z Pe tE Ee uL uL e Pe Peθσσ--==--=--。
化工工程中的化学反应工程与动力学分析

化工工程中的化学反应工程与动力学分析摘要:化学反应工程中的反应机理研究对于理解分子级别的转化过程至关重要。
本文探讨了反应机理的概念及其在化学反应中的应用。
反应机理涵盖了中间体形成、活化能克服以及可能的反应路径等内容。
深入探究反应机理有助于揭示关键步骤和限制因素,为设计更高效、具有特定选择性的反应条件提供指导。
通过理解反应中间体的形成和消耗,以及各步骤的能量变化,工程师可以优化反应条件,提高产率和选择性,并降低副产物生成。
这种了解有助于更精准地控制反应过程,实现所需产品的高效合成。
对反应机理的深入理解推动着工业生产向更可持续、高效的方向发展,为化工工程领域带来重要的进步与发展。
关键词:化工工程;化学反应工程;动力学;分析引言化学反应工程与动力学分析是化工领域中探索如何在微观层面控制和优化化学变化的关键。
这一领域涉及着从基础的化学反应原理到复杂的工业应用的广泛内容。
本文旨在深入研究化学反应的动力学特性,包括反应速率、反应机理以及对反应过程的影响因素。
动力学原理的理解对于预测和优化化学反应至关重要,因为它们揭示了反应速率随时间和条件变化的规律。
此外,我们将探讨化学反应动力学在工程实践中的应用,包括如何利用这些原理来提高工业生产的效率、改善产品质量,并探索创新的反应设计。
深入了解这些概念将为化工工程师提供关键见解,从而为实现更可持续和高效的化学过程打下基础。
一、化学反应工程基本概念化学反应工程是将化学反应原理应用于工业生产的领域。
它不仅关注反应本身,还牵涉到反应过程的各个环节,包括设计、优化和控制。
工程师在化学反应工程中需要综合考虑多个因素:首先是原料的选择,包括原料的纯度、可获得性和成本等。
其次是反应条件的设定,如温度、压力和反应物浓度等,对于反应速率和产物选择性具有重要影响。
反应器设计也是关键,不同反应类型可能需要不同类型的反应器以最大程度地利用资源和提高产率。
此外,工程师还需考虑产物的分离和纯化方法,确保产品符合质量标准。
化学反应工程知识点

化学反应工程知识点1.反应机理和动力学反应机理是指反应的分子层面的步骤和中间产物,它对理解和控制反应过程非常重要。
动力学研究反应速率与反应物浓度的关系,了解反应速率规律,通过动力学模型可以预测反应速率和产物选择性。
2.反应条件的选择反应条件的选择包括温度、压力、反应物浓度、反应物配比和催化剂等。
化学反应的速率和选择性往往受到反应条件的影响,优化反应条件可以提高反应速率和产物质量。
3.反应器的设计和优化反应器是进行化学反应的设备,其设计和优化对反应过程的效率和产品质量具有重要影响。
常见的反应器类型有批式反应器、连续式反应器和循环式反应器等。
反应器的选择和设计要考虑反应物性质、反应过程的控制方式、热传导和质量传递等因素。
4.反应工艺的控制反应工艺的控制包括对反应过程的监测和调节,以维持所需的反应条件和优化产品质量。
常用的控制策略有温度、压力和反应物供给的控制等。
控制系统的设计和优化需要考虑反应机理、反应动力学和工艺实际操作的特点。
5.安全与环保化学反应过程中会产生化学品和能量的变化,单个反应步骤可能会产生副产物和废物。
因此,反应工程也需要关注安全性和环保性。
安全性考虑的因素包括反应物和产物的毒性、易燃性和爆炸性等,以及反应条件的选择和操作的威胁。
环保方面,需要考虑减少废物的生成,回收利用资源,优化反应条件以减少能耗和污染物排放。
6.规模放大与工业化化学反应工程要实现从实验室到工业生产的规模放大和工艺转化。
这涉及到规模放大的技术、成本评估和安全规范,以及将实验室的合成路线或方法转化为适合大规模生产的工艺。
同时,也需要考虑工艺的稳定性和连续运营的可行性。
以上是化学反应工程的一些基本知识点,化学反应工程涵盖了多个学科领域,是化学工程和化学的交叉学科。
化学反应工程的研究和应用有助于解决实际生产中的技术问题,提高反应过程的效率和产品质量,同时也倡导可持续发展和环保意识。
化学反应工程的定义
化学反应工程的定义
化学反应工程是一门研究化学反应过程的学科,它涉及到化学反应的设计、优化和控制,以及相关的反应器的设计和操作。
化学反应工程的目标是通过科学的方法和工程技术,实现化学反应的高效、安全和可持续发展。
化学反应工程主要包括以下几个方面的内容:
1. 反应过程的设计和优化:研究如何选择合适的反应条件(温度、压力、反应物浓度等)和催化剂,以提高反应的转化率、选择性和产率,同时降低能耗和废物产生。
2. 反应器的设计和操作:研究如何设计和选择合适的反应器类型(如批式反应器、连续流动反应器、固定床反应器等),以及反应器的尺寸、形状和内部结构,以实现理想的反应条件和反应效果。
3. 反应工艺的控制:研究如何实现反应过程的自动化和精确控制,包括反应温度、反应物添加速率、反应物浓度等参数的控制,以确保反应的稳定性和一致性。
4. 安全与环保:研究如何评估和管理化学反应过程中的安全风险,设计和实施安全措施,以保障工作人员的安全和环境的保护。
通过化学反应工程的研究和应用,可以优化化学反应过程,提高产品质量和产量,降低生产成本和能耗,减少环境污染和废物排放,为化学工业的可持续发展提供科学的支持和指导。
化学反应工程原理 第二版 华东理工大学出版社
AoC 2121t an n p n n A Ao Po P )()(--=-βAf Ao Pf C C C -=βAoPf C C =ϕ1 基本概念 1.1 优化:在一定的范围内,选择一组优惠的决策变量,使系统对于确定的评价标准达到最佳的状态。
1.2 反应速率:反应系统中某一物质在单位时间、单位反应区内的反应量。
1.3 反应转化率:反应物中某一组分转化掉的量(摩尔)与其初始量(摩尔)的比值。
常用x 表示。
1.4 选择率:对于复杂反应过程,同一反应原料可以生成几种不同的产物和无用的副产物。
此时,不同产物之间的分配比例对该反应过程的经济效益是一个非常重要的指标。
产物之间的这种分配比例可以用反应选择率 表示。
定义为已经转化掉的反应物量(摩尔)中,转化为目的产物的摩尔分率。
例:(主反应) (副反应)或又称为平均选择率。
瞬时选择率 β1.5 反应收率:得到的产物的量与投入反应系统的原料的量的比值φ。
该指标综合了选择率和反应速率两个指标的特点。
可采用摩尔收率和质量收率来表示。
以摩尔收率为例:总收率1.6 单耗:产品的原料消耗若以每份产品所需的反应原料份数来表示,就称为原料单耗,也可以用摩尔分率或质量分率来表示。
单耗与收率互成倒数。
1.7 返混:使早先进入的存在于反应器内的物料有机会与刚进入的反应物料相混合,这种混合现象称为返混现象。
1.8 排除了一切物理传递过程的影响,得到的化学反应动力学称为微观动力学或本征动力学。
在包含物理过程影响的条件下所测得的反应动力学称为宏观动力学(或称为表观反应动力学)。
1.9 基元反应和非基元反应:如果一个化学反应,反应物分子在碰撞中相互作用直接转化为生成物分子,这种化学反应称为基元反应(elementary reaction),否则就是非基元反应。
1.10 反应机理或反应历程:复杂反应要经过若干个基元反应才能完成,这些基元反应代表了反应所经过的途径,动力学上就称为反应机理或反应历程。
工业生产中的化学反应工程分析
工业生产中的化学反应工程分析化学反应工程是一门交叉学科,涉及到化学、化工、机械、控制等方面的知识。
在工业生产中,很多产品都要通过化学反应来得到,因此化学反应工程的分析和优化对于工业生产的发展和创新至关重要。
一、化学反应工程的基本概念化学反应是指两种或以上物质的相互作用,形成新的物质。
化学反应包括各种类型,如酸碱反应、氧化还原反应、复分解反应等。
在工业生产中,化学反应的目的是制得具有一定的市场需求和经济效益的化学品。
化学反应工程是将化学反应过程应用于工业生产中的技术方法。
在化学反应工程中,需要考虑反应的标准条件、反应速率、反应平衡、化学动力学等因素,以及反应产生的能量、质量传递等问题。
二、反应器设计的基本原则反应器设计是化学反应工程的重要组成部分,其目的是确保反应达到预期目标的同时,保证操作安全和经济效益。
反应器设计的基本原则包括以下几个方面:1.反应器的选择:反应器的类型有很多种,如批式反应器、连续式反应器、循环式反应器等。
对于不同种类的反应,要选择适合的反应器。
2.反应器的尺寸:反应器的尺寸决定了反应的规模,要根据生产需求和经济效益来确定反应器的尺寸。
3.反应器的构造:反应器的构造要符合反应的特点,比如要考虑反应的温度、压力、催化剂、反应介质等。
4.反应器的操作:反应器的操作要安全可靠,保证反应达到预期目标的同时,最大限度地节约资源和成本。
三、化学反应过程的分析和优化化学反应工程的核心是分析和优化化学反应过程。
化学反应过程的分析和优化可以通过下面几种方法来实现:1.化学反应的机理研究:了解化学反应的机理有助于优化反应过程,提高反应效率和产物质量。
2.反应动力学分析:反应动力学研究反应速率与反应物浓度、温度等因素的关系,有助于预测反应过程的发展趋势。
3.反应条件的调节:反应条件包括反应温度、压力、催化剂等,通过调节反应条件,可以改善反应过程,提高化学品的收率和品质。
4.反应器的操作和控制:反应器的操作和控制是反应工程的关键,通过智能化的控制系统,可以实时调节反应条件和采取相应的措施。
化学反应工程基础知识总结(笔记)
化学反应工程基础知识总结(笔记)1、化学反应工程是一门研究涉及化学反应的工程问题的学科。
如何将其在工业规模上实现是化学反应工程的主要任务。
2、理想置换反应器的特点:①由于流体沿同一方向,以相同速度向前推进,在反应器内没有物料的返混,所有物料通过反应器的时间都是相同的②在垂直于流动方向上的同一截面,不同径向位置的流体特性是一致的③在定常态下操作,反应器内状态只随轴向位置改变,不随时间改变。
3、全混流反应器的特性①物料在反应器内充分返混②反应器内各物料参数均一③反应器的出口组成与器内物料组成相同④反应过程中连续进料与出料,是一定常态过程。
4、返混的定义:物料在反应器内不仅有空间上的混合而是有时间上的混合,这种混合过程称返混。
5、非均相催化反应过程步骤①反应组分从流体主体向固体催化剂外表面传递②反应组分从外表面向催化剂内表面传递③反应组分在催化剂表面的活性中心上吸附④在催化剂表面上进行化学反应⑤反应产物在催化剂表面上解吸⑥反应产物从催化剂内表面向外表面传递⑦反应产物从催化剂的外表面向流体主体传递6、兰格缪尓(Langmuir)吸附模型条件①催化剂表面上活性中心分布是均匀的②吸附活化能和脱附活化能与表面吸附的程度无关③每个活性中心仅能吸附一个气相分子④被吸附分子间互不影响,也不影响空位对气相分子的吸附。
7、焦姆金(Temkhh)吸附模型:一般吸附活化能随覆盖率的增加而增大,脱附活化能则随覆盖率的增加而减小,因此吸附热必然随覆盖率的增加而减小。
8、催化剂颗粒内气体扩散:多孔催化剂颗粒内的扩散现象是很复杂的。
除扩散路径极不规则外,孔的大小不同时,气体分子扩散机理亦有所不同。
当孔径较大时,分子的扩散阻力要是由于分子间碰撞所致,这种扩散通常所称的分子扩散或容积扩散。
当微孔的孔径小于分子的平均自由程时,分子与孔壁的碰撞机会超过了分子间的相互碰撞,从而使分子与孔壁的碰撞成为扩散阻力的主要因素,称为克努森(Knudson)扩散。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第一章1. 化学反应工程是一门研究 (化学反应个工程问题)的科学。
2. 所谓数学模型是指 (用数学方法表达各变量间的关系)。
3. 化学反应器的数学模型包括 (动力学方程式、 物料横算式子、 热量衡算式、动量衡算式 和 参数计算式)4. 所谓控制体积是指 (能把反应速率视作定值的最大空间范围)。
5. 模型参数随空间而变化的数学模型称为 ( 分布参数模型)。
6. 模型参数随时间而变化的数学模型称为 (非定态模型)。
7. 建立物料、热量和动量衡算方程的一般式为 (累积量=输入量-输出量)。
第二章1. 均相反应是指 (在均一的液相或气相中进行的反应)。
2. 对于反应aA + bB → pP + sS ,则r P =( p/a )r A 。
3.着眼反应物A 的转化率的定义式为(转化率Xa=转化了的物料A 的量/反应开始的物料A 的量)。
4. 产物P 的收率ΦP 与得率ХP 和转化率x A 间的关系为( Xp/Xa )。
5. 化学反应速率式为r A =k C C A αC B β,用浓度表示的速率常数为k C ,假定符合理想气体状态方程,如用压力表示的速率常数k P ,则k C =[ (RT)的a+B 次方]k P 。
6.对反应aA + bB → pP + sS 的膨胀因子的定义式为 (P+S )-(A+B))/A 。
7.膨胀率的物理意义为 (反应物A 全部转化后系统的体积变化率)。
8. 活化能的大小直接反映了 (反应速率) 对温度变化的敏感程度。
9. 反应级数的大小直接反映了(反应速率) 对浓度变化的敏感程度。
10.对复合反应,生成主产物的反应称为 (主反应),其它的均为(副反应)。
11. 平行反应A → P 、A → S 均为一级不可逆反应,若E 1>E 2,选择性S p 与 (A 的浓度)无关,仅是 (A 的浓度) 的函数。
12. 如果平行反应A → P 、A → S 均为一级不可逆反应,若E 1>E 2,提高选择性S P 应(提到温度)。
13. 一级连串反应A → P → S 在平推流反应器中,为提高目的产物P 的收率,应(降低)k 2/k 1。
14. 产物P 的收率的定义式为 (生成的全部P 的物质的量/反应掉的全部A 的物质的量)15. 产物P 的瞬时收率φP 的定义式为(生成的物质的量/反应的A 的物质的量)16. 产物P 的选择性S P 的定义式为(单位时间内产物P 的物质的量/单位时间内生成产物S的物质的量)17. 由A 和B 进行均相二级不可逆反应αA A+αB B = αS S ,速率方程为:r A =-dC A /dt=kC A C b 。
求: (1)当C A0/C B0=αA /αB 时的积分式(2)当C A0/C B0=λ≠αA /αB 时的积分式18. 反应A → B 为n 级不可逆反应。
已知在300K 时要使A 的转化率达到20%需12.6min ,而在340K 时达到同样的转化率仅需3.20min ,求该反应的活化能E 。
第三章1. 理想反应器是指(理想混合反应器 平推流反应器)。
2. 全混流反应器的空时τ是 (反应器容积) 与(进料的体积流量)之比。
3. 全混流反应器的放热速率Q G ={ 00()A A Hr Ft y x ∆ }。
4. 全混流反应器的移热速率Q r ={ 012()pm Ft C T T - }5. 全混流反应器的定常态操作点的判据为{ G r Q Q = }。
6. 全混流反应器处于热稳定的定常态操作点的判据为{ G r Q Q = G r dQ dQ dT dT> }。
7. 全混流反应器的返混 (无限大)。
8. 平推流反应器的返混为 (为零)。
9. 平推流是指 (反应物料以一致的方向向前移动)。
10. 全混流是指 (刚进入反应器的新鲜物料与已存在的反应器中的物料能达到瞬间的完全混合)。
11. 平推流的特征为 (所有物料颗粒在反应器中的停留时间相同不存在反混)。
12. 全混流的特征为 (反应器中各处浓度温度相等 且都与出口处一致 反混无限大)。
13. 如果将反应器出口的产物部分的返回到入口处与原始物料混合,这类反应器为 (循环反应器)。
14. 对循环反应器,当循环比β→0时为 (平推流) 反应器,而当β→∞时则相当于(全混釜)反应器。
15. 对于反应级数n <0的反应,为降低反应器容积,应选用 (全混流) 反应器为宜。
16. 对于反应级数n >0的反应,为降低反应器容积,应选用 (平推流) 反应器为宜。
17. 对于可逆放热反应如何选择操作温度?答:对于放热反应要使反应速率尽可能保持最大必须随转化率的提高,按最优温度曲线相应降低温度,这是由于可逆放热反应,由于逆反应速率也随反应温度的提高而提高,净反应速率出现一极大值;而温度的进一步提高将导致正逆反应速率相等而达到化学平衡。
18. 对于反应,r R =k 1C A 2,E 1;r S =k 2C A ,E 2,当E 1>E 2时如何选择操作温度可以提高产物的收率?答:对于平行反应ART E E A RT E RTE S R R C e k k C e k e k r r S 12212010/20/10---===,所以,当1E >2E 时应尽可能提高反应温度,方可提高R 的选择性,提高R 的收率。
19. 在间歇釜中一级不可逆反应,液相反应A → 2R ,r A =kC A kmol/m 3·hk=9.52×109exp[-7448.4/T] h -1C A 0=2.3 kmol/m 3,M R =60,C R 0=0,若转化率x A =0.7,装置的生产能力为50000kg 产物R/天。
求50℃等温操作所需反应器的有效容积?(用于非生产性操作时间t 0=0.75 h )解:)/(22.3230m kmol x C C A A R ==A x A A x AA A x k x dx k kC dx C t A A -=-==⎰⎰11ln 111000 92.0502734.7448ex p 1052.99=⎥⎦⎤⎢⎣⎡+-⨯=k )(31.17.011ln 92.01h t =-=24500000=+t t M VC R R )(2.226022.32406.2500003m V =⨯⨯⨯=20. 应用两个按最优容积比串联的全混流釜进行不可逆的一级液相反应,假定各釜的容积和操作温度都相同,已知此时的速率常数k=0.92h -1,原料液的进料速度v 0=10m 3/h ,要求最终转化率x A =0.9,试求V 1、V 2和总容积V 。
解:对于一级不可逆反应应有21010111)1(1)1(1)1(A A A A A A A x kC x kC x x r -=⎥⎦⎤⎢⎣⎡-∂∂=∂-∂ 代入⎥⎥⎦⎤⎢⎢⎣⎡----=∂-∂+-i A i A i A iA i A i A r r x x x r ,1,1,,,,111)1( 得 ⎥⎦⎤⎢⎣⎡----=-)1(1)1(11)1(1102001210A A A A A A A A x kC x kC x x x kC整理得 022121=+-A A A x x x∵9.02=A x , ∴6838.01=A x ∴)(35.2)6838.01(92.06838.0)1(111h x k x A A =-=-=τ)(5.233101m v V ==τ)(35.2)9.01(92.06838.09.0)1(2122h x k x x A A A =--=--=τ)(5.233202m v V ==τ总容积)(47321m V V V =+=21. 用两串联全混流反应器进行一个二级不可逆等温反应,已知在操作温度下k=0.92m 3/(kmol.h ),C A 0=2.30kmol/m 3,v 0=10m 3/h ,要求出口x A =0.9,计算该操作最优容积比V 1/V 2和总容积V 。
解:31202120111)1(2])1(1[)1(A A A A A A A x kC x kC x x r -=-∂∂=∂-∂代入]11[1)1(1,2,0,1,1,1,A A A A A A r r x x x r ----=∂-∂])1(1)1(1[1)1(221,2021,201,31,20A A A A A A A x kC x kC x x kC ---=-741.0099.001.33112131==-+-A A A A x x x x∴ h x kC x x A A A A 22.5)741.01(3.292.1741.0)1(2210011=-⨯⨯=--=τh x kC x x A A A A 51.7)9.01(3.292.0741.09.0)1(2220122=-⨯⨯-=--=τ 695.051.722.52121===ττV V总容积021v V V V ⨯=+=τ ∴ 33.127)22.551.7(10m V =+⨯=22.在平推流反应器中进行等温一级反应,出口转化率可达0.85。
现将反应转移至一个等体积的全混流反应器中进行,操作条件完全不变,试问出口转化率将为多少?解 : 00110000102121111ln()(1)1(1)11ln()(1)10.850.655xA xA A A A A A A A A A A A A A A A A A A dx dx V C C v KC KC x K x C C x KC K x x K x K x x x ττττ====---==-==--==⎰⎰23. 等温间歇反应器反应时间与反应物浓度的关系在间歇反应器中进行等温二级反应A →B,r A =0.01C A 2mol/(l.s),当C A0为1mol/l 时,求反应至C A =0.01mol/l 所需时间。
解: 00.0102010.01111()99000.010.011A A A x C A A A A C A A A dx dC dC C r r C s τ==-=---=-=⎰⎰⎰24. 液相反应A →R 在一全混釜中进行,C A0=1mol/l ,反应速率常数k =1l/(mol.s ),求:1) 平均停留时间为1s 时该反应器的x A ;2) 若v 0=1l/s ,x A =0.56,求反应器的体积。
第四章1. 停留时间分布的密度函数在t <0时,E (t )=(0)。
2. 停留时间分布的密度函数在t ≥0时,E (t )(>0)。
3. 当t=0时,停留时间分布函数F (t )=(0)。
4. 当t=∞时,停留时间分布函数F (t )=(1)。
5. 停留时间分布的密度函数E (θ)={ t }E (t )。
