糖尿病新药Victoza、Onglyza艰难上市
沙格列汀的市场前景评估教学文案

沙格列汀作者:辛思名称:沙格列汀英文名称:saxagliptin原研商品名:ONGLYZA原研企业:施贵宝申报类别:化药6类原研上市时间:2009年8月在美国首次上市;随后在英、德、欧盟、日本等主要国家上市,2011年在中国获批进口。
受理企业和时间:施贵宝(原研进口)、科伦、石药、恒瑞、齐鲁、正大天晴、北京万生、江苏奥赛康、河北天成等规格:5mg、2.5mg适应症:II型糖尿病。
目前最快进度:原研上市,国内仿制企业半数以上获得临床批文。
预测最早上市时间:2019年获批可能性:★★★★(口服)新药看点:。
预计未来市场规模:3亿预计临床前研发费用:800-1500万生产批文转让费用:3000万以上临床批文转让费用:1000万项目并购价值:★★☆新药述评:2型糖尿病无论在世界,还是中国,都是大病种。
由于活动量和体力劳动的减少,以及高热量食物的摄取增加,2000年全球估计有1.7亿2型糖尿病患者,预测到2030年将翻倍,达到3.6亿,届时糖尿病患者将占当时全球人口的4.4%。
中国的糖尿病患者人数,2010年估计在4000万人左右,占我国总人口的3%左右。
预计到2020年糖尿病患者人数将达到6300万人。
糖尿病到目前为止仍无根治性的治疗方法,除了运动和饮食控制外,主要就是靠长期药物控制。
20世纪,糖尿病的治疗药取得了长足的进步,先后开发出了胰岛素、二甲双胍、磺酰脲类、噻唑烷二酮类、糖苷酶抵制剂类等多种不同机理的降糖药。
尽管这些药对于控制血糖,减少并发症起到了重要的作用,但由于糖尿病患者胰岛功能的进行性衰退,糖尿病的发展仍具有渐进性,约有半数的患者不能将HbA1c(糖化血红蛋白)指标保持在推荐水平(7%以下)。
医学研究表明,2型糖尿病发病和进展的一个重要原因是胰岛功能的进行性衰退,包括β细胞胰岛素分泌缺陷和α细胞胰升糖素不适当的分泌增加,造成胰岛素/胰升糖素比例失调。
2型糖尿病的核心是胰岛β细胞和α细胞的异常。
1型糖尿病即将批准上市

1型糖尿病新药即将批准上市1型糖尿病简介1型糖尿病是一种自身免疫性疾病,患者的胰岛素分泌细胞被自身免疫系统攻击并破坏,导致胰岛素分泌不足或缺乏。
这种病多发于儿童和青少年,也可能发生在成年人身上。
患者需要终身依赖外源性胰岛素治疗,以维持血糖水平的稳定。
现有治疗方案的局限性目前,1型糖尿病的治疗主要依赖于注射胰岛素。
患者需要频繁监测血糖水平,并根据血糖水平调整胰岛素剂量。
这种治疗方式虽然有效,但也存在一些局限性:1.注射胰岛素可能导致低血糖等不良反应。
2.频繁注射给患者带来了生活质量的影响。
3.胰岛素治疗无法从根本上解决胰岛素分泌细胞被破坏的问题。
新药研发进展近年来,科研人员一直在努力研发新的1型糖尿病治疗方法。
其中,一种名为”Teplizumab”的新药已经完成了临床试验,有望在不久的将来获得批准上市。
Teplizumab是一种人源化单克隆抗体,能够特异性结合到T细胞表面的CD3受体,从而抑制T细胞的活性,阻止自身免疫反应对胰岛素分泌细胞的破坏。
临床试验结果表明,Teplizumab能够延缓1型糖尿病的发病进程,改善患者的胰岛素分泌功能。
与传统的胰岛素治疗相比,Teplizumab具有以下优势:1.通过抑制自身免疫反应,从根本上延缓疾病进展。
2.改善胰岛素分泌功能,减少外源性胰岛素的依赖。
3.给药方式更为便捷,两周给药一次,减少注射频率。
新药上市前景Teplizumab的临床试验结果令人鼓舞,有望为1型糖尿病患者带来新的治疗选择。
专家预测,该药有望在未来1-2年内获得批准上市。
一旦上市,Teplizumab有望惠及广大1型糖尿病患者,特别是新诊断的患者。
早期干预能够更好地保护残存的胰岛素分泌细胞,延缓疾病进展。
对于已经使用胰岛素治疗多年的患者,Teplizumab也可能带来治疗方案的优化,减少胰岛素用量,提高生活质量。
结语1型糖尿病是一种严重的慢性疾病,给患者的生活带来了巨大影响。
Teplizumab等新药的研发为患者带来了新的希望。
沙格列汀片saxagliptin用于治疗成人的2型糖尿病
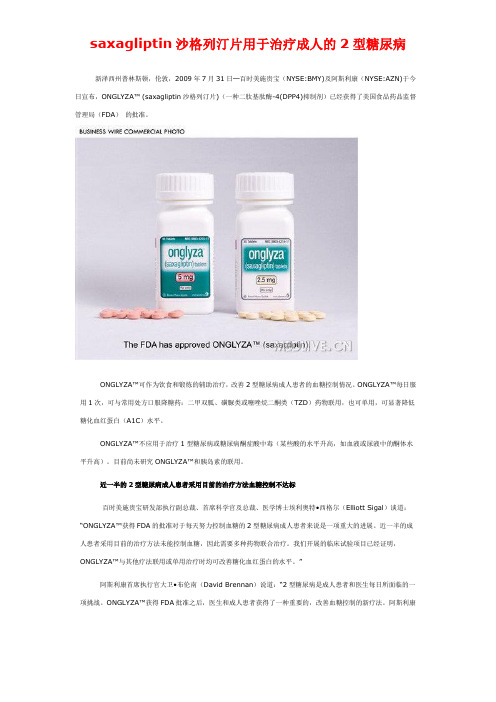
新泽西州普林斯顿,伦敦,2009年7月31日─百时美施贵宝(NYSE:BMY)及阿斯利康(NYSE:AZN)于今日宣布,ONGLYZA™ (saxagliptin沙格列汀片)(一种二肽基肽酶-4(DPP4)抑制剂)已经获得了美国食品药品监督管理局(FDA)的批准。
ONGLYZA™可作为饮食和锻炼的辅助治疗,改善2型糖尿病成人患者的血糖控制情况。
ONGLYZA™每日服用1次,可与常用处方口服降糖药:二甲双胍、磺脲类或噻唑烷二酮类(TZD)药物联用,也可单用,可显著降低糖化血红蛋白(A1C)水平。
ONGLYZA™不应用于治疗1型糖尿病或糖尿病酮症酸中毒(某些酸的水平升高,如血液或尿液中的酮体水平升高)。
目前尚未研究ONGLYZA™和胰岛素的联用。
近一半的2型糖尿病成人患者采用目前的治疗方法血糖控制不达标百时美施贵宝研发部执行副总裁、首席科学官及总裁、医学博士埃利奥特•西格尔(Elliott Sigal)谈道:“ONGLYZA™获得FDA的批准对于每天努力控制血糖的2型糖尿病成人患者来说是一项重大的进展。
近一半的成人患者采用目前的治疗方法未能控制血糖,因此需要多种药物联合治疗。
我们开展的临床试验项目已经证明,ONGLYZA™与其他疗法联用或单用治疗时均可改善糖化血红蛋白的水平。
”阿斯利康首席执行官大卫•布伦南(David Brennan)说道:“2型糖尿病是成人患者和医生每日所面临的一项挑战。
ONGLYZA™获得FDA批准之后,医生和成人患者获得了一种重要的,改善血糖控制的新疗法。
阿斯利康与百时美施贵宝之间开展了密切合作,以期进一步了解如何最好地治疗这种颇具挑战性的疾病,从而帮助成人患者达到治疗目标。
ONGLYZA™正是我们合作的成果。
”ONGLYZA™的获批基于一个临床开发项目,该项目包括约5000名受试者,其中4000多名使用了ONGLYZA™。
在控制饮食和锻炼基础上,该开发项目的组成包括:将ONGLY ZA™加用于其他口服降糖药(包括二甲双胍、磺脲类中的格列苯脲和TZDs)的研究;在初次接受治疗的成人糖尿病患者中,开始便联合使用二甲双胍和ONGLYZA™的研究;以及单药治疗研究。
国家药监局附条件批准纳鲁索拜单抗注射液上市

国家药监局附条件批准纳鲁索拜单抗注射液上市
佚名
【期刊名称】《中国处方药》
【年(卷),期】2024(22)1
【摘要】近日,国家药品监督管理局通过优先审评审批程序附条件批准上海津曼特生物科技有限公司申报的纳鲁索拜单抗注射液(商品名:津立生)上市。
该药品用于治疗不可手术切除或手术切除可能导致严重功能障碍的骨巨细胞瘤成人患者。
纳鲁索拜单抗注射液(JMT103)为重组全人源抗核因子-κB受体活化因子配体(RANKL)单克隆抗体,通过与细胞表面的RANKL特异性结合。
【总页数】1页(PI0001)
【正文语种】中文
【中图分类】R73
【相关文献】
1.国家药监局附条件批准卡度尼利单抗注射液上市
2.国家药监局批准佩索利单抗注射液上市
3.国家药监局附条件批准伊基奥仑赛注射液上市
4.国家药监局附条件批准纳基奥仑赛注射液上市
5.国家药监局批准仑卡奈单抗注射液上市
因版权原因,仅展示原文概要,查看原文内容请购买。
最具潜力十大新药

最具潜力十大新药5月4日美国行业评估商标准普尔(Standard&Poor’s)在其数据网站上发布了10个进入研发后期、预计未来两年有可能在美国上市的最具市场前景的新药汇总报告。
这十个新药分别为:1.Denosumab (骨质疏松症)/安进制药(标准普尔信用评级:A+)入选原因:因为安进公司的大分子药物核心产品组合处于高度成熟期,最近几年正面临着销售低速增长。
由于种种原因,占该公司销售额90%以上的高端产品阿法达贝泊汀((darbepoetin alfa,Aranesp)、阿法依泊汀(Epoetin Alfa,Epogen)、聚乙二醇化非格司亭(pegfilgrastim,Neulasta)、非格司亭(filgrastim,Neupogen)及依那西普(etanercept,Enbrel),预计在今后5年不会有实质性增长(还可能有所下滑)。
状态:2008年12月向FDA提交申请,如在规定时限内获得FDA批准,预计该产品将在2009年后期上市。
简介:Denosumab是一种针对核因子k B配体受体活化因子(RANKL)的人源化单克隆抗体。
RANKL是骨代谢过程中重要分子,是骨重吸收主要信号。
安进公司已经完成Denosumab对更年期妇女和药物引起的乳腺癌及前列腺癌患者骨质疏松的治疗和预防的III期临床研究,取得了肯定结果。
预防前列腺癌患者骨转移和预防乳腺癌、前列腺癌及实体瘤患者骨相关事件的III期临床试验将分别在2009年底和2010年结束。
用于预防骨质疏松患者骨折,每年只需用药两次,与目前需要每天或每周给药的药物相比,其依从性将大大提高。
2. Brilinta (AZD6140; 动脉血栓)/阿斯利康(S&P credit rating, AA-)入选原因: 阿斯利康公司最近两年在进入最后阶段的药物研发方面取得了长足进步,无论内部研发还是外部合作方面都有所改观,而此前的2006年则显得较弱。
DPP4新药瑞格列汀,四大降糖优势成“新宠”

DPP4新药瑞格列汀,四大降糖优势成“新宠”
提起来列汀类降糖药物,想必大家并不陌生。
市面上常见的有西格列汀,维格列汀、阿格列汀、沙格列汀和利格列汀,这五种列汀药物又被称为“五朵金花”。
这类药物具有全新的作用机制,通过减少内源性胰高血样肽-1的降解,进而发挥降糖作用。
今天咱们要说的是被称为“国货之光”的瑞格列汀。
瑞格列汀同样也属于DPP4抑制剂,是我国国内一家医药公司,自主研发的一款新的DPP4抑制剂。
在2023年6月经过国家药品监督管理局批准上市,为糖尿病患者的个体化治疗,提供了新的选择。
那么,该药物有哪些优势呢?今天咱们就来盘点。
一、进入国家医保
2023年12月国家公布的医保目录中,通过医保谈判,磷酸瑞格列汀片首次纳入国家医保目录,能够让更多的患者享受比较实惠的价格,这对于大多数的糖尿病患者是非常友好的,减轻了他们的经济负担。
二、安全性更高
研究表明,该药物使用过程中,具有不引起体重增加、不产生低血糖、胃肠道副作用低等优势,非常适合于低血糖风险高和需要减重的患者。
且大数据表明,即使是在肝肾功能不全的患者中,也可安全使用。
三、降糖作用温和
瑞格列汀降糖作用比较温和,在众多的口服降糖药物中,属于中等水平。
因此,大多数患者单独服用该药物不能很好的降低血糖水平时,可以与其他降糖药物联合使用。
四、给药方案更加灵活
需要明确的是,该药物可单药也可与二甲双胍等其他降糖药物联合使用。
且药动学结果显示,该药物生物利用度不受进食影响,饭前饭后服用均可。
服用方案也比较灵活,既可一天一次给药,也可以一天两次服用,这在一定程度上也提高了患者的依从性。
传奇降糖药从毒蜥蜴到一周一次治疗

传奇降糖药从毒蜥蜴到一周一次治疗作者:来源:《科学大观园》2019年第12期随着人们生活水准的提高,这种曾被称为“富贵病”的糖尿病患病率在全球范围内正处于快速上升期,日益成为严重威胁人类健康的全球性慢性疾病。
一个世纪以前,班廷将胰岛素用到了糖尿病的治疗上,揭开了人类攻克糖尿病的历史巨幕。
在糖尿病治疗领域,不乏传奇的故事,而形形色色的降糖药背后也有许多故事。
比如,从苹果树皮中“孕育”出的那些被称作“格列净”的SGLT2抑制剂;再比如,从毒蜥蜴身上找到的GLP-1受体激动剂。
百泌达和百达扬是最早获批的此类药物,已有近20万中国糖尿病患者使用,如果能顺利进入到医保的行列,这将为更多2型糖尿病患者带来福音。
这经典的GLP-1受体激动剂,到底是怎样一步步走到我们跟前的呢?来自狗狗的灵感19世纪下半叶,欧洲生理学家开始关注胰腺内外分泌的机制。
这段时间,内分泌学接连迎来了几个重大突破。
一、证实了胰腺是糖尿病的起源部位。
二、1901年美国医生Eugene opie将胰腺的两个功能区分开了:胰腺的外分泌腺主要分泌胰液,调节消化功能;内分泌腺是胰岛,主要调节血糖。
三、1905年科学家在胃肠道内发现了第一种动物激素——肠促胰液素。
肠促胰液素,顾名思义,促进胰液的分泌。
换句话说,肠促胰液素可以促进胰腺外分泌腺的分泌。
这引起了科学家们的强烈好奇:既然胃肠道可以分泌促进胰腺外分泌的激素,那存不存在促进胰腺内分泌的激素呢?20世纪20年代,随着胰岛素的发现,科学家们决定组成“阵线联盟”,一起揭开胃肠分泌胰腺内分泌激素的秘密。
幸运的是,1930年,比利时生理学家Jean La Barre 和他的同事,在对十二指肠提取物进行实验时发现了两个有趣的现象:一个是他们发现,肠促胰液素在复杂的狗狗实验中刺激了狗狗胰腺内分泌腺的分泌;另一个是,十二指肠提取物中的某种成分降低了狗狗的血糖浓度,但对狗狗的胰腺外分泌腺没有影响。
La Barre怀疑,狗狗血糖降低正是因为这种特殊成分刺激了胰岛的分泌,于是,便把它命名为“肠促胰素”。
糖尿病治疗的新进展

糖尿病治疗的新进展糖尿病(Diabetes)是一种常见的代谢疾病,发病率逐年上升,严重影响人们的健康和生产生活质量。
糖尿病患者的胰岛细胞功能障碍造成胰岛素的分泌不足或者胰岛素抵抗,导致血糖升高,进而损害器官和组织,引起一系列并发症,如心血管疾病、眼病、肾病等。
传统的糖尿病治疗方法包括:饮食管理、体育锻炼、口服药物和注射胰岛素。
然而,随着科技进步和药学研究的不断深化,糖尿病治疗的新进展不断涌现,为患者的康复提供了更好的选择。
一、生物仿制药(Biosimilars)生物仿制药是与已有的原始生物药等效的一种生物相似药物,通过与原始药物的分子结构以及生物学特性相似度和生物等效性逐一比较,达到了与原始药物同样的药效和安全性,但价格却更低廉。
在糖尿病治疗中,生物仿制药也逐渐成为了医生和患者更为关注的一种新选择。
例如,卡格列净(Canagliflozin)是一种可信赖的药物,是新型的二糖基肝糖尿病酯酶(SGLT2)抑制剂,采用口服给药方式,能够有效调节血糖水平,降低患者的血糖,提高胰岛素的分泌,缓解患者的症状。
同时,卡格列净也被生物制药公司仿制生产,并被各大医院广泛使用,成为治疗糖尿病的新药物选择。
二、创新药物研究除了传统的糖尿病治疗方法外,研究人员也在不断尝试推出一些创新药物。
例如,GLP-1受体激动剂是一类基于胰高血糖素样肽-1(GLP-1)的药物,能够刺激胰岛素的分泌,降低血糖水平,同时也减轻了胰岛素的IDDM(摄入性糖尿病)的风险;另一方面,大约50%的糖尿病患者存在不同程度的食欲控制障碍,因此应用可食用的、能够刺激食欲的胜肽Y(Y-Peptide)药物,也成为了一个研究的热点问题。
此外,基于人体自身生理和代谢特点,研究人员也在尝试将微生物代谢产物应用于糖尿病的治疗中。
肠道微生物是人体中的重要代谢器官,具有极高的多样性,可以发挥多种代谢功能,包括葡萄糖代谢、胰岛素生成等,它们可以作为治疗糖尿病的关键诱导物质,刺激机体的代谢、恢复胰岛素的正常生成功能、维护人体内部环境的稳定等,从而达到治疗糖尿病的效果。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
糖尿病新药Victoza、Onglyza艰难上市
近日,诺和诺德的Victoza及百时美施贵宝的Onglyza分别获准在欧洲和美国上市。
“文迪亚事件”之后,糖尿病新药上市遭到重挫,低迷到冰点的上市状况直到今年三季度才开始解冻:诺和诺德的Victoza及百时美施贵宝的Onglyza分别获准在欧洲和美国上市。
在这个新药研发低产出周期里,企业需要付出巨大的经费和时间成本,且需要面对药品安全事件所致的药监部门新药准入门槛的提高。
在这样的前提下,能够得以上市销售的新药不可谓不是个“幸运儿”。
但是,在上市之后,所有的新药都不得不直接面对金融危机、政府医疗卫生经费缩减以及一些国家基本药物制度推行等“烦心事”,如今新药所能创造的价值已远不如制药行业的鼎盛时期。
糖尿病新药也是如此。
在这个大得似乎没有什么可不放心的“大病”市场,似乎只要去做就一定会有所获。
然而,当新药突破重重障碍终于得以上市销售之时,先有狼,后有虎,不仅有口服剂型与注射剂型之争,还有同类产品之夺,更有后来者紧跟。
“大病”仍有可为
尽管在目前这个世道,业界普遍认为有特色和疗效“小病”的市场竞争不会那么激烈,将更有作为,但是,“大病”市场从来并且仍然是各大制药公司的必争之地,诺和诺德、礼来、赛诺菲安万特、诺华、百时美施贵宝等制药“大鳄”仍然在这个领域投下重注,加紧开发新药。
的确,糖尿病作为这个时代最为严重的健康问题之一,已经成为社会负担的主要疾病。
全球每10秒就产生两个人患上糖尿病,每年有380万人死于糖尿病及其并发症,与AIDS的死亡人数大体相同。
根据最新的权威数据,目前全球糖尿病患者总数达到2.46亿,预计到2025年,这个数字将升至3.8亿。
在全球范围内,糖尿病相关疾病的直接医疗护理费用占到年度医疗护理总费用的2.5%~15%,其中大部分费用与早产儿死亡及其可预防的并发症相关,包括心脏病、中风、肾衰竭、失明、截肢以及勃起功能障碍在内的血液循环不良相关的疾病。
1型糖尿病患者常见于儿童或年轻人,必须每天进行注射胰岛素治疗才能存活,其发病率以每年3%的速度增长。
2型糖尿病则更为制药企业所重视,因为有90%-95%的糖尿病患者属于该型,并且目前有超过60%的2型糖尿病患者没能达到良好的血糖控制效果。
由于2型糖尿病患者往往没有典型的口渴、尿频、疲劳和伤口愈合慢等症状,往往导致诊断和治疗延迟,并发症的发生率相当高。
触目惊心的数字背后意味着巨大的商机,糖尿病市场自然是各大制药公司的必争之地。
但是,要想从中夺得一杯羹绝非易事。
突破“文迪亚”路障
GSK“文迪亚(Avandia)事件”对于欲在糖尿病市场上市销售的新药而言是个沉重的打击。
其大幅增加服用者心脏病发作的风险,心脏病死亡率也相应上升。
由此,2008年12月,美
国FDA发布公告称,2型糖尿病新药要想获得上市,要接受更为严格的药物安全审查,要保证不会增加患者心脏疾病发作的风险。
这个新药上市低谷一直到今年二季度才有了转机——该季度美国FDA批准了13个新分子实体,比之前明显增加。
今年三季度,欧美市场最新上市的两个糖尿新药引人瞩目,分别是诺和诺德的Victoza和百时美施贵宝的Onglyza,都用于治疗2型糖尿病。
Victoza(liraglutide,利拉鲁肽)于7月获得欧盟的上市批准,成为第一个获得批准用于2型糖尿病的一天一次的人胰高血糖素样肽-1(GLP-1)类似物药物。
目前该药在美国与日本的上市申请还在审批中。
Onglyza(saxagliptin)也在7月获得了美国食品药品管理局(FDA)的批准,是DPP-4(二肽基肽酶-4)抑制剂,为口服制剂,由百时美施贵宝生产,与阿斯利康联合销售。
注射口服龙虎斗
近几年,最有竞争力的2型糖尿病新药,基本就是口服剂型和注射剂型两大对立阵营之间的竞争。
口服剂型的几个新药均为DPP-4抑制剂,默沙东的Januvia和诺华的Galvus。
DPP-4抑制剂虽有口服这个患者容易接受的天然优势,但其疗效备受争议,而且没有减轻体重的益处。
由于2型糖尿病通常并存其他高风险情况,如高血压、高胆固醇和肥胖症,其中体重增加是最大挑战之一,体重增加还是许多糖尿病药物的常见副作用。
而这些治疗难点,恰恰是各制药公司相关药物的开发切点。
GLP-1类似物新药虽为注射剂型,却有着其他药物所没有的降低血糖兼顾减轻体重的疗效优势。
但是,礼来的G LP-1类似物Byetta(艾塞那肽)自2005年5月上市以来饱受口服药产品的市场份额争抢,连赛诺菲安万特的减肥药Acomplia(选择性大麻素受体Ⅰ型拮抗剂)都加入了竞争行列。
Acomplia于2006年7月在25个欧盟成员国上市,是世界上第一个改善超重或肥胖者伴有2型糖尿病及脂代谢紊乱者的补充治疗药物。
在这些不利因素的影响下,2008年Byetta销售增长缓慢,去年销售额仅为6.79亿美元,远未达到“重磅炸弹”药物10亿美元的年销售额。
不过,美国糖尿病协会和欧洲糖尿病研究协会联合发出的最新修订治疗建议,首次将GLP-1受体激动剂作为2型糖尿病的有效治疗方法,而在此新治疗建议中并未包括DPP-4抑制剂,这是GLP-1的一个重大利好。
GLP-1王者之争
“大病”市场的争夺战之胜负,关键还是在于疗效和临床价值,上市新药要想有大的发展,必须证明其有独特价值,因为这个市场只买疗效的账。
如今,GLP-1阵营加入了诺和诺德的Victoza,该药将对Byetta形成直接攻势。
同为既能有效控制血糖,又能降低体重的GLP-1类似物,Victoza每日只需注射一次。
此外,与Byetta 对比的临床试验结果表明,在低血糖控制与恶心的副作用方面,Victoza有明显的优势。
另一方面,虽然Byetta占据了市场先机,但诺和诺德作为专攻糖尿病的制药企业,其在新药推广方面,拥有成熟的全球销售渠道,这是其他公司无法比拟的特色。
不过,Amylin公司、礼来和Alkermes公司正在努力开发一种Byetta的长效缓释剂。
每周用药一次的产品正在进行临床试验,每月用药一次的产品也在研究之中。
糖尿病市场上,还将不断涌现新的进入者。
勃林格殷格翰公司的DPP-4抑制剂linagliptin,是一种每日口服一次的片剂,目前处于Ⅲ期临床试验开发阶段。
罗氏的糖尿病药物GLP-1类似物Taspoglutide也已进入Ⅲ期临床试验阶段
剂,目前处于Ⅲ期临床试验开发阶段。
罗氏的糖尿病药物GLP-1类似物Taspoglutide也已进入Ⅲ期临床试验阶段。
药品名通用名生产商规格参考价
诺和力利拉鲁肽注射液丹麦诺和诺德
公司
3ml:18mg ¥860.00
万苏敏盐酸吡格列酮分散片江苏万邦生化
医药股份有限
公司
15mg*30片¥149.00
格华止盐酸二甲双胍中美上海施贵
宝
500mg*20片¥31.20
天保康注射液葛根素注射液
浙江康恩贝制
药股份有限公
司
100mg/2mLx10
支
¥130.00
丽珠广乐片胰激肽原
酶肠溶片
上海丽珠
制药有限
公司
120iu24
片
¥33.80。
