工艺流程题目
高考化学工艺流程题目专项练习

高考化学工艺流程题目专项练习1.废旧印刷电路板是一种电子废弃物,其中铜的含量达到矿石中的几十倍。
湿法技术是将粉碎的印刷电路板经溶解、萃取、电解等操作得到纯铜等产品。
某化学小组模拟该方法回收铜和制取胆矾,流程简图如下:流程中有三处实现了试剂的循环使用,已用虚线标出两处,第三处的试剂是________。
循环使用的NH4Cl 在反应Ⅰ中的主要作用是_________________________________________。
【答案】H2SO4防止由于溶液中的c(OH-)过高,生成Cu(OH)2沉淀【解析】操作④得到的H2SO4可以利用到反应Ⅲ中,所以第三处循环的试剂为H2SO4;NH4Cl水解溶液呈酸性,可以中和溶液中的OH―,防止由于溶液中的c(OH-)过高,生成Cu(OH)2沉淀。
2.毒重石的主要成分为BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2·2H2O的流程如下:pH pHCa2+Mg2+Fe3+开始沉淀时的pH 11.9 9.1 1.9完全沉淀时的pH 13.9 11.1 3.2加入NH3·H2O调节pH=8可除去________(填离子符号),滤渣Ⅱ中含________(填化学式)。
加入H2C2O4时应避免过量,原因是_____________________________________________________________。
已知:K sp(BaC2O4)=1.6×10-7,K sp(CaC2O4)=2.3×10-9。
【答案】Fe3+Mg(OH)2、Ca(OH)2H2C2O4过量会导致生成BaC2O4沉淀,产品的产量减少【解析】根据流程图及表格中数据可知,加入NH3·H2O调节pH=8时,只有Fe3+完全沉淀而除去。
加入NaOH,调pH=12.5,对比表格中数据可知,此时Mg2+完全沉淀,Ca2+部分沉淀,所以滤渣Ⅱ中含Mg(OH)2、Ca(OH)2。
工艺流程图题目
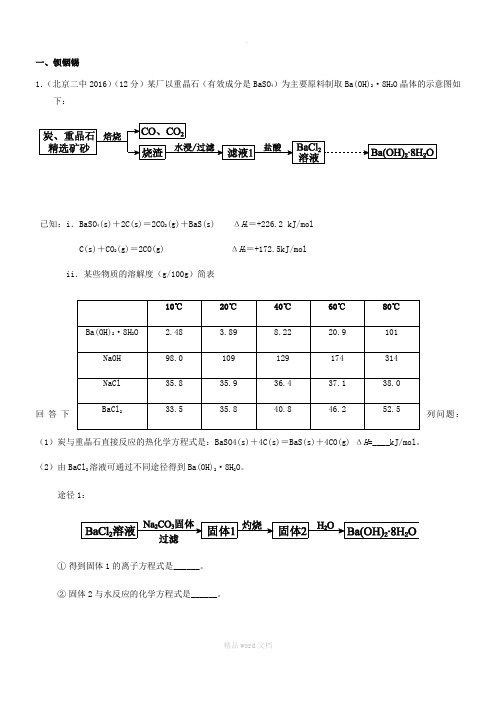
一、钡铟锡1.(北京二中2016)(12分)某厂以重晶石(有效成分是BaSO 4)为主要原料制取Ba(OH)2·8H 2O 晶体的示意图如下:已知:i .BaSO 4(s)+2C(s)=2CO 2(g)+BaS(s) ΔH 1=+226.2 kJ/molC(s)+CO 2(g)=2CO(g) ΔH 2=+172.5kJ/molii .某些物质的溶解度(g/100g )简表回答下列问题:(1)炭与重晶石直接反应的热化学方程式是:BaSO4(s)+4C(s)=BaS(s)+4CO(g) ΔH =____kJ/mol 。
(2)由BaCl 2溶液可通过不同途径得到Ba(OH)2·8H 2O 。
途径1:①得到固体1的离子方程式是______。
② 固体2与水反应的化学方程式是______。
途径2:途径2中的“操作”是加热浓缩,冷却结晶,过滤。
依据上述溶解度简表分析,过滤时的最佳温度是;(3)若向滤液1中加入CuO粉末,可直接得到含Ba(OH)2·8H2O晶体和CuS的浊液,反应化学方程式是______。
将该浊液加热到80℃左右浓缩,趁热过滤,冷却滤液至室温,再过滤,即可得到Ba(OH)2·8H2O晶体。
上述操作中趁热..过滤的原因是______。
2.(2018东城期末)(10分)从废旧液晶显示器的主材 ITO(主要成分是含铟、锡的氧化物)回收铟和锡,流程示意图如下。
资料:(1)为了加快步骤①的反应速率,可以采取的措施有______(至少答两点)。
(2)步骤①中铟的氧化物转化成In3+的离子方程式是______。
(3)步骤②中加入过量铟能够除去溶液中的Sn2+,根据所给资料分析其原因是______。
(4)步骤④和⑤中NaOH溶液的作用是______。
(5)下图是模拟精炼铟的装置图,请在方框中填写相应的物质。
1、(1)+571.2;(2)CO32-+Ba2+=BaCO3↓;BaO+9H2O=Ba(OH)2•8H2O;20℃或常温;20℃时4种物质中Ba(OH)2•8H2O溶解度最小;(3)BaS+CuO+9H2O=Ba(OH)2•8H2O+CuS;减少过滤过程中Ba(OH)2•8H2O的损失.2.(2018东城期末)(10分)(1)增大盐酸浓度、加热、将废料粉碎(2)In2O3+6H+==2In3++3H2O(3)同周期主族元素从左向右原子半径减小,金属性减弱(还原性减弱)(4)除去a、b两种滤渣中的锡和锌(5)二、铬1.(人大附2015)(10分)某厂废水中含5.00×10-3mol·L-1的Cr2O72-,其毒性较大。
高考化学解题工艺流程题

高考化学工艺流程题解题模板原料预处理的各种方法1、粉碎或研磨:增大固液(或固气或固固)接触面积,加快反应(溶解)速率,增大原料的转化率(或浸取率)。
2、煅烧或灼烧:不易转化的物质转为容易提取的物质;其他矿转化为氧化物;除去有机物;除去热不稳定的杂质3、酸浸:溶解、去氧化物(膜)、调节pH促进水解(沉淀)4、碱溶:去油污,去铝片氧化膜,溶解铝、二氧化硅,调节pH促进水解(沉淀)例题1.【2015全国Ⅰ卷】硼及其化合物在工业上有许多用途。
以铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所回答下列问题:(1)写出Mg2B2O5·H2O与硫酸反应的化学方程式_____ ________。
为提高浸出速率,除适当增加硫酸浓度浓度外,还可采取的措施有_____ ____(写出两条)【对点练习】1、步骤I前,β-锂辉石要粉碎成细颗粒的目的是2. MgSO4·7H2O可用于造纸、纺织、陶瓷、油漆工业,也可在医疗上用作泻盐。
某工业废渣主要成分是MgCO3,另外还有CaCO3、SiO2等杂质。
从此废渣中回收MgSO4·7H2O的工艺如下:第一不用硫酸浸出。
(1)“浸出”步骤中,为提高镁的浸出率,可采取的措施有(要求写出任意一条)。
调节溶液的PH:1、目的:使溶液中的。
金属阳离子形成氢氧化物完全沉淀下来而除去2、需要的物质:含主要阳离子的难溶性氧化物或氢氧化物或碳酸盐,即能与H+反应,是PH增大的物质如用MgO、Mg(OH)2等等。
3、原理:加入的物质能与溶液中的H+反应,降低了的浓度,增大PH4、PH控制的范围:大于除去离子的完全沉淀值,小于主要离子的开始沉淀的PH例题2、碳酸锂广泛应用于陶瓷和医药等领域。
以β-锂辉石(主要成分为Li2O·Al2O3·4SiO2)为原料制备Li2CO3的工艺流程如下:已知:Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2、9.7和12.4;Li2SO4、LiOH和Li2CO3在303 K下的溶解度分别为34.2 g、12.7 g和1.3 g。
与氯化亚铜有关的高三化学工艺流程题

与氯化亚铜有关的高三化学工艺流程题以下是一道与氯化亚铜有关的高三化学工艺流程题:
题目:氯化亚铜(CuCl)可用于冶金、电镀等行业。
以下是制备氯化亚铜的一种工艺流程:
步骤1:溶解
取海绵铜(主要含Cu和CuO),加入稀硫酸和NH4NO3的混合溶液,控制溶液温度在60~70℃,不断搅拌至固体全部溶解,得蓝色溶液(过程中无气体产生)。
步骤2:转化
向蓝色溶液中加入(NH4)2SO3和NH4Cl,充分反应后过滤,得到CuCl粗品。
步骤3:精制
将粗品加入适量的稀硫酸和一定量的氯化铵,在一定温度下反应一段时间,再过滤、洗涤、干燥,得到氯化亚铜产品。
回答下列问题:
1. 氯化亚铜微溶于水,不溶于醇和稀酸,可溶于Cl-浓度较大的溶液。
在潮湿空气中易水解氧化。
以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程。
2. 步骤①中N元素被还原为最低价,写出此反应的离子方程式。
3. 步骤⑤中,用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为Cu2(OH)3Cl。
CuCl被氧化为Cu2(OH)3Cl的化学方程式为。
高考化学工艺流程题

高考化学工艺流程题一、探究解题思路呈现形式:流程图、表格、图像设问方式:措施、成分、物质、原因能力考察:获取信息的能力、分解问题的能力、表达能力知识落点:根本理论、元素化合物、实验无机工业流程图题能够以真实的工业生产过程为背景,表达能力立意的命题指导思想,能够综合考察各方面的根底知识与将已有知识灵活应用在生产实际中解决问题的能力。
【例题】某工厂生产硼砂过程中产生的固体废料,主要含有MgCO 3、MgSiO 3、CaMg(CO 3)2、Al 2O 3与Fe 2O 3等,回收其中镁的工艺流程如下:原 料:矿石〔固体〕预处理:酸溶解〔表述:“浸出〞〕除 杂:控制溶液酸碱性使金属离子形成沉淀核心化学反响是:控制条件,调节PH ,使Mg 2+全部沉淀1. 解题思路明确整个流程与每一局部的目的 → 仔细分析每步发生的反响与得到的产物 → 结合根底理论与实际问题思考 → 注意答题的模式与要点在解这类题目时:首先,要粗读试题,尽量弄懂流程图,但不必将每一种物质都推出。
其次,再精读试题,根据问题去精心研究某一步或某一种物质。
第三,要看清所问题,不能答非所问,并注意语言表达的科学性在答题时应注意:前一问答复不了,并不一定会影响答复后面的问题。
分析流程图需要掌握的技巧是:Ⅱ别离提纯 Ⅰ预处理 Ⅱ别离提纯Ⅲ 复①浏览全题,确定该流程的目的——由何原料获得何产物〔副产物〕,比照原料与产物;② 了解流程图以外的文字描述、表格信息、后续设问中的提示性信息,并在下一步分析与解题中随时进展联系与调用;③ 解析流程图并思考:从原料到产品依次进展了什么反响?利用了什么原理〔氧化复原?溶解度?溶液中的平衡?〕。
每一步操作进展到什么程度最正确?每一步除目标物质外还产生了什么杂质或副产物?杂质或副产物是怎样除去的?无机化工题:要学会看生产流程图,对于比拟陌生且复杂的流程图,宏观把握整个流程,不必要把每个环节的原理都搞清楚,针对问题分析细节。
中考试题分类工艺流程题

2015中考化学试题分类汇编——工艺流程题1.安徽我国制碱工业先驱侯德榜发明了“侯氏制碱法”;其模拟流程如下: 1反应①的化学方程式________________,反应②的基本反应类型为_______; 2工业上用分离液态空气 的方法制取氢气,属于_______变化填“物理”或“化学”;3操作a 的名称是_____,实验室进行此操作所需的玻璃仪器有烧杯、玻璃棒、______;4写出NH 4Cl 的一种用途________________;1CaCO 3 =CaO+CO 2↑;分解反应;2物理;3过滤;漏斗;4做化肥或氮肥等;2. 益阳过氧化钙晶体﹝CaO 2·8H 2O ﹞较稳定,呈白色,微溶于水,广泛应用于环境杀菌、消毒;以贝壳为原料制备CaO 2流程如下:1气体X 是CO 2,其名称是 二氧化碳 ;将过氧化钙晶体与溶液分离的方法是 过滤 ;2反应Y 需控制温度在0~5℃,可将反应容器放在 冰水混合物 中,该反应是化合反应,反应产物是CaO 2·8H 2O,请写出化学方程式CaO 2+H 2O 2+7H 2O =CaO 2·8H 2O ;获得的过氧化钙晶体中常含有CaOH 2杂质,原因是 CaO 或CaOH 2过量,且CaOH 2微溶 ;3CaO 2的相对分子质量为 72 ,过氧化钙晶体﹝CaO 2·8H 2O ﹞中H 、O 元素的质量比为 1∶10 ;4为测定制得的过氧化钙晶体中CaO 2·8H 2O 的质量分数,设计的实验如下:称取晶体样品50g,加热到220℃充分反应方程式为2CaO 2·8H 2O2CaO +O 2↑+16H 2O ↑,杂质不发生变化,测得生成氧气的质量为,请计算样品中CaO 2·8H 2O 的质量分数CaO 2·8H 2O 相对分子质量为216,写出必要的计算过程; 解:设样品中CaO 2·8H 2O 的质量为x 2CaO 2·8H 2O2CaO +O 2↑+16H 2O ↑432 32x ∴x =g∴ 样品中CaO 2·8H 2O 的质量分数为=% 答:样品中CaO 2·8H 2O 的质量分数为=%3. 呼和浩特空气中氮气的含量最多,氮气在高温、高能量条件下可与某些物质发生反应;下图是以空气和其他必要的原料合成氮肥NH 4NO 3的工业流程;请按要求回答下列问题:1步骤①中发生的是%1005032.4________变化填“物理”或“化学”;2写出步骤③中发生反应的化学方程式_________________________________; 3上述化学反应中属于化合反应的有________个;4右图是化肥硝酸铵包装袋上的部分说明:硝酸铵应具有的性质是A.易溶于水 B.有挥发性 C.受热易分解施用该类肥料时,要避免与碱性物质混合使用,写出硝酸铵与熟石灰反应的化学方程式__________________________________;1物理 2 4NH3+5O2=4NO+6H2O334A C 2NH4NO3+CaOH2=CaNO32+2H2O+2NH3↑4. 宜宾黄铜是Zn以主要添加元素的铜合金;黄铜渣中约含Zn7%、ZnO31%、Cu50%、CuO5%,其余为杂质;处理黄铜渣可得到硫酸锌,其主要流程如下杂质不溶于水、不参与反应:已知:ZnO+H2SO4=ZnSO4+H2O; CuO+H2SO4=CuSO4+H2O(1)步骤Ⅰ中产生气体的化学方程式为 ;2溶液A中的金属阳离子有填化学式3步骤Ⅰ、Ⅱ中均包含的操作名称为 ,此操作和步骤Ⅲ中的蒸发操作都要用到的玻璃仪器是 ;4溶液A 填“大于”、“小于”或“等于”溶液C的质量;5. 南昌炼铁产生的废渣中含有大量CuS及少量铁和铁的化合物,工业上以该废渣为原料生产CuCl2的流程图如下,下列有关说法错误的是A.操作1中粉碎的目的是增大反应物的接触面积B.操作2中,CuS、NaCl和O2在高温条件下反应生产CuCl2和Na2SO4化学方程式为CuS + 2NaCl +2O2 ===CuCl2+ Na2SO4C.操作3的名称是过滤D.流程图中能循环利用的物质是NaCl和Na2SO46. 扬州醋酸钙CaAC2是国家允许使用的补钙制剂之一;以蛋壳为原料回收膜并制备醋酸钙的一种工艺流程如下;⑴写出煅烧时的化学方程式 ;CO2的任意排放会引发的环境问题是 ;CO2与CH4一定条件下化合生成甲醛HCHO,则此反应中与最佳质量比是 ;下列做法能减少二氧化碳排放的是 ;填序号⑵在反应I中制备石灰乳,而不是制备澄清石灰水的目的是 ;写出熟石灰的一种用途;⑶在反应II 中醋酸过量的目的是 ;写出反应II 的化学方程式 ; ⑷膜分离时,盐酸不能过量的主要原因是 ;根据煅烧产生的CO 2和蛋壳的主要成分为CaCO 3,可以确定化学方程式;CO 2的任意排放会引发温室效应;根据,计算CO 2与CH 4的质量比是44:16=11:4;⑵石灰乳中的CaOH 2含量比澄清石灰水中多,更利于提高醋酸钙的产量;⑶保证与CaOH 2完全反应,提高醋酸钙的含量;⑷加入盐酸就是为了将蛋壳与膜分开,过量的话会与CaCO 3反应,会使制作醋酸钙的原料量减少; 7. 扬州含锌废渣和各种锌矿如菱锌矿都有着重要的用途I.以含锌废渣主要成分为ZnO,杂质为FeO ﹑CuO 为原料制备七水硫酸锌ZnSO4·7H2O 的流程如下;⑴粉碎的目的是 ;⑵若实验室用质量分数为98%的硫酸配制200g25%的硫酸,需要的玻璃仪器有胶头滴管﹑玻璃棒﹑ 和 ,此处玻璃棒的作用是 ;⑶物质X 是 ,滤渣中含有的金属单质有 ,除铜时发生的反应属于 反应填基本反应类型↑+23a CO CaO CO C 高温HCHO CH CO 242→+一定条件O H AC Ca HAC OH Ca 2222)(2)(+=+⑷流程中获得七水硫酸锌前省略的操作是 ﹑冷却结晶﹑ 洗涤和低温烘干;⑸某温度下,FeOH 3分解得到一种铁﹑氧质量比21:8的氧化物,该氧化物的化学式 ;⑹除铁过程中,温度pH 对除铁效果的影响分别对如图所示;由图可知,除铁时温度应控制在 ℃为宜,pH 应控制在 为宜;II.以某菱锌矿ZnCO3含量为%为原料制备锌的原理如下假设杂质不参加反应:则100吨这样的菱锌矿理论上最多制得锌多少吨写出计算过程⑴固体的表面积越大,化学反应速率越快;含锌废渣粉碎的目的是增大接触面积,加快反应速率,充分反应;⑵浓硫酸稀释过程中需用用到:量筒、滴管、细口瓶、玻璃棒和烧杯,通过比较可知,还缺少烧杯和量筒;此处玻璃棒的作用是搅拌,将热量及时地扩散;⑶加入过量的X,目的是除去铜,本小题实质是物质的除杂,既要除去杂质又要避免引入新的杂质,考虑到金属活动性顺序,故X 可以是锌,滤渣含有锌和置换的铜,这个反应过程是置换反应;⑷这是分离可溶性固体和液体的方法:先将热的饱和溶液冷却,晶体就会析出,将此有晶体析出的饱和溶液,过滤,用少量的水洗涤,再低温烘干;所以操作的步骤是:加热浓缩,冷却结晶,过滤,洗涤和低温烘干↑+23n CO ZnO CO Z 高温2CO Zn COZnO ++高温⑸FeOH 3分解得到一种铁﹑氧质量比21:8的氧化物,铁的氧化物有三种,Fe 2O 3,FeO, Fe 3O 4.比较铁氧的质量比21:8只有Fe 3O 4符合题意;⑹关键看懂两张图的X 轴和Y 轴代表的含义,为了除铁效果最佳,我们需要找出最高除铁率对应的温度和pH.II.题目要求求出理论上最多制得锌多少吨 故设理论上最多制得锌的质量为X, 根据题意可知ZnCO3的质量是=100t×%=由两个方程式可知道ZnCO 3 ~ Zn 125 65X x=8. 雅安 绿矾又名七水硫酸亚铁FeSO 4·7H 2O,其用途广泛,可用于制铁盐、氧化铁颜料、净水剂、防腐剂、消毒剂等;绿矾FeSO 4·7H 2O 的一种综合利用工艺如下: 1细铁丝在氧气中可以燃烧,请写出铁在氧气中燃烧的化学方程式 ;2绿矾与NH 4HCO 3在溶液中反应,有CO 2生成,反应的化学方程式为 ;↑+23n CO ZnO CO Z 高温2CO Zn CO ZnO ++高温t5.6212565=X3隔绝空气进行“焙烧”,铁元素的转化途径是,实际作还原剂的是CO;写出“焙烧”过程中各步反应的化学方程式:A.;;;4.母液“除杂”后,欲得到NH 42SO 4粗产品,操作步骤依次为蒸发浓缩、____________、过滤、洗涤、干燥;13Fe+2O 2Fe 3O 42分2FeSO 4·7H 2O + 2NH 4HCO 3 = FeCO 3+NH 42SO 4+ CO 2↑+ 8H 2O 2分3CO 2+C 2CO 2分 FeO+CO Fe+CO 22分4降温结晶或冷却热的饱和溶液2分9. 厦门黄铜矿主要万分CuFeS 2经初步处理后,所得溶液甲中的溶质为Fe 2SO 43、CuSO 4及H 2SO 4;某同学通过废铁屑与溶液甲反应,制取补血剂原料碳酸亚铁并回收铜;主要步骤如图7所示:1Fe 2SO 43与铁反应的化学方程式: x Fe 2SO 43+ y Fe= z FeSO 4,其中x 、y 、z 为化学计点燃高温高温量数,z的值为_____________;2步骤Ⅰ中,生成铜的化学方程式:__________________________;3步骤Ⅰ中,废铁屑含有少量铁锈,对产物的成分没有影响,原因是____________________________________________________;4步骤Ⅱ中加入一种可溶性试剂可实现其转化,从复分解反应发生的条件分析,该试剂可以是_____________填化学式;5步骤Ⅲ回收铜的方法为_______________________________________;132Fe+CuSO4=Cu+FeSO43铁锈与硫酸反应生成硫酸铁2分4Na2CO3或其他合理答案,2分5加入过量的稀硫酸,过滤、洗涤、干燥10. 广东现有工厂丢弃的废铜屑铜屑表面呈绿色,其中混有少量生锈铁屑;课外活动小组同学欲利用其制取胆矾,他们设计了下面的两种制取流程;已知Cu+Fe2SO43=2FeSO4+CuSO4,请回答:1铜屑表面呈绿色的物质化学式是Cu2OH2CO3,俗称 ,操作所用到的玻璃仪器有:烧杯、玻璃棒和 ;2溶液A的溶质有只写一种;铁锈与稀硫酸反应的化学方程式为:;3两种方法比较,符合绿色化学要求的是方法 ;方法II 的化学方程式为: 2Cu + 2H 2SO 4 + = 2CuSO 4 + ,操作实验步骤为: ,降温结晶;11.佛山现代循环经济要求综合考虑环境污染和经济效益;高纯氧化铁可作现代电子工业的材料,以下是用硫铁矿烧渣主要成分为Fe 2O 3、FeO 、SiO 2为原料制备高纯氧化铁Fe 2O 3的生产流程示意图:NH 42CO 3溶液呈碱性,40 ℃以上时NH 42CO 3分解; 1实验室中,操作Ⅰ、操作Ⅱ用到的玻璃仪器有玻璃棒、烧杯、 等; 2滤液Ⅰ中主要的阳离子是 等;3加适量氨水的目的是 ; 4根据题中信息,加入NH 42CO 3后,该反应必须控制的条件是 ;5滤液Ⅱ中可回收的产品是 写化学式;6写出在空气中煅烧FeCO 3的化学反应方程式 ; 1漏斗 2H + Fe 2+ 3中和过量的H 2SO 4 4控制溶液的温度在40℃以下5NH 42SO 4 64FeCO 3+O 22Fe 2O 3+4CO 2高温12.北京生物浸出技术在金属冶炼中应用广泛;嗜热细菌在65-80℃酸性水溶液及氧气存在下,能氧化黄铜矿主要成分产生硫酸盐,进而生产铜和绿矾,主要流程如下:⑴分离出矿渣的操作是 ;⑵若试剂b 为Fe 粉,反应①的化学方程式为 ;⑶氢氧化铁与试剂a 发生中和反应,反应②的化学方程式为 ;1过滤2313.北京某烟气脱硫的工艺不仅能消除,还能将其转化为石膏等产品,实现“变废为宝”;主要物质转化关系如下:⑴设备1中,通过喷淋水脱去烟气中的,该反应的化学方程式为 ;⑵设备2中,加入的目的是将转化为 ;⑶设备3中,反应前后化合价发生改变的元素是 ;123O ;S14.揭阳某金属冶炼厂的工业废渣中含有泥沙和某些单质,其中单质含有铜、锌和少部分硫;现欲回收铜和锌,并对硫进行处理,主要流程如下图所示:2CuFeS 44CuSO +Fe=Cu+FeSO ()()24242332Fe OH +3H SO =Fe SO +6H O 2SO 42CaSO 2H O ⋅2SO 3CaCO 23H SO 2223SO +H O=H SO 3CaSO1在废气A中,一定含有的有害气体是填化学式;操作①的操作名称是 ;2溶液D中含有的溶质是填化学式;3写出加入Zn后发生的化学方程式写出其中之一即可 ;1SO2;过滤; 2ZnSO4、CuSO4和H2SO43Zn+H2SO4=ZnSO4+H2↑或Zn+CuSO4=Cu+ZnSO415.2015德阳工业烟气通常含有二氧化硫,在排放前需经脱硫处理.如图是两种常用脱硫工艺中含硫物质的转化路径部分产物已略.请回答下列问题:1反应Ⅰ的化学方程式是SO2+2NaOH=Na2SO3+H2O .2反应Ⅱ所属的基本反应类型是复分解反应,CaSO3中Ca、S、O元素的质量比是5:4:6 .3已知原料NaOH的价格为元/kg、CaOH2的价格为元/kg.两种工艺中,处理相同质量的SO2,双碱法所需的原料成本更低,其原因是通过反应II实现了NaOH的循环利用,减少了NaOH的用量,所以成本降低.16.陕西工业上用纯碱和石灰石为原料制备烧碱的简要工艺流程如下图所示,请回答;1石灰石、生石灰、熟石灰均能与下列填字母发生化学反应;A.水 B.盐酸 C.二氧化碳2步骤④发生反应的化学方程式是 ;3某研究性学习小组的同学想检验上述工艺中的烧碱溶液里是否含有纯碱,甲同学选择了一种酸溶液,乙同学选择了一种碱溶液,丙同学也选择了一种溶液,该溶液中溶质与甲、乙同学所用溶液中溶质的物质类别不同,他们都能达到检验目的;你认为丙同学所选溶液中的溶质可能是填一种物质的化学式;17.2015株洲镁是一种用途很广的金属,目前世界上60%的镁是从海水主要含NaCl和MgCl2等中提取的.主要步骤如下:1上述步骤中试剂①应过量,理由是使MgCl2完全转化为沉淀.2请写出MgOH2沉淀与试剂②发生中和反应的化学方程式MgOH2+2HCl=MgCl2+2H2O .3无水MgCl2在熔融状态下通电得到金属镁和物质A,氢气在物质A中燃烧生成物质B,则物质A和B的化学式分别为:A Cl2,B HCl .。
工艺流程题(二)

工业碳酸钠母液Na2CO3·H2O趁热过滤工艺流程题(二)6、(2008广东19)碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。
工业碳酸钠(纯度约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺路线如下:已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示:回答下列问题:(1)滤渣的主要成分为。
(2)“趁热过滤”的原因是(3)若在实验室进行“趁热过滤”,可采取的措施是(写出1种)。
(4)若“母液”循环使用,可能出现的问题及其原因是(5)已知:Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g) ΔH1= +532.36 kJ·mol-1Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g) ΔH2= +473.63 kJ·mol-1写出Na2CO3·H2O脱水反应的热化学方程式。
7、(2008广东23)硅单质及其化合物应用范围很广。
请回答下列问题:(1)制备硅半导体材料必须先得到高纯硅。
三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:①写出由纯SiHCl3制备高纯硅的化学反应方程式。
②整个制备过程必须严格控制无水无氧。
SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式;H2还原SiHCl3过程中若混O2,可能引起的后果是。
(2)下列有关硅材料的说法正确的是(填字母)。
A、碳化硅化学性质稳定,可用于生产耐高温水泥B、氮化硅硬度大、熔点高,可用于制作高温陶瓷和轴承C、高纯度二氧化硅可用于制造高性能通讯材料—光导纤维D、普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高E、盐酸可以与硅反应,故采用盐酸为抛光液抛光单晶硅(3)硅酸钠水溶液俗称水玻璃。
取少量硅酸钠溶液于试管中,逐滴加入饱和氯化铵溶液,振荡。
工艺流程高考题

工艺流程高考题工艺流程是指对某种产品的生产过程进行规划、组织和控制的系统性操作方法。
它是工艺技术与生产管理的结合,是将产品从原料采购到最终交付市场的全过程把握的工作。
高考题目如下:题目:某公司的产品生产工艺流程包括原料准备、生产加工、质量检验和包装等环节,请根据以下要求,完成流程图。
1. 原料准备:该公司的产品原料是从供应商那里购买的,需要通过仓库管理和检验才能进入生产加工环节。
2. 生产加工:原料进入生产车间后,分为多个工序进行处理和加工。
其中包括:搅拌、制模、烘干、装配等工序。
每个工序都需要严格控制时间和质量。
3. 质量检验:每个工序完成后,需要进行质量检验。
不合格产品将被退回到上一工序进行修正或报废处理。
4. 包装:经过质量检验合格的产品将进行包装,并按照订单要求进行封装和标识。
要求:1. 画出上述工艺流程的流程图,并准确标注各个环节的名称和顺序。
2. 在流程图中添加两个支线:仓库管理和检验,并标明其与其他环节的调用关系。
参考答案:【答案解析】请参考以下流程图:▼原料准备 ------> 仓库管理 ------> 检验 ------> 生产加工 ------> 质量检验 ------> 包装▲【答案说明】该流程图准确地展示了某公司产品的工艺流程。
1. 原料准备、生产加工和包装是主要的三个环节,顺序依次进行。
原料经过仓库管理和检验后才能进入生产加工环节。
2. 仓库管理和检验是两个支线环节,它们分别与原料准备和生产加工环节相连。
仓库管理确保原料储存和调配的正常进行,检验环节保证原料质量符合要求。
3. 质量检验是在生产加工环节的每个工序完成后进行的,也是一个关键环节,以确保产品质量的稳定。
4. 包装是最后一步,质量检验合格的产品才能被封装和标识,然后送往市场。
【注意事项】在回答此类问题时,应注意以下几点:1. 流程图的画法要清晰明了,必要时可以使用箭头和支线来表示调用关系。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
工艺流程题
1.(安徽)我国制碱工业先驱侯德榜发明了“侯氏制碱法”。
其模拟流程如下:
(1)反应①的化学方程式________________,反应②的基本反应类型为_______。
(2)工业上用分离液态空气的方法制取氢气,属于_______变化(填“物理”或“化学”)。
(3)操作a的名称是_____,实验室进行此操作所需的玻璃仪器有烧杯、玻璃棒、______.
(4)写出NH4Cl的一种用途________________.
(1)CaCO3 =CaO+CO2↑;分解反应。
(2)物理;(3)过滤;漏斗。
(4)做化肥或氮肥等。
2。
(益阳)过氧化钙晶体﹝CaO2·8H2O﹞较稳定,呈白色,微溶于水,广泛应用于环境杀菌、消毒.以贝壳为原料制备CaO2流程如下:
(1)气体X是CO2,其名称是二氧化碳;将过氧化钙晶体与溶液分离的方法是过滤.
(2)反应Y需控制温度在0~5℃,可将反应容器放在冰水混合物中,该反应是化合反应,反应产物是CaO2·8H2O,请写出化学方程式CaO2+H2O2+7H2O=CaO2·8H2O 。
获得的过氧化钙晶体中常含有Ca(OH)2杂质,原因是CaO或Ca(OH)2过量,且Ca(OH)微溶。
2
(3)CaO2的相对分子质量为72 ,过氧化钙晶体﹝CaO2·8H2O﹞中H、O元素的质量比为1∶10 。
(4)为测定制得的过氧化钙晶体中CaO2·8H2O的质量分数,设计的实验如下:称取晶体样品50g,加热到220℃充分反应(方程式为2CaO2·8H2O错误!2CaO+O2↑+16H2O↑,杂质不发生变化),测得生成氧气的质量为 3.2g,请计算样品中CaO2·8H2O的质量分数(CaO2·8H2O相对分子质量为216),写出必要的计算过程。
解:设样品中CaO2·8H2O的质量为x
2CaO2·8H2O错误!2CaO+O2↑+16H2O↑
432 32
x 3.2
∴x=43.2(g)
∴样品中CaO2·8H2O的质量分数为=86。
4%
答:样品中CaO2·8H2O的质量分数为=86.4%
3.(呼和浩特)空气中氮气的含量最多,氮气在高温、高能量条件下可与某些物质发生反应。
下图是以空气和其他必要的原料合成氮肥(NH4NO3)的工业流程。
请按要求回答下列问题:(1)步骤①中发生的是________变化(填“物理”或“化学”).
(2)写出步骤③中发生反应的化学方程式_________________________________。
(3)上述化学反应中属于化合反应的有________个。
硝酸铵应具有的性质是(填字母)。
A.易溶于水 B.有挥发性 C.受热易分解
施用该类肥料时,要避免与碱性物质混合使用,写出硝酸铵与
熟石灰反应的化学方程式__________________________________
高温 1)物理(2) 4NH 3+5O 2=4NO +6H 2O
(3)3
(4)A C 2NH 4NO 3+Ca(OH)2 =Ca(NO 3)2 +2H 2O +2NH 3↑
4。
(宜宾)黄铜是Zn 以主要添加元素的铜合金。
黄铜渣中约含Zn 7%、ZnO 31%、Cu 50%、CuO 5%,其余为杂质.处理黄铜渣可得到硫酸锌,其主要流程如下(杂质不溶于水、不参与反应):
已知:ZnO +H2SO4=ZnSO4+H2O; CuO +H2SO4=CuSO4+H2O
(1) 步骤Ⅰ中产生气体的化学方程式
为 。
(2) 溶液A 中的金属阳离子有 (填化学式)
(3) 步骤Ⅰ、Ⅱ中均包含的操作名称为 ,此操作和步骤Ⅲ中的蒸发操作都要用到的玻璃仪器是 。
(4)溶液
A (填“大于”、“小于”或“等于”)溶液C 的质量.
5. (南昌) 炼铁产生的废渣中含有大量CuS 及少量铁和铁的化合物,工业上以该废渣为原
料生产CuCl 2的流程图如下,下列有关说法错误的是()
A . 操作1中粉碎的目的是增大反应物的接触面积
B . 操作2中,CuS 、NaCl 和O 2在高温条件下反应生产CuCl 2和Na 2SO 4
化学方程式为CuS + 2NaCl +2O 2 ===CuCl 2 + Na 2SO 4
C . 操作3的名称是过滤
D . 流程图中能循环利用的物质是NaCl 和Na 2SO 4
6。
(扬州)醋酸钙[Ca (AC )2]是国家允许使用的补钙制剂之一。
以蛋壳为原料回收膜并制备醋酸钙的一种工艺流程如下.
⑴写出煅烧时的化学方程式。
CO 2的任意排放会引发的环境问题是。
CO 2与CH 4一定条件下化合生成甲醛(HCHO ),则此反应中与最佳质量比是。
下列做法能减少二氧化碳排放的是。
(填序号)
⑵在反应I 中制备石灰乳,而不是制备澄清石灰水的目的是.写出熟石灰的一种用途。
⑶在反应II 中醋酸过量的目的是。
写出反应II 的化学方程式。
⑷膜分离时,盐酸不能过量的主要原因是。
根据煅烧产生的CO 2和蛋壳的主要成分为CaCO 3,可以确定化学方程式.CO 2的任意排放会引发温室效应;根据,计算CO 2与CH 4的质量比是44:16=11:4。
⑵石灰乳中的Ca(OH)2含量比澄清石灰水中多,更利于提高醋酸钙的产量;⑶保证与Ca (OH)2完全反应,提高醋酸钙的含量;⑷加入盐酸就是为了将蛋壳与膜分开,过量的话会与CaCO 3反应,会使制作醋酸钙的原料量减少。
7. (扬州)含锌废渣和各种锌矿(如菱锌矿)都有着重要的用途
I 。
以含锌废渣(主要成分为ZnO,杂质为FeO ﹑CuO )为原料制备七水硫酸锌(ZnSO4·7H2O )的流程如下。
⑴粉碎的目的是。
⑵若实验室用质量分数为98%的硫酸配制200g25%的硫酸,需要的玻璃仪器有胶头滴管﹑玻璃棒﹑和,此处玻璃棒的作用是.
⑶物质X 是,滤渣中含有的金属单质有,除铜时发生的反应属于反应(填基本反应类型)
⑷流程中获得七水硫酸锌前省略的操作是﹑冷却结晶﹑洗涤和低温烘干。
⑸某温度下,Fe(OH)3分解得到一种铁﹑氧质量比21:8的氧化物,该氧化物的化学式。
⑹除铁过程中,温度pH对除铁效果的影响分别对如图所示。
由图可知,除铁时温度应控制在℃为宜,pH应控制在为宜。
II.以某菱锌矿(ZnCO3含量为62。
5%)为原料制备锌的原理如下(假设杂质不参加反应):则100吨这样的菱锌矿理论上最多制得锌多少吨?(写出计算过程)
⑴固体的表面积越大,化学反应速率越快.含锌废渣粉碎的目的是增大接触面积,加快反应速率,充分反应。
⑵浓硫酸稀释过程中需用用到:量筒、滴管、细口瓶、玻璃棒和烧杯,通过比较可知,还缺少烧杯和量筒.此处玻璃棒的作用是搅拌,将热量及时地扩散。
⑶加入过量的X,目的是除去铜,本小题实质是物质的除杂,既要除去杂质又要避免引入新的杂质,考虑到金属活动性顺序,故X可以是锌,滤渣含有锌和置换的铜,这个反应过程是置换反应。
⑷这是分离可溶性固体和液体的方法:先将热的饱和溶液冷却,晶体就会析出,将此有晶体析出的饱和溶液,过滤,用少量的水洗涤,再低温烘干。
所以操作的步骤是:加热浓缩,冷却结晶,过滤,洗涤和低温烘干
⑸Fe(OH)3分解得到一种铁﹑氧质量比21:8的氧化物,铁的氧化物有三种,Fe2O3,FeO,Fe3O4。
比较铁氧的质量比21:8只有Fe3O4符合题意。
⑹关键看懂两张图的X轴和Y轴代表的含义,为了除铁效果最佳,我们需要找出最高除铁率对应的温度和pH。
II。
题目要求求出理论上最多制得锌多少吨
故设理论上最多制得锌的质量为X,
根据题意可知ZnCO3的质量是=100t×62。
5%=62.5t
由两个方程式可知道
ZnCO3 ~ Zn
125 65
62.5t X x=32.5t
8. (雅安)绿矾又名七水硫酸亚铁(FeSO4·7H2O),其用途广泛,可用于制铁盐、氧化铁颜料、净水剂、防腐剂、消毒剂等。
绿矾(FeSO4·7H2O)的一种综合利用工艺如下:(1)细铁丝在氧气中可以燃烧,请写出铁在氧气中燃烧的化学方程式。
(2)绿矾与NH4HCO3在溶液中反应,有CO2生成,反应的化学方程式为。
(3) 隔绝空气进行“焙烧”,铁元素的转化途径是,实际作还原剂的是CO。
写出“焙烧”过程中各步反应的化学方程式:
A.;
B。
____________________________________________;
C.____________________________________________.。
