溶解度曲线专项训练(精练版)
2024年中考化学专题强化训练溶解度曲线
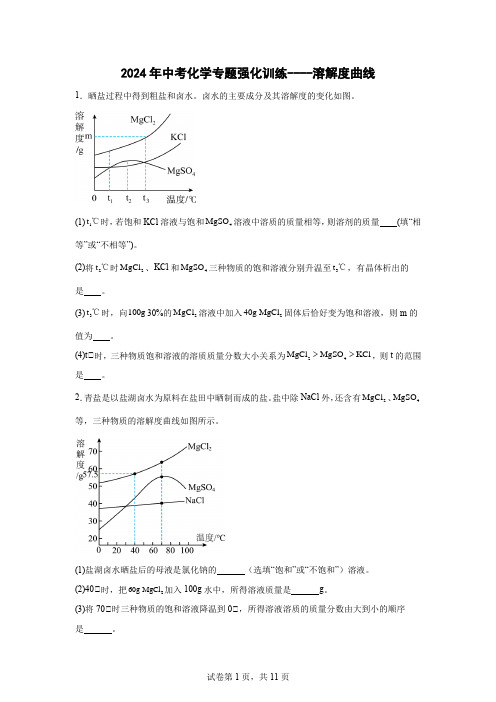
2024年中考化学专题强化训练----溶解度曲线1.晒盐过程中得到粗盐和卤水。
卤水的主要成分及其溶解度的变化如图。
(1)1t ℃时,若饱和KCl 溶液与饱和4MgSO 溶液中溶质的质量相等,则溶剂的质量 (填“相等”或“不相等”)。
(2)将2t ℃时2MgCl 、KCl 和4MgSO 三种物质的饱和溶液分别升温至3t ℃,有晶体析出的是 。
(3)3t ℃时,向100g 30%的2MgCl 溶液中加入240g MgCl 固体后恰好变为饱和溶液,则m 的值为 。
(4)t℃时,三种物质饱和溶液的溶质质量分数大小关系为24MgCl MgSO KCl >>,则t 的范围是 。
2.青盐是以盐湖卤水为原料在盐田中晒制而成的盐。
盐中除NaCl 外,还含有2MgCl 、4MgSO 等,三种物质的溶解度曲线如图所示。
(1)盐湖卤水晒盐后的母液是氯化钠的 (选填“饱和”或“不饱和”)溶液。
(2)40℃时,把260g MgCl 加入100g 水中,所得溶液质量是 g 。
(3)将70℃时三种物质的饱和溶液降温到0℃,所得溶液溶质的质量分数由大到小的顺序是 。
(4)氯化钠中含有少量硫酸镁,若要提纯氯化钠,可采用的方法是。
3.某同学进行了如图1所示实验,结合硝酸钾和氯化钠的溶解度曲线回答下列问题。
(1)20℃时,氯化钠的溶解度是g;(2)若氯化钠中混有少量硝酸钾,可采用的方法提纯氯化钠;(3)图1中烧杯℃为硝酸钾的(填“饱和”或“不饱和”)溶液;若通过升高温度使℃中固体继续溶解,则其溶液中溶质的质量分数(填“增大”“减小”或“不变”)。
4.如图是A、B、C三种固体物质的溶解度曲线,据图作答:(1)P点的意义是。
(2)A、B、C三种物质中,溶解度随着温度上升而减小的物质是。
(3)t2℃时,将30g A物质加入50g水中可形成g溶液。
5.如图是某苏打气泡水的标签。
(1)该气泡水中溶剂的化学式是。
C H O。
从赤藓糖醇的化学式中能获得与其有关的(2)赤藓糖醇是一种甜味剂,其化学式为4104信息是(任写一条)。
溶解度曲线专项练习

溶解度曲线专项练习1.(2014•昆明)如图是甲、乙两种固体物质的溶解度曲线。
下列说法不正确的是()A.10℃时,甲和乙的溶解度相等B.甲的溶解度受温度影响比乙大C.20℃时,将25g甲加入50g水中,可形成75g溶液D.将30℃时甲的饱和溶液降温至10℃,有晶体析出2.(2015•昆明)某固体物质的溶解度曲线如图所示。
下列说法不正确的是()A.40℃和85℃时,该物质的溶解度均为40gB.该物质在60℃时的溶解度比40℃时的溶解度大C.40℃时该物质饱和溶液中溶质的质量分数为40%D.将85℃时该物质的饱和溶液降温至60℃,此过程中不会析出晶体3.(2016•昆明)甲物质的溶解度(S)随温度(t)变化曲线如图所示,下列说法正确的是()A.20℃时,甲易溶于水B.60℃时,甲的溶解度约为0.6C.将80℃时甲的溶液降温至40℃,一定析出甲晶体D.90℃时,在50g水中加入0.7g甲,充分搅拌后得到饱和溶液4.(2017•昆明)如图是甲、乙两物质的溶解度曲线,下列说法正确的是()A.t2℃时,甲的溶解度为50B.甲、乙的溶解度都随温度的升高而增大C.将甲溶液从t2℃降温至t1℃,一定有晶体析出D.t1℃时,甲、乙两种饱和溶液的溶质质量分数相等5.如图是甲、乙两物质的溶解度曲线,下列说法正确的是()A.甲的溶解度大于乙的溶解度B.t2℃时,把30g甲溶解到50g水中,得到80g的饱和溶液C.分别将t2℃时甲、乙的饱和溶液降温到t1℃,溶质质量分数相等D.t1℃时,甲、乙两物质的溶解度相等6.右图为A、B、C三种物质的溶解度曲线,请据图判断下列叙述中不正确...的是()A.t1℃时,B物质的溶解度为40gB.t2℃时,三种物质的溶解度由大到小的顺序为:A﹥B﹥CC.要将C的不饱和溶液转化为饱和溶液可以采取降温的方法D.要使A从其浓溶液中析出,可采用冷却热饱和溶液法7.甲、乙两种物质的溶解度曲线如右图所示,下列说法中正确的是( )A.30 ℃时,50 g水可以溶解25 g甲物质B.升温能使甲物质的不饱和溶液变为饱和溶液C.20 ℃时,甲、乙两种物质的溶解度相同D.30 ℃时,乙物质的溶解度比甲物质的溶解度大8.右图是KNO3和NaCl的溶解度曲线。
中考化学《溶解度及溶解度曲线》专项练习题(附答案解析)

中考化学《溶解度及溶解度曲线》专项练习题(附答案解析)1. 甲、乙、丙三种固体物质的溶解度曲线如右图所示。
下列说法不正确的是()A. T2℃时,取等质量的甲、乙分别配制成饱和溶液,所需水的质量:甲>乙B. T2℃时,将甲、乙的饱和溶液均降温到T1℃,得到的溶液仍饱和C.若甲中混有少量的丙,可采用降温结晶的方法提纯甲D. T2℃时,甲、乙各30g分别加入100g水中,均形成饱和溶液2. 下图是甲、乙两种固体物质的溶解度曲线。
下列说法中错误的是( )A. 20℃时,甲、乙饱和溶液中溶质质量分数相等B. 40℃时,甲的溶解度大于乙的溶解度C. 40℃时,乙的饱和溶液中溶质的质量分数为40%D. 将40℃甲的饱和溶液降温到20℃,会有晶体析出3. KNO3与KCl的溶解度曲线如右图所示。
下列说法正确的是( )A. KNO3的溶解度比KCl的溶解度大B. t1温度下的KCl的饱和溶液升温至t2,有晶体析出C. A点所表示的KCl饱和溶液溶质的质量分数为29%D. 冷却热的KNO3饱和溶液可获得KNO3晶体4. ZnSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示。
下列说法正确的是( )A. N点对应的ZnSO4溶液升温或降温均都可能析出晶体B. M点对应的ZnSO4溶液是不饱和溶液C. ZnSO4饱和溶液的溶质质量分数随温度升高而增大D. 40℃时,ZnSO4的溶解度为41g5. 下图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )A. 甲的溶解度大于乙的溶解度B. 降温可使接近饱和的丙溶液变为饱和溶液C. 将t2°C甲、乙、丙的饱和溶液降温至t1℃,所得溶液的溶质质量分数℃乙>甲=丙D. P点表示t1℃时甲、丙两种物质的溶解度都是25g6. 下图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )A. 乙中含有少量甲,可用冷却热饱和溶液的方法提纯甲B. t3℃时,甲的溶液溶质质量分数一定大于乙的溶液溶质质量分数C. t3℃时,将等质量的甲、乙两种物质的饱和溶液分别降温至t2℃,析出晶体的质量甲一定大于乙D. t1℃时,乙的不饱和溶液只有通过蒸发溶剂的方法才能转变成饱和溶液7.甲、乙、丙三种固体物质的溶解度曲线如图所示。
初三化学溶解度曲线习题(含答案)

实用文档一、单选题(本大题共16小题,共32.0分)1.对“10%的食盐溶液”的含义解释错误的是()A. 100g食盐溶液中溶解了10g食盐B. 100g水中溶解了10g食盐C. 将10g氯化钠溶解在90g水中所得的溶液D. 将食盐和水按1:9的质量比配成的溶液2.下列洗涤或去污过程利用乳化原理的是()A. 用洗洁精洗去餐具上的油污B. 用刷子刷去杯子上的油污C. 用酒精除去衣服上的碘D. 用汽油除去衣服上的油污3.下列物质放入水中,能形成溶液的是()A. 面粉B. 冰块C. 花生油D. 蔗糖4.在蒸馏水中加入NaOH颗粒,不断搅拌,用温度传感器记录溶解过程的温度变化如图a、c两点观察到溶液中有固体存在,b点固体完全消失。
下列说法不正确的是()A. NaOH固体溶于水是放热过程B. a、c两点时,NaOH的溶解度相同C. b点时,该溶液一定是不饱和溶液D. c点时的溶剂质量等于a点时的溶剂质量5.如图,在分别盛有100g水的烧杯中放入KNO3充分溶解,则说法正确的是()A. 甲、乙混合后为t1℃的不饱和溶液B. 乙升温至t2℃,溶液质量增加C. 乙、丙溶液中溶质质量相等D. 丙降温至t1℃,有晶体析出6.曼曼用盛有150g水的烧杯进行如图操作,得到相应的溶液①~③。
下列说法正确的是()A. 固体W的溶解度曲线是图乙中的bB. ①~③溶液中,只有②是饱和溶液C. ①~③溶液中,溶质质量分数的大小关系是③>②>①D. 若将②升温至t2℃,固体不能全部溶解7.要将一瓶接近饱和的石灰水变成饱和溶液,小明选择了如下方法。
其中可行的是()①加入CaO ②加入Ca(OH)2 ③升高温度④降低温度。
A. ②③B. ②④C. ①②③D. ①②④8.下列关于硝酸钾的溶解度的说法,正确的是()A. 20℃时,20g硝酸钾溶解在100g水里,所以20℃时硝酸钾的溶解度是20gB. 20℃时,20g硝酸钾溶解在水里制成饱和溶液,所以20℃时硝酸钾的溶解度是20gC. 把31.6g硝酸钾溶解在100g水里,形成饱和溶液,所以20℃时硝酸钾的溶解度是31.6gD. 20℃时,31.6g硝酸钾溶解在100g水里,形成饱和溶液,所以20℃时硝酸钾的溶解度是31.6g9.如图所示,甲、乙试管中分别盛有硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体。
溶解度曲线 专题训练Microsoft Word 文档

溶解度曲线专题训练1.如图是A 、B 、C 三种物质的溶解度曲线,回答问题: ⑴t 1℃时A 、B 、C 的溶解度大小关系是 。
⑵t 2℃时A 、B 、C 的饱和溶液的溶质质量分数大小关系是 。
⑶将t 2℃时等质量的A 、B 、C 的饱和溶液降温到t 1℃时,析出晶体最多的是 ,无晶体析出的是 ,此时所得到溶液中溶质质量分数的大小关系是 。
⑷在t 1℃时将接近饱和的A 的溶液变饱和可采用的方法是 。
⑸t 2℃时将25gA 投入到50g 水中充分溶解后,形成溶液的质量是 g ,其溶质的质量分数为 。
⑹当A 中混有少量B 时,提纯A 一般用 ;当B 中混有少量A 时,提纯B 一般用 。
分离A 和B 的混合物一般用_____________________。
(7)t 2℃时, (能、不能)配制出溶质质量分数为30%的A 溶液。
(8)t 2℃时,溶解10gA 物质至少需要 g 水。
2、右图是a 、b 、c 三种物质的溶解度曲线,a 与c 的溶解度曲线相交于P 点。
据图回答:(1)P 点的含义 。
(2)写出溶解度变化趋势和C 相似的两种不同状态的物质的化学式 。
(3)t 1℃时15g c 物质加入到50g 水中不断搅拌,形成溶液后还有 g 没溶解,若要继续溶解完,可以 。
(4)将t 1℃时a 、b 、c 三种物质饱和溶液的温度升高到t 2℃时,三种 溶液的溶质质量分数大小关系是` 。
(5)t 2℃时用等质量的a 、b 、c 三种物质配饱和溶液,所得饱和溶液质量由大到小的顺序是: 。
(6)当温度 时,a 物质饱和溶液溶质质量分数大于b 物质饱和溶液溶质质量分数3、下图是a 、b 两种固体物质的溶解度曲线。
⑴图中a 物质的溶解度曲线比b 物质的陡,说明:; ⑵若要想在200g 水中溶解更多的a 物质,可采取的措施是:⑶当温度 时,a 、b 两物质饱和溶液溶质质量分数相同。
(4)40℃时,将20g a 物质放入50g 水中,充分搅拌,所得溶液的溶质质量分数是 。
溶解度曲线练习题

溶解度曲线练习题1.(安徽)甲、乙两种物质的溶解度曲线如右图所示。
下列说法正确的是( )A. 甲的溶解度大于乙的溶解度B. 两种物质的溶解度都随温度升高而增大C. t1℃时, 甲、乙两种物质的溶液中, 溶质质量分大于bC.图乙中a、b溶液一定是不饱和溶...D.30℃时a、b溶液溶质质量分数不相等数相等D. t1℃时, 甲饱和溶液溶质质量分数为50%2.(呼和浩特)20℃时,将等质量的a、b两种固体,分别加入到盛有lO0g水的烧杯中,充分搅拌后现象如图甲,升温到50℃时,现象如图乙,a、b两种固体的溶解度曲线如图丙。
下列说法正确的是,..)A.图丙中M表示b的溶解度曲线B.图甲溶液中溶质的质量分数a3.(苏州)实验室配制50g溶质质量分数为15%的氯化钠溶液。
下列说法中错误的是... )A.实验的步骤为计算、称取、量取、溶解、转移B.溶解过程中玻璃棒的作用是搅拌, 以加快氯化钠的溶解速率C.把配制好的氯化钠溶液倒入刚用蒸馏水润洗过的试剂瓶中, 并贴上标签D.量取水时, 用规格为50mL的量筒量取42.5mL蒸馏水4.(苏州)A.B.C三种物质的溶解度曲线如图5所示。
下列分析正确的是...)A.t1℃时, A.C两种物质的饱和溶液中溶质的质量相等B.t2℃时, 把50gA放入50g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1∶3C.将t2℃时, A.B.C三种物质的饱和溶液降温至t1℃, 所得溶液的溶质质量分数的大小关系是B>C=AD.将C的饱和溶液变为不饱和溶液, 可采用升温的方法5.(重庆B卷.下图是甲、乙两种固体物质在水中的溶解度曲线。
下列说法不正确的是. )A.10 ℃时, 甲、乙两种物质的饱和溶液浓度相同B.保持20 ℃, 蒸发溶剂可使接近饱和的乙溶液变成饱和溶液C.30 ℃时, 将40g 甲物质加人50g水中, 充分溶解后溶液的质量为80gD 、10 ℃时, 将两种饱和溶液升温至30 ℃, 溶液中溶质的质量分数都增大6.(宜宾)右图为甲、乙两种盐的溶解度曲线。
(完整)初中化学考溶解度曲线练习及答案.doc

云南学诚教育初三化学专题练习专题五溶解度曲线1.a 、 b 两种物质的溶解度曲线如图所示。
下列说法不正确的是A. 将 t 1℃时 b 的饱和溶液加水可变为不饱和溶液B. 将 t 2℃时 a 的饱和溶液降温至t 1℃,溶液质量不变C.t 2℃时,两种物质的饱和溶液中溶质质量分数a> bD. 将 t 2℃时 a、 b 的饱和溶液分别降温至t 1℃,两溶液的溶质质量分数相等2.下图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是A.t 2℃时,甲、乙两种物质的溶解度相等B. 甲的溶解度随温度的升高而增大C.分别将 t 3℃时甲、乙、丙的饱和溶液降温至t 1℃,则所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙D.t 1℃时,丙的饱和溶液中溶质的质量分数为40%3. 下图是甲、乙、丙三种固体物质的溶解度曲线,将甲、乙、丙三种物质t 2℃时的饱和溶液降温至 t 1℃,所得溶液的溶质质量分数关系正确的是A. 甲>乙>丙B.甲=乙=丙C. 甲 =乙>丙D.丙>甲=乙4.(多选)甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是A.t 1℃时,甲物质的溶解度为20gB.t 1℃时, 30g 甲加入到 50g 水中最多可得70g 溶液C.t 2℃时,乙物质的饱和溶液升温变成不饱和溶液D.t 2℃时,甲乙两物质的饱和溶液分别降温到t 1℃时,所得溶液溶质质量分数的大小关系是:甲<乙5.(多选)甲、乙两种固体物质的溶解度曲线如图所示。
20℃时,进行了如下图所示的实验,下列叙述正确的是A.甲的溶解度大于乙的溶解度B.实验过程中,属于不饱和溶液的是A 溶液和 C 溶液C.实验过程中,只有 B 溶液和 D 溶液属于饱和溶液D.实验过程中, B 溶液与 E 溶液中溶质的质量分数相同6.(多选)甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是A.t 2℃时将 50g 甲物质放入 50g 水中,充分搅拌后得到 100g 甲溶液B.t2℃时配制等质量的三种物质的饱和溶液,甲所需要的水最少C.分别将 t 2℃时三种物质的饱和溶液降温到t 1℃,所得溶液中溶质的质量分数的大小关系是乙>甲>丙D.分别将 t 2℃时三种物质的饱和溶液降温到t 1℃,甲溶液中析出的晶体最多丙溶液中无晶体析出7.甲、乙、丙三种物质的溶解度曲线如下图所示。
溶解度曲线专题练习
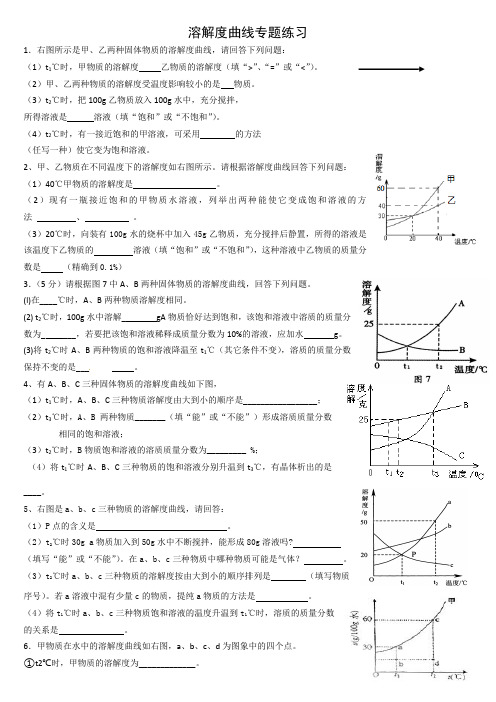
溶解度曲线专题练习1.右图所示是甲、乙两种固体物质的溶解度曲线,请回答下列问题:(1)t1℃时,甲物质的溶解度乙物质的溶解度(填“>”、“=”或“<”)。
(2)甲、乙两种物质的溶解度受温度影响较小的是物质。
(3)t2℃时,把100g乙物质放入100g水中,充分搅拌,所得溶液是溶液(填“饱和”或“不饱和”)。
(4)t2℃时,有一接近饱和的甲溶液,可采用的方法(任写一种)使它变为饱和溶液。
2、甲、乙物质在不同温度下的溶解度如右图所示。
请根据溶解度曲线回答下列问题:(1)40℃甲物质的溶解度是。
(2)现有一瓶接近饱和的甲物质水溶液,列举出两种能使它变成饱和溶液的方法、。
(3)20℃时,向装有100g水的烧杯中加入45g乙物质,充分搅拌后静置,所得的溶液是该温度下乙物质的溶液(填“饱和”或“不饱和”),这种溶液中乙物质的质量分数是(精确到0.1%)3.(5分)请根据图7中A、B两种固体物质的溶解度曲线,回答下列问题。
(l)在____℃时,A、B两种物质溶解度相同。
(2) t2℃时,100g水中溶解_ gA物质恰好达到饱和,该饱和溶液中溶质的质量分数为_ ___,若要把该饱和溶液稀释成质量分数为10%的溶液,应加水g。
(3)将t2℃时A、B两种物质的饱和溶液降温至t1℃(其它条件不变),溶质的质量分数保持不变的是____ 。
4、有A、B、C三种固体物质的溶解度曲线如下图,(1)t1℃时,A、B、C三种物质溶解度由大到小的顺序是_________________;(2)t3℃时,A、B两种物质_______(填“能”或“不能”)形成溶质质量分数相同的饱和溶液;(3)t2℃时,B物质饱和溶液的溶质质量分数为_________ %;(4)将t1℃时A、B、C三种物质的饱和溶液分别升温到t3℃,有晶体析出的是____。
5、右图是a、b、c三种物质的溶解度曲线,请回答:(1)P点的含义是。
(2)t2℃时30g a物质加入到50g水中不断搅拌,能形成80g溶液吗?(填写“能”或“不能”)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
溶解度曲线专项训练(必考,2~7分)(限时:45分钟分值:39分)考向1 一条曲线1.(2017泸州)溴酸银(AgBrO3)的溶解度随温度变化曲线如图所示,下列说法不正确的是( )第1题图A. 升高温度溴酸银的溶解度增大B. 40 ℃时溴酸银易溶于水C. 90 ℃时溴酸银溶液的溶质质量分数一定小于%D. 溴酸银可用降温结晶的方法从溶液中析出2. (2017北京改编)依据实验和溶解度曲线回答。
25 ℃时,向下列4只盛有100 g水的烧杯中,分别加入不同质量的KCl固体,充分溶解。
第2题图(1)①中溶液的质量为________g。
(2)上述溶液为饱和溶液的是________(填序号)。
(3)能将不饱和KCl溶液变为饱和KCl溶液的方法是________。
A. 升高温度B. 加水C. 加KCl固体D. 倒出部分溶液(4)④中溶液的溶质质量分数约为________。
考向2 两条曲线3.(2017连云港)如图是甲、乙固体的溶解度曲线。
下列说法正确的是( )第3题图A. 图中P点所表示的溶液是t3℃时甲的饱和溶液B. 可用t1℃时20%的甲溶液配制10%的甲溶液C. 若甲中含有少量乙,可采用冷却热饱和溶液的方法提纯甲D. 分别将t3℃等质量的甲、乙饱和溶液降温至t2℃,所得溶液中溶质质量相等4. (2017重庆A改编)两个烧杯中分别盛装X、Y的饱和溶液,两支试管中分别装有NaOH和NH4NO3固体,向两支试管中分别滴加适量水,现象如图一所示,结合图二判断下列说法正确的是( )第4题图A. Y的溶解度曲线为a曲线B. 降温可使X的饱和溶液变浑浊C. X的饱和溶液从t2℃降温到t1℃,溶质的质量分数变大D. t3℃时,若X、Y的饱和溶液质量相等,则溶剂质量X____Y(填“>”、“<”或“=”)5. (2017兰州)甲、乙两种固体物质的溶解度曲线如图所示,请回答问题:(1)t1℃时,甲、乙两种物质的溶解度大小关系为甲________乙(填“<”、“>”或“=”)。
(2)P点的含义________________________。
(3)t2℃时,把20 g固体甲放入50 g水中,充分搅拌,所得溶液的质量是________g。
第5题图(4)欲将t2℃时乙物质的不饱和溶液变为该温度下的饱和溶液,可采取的一种方法是________________________________________________________________________。
(5)如果甲物质中含有少量乙物质,若要提纯甲,一般采用____________的方法。
6. (2017绥化)图1为甲、乙两种物质(均不含结晶水)的溶解度曲线图。
请回答下列问题。
图1图2第6题图(1)在10 ℃时,甲的溶解度________乙的溶解度。
(选填“>”、“<”或“=”)(2)在20 ℃时,向盛有50 g水的烧杯中加入25 g甲物质,充分搅拌后溶液质量是________g。
(3)取乙进行如图2实验,属于饱和溶液的是______,溶质质量分数最大的是________。
(选填字母序号)7. (2017安顺)(1)以下是有关CO2气体溶解度的几组数据:CO2在水中的溶解度(单位:mL)请根据数据分析:①根据CO2在水中的溶解度表,叙述外界条件是如何影响气体溶解度的____________________________、__________________________;②打开可乐瓶有气体溢出,说明原瓶中的压强________(填:“小于”、“等于”或“大于”)瓶外大气压强。
(2)如图是无结晶水合物的固体甲和乙在水中的溶解度曲线,请根据该曲线图回答下列问题:第7题图① 20 ℃时,150 g水中溶解________g甲物质恰好形成饱和溶液;②现有60 ℃的乙的饱和溶液,与该溶液有关的量有:A.水的质量B. 溶液中溶质的质量C. 溶液的质量D. 乙的质量分数E. 60 ℃时乙的溶解度保持温度不变,将该饱和溶液稀释,不变的量是________(填序号,下同);如果将该饱和溶液降温至20 ℃,不变的量是________。
考向3 三条曲线8. (2017江西样卷三)甲、乙、丙三种固体物质的溶解度曲线如图所示。
据图判断,下列说法正确的是( )第8题图A. 甲、乙、丙三种固体物质的溶解度随温度升高而增大B. t1℃时,把甲、乙、丙三种物质的饱和溶液升温到80 ℃,溶质质量分数大小为:乙>甲>丙C. 若乙物质中混有少量的甲,应采取降温结晶的方法提纯乙D. t2℃时,把15 g乙物质加到50 g水中,充分搅拌后所得溶液的质量是________g第9题图9. (2017黔东南州)A、B、C三种固体物质的溶解度曲线如图所示。
据图回答问题:(1)温度为______℃时,A与C物质的溶解度相等。
(2)t2℃时,把A、B物质各30 g分别加到50 g水中,不能形成饱和溶液的是________(填字母代号)。
(3)t2℃时,将等质量A、B、C三种物质的饱和溶液降温至t1℃。
所得的三种溶液中,溶剂质量的大小关系是________________(用字母代号和“>”、“<”或“=”填写)。
10. (2017贺州节选)如图1是A、B、C三种物质的溶解度曲线图。
请回答:第10题图1 第10题图2①t1℃时,溶解度相等的两种物质是________。
②B的饱和溶液中混有少量的物质A,要除去A得到较纯的B物质,可采用的结晶方法是________________________。
③如图2所示,在大烧杯中加入一定量的硝酸铵固体后,甲试管内出现的现象是_____________________,乙试管内的溶液为________溶液(填“饱和”或“不饱和”)。
11. (2017十堰)如图所示是KNO3、NaCl、Ca(OH)2三种物质的溶解度曲线,完成下列问题。
第11题图(1)P点的含义是____________________。
(2)当氯化钠溶液中混有少量的硝酸钾时,提纯的方法是________________。
(3)若满足Q点指标的Ca(OH)2溶液中加入少量生石灰,则溶液中的溶质质量将________(填“增加”、“减少”或“不变”)。
(4)下列说法正确的是________(填序号)。
①10 ℃时,这三种物质的溶液中,溶质的质量分数由大到小的顺序为NaCl>KNO3>Ca(OH)2② 20 ℃时,KNO3和NaCl两种物质的饱和溶液中溶质的质量一定相等③30 ℃时,将等质量的KNO3和NaCl两种物质分别配成饱和溶液,所得溶液质量NaCl>KNO3答案1. B 【解析】2. (1)110 (2)④(3)C (4)26%3.C 【解析】P点位于甲的溶解度曲线下方,是甲t3℃的不饱和溶液,A错误;t1℃时甲的溶解度为20 g,其饱和溶液溶质质量分数最大为20 g120 g×100%≈%,所以该温度下不可能有20%的甲溶液,B错误;甲的溶解度受温度影响较大,乙的溶解度受温度影响较小,提纯甲可用冷却热饱和溶液的方法,C正确;t3℃等质量的甲、乙饱和溶液降温到t2℃,甲析出晶体多,所以所得溶液中溶质质量甲<乙,D错误。
4. A >【解析】氢氧化钠固体溶于水放热,温度升高,X的饱和溶液变浑浊,说明X的溶解度随温度升高而减小,随温度降低而增大;硝酸铵固体溶于水吸热,温度降低,Y的饱和溶液变浑浊,说明Y的溶解度随温度升高而增大,随温度降低而减小。
据此可知:X的溶解度曲线为b曲线,Y的溶解度曲线为a曲线,A正确;X的溶解度随温度升高而减小,升温可使X的饱和溶液变浑浊,B错误;根据b曲线可知,X的饱和溶液从t2℃降温到t1℃,没有晶体析出,则溶质质量分数不变,C错误;t3℃时,X的溶解度小于Y的溶解度,此时X、Y的等质量饱和溶液中,溶质质量关系为X<Y,则溶剂质量关系为X>Y。
5. (1)< (2)t3℃时,甲、乙两种物质的溶解度相等(3)(4)增加溶质(或蒸发溶剂) (5)降温结晶(或冷却热饱和溶液)【解析】(1)从图像可以看出在t1℃时,甲的溶解度小于乙的溶解度。
(2)两条溶解度曲线的交点,表示该温度下这两种物质的溶解度相等。
(3)在t2℃时甲的溶解度为25 g,即100 g 水中最多溶解25 g甲,则该温度下50 g水中最多溶解 g甲,故所得溶液质量为 g。
(4)将t2℃时乙物质的不饱和溶液变为该温度下的饱和溶液,可选择增加溶质、蒸发溶剂等方法。
(5)甲的溶解度受温度变化影响比较大,乙的溶解度受温度变化影响不大,则提纯甲物质可采用降温结晶或冷却热饱和溶液的方法。
6. (1)>(2)70 (3)AC B【解析】(1)在10 ℃时,甲的溶解度大于乙的溶解度。
(2)根据溶解度的意义可知,50 g 水中最多溶解20 g甲,故加入25 g甲完全溶解形成70 g溶液。
(3)10 ℃时,乙的溶解度为20 g,因此图2中A烧杯内形成的是该温度下的饱和溶液,升温至30 ℃时再加入30 g乙物质,30 ℃时乙的溶解度为60 g,因此B烧杯内溶液是不饱和溶液,降温到20 ℃时析出晶体,故C烧杯溶液为饱和溶液,比较三个烧杯内溶解溶质质量发现,B烧杯溶解得最多,故其溶质质量分数最大。
7.(1)①相同温度下,压强越大气体物质溶解度越大相同压强下,温度越高气体物质溶解度越小②大于(2)①45②BE AE【解析】(1)比较同一压强,不同温度下二氧化碳的溶解度可知,气体的溶解度随温度升高而减小,比较同一温度,不同压强下二氧化碳的溶解度可知,气体的溶解度随压强增大而增大;可乐中溶解有较多的二氧化碳,将可乐瓶的瓶盖打开有气体溢出,说明二氧化碳的溶解度减小了,而该过程中温度不变,由此可推断,打开瓶盖后,瓶内压强变小了,即原瓶中的压强较瓶外压强大。
(2)20 ℃时甲的溶解度为30 g,所以该温度下150 g水中溶解45 g甲时恰好形成饱和溶液;温度不变,60 ℃时乙的饱和溶液,稀释该溶液时,溶液中溶质的质量不变,60 ℃时乙的溶解度不变,水的质量增加,溶液的质量增加,乙的质量分数变小;将饱和溶液降温至20 ℃时,有晶体析出,所以该过程中水的质量不变,60 ℃时乙的溶解度不变,溶液中溶质的质量减小,溶液的质量减小,乙的质量分数减小。
8. B【解析】根据溶解度曲线图可知,甲、乙的溶解度随温度升高而增大,丙的溶解度随温度升高而减小,A错误;t1℃时,甲、乙、丙三种物质的溶解度关系为乙>甲=丙,该温度时三种物质饱和溶液溶质质量分数大小关系为乙>甲=丙,升温至80 ℃,只有丙析出晶体,溶质质量分数减小,甲、乙没有析出晶体,溶质质量分数不变,此时所得溶液的溶质质量分数大小关系为乙>甲>丙,B正确;甲、乙的溶解度均随温度升高而增大,且甲的溶解度受温度影响较大,不可用降温结晶的方法提纯乙,C错误;t2℃时,乙的溶解度是25 g,此时将15 g乙加到50 g水中,只能溶解 g,所得溶液的质量为 g+50 g= g。
