氨基酸分析仪实验指导
化合物与酶结合位点实验氨基酸点突变实验方案-概述说明以及解释

化合物与酶结合位点实验氨基酸点突变实验方案-概述说明以及解释1.引言1.1 概述概述部分的内容:在生物学研究中,化合物与酶结合位点的研究是一个重要的领域。
酶是生物体内极其重要的蛋白质分子,其参与了无数个生物反应的催化过程。
而化合物与酶结合位点的相互作用在酶催化反应中起着至关重要的作用。
化合物与酶结合位点是指一种物质与酶表面的特定区域结合形成的结构。
通过结合位点,化合物能够与酶发生特异性的相互作用,从而影响酶的活性。
这种相互作用可以是氢键、离子键或范德华力等各种非共价力。
研究化合物与酶结合位点的重要性在于,它可以揭示酶的催化机制以及生物反应的调控机理。
通过了解化合物和酶结合位点的相互作用,我们可以探索酶的催化过程中的关键步骤,并进一步理解生物体内各种生物化学反应的发生原理。
此外,研究化合物与酶结合位点还可以为药物研发提供重要的信息。
许多药物的作用机制就是通过与酶的结合位点相互作用,从而达到治疗疾病的目的。
本文的目的是通过氨基酸点突变实验来探究化合物与酶结合位点的相互作用。
氨基酸点突变实验是一种常用的实验手段,通过改变酶结合位点上的特定氨基酸残基,来研究其对结合位点的影响。
通过这种实验,我们可以了解到哪些氨基酸在结合位点中起到重要作用,并进一步明确酶催化反应中的关键步骤。
接下来的正文将详细介绍化合物与酶结合位点的重要性以及氨基酸点突变实验的原理,并设计相应的实验方案和步骤。
最后,结论部分将对实验结果进行分析,并对化合物与酶结合位点的认识和启示进行阐述,同时展望未来进一步研究的方向。
1.2文章结构1.2 文章结构本文主要分为引言、正文和结论三个部分来探讨化合物与酶结合位点实验和氨基酸点突变实验的方案。
在引言部分,首先会进行概述,介绍化合物与酶结合位点的重要性以及氨基酸点突变实验的原理。
接着,会详细阐述本文的结构,并列出各个部分的内容和意义。
最后,明确本文的目的,即为研究化合物与酶结合位点实验中氨基酸点突变的实验方案。
生化实验指导
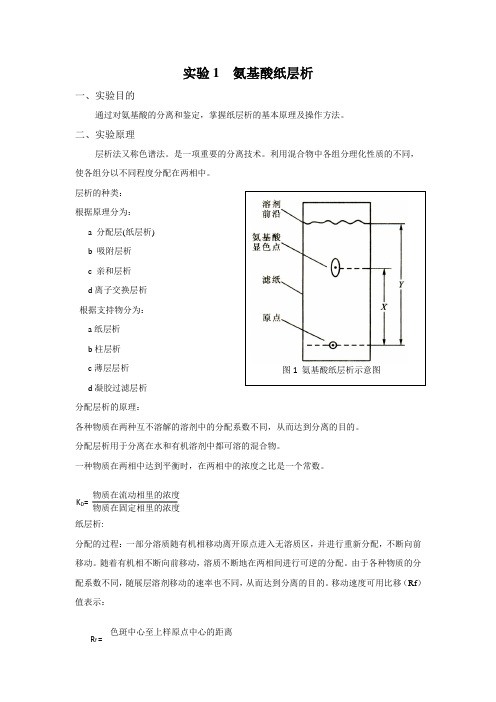
实验1 氨基酸纸层析一、实验目的通过对氨基酸的分离和鉴定,掌握纸层析的基本原理及操作方法。
二、实验原理层析法又称色谱法。
是一项重要的分离技术。
利用混合物中各组分理化性质的不同,使各组分以不同程度分配在两相中。
层析的种类: 根据原理分为: a 分配层(纸层析) b 吸附层析 c 亲和层析 d 离子交换层析 根据支持物分为: a 纸层析 b 柱层析 c 薄层层析 d 凝胶过滤层析 分配层析的原理:各种物质在两种互不溶解的溶剂中的分配系数不同,从而达到分离的目的。
分配层析用于分离在水和有机溶剂中都可溶的混合物。
一种物质在两相中达到平衡时,在两相中的浓度之比是一个常数。
物质在流动相里的浓度物质在固定相里的浓度 纸层析:分配的过程:一部分溶质随有机相移动离开原点进入无溶质区,并进行重新分配,不断向前移动。
随着有机相不断向前移动,溶质不断地在两相间进行可逆的分配。
由于各种物质的分配系数不同,随展层溶剂移动的速率也不同,从而达到分离的目的。
移动速度可用比移(Rf )值表示:色斑中心至上样原点中心的距离K D =图1 氨基酸纸层析示意图R f =溶剂前缘至上样原点中心的距离载体:滤纸固定相:滤纸吸附的水流动相:水饱和酚极性:谷氨酸>丙氨酸>脯氨酸对于水-饱和酚的溶剂体系,氨基酸极性越小,KD 值越大,Rf值也越大,一定时间内随流动相迁移的距离远,反之迁移距离小。
三、实验材料仪器⑴层析缸;⑵层析滤纸;⑶电吹风机;⑸喷雾器;⑹毛细管。
试剂⑴氨基酸标准液(6mg/mL);⑵氨基酸混合液(6mg/mL)⑶展层剂:水饱和苯酚溶液。
⑷显色剂:0.3%茚三酮丙酮溶液四、操作步骤1、层析滤纸的准备用铅笔在层析滤纸上距离一端2-3cm处划线并标记点样位置。
2、点样(少量多次)用毛细管平口端蘸取少量样品溶液,点样于滤纸的相应位置,要求样品斑点直径不超过0.5cm,干燥后再点样,重复3次。
3、展层将滤纸放入层析缸,使滤纸浸入液面以下,但不要使液面没过点样线。
生物化学实验-氨基酸分析实验报告

生物化学实验-氨基酸分析实验报告实验名称(titleofexperimetn)氨基酸薄层层析实验地点(labno.)指导老师(instructor)实验日期(dateofexperiment)合作者(partner)总分(totalscore)xx教师签名(signature)李某某批改日期(date)【实验报告第一部分(预习报告内容):①实验原理、②实验材料(包括实验样品、主要试剂、主要仪器与器材)、③实验步骤(包括实验流程、操作步骤和注意事项);评分(满分30分):xx】一、预习报告实验原理:层析(chromatography):利用混合物各组分物理化学性质的差异,将多组分混合物进行分离及测定的方法。
固定相(stationaryphase)层析体质的一个基质。
能与待分离的化合物进行可逆的吸附、溶解、交换等作用。
流动相(mobilephase)在层析过程中推动固定相上贷分离的物质朝着一个方向运动的液体或气体。
迁移率(rateofflow,rf)一定条件下,在特定时间内某一组份在固定相移动的距离与流动相本身移动的距离之比值,rf值≤1。
层析原理:层析体系由一个固定相和一个流动相组成。
流动相对固定相做相对运动,从而推动待分离的混合物样品通过固定相向前移动。
样品中各组份物理化学性质不同,与两相发生相互作用的能力不同,被流动相推动前进时受到的阻力和移动速度不同,一定时间后,不同组份就可以在固定相上分离。
根据固定相基质的形式,层析可分为纸层析、薄层层析和柱层析。
薄层层析是在玻璃或塑料等光滑表面铺一层很薄的基质进行层析。
薄层层析(thinlayerchromatography,tlc):是将吸附剂均匀地在玻璃板上铺成薄层(固定相),再把样品点在薄层板一端,再把板的这端浸入适当的溶剂(流动相)在薄层板上扩展。
并在此过程中通过吸附——解吸附——再吸附——再解吸附的反复进行,而将样品各组份分离出来。
本次实验:具体原理:当流动相在固定相上流动时,由于吸附剂对不同氨基酸的吸附力不一样,不同氨基酸在展开溶剂中的溶解度不一样,点在薄板上的混合氨基酸样品随着展开剂的移动速率也不同,因而可以彼此分开。
氨基酸分析仪的基本分析原理

氨基酸分析仪的基本分析原理
氨基酸分析仪是一种用于定量分析样品中各种氨基酸的仪器。
其基本分析原理是通过将样品中的氨基酸分离、检测和定量,从而确定样品中各种氨基酸的含量。
首先,样品中的氨基酸需要被分离出来。
一种常用的方法是利用离子交换色谱技术。
离子交换色谱是通过样品中氨基酸的酸性基团和碱性基团与固定在色谱柱上的阴、阳离子交换剂之间的离子交换作用进行分离的。
通过调整溶剂和柱温等条件,可以实现对氨基酸的选择性分离。
其次,分离出的氨基酸需要被检测。
最常用的检测方法是紫外吸收检测。
氨基酸在紫外区域有特定的吸收峰,对应着特定的波长。
通过测量样品在不同波长下的吸光度,可以得到吸收峰的强度。
根据吸光度和吸光度与浓度之间的关系,可以计算出样品中各种氨基酸的浓度。
最后,根据样品中氨基酸的浓度,通过一定的计算公式,可以定量地确定样品中各种氨基酸的含量。
通常,会利用标准曲线法,即利用已知浓度的氨基酸标准溶液制备一系列浓度不同的标准曲线。
将样品中各种氨基酸的吸光度值与标准曲线进行比较,就可以得到各种氨基酸的浓度。
综上所述,氨基酸分析仪通过分离、检测和定量的步骤,可以对样品中的氨基酸进行分析,从而确定样品中各种氨基酸的含量。
氨基酸的测定

甲醛滴定法 (以测定氨杞精口服液中的氨基酸含量为例)
计算: 氨基酸态氮=〔 c×(V2-V1)
×0.014×100) 〕/W×100 V1——用中性红为指示剂
时,碱液所消耗的体积 V2——用百里酚酞乙醇液
为指示剂时标液消耗量
应用: 氨杞精口服液是由天然原料提
取的氨基酸粉(含20多种氨基酸), 加上构祀子、黄精煎煮液配制而 成的口服液。其中氨基酸为主要 有效成份, 采用甲醛滴定法测定 氨基酸的总量做为质量控制方法, 操作简便 。
仪器 附磁力搅拌器的酸度计;25mL酸式 滴定管; 10mL胖肚吸管。
双语例句
电位滴定法 (以测定酱油中的氨基酸含量为例)
操作方法:
(1)样品处理:先测出待测酱油的比重,然后吸取酱油5.00mL于
100mL容量瓶中,加水定容。吸取定容液20.00mL于250mL烧杯中,
加水60mL,放入磁力转子,开动磁力搅拌器使转速适当。用
个别氨基酸的定量测定
a)赖氨酸 b)色氨酸 c)苯丙氨酸 d)酪氨酸 e)脯氨酸 f)羟脯氨酸 g)胱氨酸 h)谷氨酸
氨基酸的分离及测定
a)薄层色谱法 b)氨基酸自动分析仪法 c)气相色谱法 d)高效液相色谱法
茚三酮法 (以测定蜂蜜及果葡糖浆中的氨基酸含量为例)
反应原理
氨基酸在一定pH条件下与茚三酮起反应,生成蓝紫色化合物,可 比色(570nm)定量。 注意:茚三酮受阳光、温度、湿度、空气等影响易被氧化呈淡红或深 红色,使用前要进行纯化,方法如下:
结论
1)采用茚三酮显色法测定的 蜂蜜及果葡糖浆的氨基酸含 量在0~150 μg/mL范围,该 法具有线性好、准确性及精 密度高等特点。
2)蜂蜜与果葡糖浆混合物中 的氨基酸含量和果葡糖浆掺 入量呈良好的负线性关系。 采用茚三酮显色法测定蜂蜜 样品的氨基酸含量,可以快 速判断蜂蜜中是否掺入了果 葡糖浆。
氨基酸分析指导原则

附件:氨基酸分析指导原则草案公示稿氨基酸分析指导原则氨基酸分析系指采用适宜的方法测定蛋白质、多肽或其他药物制剂中氨基酸组成和/或含量。
药品中氨基酸分析通常采用基于高效液相色谱法分离的衍生化法,涉及样品的水解、衍生化反应、分离检测和数据处理等操作。
本指导原则概述了药品中氨基酸分析的基本要求、蛋白质和多肽样品的水解、常用测定方法及其数据分析,为药品中氨基酸的分析提供指导。
1 基本要求1.1仪器氨基酸分析使用的仪器通常是高效液相色谱仪或氨基酸分析仪。
高效液相色谱仪适用于柱前衍生化产物的分离检测;对于柱后衍生化法,由于离子交换分离过程的复杂性和对柱后衍生化反应装置的特殊要求等,一般使用商品化的氨基酸分析仪。
1.2内标物氨基酸分析常采用内标法,内标物应是非天然存在的一级氨基酸,易于获取且价格便宜,在水解过程保持稳定,其色谱响应应与浓度成线性关系,具有独特的保留时间且与待测氨基酸能有效分离。
常用的内标物包括正亮氨酸、α-氨基丁酸、正缬氨酸、肌氨酸和硝基酪氨酸等。
内标物应在水解前或衍生化反应前添加到氨基酸混合物中,以消除由于水解、衍生化、取样、进样、溶液稳定性和色谱条件变化所导致的差异。
1. 3方法验证用于品种项下的氨基酸分析方法,包括样品水解,应参照分析方法验证指导原则(通则9101)进行方法学验证。
1.4水解管的清洗与要求为避免如手套粉末和指纹残留物等对分析结果的影响,水解管应清洗干净。
或使用一次性的水解管。
清洗方法:将水解管用1mol/L盐酸溶液中煮沸1小时,或将其浸泡在浓硝酸或浓盐酸-浓硝酸(1:1)混合液中1小时,再依次用高纯水、HPLC级甲醇冲洗,烘干并密封保存,以免再次污染。
2 蛋白质和多肽样品的水解蛋白质或多肽样品中的氨基酸是以结合形式存在,必须经过水解处理,形成游离氨基酸后才能进行氨基酸分析。
水解方法主要有酸水解,同时辅以碱水解。
酸水解中使用最广泛的是盐酸水解,所得氨基酸不消旋,但该方法引起一些氨基酸的破坏或部分破坏,如色氨酸被破坏,丝氨酸、苏氨酸和半胱氨酸被部分破坏,门冬酰胺和谷氨酰胺脱酰胺分别转化为门冬氨酸和谷氨酸。
L-色氨酸含量和纯度的测定实验指导书

L-色氨酸含量和纯度的测定 实验指导书一、实验目的1.了解对二甲氨基苯甲醛与L-色氨酸的反应机理;2.了解高效液相色谱分析的基本原理;3.掌握L-色氨酸的测定方法。
二、概述和原理L-色氨酸的分析方法主要有氨基酸自动分析仪分析法、高效液相色谱分析法、毛细管电泳法、薄层色谱法和分光光度法等。
本实验主要采用分光光度法进行L-色氨酸含量测定。
分光光度法测定L-色氨酸的基本原理为:在硫酸溶液中,L-色氨酸与对二甲氨基苯甲醛发生缩合反应,生成的希夫碱对二甲氨基苯甲醛缩色氨酸为蓝色,颜色深度在一定范围内与L-色氨酸含量成线性关系,可在分光光度计下定量测定。
高效液相色谱是色谱法的一个重要分支,其系统主要由储液器、泵、进样器、色谱柱、检测器、记录仪等几部分组成,由于该法具有高效、快速和灵敏等特点,不仅可用于L-色氨酸含量的测定,还可用于纯度的测定。
其工作原理为:储液器中的流动相被高压泵打入系统,样品溶液经进样器进入流动相,被流动相载入色谱柱(固定相)内,由于样品溶液中的各组分在两相中具有不同的分配系数,在两相中作相对运动时,经过反复多次的吸附-解吸的分配过程,各组分在移动速度上产生较大的差别,被分离成单个组分依次从柱内流出,通过检测器时,样品浓度被转换成电信号传送到记录仪,数据以图谱形式打印出来。
三、实验试剂及仪器1.试剂浓硫酸;对二甲氨基苯甲醛;亚硝酸钠;L-色氨酸标准品;磷酸二氢钾;冰醋酸;甲醇(液相纯);纯净水;乙腈(液相纯)。
2.仪器紫外可见分光光度计,Agilent 1200 Series高效液相色谱仪。
四、发酵液中L-色氨酸含量的测定1.对二甲氨基苯甲醛溶液(3 g/L)制备准确称取0.3 g对二甲氨基苯甲醛,溶于100 mL 1:1浓硫酸中。
2.亚硝酸钠溶液(2%)制备准确称取亚硝酸钠0.2 g于10 mL容量瓶中,以蒸馏水定容,新鲜配制。
3.L-色氨酸标准储备液(100 mg/L)制备准确称取25 mg L-色氨酸标准品,用纯水定容于250 mL棕色容量瓶中,制得浓度为100 mg/L的L-色氨酸标准储备液,于4 ℃冰箱保存备用。
氨基酸测定仪测定操作规程

氨基酸测定仪测定操作规程1. 引言本操作规程旨在指导使用氨基酸测定仪进行氨基酸测定的操作流程,并确保准确、可靠地测定样品中氨基酸的含量。
2. 仪器和试剂准备•氨基酸测定仪•相应的试剂盒和标准品•电子天平•移液器和移液枪•显微镜和玻璃片3. 样品处理1.准备样品:选择需要测定氨基酸含量的样品,并记录每个样品的相关信息,如样品编号、来源等。
2.样品预处理:根据样品的特性,选择合适的预处理方法,如样品酶解、样品脱蛋白等,以保证测定结果的准确性。
3.样品稀释:根据测定方法的要求,将样品适当稀释,以确保在仪器检测范围内。
4. 仪器设置1.开启仪器:按照仪器的使用说明,正确开启氨基酸测定仪,并进行初始化操作。
2.设置参数:根据测定方法的要求,设置仪器的相应参数,如测定波长、积分时间等。
3.校准仪器:使用标准品进行仪器的校准,确保仪器的准确性和精确度。
5. 操作步骤1.取样和试剂加入:使用移液器或移液枪,取出预处理好的样品,加入试剂,并记录试剂的加入量。
2.反应和测定:将样品和试剂混合均匀,然后放入氨基酸测定仪中进行反应和测定。
确保每次测定都按照相同的时间进行,以保证结果的可比性。
3.数据记录与分析:根据仪器的测定结果,记录每个样品的氨基酸含量,并进行数据分析,如平均值、标准差等。
6. 结果计算与报告1.结果计算:根据仪器的测定结果和标准品的浓度,计算出样品中每种氨基酸的含量。
这部分可以使用计算软件或者自行编写程序进行计算。
2.报告撰写:根据实验结果,撰写相应的实验报告,并进行结果解释和结论汇总。
7. 安全注意事项•在操作过程中,严格遵守实验室的安全操作规程,佩戴实验室必要的防护用品。
•注意试剂的储存和使用方法,避免接触皮肤和吸入。
•避免样品交叉污染和仪器污染,每次操作后清洗仪器和工作台面。
8. 管理和维护1.仪器管理:定期对仪器进行维护和保养,保持仪器的良好状态。
如清洁仪器外壳、调试仪器等。
2.试剂管理:根据试剂的要求进行存储和保管,防止试剂过期或受污染。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
氨基酸分析仪实验
测试中心吕雪娟
一、实验目的
了解氨基酸分析仪的主要结构及工作原理,掌握氨基酸分析的过程,前处理方法。
二、原理
氨基酸分析仪的分析原理是基于各种a一氨基酸的酸碱性、极性及分子大小的差异,用阳离子交换树脂在柱上进行层析分离,用几种不同pH值和离子强度的缓冲溶液依次将它们洗脱,从柱子上分离和洗脱下来的各种氨基酸在反应柱中与茚三酮进行加热反应,反应产物用可见光分光光度计进行检测,根据检测信号的大小计算出各种氨基酸的含量。
氨基酸和茚三酮反应
氨基酸分析仪结构示意图
二、操作步骤
1.准备工作
1.1缓冲液和茚三酮溶液的配制及正确放置
1.2氮气压力调整
1.2.1打开氮气钢瓶阀,调节其压力至50-100KPa(0.5-1.0Kgf/cm2)。
1.2.2顺时针轻轻旋转氮气调节器,使压力读数为34-40KPa(0.35-0.4Kgf /cm2)。
1.2.3脱气瓶中液体的更换
1.3放置自动进样器清洗瓶,向清洗瓶(C-1,1L)中盛上蒸馏水,放置于指定的位置并拧上盖子。
2.开稳压器
3.启动L-8800ASM应用程序
3.1系统初始化,OK
3.2打开Module Operation界面
3.3泵1流速设定----缓冲液的清洗,打开泵1的排液阀;清洗完毕,关闭泵1;
3.4泵2流速设定—一缓冲液的清洗,打开泵2的排液阀;清洗完毕关闭泵2;
3.5自动进样器流路和针头清洗,除气泡,重复此过程三次。
3.6泵的压力归零
4.分析程序
4.1选择应用程序
4.2选择分析方法
4.3输入待测样品的信息,编辑样品表,保存;
4.4打开数据采集监控画面
4.5选择样品表
4.6打开泵1和泵2
4.7按样品表顺序放置样品。
4.8单击监控屏幕下方的Start Series按钮,开始样品测试。
4.9开始结束后,关闭采集监控画面
4.10关闭L-8800ASM应用程序
4.11关电源
三、实验报告要求
1.实验原理及分析条件;
2.实验结果。
