ELLMAN试剂法测定自由巯基和二硫键
Ellman’s assay

5,5-二硫二硝基苯甲酸 DTNB 现货供应产品描述:DTNB为Ellman试剂。
它用于比色法测定生物样品中巯基。
它易溶于水。
在巯基化合物的存在下,无色的DTNB将被转变成黄色的5-巯基-2-硝基苯甲酸。
由于5-巯基-2-硝基苯甲酸在412 nm处具有最大吸收,DTNB的吸收光谱并不干扰巯基的测定。
配置方法:准确称取0.198gDTNB用50mMNa2HPO4(pH=7.0)配制成50ml溶液,存放于棕色瓶中,于暗处低温保存备用。
应该注意的是配置缓冲、浓度,储存时要避免见光。
应用举例:半胱氨酸中自由巯基的定量检测方法一、试剂的配制:1、Tris-HCL缓冲液(0.25M):DDW准确配制后,用盐酸调节pH=8.3;2、半胱氨酸标准溶液(1mM):准确称取0.017563gL-半胱氨酸(175.63),用1ml甲酸溶解,以DDW定容至100ml;3、DTNB(分子量:396.35)标准溶液(10mM):准确称取0.198175gDTNB用50mMNa2HPO4(pH=7.0)配制成50ml溶液,存放于棕色瓶中,于暗处低温保存备用4、DTNB分析溶液(0.1mM):由1体积10mMDTNB标准液加99体积0.25M的Tris缓冲液配制而成,现用现配。
二、标准曲线的制作;1、25℃条件下,用Tris缓冲液稀释半胱氨酸标准液配成梯度的稀释液(5.0ml),其浓度分别为:0.00mM、0.025mM、0.05mM、0.1mM、0.15mM、0.2mM;2、取上述各浓度溶液1ml分别加入到5ml预先恒温于25℃水中的DTNB分析溶液,摇匀,准确静止10min,立即于波长412nm处测定吸光度值(A)。
根据目的蛋白的吸光度在标准曲线上读出对应的浓度即可Product Name:DTNBProduct Number:D8130Product Brand:SigmaCAS Number:69-78-3Molecular Formula:[-SC6H3(NO2)CO2H]2 Molecular Weight:396.35Ordering Information。
ellman测巯基
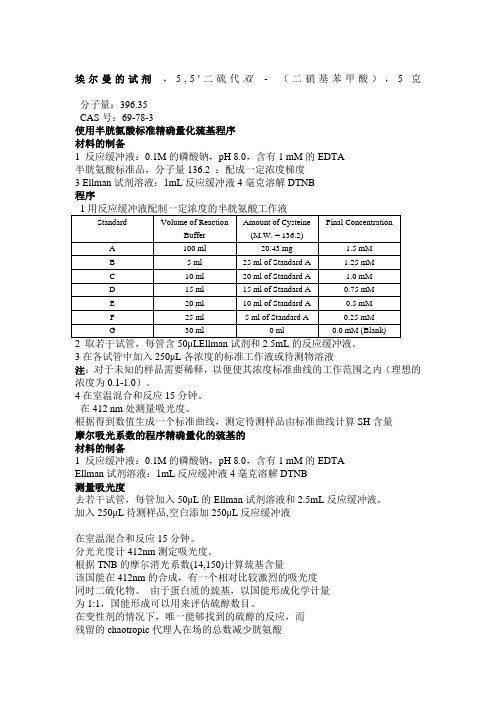
埃尔曼的试剂,5,5'二硫代双-(二硝基苯甲酸),5克分子量:396.35CAS号:69-78-3使用半胱氨酸标准精确量化巯基程序材料的制备1 反应缓冲液:0.1M的磷酸钠,pH 8.0,含有1 mM的EDTA半胱氨酸标准品,分子量136.2 :配成一定浓度梯度3 Ellman试剂溶液:1mL反应缓冲液4毫克溶解DTNB程序3在各试管中加入250μL各浓度的标准工作液或待测物溶液注:对于未知的样品需要稀释,以便使其浓度标准曲线的工作范围之内(理想的浓度为0.1-1.0)。
4在室温混合和反应15分钟。
在412 nm处测量吸光度。
根据得到数值生成一个标准曲线,测定待测样品由标准曲线计算SH含量摩尔吸光系数的程序精确量化的巯基的材料的制备1 反应缓冲液:0.1M的磷酸钠,pH 8.0,含有1 mM的EDTAEllman试剂溶液:1mL反应缓冲液4毫克溶解DTNB测量吸光度去若干试管,每管加入50μL的Ellman试剂溶液和2.5mL反应缓冲液。
加入250μL待测样品,空白添加250μL反应缓冲液在室温混合和反应15分钟。
分光光度计412nm测定吸光度。
根据TNB的摩尔消光系数(14,150)计算巯基含量该国能在412nm的合成,有一个相对比较激烈的吸光度同时二硫化物。
由于蛋白质的巯基,以国能形成化学计量为1:1,国能形成可以用来评估硫醇数目。
在变性剂的情况下,唯一能够找到的硫醇的反应,而残留的chaotropic代理人在场的总数减少胱氨酸目前可以衡量的。
经处理后减少的蛋白质与chaotropes及DTNB能够产生的半胱氨酸总数(半胱氨酸巯基加半胱氨酸-β-半胱氨酸)。
- -反应是敏感的碱性pH值(俄亥俄州)与RS竞争),酸性pH值(二硫化物可以打破),氧(R的巯基再氧化),以及温度(热致变色)。
因此,通常的反应是进行了过多的DTNB的蛋白质,在中性pH值固定的温度,erature,有时在厌氧条件。
巯基和二硫键含量的测定

巯基和二硫键含量的测定巯基和二硫键是有机化合物中常见的官能团和键。
巯基是由硫原子与氢原子组成的官能团,常用符号为-SH。
巯基的存在使得有机化合物具有一些特殊的性质和反应。
二硫键是两个硫原子之间的共价键,常见于含有硫原子的化合物中。
测定巯基和二硫键含量对于分析有机化合物的结构和性质具有重要意义。
测定巯基含量的方法有多种,常用的方法是使用巯基化合物与碘酸钾反应生成二硫键,然后用碘化钠溶液滴定反应产生的碘。
通过滴定测定巯基化合物中巯基含量的方法简便、快速,并且具有较高的准确性。
测定二硫键含量的方法也有多种。
常用的方法是使用碱性过氧化氢溶液氧化含有二硫键的化合物,然后通过滴定测定溶液中剩余的过氧化氢含量。
二硫键的含量可以通过计算过氧化氢的消耗量来确定。
巯基和二硫键的含量对于有机化合物的性质和反应有着重要的影响。
巯基的存在使得有机化合物具有较强的亲核性,容易与电子不足的化合物发生反应。
巯基化合物还可以形成二硫键,增加化合物的稳定性。
二硫键的存在使得化合物具有较高的氧化还原性,容易参与氧化还原反应。
巯基和二硫键含量的测定在有机化学研究和工业生产中有着广泛的应用。
通过测定巯基和二硫键含量,可以判断有机化合物的结构和性质。
这对于有机合成的设计和优化具有重要的意义。
同时,在某些特定的工业过程中,测定巯基和二硫键含量也可以用于监测反应过程的进展和产物的纯度。
巯基和二硫键是有机化合物中常见的官能团和键。
测定巯基和二硫键含量对于分析有机化合物的结构和性质具有重要意义。
巯基和二硫键含量的测定方法简便、快速,并且具有较高的准确性。
巯基和二硫键含量的测定在有机化学研究和工业生产中有着广泛的应用。
通过测定巯基和二硫键含量,可以判断有机化合物的结构和性质,对于有机合成的设计和优化具有重要的意义。
同时,在某些特定的工业过程中,测定巯基和二硫键含量也可以用于监测反应过程的进展和产物的纯度。
ELLMAN试剂法测定自由巯基和二硫键

E L L M A N试剂法测定自由巯基和二硫键This manuscript was revised by the office on December 22, 2012E L L M A N试剂测定自由巯基试验基于的原理:5,5’-dithiobis-2-nitrobenzoicacid(DTNB)5,5-二硫基-双(2-硝基苯甲酸)5,5-二硫基-双(2-硝基苯甲酸)(DTNB)在412nm没有吸收,与巯基反应后,生成2-硝基-5-巯基苯甲酸(TNB)[1]。
TNB2-在412nm有很强的吸收,可以用于对肽段的自由巯基进行定量分析[2]。
DTNBTNB2-根据文献记载,TNB的吸光系数在13.6*103M-cm-~14.25*103M-cm-之间[3,4]。
吸光度测量的最灵敏范围在0.2-0.7之间。
A=εbc,其中A为吸光度,ε是摩尔吸收光系数或消光系数,ε单位为升/(摩尔·厘米)[L/(mol·cm)]。
以吸光度下限0.2来计算(吸光系数取14.15*103M-cm-),需要TNB的浓度为c=0.2/(14.15*103LM-cm-*1cm)=1.4*10-5mol/L(1.4*10-8mol/ml),需要蛋白浓度为1.4*10-5mol/L*18790g/mol=0.2631g/L=0.2631mg/ml.我们的条件可以达到这个检测限度。
ELLMAN试剂法测定自由巯基主要的影响因素有:1.EDTA的适量加入有助于TNB显色的稳定和成梯度线性关系[5]。
2.在不同缓冲液中,TNB的最大吸收波长略微不同,所以它们在412nm的吸收也不3.同,要根据选择的缓冲液来确定[5]。
另外,TNB的分光光度法分析对SDS很敏感[6]。
4.DTNB随着pH的升高,降解速度加快。
在pH7.0,其降解速度为0.02%/h,在5.pH值8.0,其降解速度为0.2%/h,随着pH值得升高,降解速度加快,在pH12时,15min之内会完全降解[7,8]。
ellman测巯基
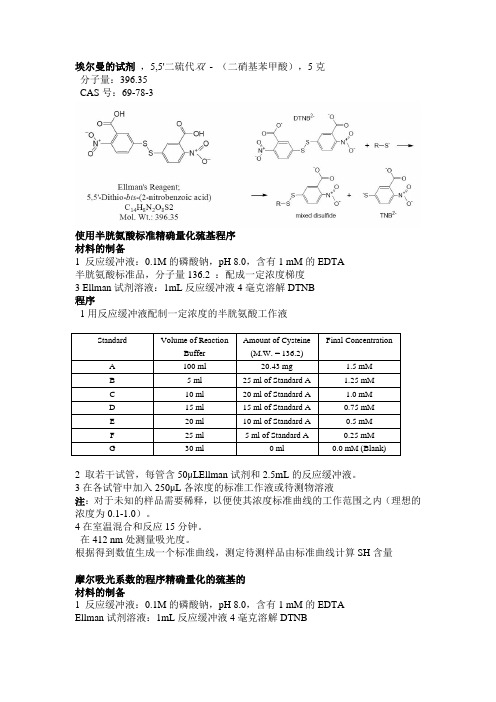
埃尔曼的试剂,5,5'二硫代双- (二硝基苯甲酸),5克分子量:396.35CAS号:69-78-3使用半胱氨酸标准精确量化巯基程序材料的制备1 反应缓冲液:0.1M的磷酸钠,pH 8.0,含有1 mM的EDTA半胱氨酸标准品,分子量136.2 :配成一定浓度梯度3 Ellman试剂溶液:1mL反应缓冲液4毫克溶解DTNB程序1用反应缓冲液配制一定浓度的半胱氨酸工作液2 取若干试管,每管含50μL Ellman试剂和2.5mL的反应缓冲液。
3在各试管中加入250μL各浓度的标准工作液或待测物溶液注:对于未知的样品需要稀释,以便使其浓度标准曲线的工作范围之内(理想的浓度为0.1-1.0)。
4在室温混合和反应15分钟。
在412 nm处测量吸光度。
根据得到数值生成一个标准曲线,测定待测样品由标准曲线计算SH含量摩尔吸光系数的程序精确量化的巯基的材料的制备1 反应缓冲液:0.1M的磷酸钠,pH 8.0,含有1 mM的EDTAEllman试剂溶液:1mL反应缓冲液4毫克溶解DTNB测量吸光度去若干试管,每管加入50μL的Ellman试剂溶液和2.5mL反应缓冲液。
加入250μL待测样品,空白添加250μL反应缓冲液在室温混合和反应15分钟。
分光光度计412nm测定吸光度。
根据TNB的摩尔消光系数(14,150)计算巯基含量该国能在412nm的合成,有一个相对比较激烈的吸光度同时二硫化物。
由于蛋白质的巯基,以国能形成化学计量为1:1,国能形成可以用来评估硫醇数目。
在变性剂的情况下,唯一能够找到的硫醇的反应,而残留的chaotropic代理人在场的总数减少胱氨酸目前可以衡量的。
经处理后减少的蛋白质与chaotropes及DTNB能够产生的半胱氨酸总数(半胱氨酸巯基加半胱氨酸-β-半胱氨酸)。
- -反应是敏感的碱性pH值(俄亥俄州)与RS竞争),酸性pH值(二硫化物可以打破),氧(R的巯基再氧化),以及温度(热致变色)。
ELLM试剂法测定自由巯基和二硫键

E L L M试剂法测定自由巯基和二硫键Prepared on 22 November 2020ELLMAN试剂测定自由巯基试验基于的原理:5,5’-dithiobis-2-nitrobenzoicacid(DTNB)5,5-二硫基-双(2-硝基苯甲酸)5,5-二硫基-双(2-硝基苯甲酸)(DTNB)在412nm没有吸收,与巯基反应后,生成2-硝基-5-巯基苯甲酸(TNB)[1]。
TNB2-在412nm有很强的吸收,可以用于对肽段的自由巯基进行定量分析[2]。
DTNBTNB2-根据文献记载,TNB的吸光系数在*103M-cm-~*103M-cm-之间[3,4]。
吸光度测量的最灵敏范围在之间。
A=εbc,其中A为吸光度,ε是摩尔吸收光系数或消光系数,ε单位为升/(摩尔·厘米)[L/(mol·cm)]。
以吸光度下限来计算(吸光系数取*103M-cm-),需要TNB的浓度为c=(*103LM-cm-*1cm)=*10-5mol/L*10-8mol/ml),需要蛋白浓度为*10-5mol/L*18790g/mol=L=ml.我们的条件可以达到这个检测限度。
ELLMAN试剂法测定自由巯基主要的影响因素有:1.EDTA的适量加入有助于TNB显色的稳定和成梯度线性关系[5]。
2.在不同缓冲液中,TNB的最大吸收波长略微不同,所以它们在412nm的吸收也不3.同,要根据选择的缓冲液来确定[5]。
另外,TNB的分光光度法分析对SDS很敏感[6]。
4.DTNB随着pH的升高,降解速度加快。
在,其降解速度为%/h,在5.pH值,其降解速度为%/h,随着pH值得升高,降解速度加快,在pH12时,15min之内会完全降解[7,8]。
6.摩尔吸收光系数在不同的温度下不同,随温度的升高而下降[4].试验方案主要材料:1.材料PEG-G-CSF批号:080229浓度mlG-CSF批号:080126浓度ml10k超滤膜PALL2.试剂SequencingGradeModifiedTrypsin,Promega,lot#237826。
ellman测巯基

埃尔曼的试剂,5,5'二硫代双- (二硝基苯甲酸),5克分子量:396.35CAS号:69-78-3使用半胱氨酸标准精确量化巯基程序材料的制备1 反应缓冲液:0.1M的磷酸钠,pH 8.0,含有1 mM的EDTA 半胱氨酸标准品,分子量136.2 :配成一定浓度梯度3 Ellman试剂溶液:1mL反应缓冲液4毫克溶解DTNB程序1用反应缓冲液配制一定浓度的半胱氨酸工作液Standard Volume of ReactionBuffer Amount of Cysteine(M.W. = 136.2)Final ConcentrationA 100 ml 20.43 mg 1.5 mMB 5 ml 25 ml of Standard A 1.25 mMC 10 ml 20 ml of Standard A 1.0 mMD 15 ml 15 ml of Standard A 0.75 mME 20 ml 10 ml of Standard A 0.5 mMF 25 ml 5 ml of Standard A 0.25 mMG 30 ml 0 ml 0.0 mM (Blank)2 取若干试管,每管含50μL Ellman试剂和2.5mL的反应缓冲液。
3在各试管中加入250μL各浓度的标准工作液或待测物溶液注:对于未知的样品需要稀释,以便使其浓度标准曲线的工作范围之内(理想的浓度为0.1-1.0)。
4在室温混合和反应15分钟。
在412 nm处测量吸光度。
根据得到数值生成一个标准曲线,测定待测样品由标准曲线计算SH含量摩尔吸光系数的程序精确量化的巯基的材料的制备1 反应缓冲液:0.1M的磷酸钠,pH 8.0,含有1 mM的EDTAEllman试剂溶液:1mL反应缓冲液4毫克溶解DTNB测量吸光度去若干试管,每管加入50μL的Ellman试剂溶液和2.5mL反应缓冲液。
加入250μL待测样品,空白添加250μL反应缓冲液在室温混合和反应15分钟。
ELLMAN试剂法测定自由巯基和二硫键

E L L M A N试剂法测定自由巯基和二硫键标准化工作室编码[XX968T-XX89628-XJ668-XT689N]E L L M A N试剂测定自由巯基试验基于的原理:5,5’-dithiobis-2-nitrobenzoicacid(DTNB)5,5-二硫基-双(2-硝基苯甲酸)5,5-二硫基-双(2-硝基苯甲酸)(DTNB)在412nm没有吸收,与巯基反应后,生成2-硝基-5-巯基苯甲酸(TNB)[1]。
TNB2-在412nm有很强的吸收,可以用于对肽段的自由巯基进行定量分析[2]。
DTNBTNB2-根据文献记载,TNB的吸光系数在13.6*103M-cm-~14.25*103M-cm-之间[3,4]。
吸光度测量的最灵敏范围在0.2-0.7之间。
A=εbc,其中A为吸光度,ε是摩尔吸收光系数或消光系数,ε单位为升/(摩尔·厘米)[L/(mol·cm)]。
以吸光度下限0.2来计算(吸光系数取14.15*103M-cm-),需要TNB的浓度为c=0.2/(14.15*103LM-cm-*1cm)=1.4*10-5mol/L(1.4*10-8mol/ml),需要蛋白浓度为1.4*10-5mol/L*18790g/mol=0.2631g/L=0.2631mg/ml.我们的条件可以达到这个检测限度。
ELLMAN试剂法测定自由巯基主要的影响因素有:1.EDTA的适量加入有助于TNB显色的稳定和成梯度线性关系[5]。
2.在不同缓冲液中,TNB的最大吸收波长略微不同,所以它们在412nm的吸收也不3.同,要根据选择的缓冲液来确定[5]。
另外,TNB的分光光度法分析对SDS很敏感[6]。
4.DTNB随着pH的升高,降解速度加快。
在pH7.0,其降解速度为0.02%/h,在5.pH值8.0,其降解速度为0.2%/h,随着pH值得升高,降解速度加快,在pH12时,15min之内会完全降解[7,8]。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
ELLMAN试剂测定自由巯基
试验基于的原理:
5,5’-dithiobis-2-nitrobenzoic acid (DTNB) 5,5-二硫基-双(2-硝基苯甲酸) 5,5-二硫基-双(2-硝基苯甲酸)(DTNB)在412nm没有吸收,与巯基反应后,生成2-硝基-5-巯基苯甲酸(TNB)[1]。
TNB2-在412nm有很强的吸收,可以用于对肽段的自
2-
吸光度
0.2来计算-*1cm)
1.4*10
1.
2.
不
3.同,要根据选择的缓冲液来确定[5]。
另外,TNB的分光光度法分析对SDS很敏
感[6]。
4.DTNB随着pH的升高,降解速度加快。
在pH7.0,其降解速度为0.02%/h,在
5.pH值8.0,其降解速度为0.2%/h,随着pH值得升高,降解速度加快,在pH 12
时,15min之内会完全降解[7,8]。
6.摩尔吸收光系数在不同的温度下不同,随温度的升高而下降[4].
试验方案
主要材料:
1.材料
PEG-G-CSF 批号:080229 浓度4.32mg/ml
G-CSF 批号:080126 浓度6.9mg/ml
小瓶。
NO
B液:0.1%TFA/90%乙腈/H2O
3.仪器
质谱仪:BRUKER DALTONICS MALTI-TOF-TOF autoflexⅢ(厂内编号
KC2007-011)
Beckman 22R台式离心机(厂内编号AM-039)
Beckman DU-800 紫外分光光度计(厂内编号KC2007-005)
恒温循环仪:JULABO F12-ED(厂内编号KC2008-003)
反相柱:Symmetry C18 5um 300à
高压液相仪器:,(UV/Visible Detector)
试验过程:
一、缓冲液替换
PEG-G-CSF和G-CSF进行缓冲液替换,超滤替换缓冲液为50mM NH4HCO3,
稀释
中加入
G-CSF
+DTT
相分离
收样:
SF
+DTT
相分离
集到
之间的
交由崔
文喜冻
干
四、ELLMAN试剂测定自由巯基
由于收集到的PEG肽段已经是自由巯基,所以可以跳过还原二硫键这一步。
根据我们所查找到得文献,采用的参数如下:
反应缓冲液:0.10M 磷酸钠+0.001M EDTA ,pH 7.27
温度:25℃
在这些参数下,摩尔吸收光系数为14.15±0.09*103LM-cm-[9].
1)标准曲线
用反应缓冲液配制10umDTT,20 umDTT,40 umDTT,80 umDTT,160 umDTT,
320 umDTT。
用缓冲液配制10mM 的ELLMAN试剂。
准备两个比色皿。
①加入100ul反应缓冲液到样品管和对照管中,在412nm测定吸收值,吸收
值调节到0.
412nm final DTNB buffer
参考文献:
1)THEODOREW.T et al.Sensitive Quantitative Analysis of Disulfide Bonds in Polypeptides and Proteins. ANALYTICAL BIOCHEMISTRY 138, 18 1- I88 ( 1984).
2) W. L. ANDERSON AND D. B. WETLAUFER .A New Method for
Disulfide Analysis of Peptides. ANALYTICAL BIOCHEMISTRY 67.493-502 ( 1975).
3) Ellman, G.L., Arch. Biochem. Biophys., 74, 443. (1958).
4) Peter Eyer,et al. Molar absorption coe?cients for the reduced Ellman reagent: reassessment.. Analytical Biochemistry 312 (2003) 224–227
5) for
8)
9)
Anal.。
