(化学)有机方程式书写(有答案)
高中化学全部化学方程式汇总(有机和无机)

高中化学全部化学方程式汇总(有机和无机)【注意】以下是有机和无机化学方程式的汇总,请按需使用或参考。
为了排版整洁,请在使用时进行适当的调整和修改。
一、有机化学方程式1. 碳氢化合物反应方程式1.1 烷烃燃烧反应:CnH2n+2 + (n + (n/2 + 1)/2)O2 → nCO2 + (n + (n/2 - 1)/2)H2O1.2 烯烃燃烧反应:CnH2n + (n + n/2)O2 → nCO2 + nH2O1.3 异构烷烃燃烧反应:CnH2n + (n + n/2)O2 → nCO2 + nH2O2. 醇类反应方程式2.1 醇的燃烧反应:CnH2n+1OH + (n + (n+1)/2)O2 → nCO2 + (n+1)H2O2.2 醇的脱水反应:CnH2n+1OH → CnH2n + H2O3. 酚类反应方程式3.1 酚的燃烧反应:C6H6O + 15/2O2 → 6CO2 + 3H2O 3.2 酚的酸碱中和反应:C6H6O + NaOH → C6H5ONa + H2O 4. 酯类反应方程式4.1 酯的酸水解反应:RCOOR' + H2O → RCOOH + R'OH 4.2 酯的碱水解反应:RCOOR' + NaOH → RCOONa + R'OH 5. 醛和酮类反应方程式5.1 氧化性还原反应:RCHO + [O] → RCOOH5.2 醛的酸碱反应:RCHO + NaOH → RCOONa + H2O 6. 醚类反应方程式6.1 醚的加热裂解反应:ROR' → R'H + R'OH6.2 醚的酸水解反应:ROR' + H2O → ROH + R'OH7. 脂肪酸类反应方程式7.1 脂肪酸的酸碱反应:RCOOH + NaOH → RCOONa + H2O7.2 脂肪酸的酯化反应:RCOOH + R'OH → RCOOR' + H2O二、无机化学方程式1. 钠和氧的反应方程式4Na + O2 → 2Na2O2. 钙和水的反应方程式Ca + 2H2O → Ca(OH)2 + H23. 硝酸和铜的反应方程式Cu + 4HNO3 → Cu(NO3)2 + 2NO2 + 2H2O 4. 二氧化碳和水的反应方程式CO2 + H2O → H2CO35. 硝酸和氢氧化钠的反应方程式2NaOH + HNO3 → NaNO3 + H2O6. 硫化氢和氯的反应方程式H2S + Cl2 → 2HCl + S7. 氧化锌和硫酸的反应方程式ZnO + H2SO4 → ZnSO4 + H2O8. 氯气和钾溶液的反应方程式Cl2 + 2KOH → KCl + KClO + H2O9. 溴和钾的反应方程式2K + Br2 → 2KBr10. 硫和氧的反应方程式S + O2 → SO2以上是高中化学的部分有机和无机方程式的汇总,希望能对你的学习有所帮助。
初中化学方程式书写及其计算(含答案)

化学方程式书写及其计算(基础)学习目标1.掌握化学方程式的书写原则和步骤;了解几种化学方程式的配平方法;能熟记并能书写常见反应的化学方程式。
2.掌握有关反应物、生成物质量的计算;掌握解计算题的基本格式。
化学方程式书写及其计算(基础)要点一、化学方程式的书写原则和步骤要点二、化学方程式的配平要点三、利用化学方程式计算的步骤及格式要点梳理要点一、化学方程式的书写原则和步骤1.书写化学方程式时应遵循两条原则:(1)必须以客观事实为依据,不能凭空臆造事实上不存在的物质和化学反应。
(2)要遵守质量守恒定律。
这一原则要求书写化学方程式时一定要配平,使反应前后的各种原子的个数相等。
2.书写化学方程式的五个步骤(以高锰酸钾受热分解为例):(1)“写”:根据实验事实,短线左边写反应物的化学式,右边写生成物的化学式,不止一种物质的用加号连接。
KMnO4─K2MnO4+MnO2+O2(2)“配”:调整化学式前边的化学计量数,使短线左右两边同种原子的数目相等。
2KMnO4─K2MnO4+MnO2+O2(3)“注”:注明反应条件、气体放出符号“↑”和沉淀符号“↓”。
如果反应物和生成物中都有气体或都有固体,气体生成物或固体生成物就不要注“↑”或“↓”。
(4)“改”:配平后必须把短线改为等号。
2KMnO4K2MnO4+MnO2+O2↑(5)“查”:一查化学式;二查配平(等号两边各种原子的总数是否相等);三查条件;四查生成物的状态。
【要点诠释】化学方程式的书写歌诀:左写反应物、右写生成物;写准化学式,系数要配平;中间连等号,条件要注清;生成气沉淀,箭头(↑↓)来标明。
化学方程式书写及其计算(基础)要点一、化学方程式的书写原则和步骤要点二、化学方程式的配平要点三、利用化学方程式计算的步骤及格式要点梳理要点二、化学方程式的配平化学方程式的配平是指根据质量守恒定律,在化学式前面配上适当的化学计量数,使式子左、右两边同种原子的数目相等。
高中经典有机化学反应方程式

章末回顾排查专练(十二)排查一、重要有机反应方程式再书写1.2.2C 2H 5OH +2Na →2C 2H 5ONa +H 2↑; 3.CH 3CH 2OH ―――――――――→浓H 2SO 4170 ℃CH 2===CH 2↑+H 2O ; 4.C 2H 5OH +HBr ――→△ C 2H 5Br +H 2O ;5.2C 2H 5OH +O 2―――――――――→Cu 或Ag △2CH 3CHO +2H 2O ;9.2CH 3CHO +O 2―――――――――→催化剂△2CH 3COOH ; 10.CH 3CHO +H 2――――――――――→催化剂△CH 3CH 2OH ; 11.CH 3CHO +2Ag(NH 3)2OH ――→△ CH 3COONH 4+2Ag ↓+3NH 3+H 2O ;12.CH 3CHO +2Cu(OH)2――→△ CH 3COOH +Cu 2O ↓+2H 2O ;13.CH 3COOH +C 2H 5OH 浓H 2SO 4△CH 3COOC 2H 5+H 2O ;14.CH 3COOC 2H 5+H 2O 稀H 2SO 4△CH 3COOH +C 2H 5OH ;15.乙二醇和乙二酸生成聚酯16.排查二、常考易错再排查 1.按碳原子组成的分子骨架分,有机物可分为链状化合物和环状化合物,环状化合物又包括脂环化合物和芳香族化合物。
按官能团分,有机物可分为烃(烷烃、烯烃、炔烃、芳香烃)和烃的衍生物(卤代烃、醇、酚、醛、酸、酯等)。
( )2.具有相同分子式,不同结构的化合物互为同分异构体。
包括碳链异构(如CH 3CH 2CH 2CH 3与)、位置异构(如CH 3CH===CHCH 3与CH 3CH 2CH===CH 2)、官能团异构(如CH 3CH 2OH 与CH 3OCH 3)、顺反异构(顺2-丁烯与反2-丁烯)、手性异构等。
( )3.发生加成反应或加聚反应的有机物分子必须含有不饱和键。
2022年高考化学有机转化关系及反应方程式书写
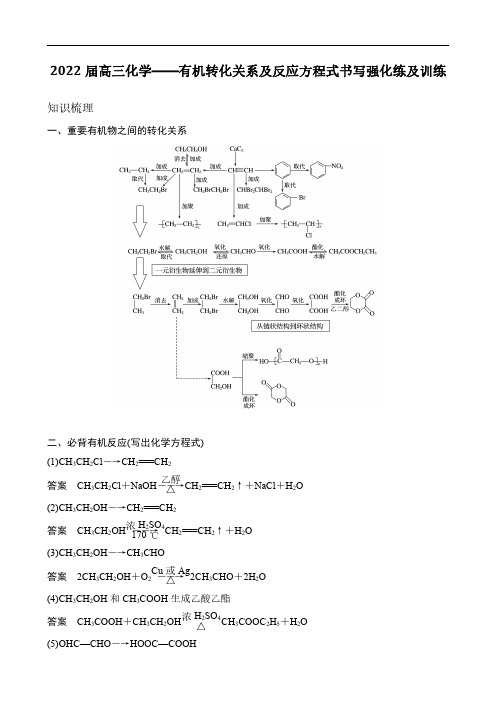
2022届高三化学——有机转化关系及反应方程式书写强化练及训练知识梳理一、重要有机物之间的转化关系二、必背有机反应(写出化学方程式)(1)CH 3CH 2Cl ―→CH 2===CH 2答案CH 3CH 2Cl +NaOH ――→乙醇△CH 2===CH 2↑+NaCl +H 2O(2)CH 3CH 2OH ―→CH 2===CH 2答案CH 3CH 2OH ――→浓H 2SO 4170℃CH 2===CH 2↑+H 2O (3)CH 3CH 2OH ―→CH 3CHO 答案2CH 3CH 2OH +O 2――→Cu 或Ag △2CH 3CHO +2H 2O(4)CH 3CH 2OH 和CH 3COOH 生成乙酸乙酯答案CH 3COOH +CH 3CH 2OH浓H 2SO 4△CH 3COOC 2H 5+H 2O (5)OHC—CHO ―→HOOC—COOH答案OHC—CHO +O 2――→催化剂△HOOC—COOH(6)乙二醇和乙二酸生成聚酯答案n HOCH 2—CH 2OH +n HOOC—COOH――→一定条件+(2n -1)H 2O (7)乙醛和银氨溶液的反应答案CH 3CHO +2Ag(NH 3)2OH ――→△CH 3COONH 4+2Ag ↓+3NH 3+H 2O(8)乙醛和新制Cu(OH)2悬浊液的反应答案CH 3CHO +2Cu(OH)2+NaOH ――→△CH 3COONa +Cu 2O ↓+3H 2O(9)答案(10)答案(11)和饱和溴水的反应答案(12)和溴蒸气(光照)的反应答案(13)和HCHO 的反应答案+(n -1)H 2O(14)酯在碱性条件的水解(以乙酸乙酯在NaOH 溶液中为例)答案CH 3COOC 2H 5+NaOH ――→△CH 3COONa +C 2H 5OH (15)和NaOH 的反应三、常考有机物的检验1.卤代烃中卤素的检验取样,滴入NaOH 溶液,加热至分层现象消失,冷却后加入稀硝酸酸化,再滴入AgNO 3溶液,观察沉淀的颜色,确定是何种卤素。
有机物所有的化学方程式

有机物所有的化学方程式
所有的化学方程式都是描述化学反应的方式,可以通过化学方程式来表示有机物的反应过程。
有机物是一类含有碳元素的化合物,其化学方程式一般由反应物和生成物组成。
下面是一些常见的有机物化学方程式的示例:
1. 烷烃燃烧反应:
烷烃是一类只含有碳和氢元素的有机物。
烷烃的燃烧反应是指它与氧气发生反应产生二氧化碳和水。
例如,甲烷的燃烧反应可以用如下方程式表示:
CH₄(g) + 2O₂(g) → CO₂(g) + 2H₂O(g)
2. 醇的酸碱反应:
醇是一类含有羟基(-OH)官能团的有机物。
醇可以与酸或碱发生反应。
例如,乙醇与氢氧化钠发生酸碱中和反应的方程式如下:CH₃CH₂OH + NaOH → CH₃CH₂ONa + H₂O
3. 醛的氧化反应:
醛是一类含有碳氧双键(C=O)官能团的有机物。
醛可以被氧化为羧酸。
例如,甲醛氧化为甲酸的方程式如下:
HCHO + [O] → HCOOH
4. 酯的酸酯化反应:
酯是一类由醇和酸反应生成的有机物。
酯的酸酯化反应是指酯与酸反应生成另一种酯和水。
例如,乙酸乙酯与苯甲酸反应生成苯乙酸乙酯和水的方程式如下:
CH₃COOC₂H₅ + C₆H₅COOH → C₆H₅COOC₂H₅ + H₂O
这些是一些常见的有机物化学方程式的示例,它们用来描述有机物反应过程中的物质变化。
在实际应用中,化学方程式能够帮助我们了解有机物之间的反应关系,并且对有机化学研究和实验有着重要的意义。
方程式的书写及答案

1.类比是学习的重要方法之一,但是往往机械类比会产生错误,因此学习化学要透过现象看本质,谨防思维定势。
下列类比中正确的是A.由Cl2与水反应类推:BrCl+H2O==HClO+HBrB.由NCl3的水解产物NH3和HClO类推:PCl3的水解产物是PH3和HClOC.由Cl2O与水反应生成HClO类推:OF2与水反应可生成HFOD.由NaH与水反应时放出H2类推:NH4H与水反应可生成H22.某物质是一种由不同的短周期元素形成的离子化合物,其阴、阳离子的个数比为2∶3,且能与水反应得到两种碱。
写出该离子化合物与足量硝酸反应生成两种盐的化学方程式____________________。
3.铝是地壳中含量最高的金属元素,其单质及合金在生产生活中的应用日趋广泛。
(1)真空碳热还原-氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:①Al2O3(s)+AlCl3(g)+3C(s)==3AlCl(g)+3CO(g) △H=a kJ·mol-1②3AlCl(g)==3Al(l)+AlCl3(g)△H=b kJ·mol-1③反应Al2O3(s)+3C(s)==2Al(l)+3CO(g)的△H=kJ·mol-1(用含a、b的代数式表示)。
(2)Al4C3是反应过程的中间产物。
请写出Al4C3与盐酸反应(产物之一是含氢量最高的烃)的化学方程式。
解析与答案:(1)根据盖斯定律知,①式与②式相加即得③式,△H= (a+b)kJ·mol-1。
(2) Al4C3与盐酸反应可视为Al4C3水解生成Al(OH)3和含氢量最高的烃CH4,而后Al(OH)3与盐酸反应生成AlCl3,反应的化学方程式为:Al4C3+12HCl==4AlCl3+3CH4↑。
总结:金属氮化物、磷化物、砷化物以及金属碳化物、硅化物等均易水解生成金属氢氧化物和氢化物。
如:Mg2Si+4H2O===2Mg(OH)2↓+SiH4↑等。
有机方程式书写(有答案)

高三化学二轮复习——有机方程式书写【训练一】写出下列反应的化学方程式(要标注反应条件和配平!):1、由甲苯制2-溴甲苯:2、由甲苯制一溴苯基甲烷():3、由甲苯制TNT(2,4,6-三硝基甲苯):4、由苯甲醛制苯甲醇:5、与Br2按1:1发生加成::6、氯乙烷与NaOH水溶液反应:7、一氯乙酸与足量NaOH水溶液混合加热反应:8、与NaOH醇溶液反应:9、的催化氧化反应:10、发生消去反应:11、乙二醇与乙二酸酯化成环反应:12、乙二醇与乙二酸酯化成高分子化合物:13、苯酚溶液滴入浓溴水:14、与溴水反应:15、乙醛发生银镜反应:16、与新制氢氧化铜反应:17、二乙酸乙二酯发生完全水解:18、一氯乙酸乙酯与足量的NaOH溶液加热反应:19、2-甲基-1,3-丁二烯发生加聚反应:20、丙烯酸甲酯发生加聚反应:【训练二】读懂信息,正确迁移:根据题给信息进行信息迁移是有机综合题的热点。
题给信息理解错了,就无法正确运用信息进行迁移。
平时多做信息题可以提高信息的理解和迁移能力!1、已知:则苯甲醛与丙醛发生上述反应的方程式为:__________________________________________________.2、已知:则两分子乙醛在上述条件下反应的化学方程式:_ 。
3、已知:请写出实现由(CH3)2CHCH=CH2分两步转变为(CH3)2CHCH2CH2OH的方程式:_________________________________________________________________________________________________________________________________________________ 4、已知:已知环氧氯丙烷可与乙二醇发生如下聚合反应:则:环氧氯丙烷与发生类似反应生成高聚物,该高聚物的结构式是:5、已知:则:+6、已知:则:+7、已知:则8、已知:①②则:⑴⑵+→9、已知:碱存在下,卤代烃与醇反应生成醚(R—O—R‘):R—X + R‘OH R—O—R ’ +HX 则:B的结构简式为:10、已知:通常情况下,多个羟基连在同一个碳原子上的分子结构是不稳定的,容易自动失水,生成碳氧双键的结构:下面是9个化合物的转变关系:(1)化合物①的名称是它跟氯气发生反应的条件A是(2)化合物⑤跟⑦可在酸的催化下去水生成化合物⑨, ⑨的结构简式是:______________ ,名称是(3)化合物⑨是重要的定香剂,香料工业上常用化合物⑧和②直接合成它。
2022高考化学有机信息方程式(结构简式)的书写(1)

2022高考化学有机信息方程式〔结构简式〕的书写(1) 有机化学信息方程式或结构简式〔含流程设计〕的书写1、以下是一种药物Ⅳ合成局部路线:H2NHOCHCOOHCH3①C2H5OH,H+②调节pHH2NHOCHCOOC2H5CH3ⅠCl一定条件COClC18H16O3NCl①NaOH②H+ⅡNClOCHCOOHCH3ⅢⅣ请答复以下问题:〔5〕OHNH2与COCl在一定条件下发生类似化合物Ⅱ转化为Ⅲ的反响,试写出该反响的化学方程式。
2、在250℃时,吲哚与乙醇酸在碱的存在下反响,可以得到植物生长素吲哚乙酸:由邻硝基甲苯1和草酸二乙酯2反响最终可合成吲哚5〔Et表示CH3CH2—〕:乙醇酸的合成:〔4〕乳酸的结构简式为,请写出乳酸与吲哚发生反响的化学方程式〔不用写反响条件〕:;3、芳香醛与活性亚甲基化合物的缩合反响在有机合成中有重要应用,化合物III 是医药中间体,其合成方法如下:反响①:OCHOOOOO化合物I化合物IICH3CH3催化剂OCHOO化合物IIICH3CH3++H2O 1化合物Ⅱ也可以由化合物IV〔C3H6Cl2〕经以下途经合成:(4) E是化合物II的同分异构体,且E是一种链状结构,在核磁共振氢谱中有3种氢, 1mol E能与2 molNaHCO3反响,写出化合物E的结构简式。
(任写一种;不考虑顺反异构。
) 〔5〕化合物I与化合物〔〕在催化剂条件下也能发生类似反响①的 COOC2H5CN反响得到另一医药中间体,写出该反响化学方程式 4、〔2022年肇庆一模〕有增长碳链是有机合成中非常重要的反响。
例如:反响①O CH 3CHO CH 3+ Br-CH-COOC2H5(Ⅱ)Zn 苯H2O OH CH 3CH-CH-COOC2H5(Ⅰ)O CH 3Cl〔4〕对二氯苯 Cl 也能与有机物(Ⅰ) (过量)发生类似反响①的系列反响,其生成有机物的结构简式为。
5、〔2022年高三期末考试〕〔16分〕有机物A可以通过不同的反响得到B和C:OBOACOOHOHCCOOHCHO〔4〕芳香族化合物D是A的同分异构体,1molD可以和3mol NaOH发生中和反响;D苯环上的一氯代物只有一种且分子中没有甲基。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高三化学二轮复习——有机方程式书写【训练一】写出下列反应的化学方程式(要标注反应条件和配平!):
1、由甲苯制2-溴甲苯:
2、由甲苯制一溴苯基甲烷():
3、由甲苯制TNT(2,4,6-三硝基甲苯):
4、由苯甲醛制苯甲醇:
5、与Br2按1:1发生加成::
6、氯乙烷与NaOH水溶液反应:
7、一氯乙酸与足量NaOH水溶液混合加热反应:
8、与NaOH醇溶液反应:
9、的催化氧化反应:
10、发生消去反应:
11、乙二醇与乙二酸酯化成环反应:
12、乙二醇与乙二酸酯化成高分子化合物:
13、苯酚溶液滴入浓溴水:
14、与溴水反应:
15、乙醛发生银镜反应:
16、与新制氢氧化铜反应:
17、二乙酸乙二酯发生完全水解:
18、一氯乙酸乙酯与足量的NaOH溶液加热反应:
19、2-甲基-1,3-丁二烯发生加聚反应:
20、丙烯酸甲酯发生加聚反应:
【训练二】读懂信息,正确迁移:根据题给信息进行信息迁移是有机综合题的热点。
题给信息理解错了,就无法正确运用信息进行迁移。
平时多做信息题可以提高信息的理解和迁移能力!
1、已知:则苯甲醛与丙醛发生上述反应的方程式为:
__________________________________________________.
2、已知:
则两分子乙醛在上述条件下反应的化学方程式:
_ 。
3、已知:
请写出实现由(CH3)2CHCH=CH2分两步转变为(CH3)2CHCH2CH2OH的方程式:
______________________________________________________________
___________________________________________________________________________________ 4、已知:已知环氧氯丙烷可与乙二醇发生如下聚合反应:
则:环氧氯丙烷与发生类似反应生成高聚物,该高聚物的结构式
是:
5、已知:则:
+
6、已知:则:
+
7、已知:则
8、已知:①②
则:⑴
⑵+→
9、已知:碱存在下,卤代烃与醇反应生成醚(R—O—R‘):
R—X + R‘OH R—O—R ’ +HX 则:
B的结构简式为:
10、已知:通常情况下,多个羟基连在同一个碳原子上的分子结构是不稳定的,容易自动失水,生成碳氧双
键的结构:
下面是9个化合物的转变关系:
(1)化合物①的名称是它跟氯气发生反应的条件A是
(2)化合物⑤跟⑦可在酸的催化下去水生成化合物⑨, ⑨的结构简式是:
______________ ,名称是
(3)化合物⑨是重要的定香剂,香料工业上常用化合物⑧和②直接合成它。
此反应的化学方程式是
11、已知:此反应称为酯交换反应,常用于
有机合成中。
则聚乙酸乙烯酯()与甲醇进行酯交换反应的化学方程式:
____ _____________。
12、已知溴乙烷跟氰化钠反应再水解可以得到丙酸:CH3CH2Br CH3CH2CN CH3CH2COOH, 则CH3CHBrCH3发生上述反应得到的是。
13、已知:CH3COONa+ NaOH Na2CO3+ CH4 ↑则:①+ NaOH+
②+ NaOH+
③用该方法生产乙烯的反应方程式为:
14、已知:则:。
