(完整版)测序常用名词解释整理
RNA-seq基础知识

RNA-seq基础知识1.RNA-Seq名词解释2.测序名词解释3.高通量测序常用名词解释4.转录组测序问题集锦RNA-Seq名词解释1.index 测序的标签,用于测定混合样本,通过每个样本添加的不同标签进行数据区分,鉴别测序样品。
2.碱基质量值(Quality Score或Q-score)是碱基识别(Base Calling)出错的概率的整数映射。
碱基质量值越高表明碱基识别越可靠,碱基测错的可能性越小。
3.Q30 碱基质量值为Q30代表碱基的精确度在99.9%。
4.FPKM(Fragments Per Kilobase of transcript per Millionfragments mapped)每1百万个map上的reads中map到外显子的每1K个碱基上的fragment个数。
计算公式为公式中,cDNAFragments 表示比对到某一转录本上的片段数目,即双端Reads数目;Mapped Reads(Millions)表示Mapped Reads总数,以10为单位;Transcript Length(kb):转录本长度,以kb个碱基为单位。
5.FC(Fold Change)即差异表达倍数。
6.FDR(False Discovery Rate)即错误发现率,定义为在多重假设检验过程中,错误拒绝(拒绝真的原(零)假设)的个数占所有被拒绝的原假设个数的比例的期望值。
通过控制FDR来决定P值的阈值。
7.P值(P-value)即概率,反映某一事件发生的可能性大小。
统计学根据显著性检验方法所得到的P 值,一般以P<0.05为显著,P<0.01为非常显著,其含义是样本间的差异由抽样误差所致的概率小于0.05或0.01。
8.可变剪接(Alternative splicing)有些基因的一个mRNA前体通过不同的剪接方式(选择不同的剪接位点)产生不同的mRNA剪接异构体,这一过程称为可变剪接(或选择性剪接,alternative splicing)。
单细胞测序 名词解释

单细胞测序名词解释嘿,朋友!今天咱们来聊聊“单细胞测序”这个听起来有点高大上的名词。
你知道吗,细胞就像是我们身体这个大城堡里的一个个小房间。
每个房间都有着独特的功能和秘密。
而单细胞测序,就像是给每个小房间都配备了一把超级精细的钥匙,让我们能够打开门,深入了解里面的一切。
比如说,我们身体里的细胞那可真是五花八门,有负责运输氧气的红细胞,有奋勇杀敌的白细胞,还有勤劳工作的肌肉细胞等等。
以前的技术呢,就像是用一把大扫帚,把一堆细胞一起扫过来研究,可这样根本搞不清楚每个细胞自己的特点和秘密。
单细胞测序可就不一样啦!它能够精准地瞄准每一个单独的细胞,就像狙击手一样,一个一个地把它们的信息都搞清楚。
想象一下,这就好比是一场盛大的舞会,以前我们只能看到一群人在那跳舞,分不清谁是谁。
但单细胞测序能让我们看清每一个舞者的动作、表情和内心的想法。
通过单细胞测序,我们可以知道在某个疾病发生的时候,到底是哪个细胞先“调皮捣蛋”了,哪个细胞还在“坚守岗位”。
这对于疾病的诊断和治疗,那可太重要啦!再比如,在研究肿瘤的时候,单细胞测序能帮我们找到那些隐藏在肿瘤组织里的“坏家伙”细胞,弄清楚它们是怎么发展壮大的,从而为治疗肿瘤找到新的突破口。
这难道不神奇吗?而且啊,单细胞测序还能让我们更清楚地了解细胞的发育过程。
就像是看着一颗小种子是怎么一点点长成参天大树的,每个阶段的变化都能明明白白。
它在免疫学、神经科学等领域也是大显身手呢!总之,单细胞测序就像是给我们打开了一扇通往细胞微观世界的神奇大门,让我们能够更加深入地探索生命的奥秘。
所以说,单细胞测序可不是一般的厉害,它是我们探索生命奥秘的强大工具,能为医学和生物学的发展带来巨大的帮助。
你说,未来它还会给我们带来多少惊喜呢?。
名词专题RNA-seq常见名词解释

名词专题RNA-seq常见名词解释前言各位亲们,文献中的很多名字是否困惑过?别怕!我们会用一个专题来解释相关的名词,以期给各位带来一些帮助。
RNA-seq:基于二代测序技术,研究特定细胞在某一功能状态下所有RNA 的功能,主要包括 mRNA 和非编码RNA。
能够全面快速地获得某一物种特定组织或器官在某一状态下的几乎所有转录本序列信息,已广泛应用于基础研究、临床诊断和药物研发等领域。
Q20,Q30:二代测序中,每测一个碱基会给出一个相应的质量值,这个质量值是衡量测序准确度的。
碱基的质量值20的错误率为1%,30的错误率为0.1%。
Q20与Q30表示质量值≧20或30的碱基所占百分比,如碱基质量值为20则表示该碱基的错误率为10^(20/(-10))=0.01=1%(根据Q=-10lgP计算,P为错误率)intron:内含子,是真核生物细胞DNA 中的间插序列。
这些序列被转录在前体RNA 中,经过剪接被去除,最终不存在于成熟RNA 分子中。
术语内含子也指编码相应RNA 内含子的DNA 中的区域。
exon:外显子,是真核生物基因的一部分,它在剪接(Splicing)后仍会被保存下来,并可在蛋白质生物合成过程中被表达为蛋白质。
外显子是最后出现在成熟RNA 中的基因序列,又称表达序列。
既存在于最初的转录产物中,也存在于成熟的RNA 分子中的核苷酸序列。
术语外显子也指编码相应RNA 外显子的DNA 中的区域。
intergenic:基因间区,指基因与基因之间的间隔序列,不属于基因结构,不直接决定氨基酸,可能通过转录后调控影响性状的区域。
UTR:Untranslated Regions, 非翻译区域。
是信使RNA (mRNA)分子两端的非编码片段。
5'-UTR 从mRNA 起点的甲基化鸟嘌呤核苷酸帽延伸至AUG 起始密码子,3'-UTR 从编码区末端的终止密码子延伸至多聚A 尾巴(Poly-A)的前端。
测序基础知识--整理

测序基础知识--整理测序: 如何计算测序深度,或产出的数据量? 10的9次⽅=1G 如果测序的read是pair-end的、且每条read长150bp,则,平均测序深度为=(reads数×150bp×2)/(3*10的10次⽅)。
即:测序得到的碱基总数/⼈类基因组的碱基对数=平均测序深度。
⽐如,我想得到30x的测序数据,那么需要的数据量是90G的数据。
(此处,还不甚了解,我觉得应该是900G的数据啊) (⼈类基因组有30亿个碱基对(3*10的10次⽅)) 测序错误率:⼀般选择的阀值是10的-3次⽅,即测序错误率是0.001。
(PCR的错误率是10的-6次⽅) coverage与depth的概念:coverage指的是测序数据覆盖的⼈类基因组的碱基数。
depth指的是平均每个碱基被测序read覆盖的次数(即被测到的次数)。
index的含义:index⽤来区分不同的样本。
单端index共6个碱基,排列组合,共4的6次⽅个碱基,⽆法区分66个样本。
故,需要采⽤双端index。
双端index,分为i5和i7端。
i5端有8个碱基,i7端有12个碱基。
测序的cycle:⼀个cycle读取⼀个碱基。
也称为:base call。
若有index序列,则测序仪会多读⼏个cycle。
⽂库构建: 加Y型adapter的⽬的:1)区分read1和read2,即DNA链的两端;2)防⽌adapter⾃连。
Y型adapter不是互补的,两端的序列不⼀致。
10ng的DNA就可以建库,测序。
WGS: 全基因组的重复率是20%,⽤picard统计duplicate的⼯具(原理:map位置相同,cigar值相同)。
建库流程:提取全基因组,打断、末端不平加A,加adapter,PCR扩增,测序。
区别cfDNA的靶向建库:cfDNA已经是断裂的⽚段,所以不需要打断、末端补平加A的步骤,只要提取游离DNA后,⽤引物扩增即可。
测序常用名词解释整理
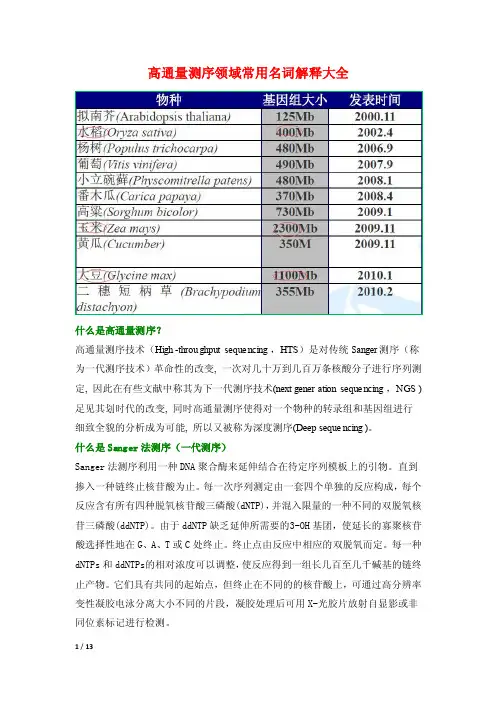
高通量测序领域常用名词解释大全什么是高通量测序?高通量测序技术(High-throug hputsequen cing,HTS)是对传统Sa nger测序(称为一代测序技术)革命性的改变, 一次对几十万到几百万条核酸分子进行序列测定, 因此在有些文献中称其为下一代测序技术(next genera tionsequen cing,NGS )足见其划时代的改变, 同时高通量测序使得对一个物种的转录组和基因组进行细致全貌的分析成为可能,所以又被称为深度测序(Deep sequen cing)。
什么是San ger法测序(一代测序)Sanger法测序利用一种DNA聚合酶来延伸结合在待定序列模板上的引物。
直到掺入一种链终止核苷酸为止。
每一次序列测定由一套四个单独的反应构成,每个反应含有所有四种脱氧核苷酸三磷酸(dNTP),并混入限量的一种不同的双脱氧核苷三磷酸(ddNTP)。
由于ddNT P缺乏延伸所需要的3-OH基团,使延长的寡聚核苷酸选择性地在G、A、T或C处终止。
终止点由反应中相应的双脱氧而定。
每一种dNT Ps和dd NTPs的相对浓度可以调整,使反应得到一组长几百至几千碱基的链终止产物。
它们具有共同的起始点,但终止在不同的的核苷酸上,可通过高分辨率变性凝胶电泳分离大小不同的片段,凝胶处理后可用X-光胶片放射自显影或非同位素标记进行检测。
什么是基因组重测序(Genome Re-sequen cing)全基因组重测序是对基因组序列已知的个体进行基因组测序,并在个体或群体水平上进行差异性分析的方法。
随着基因组测序成本的不断降低,人类疾病的致病突变研究由外显子区域扩大到全基因组范围。
通过构建不同长度的插入片段文库和短序列、双末端测序相结合的策略进行高通量测序,实现在全基因组水平上检测疾病关联的常见、低频、甚至是罕见的突变位点,以及结构变异等,具有重大的科研和产业价值。
测序相关名字注解

1、链特异性建库测序:(mRNA-Seq library(Strand-Specific) construction,ssRNA-Seq)可以确定转录本来自正链还是负链,以便更加准确的获得基因的结构以及基因表达信息,并且可以更好的发现新的基因;但链特异建库在read的随机性分布上略差,而其所得结果其他指标都是比较优秀的,其结果是准确可信的。
测序数据质量评估与预处理:质量控制Quality Control:FastQC、Fastx-toolkit 拼接Aligner:BWA,Bowtie, Tophat, SOAP2 Mapper:Tophat, Cufflinks基因定量Gene Quantification: Cufflinks, Avadis NGS质量改进Quality improvement:?Genome Analysis Toolkit(GATK)SNP: Unified Genotyper,Glfmultiple, SAMtools, Avadis NGSCNV: CNVnator Indel: Pindel, Dindel, Unified Genotyper, Avadis NGSMapping to a gene: Cufflinks, Rsamtools,?Genomic FeaturesQC分析:QUALITY CONTROL,检查表、层别法、柏拉图、因果图、散布图、直方图、管制图2、差异整合分析:Meta-analysis,对若干独立研究的统计结果进行综合差异的定量分析表达模式分析:分析基因如何表达的。
就是从DNA到蛋白质的过程,这个过程是如何进行的就是它的模式GO富集分析:可分为分子功能(Molecular Function),生物过程(biological process)和细胞组成(cellular component)三个部分。
蛋白质或者基因可以通过ID对应或者序列注释的方法找到与之对应的GO号,而GO号可对于到Term,即功能类别或者细胞定位。
测序常用名词解释整理
高通量测序领域常用名词解释大全什么是高通量测序?高通量测序技术(High-throughput sequencin,g HTS)是对传统Sanger测序(称为一代测序技术)革命性的改变, 一次对几十万到几百万条核酸分子进行序列测定, 因此在有些文献中称其为下一代测序技术(next generation sequencin,g NGS )足见其划时代的改变, 同时高通量测序使得对一个物种的转录组和基因组进行细致全貌的分析成为可能, 所以又被称为深度测序(Deep sequencing。
)什么是Sanger法测序(一代测序)Sanger法测序利用一种DNA 聚合酶来延伸结合在待定序列模板上的引物。
直到掺入一种链终止核苷酸为止。
每一次序列测定由一套四个单独的反应构成,每个反应含有所有四种脱氧核苷酸三磷酸(dNTP),并混入限量的一种不同的双脱氧核苷三磷酸(ddNTP)。
由于ddNTP 缺乏延伸所需要的3-OH 基团,使延长的寡聚核苷酸选择性地在G、A、T 或C 处终止。
终止点由反应中相应的双脱氧而定。
每一种dNTPs 和ddNTPs 的相对浓度可以调整,使反应得到一组长几百至几千碱基的链终止产物。
它们具有共同的起始点,但终止在不同的的核苷酸上,可通过高分辨率变性凝胶电泳分离大小不同的片段,凝胶处理后可用X-光胶片放射自显影或非同位素标记进行检测。
什么是基因组重测序(Genome Re-sequencin)g全基因组重测序是对基因组序列已知的个体进行基因组测序,并在个体或群体水平上进行差异性分析的方法。
随着基因组测序成本的不断降低,人类疾病的致病突变研究由外显子区域扩大到全基因组范围。
通过构建不同长度的插入片段文库和短序列、双末端测序相结合的策略进行高通量测序,实现在全基因组水平上检测疾病关联的常见、低频、甚至是罕见的突变位点,以及结构变异等,具有重大的科研和产业价值。
什么是de novo 测序de novo 测序也称为从头测序:其不需要任何现有的序列资料就可以对某个物种进行测序,利用生物信息学分析手段对序列进行拼接,组装,从而获得该物种的基因组图谱。
sanger测序法名词解释
sanger测序法名词解释Sanger测序法是一种常用的DNA测序技术。
下面是一些相关名词的解释:1. 测序:测序是指确定DNA序列的过程。
Sanger测序法是一种历史悠久且经典的测序方法,通过测量DNA链延伸反应中的DNA碱基,逐个确定DNA序列。
2. DNA:脱氧核糖核酸(Deoxyribonucleic Acid),是构成生物基因的分子,携带着生物遗传信息。
3. 碱基:DNA分子的组成单位,有四种碱基:腺嘌呤(Adenine)、鸟嘌呤(Guanine)、胸腺嘧啶(Thymine)、胞嘧啶(Cytosine)。
DNA的序列是由这四种碱基的不同排列组合而成。
4. 末端标记:Sanger测序法中,DNA的一条链被标记,通常使用荧光染料标记DNA的3'末端。
5. 核酸酶:酶是一种催化生化反应的蛋白质。
Sanger测序法中使用核酸酶,在特定条件下,通过特异性水解特定的核酸链,以确定DNA的碱基序列。
6. Dideoxy链终止法:Sanger测序法又称为dideoxy链终止法,它利用特殊的二进制去氧核糖核苷酸(dideoxynucleotide)来终止DNA链的延伸反应。
不同的二进制去氧核糖核苷酸通过荧光染料标记,然后通过凝胶电泳分离和检测,最终确定DNA的碱基序列。
7. 凝胶电泳:一种分离生物大分子(如DNA)的方法,通过将DNA放置于聚丙烯酰胺凝胶中,通过电流进行分离,根据DNA片段的大小来分析和确定DNA的碱基序列。
8. 自动测序:自动测序技术是对Sanger测序法的改进,使用高效的电泳和光学系统、电脑控制等技术来加快测序速度和提高测序质量。
与传统的手工测序相比,自动测序更准确、高通量。
高通量测序科研入门常用名词意义整理
微生物高通量测序相关名词概念解析作者:happy目录一、OTU分类和统计 (2)二、生物信息分析 (2)三、16SrRNA (3)四、Alpha多样性 (4)五、稀疏性分析(rarefaction analysis)和稀疏性曲线(rarefaction curve) (7)六、Shannon-Weiner指数 (8)七、Rank Abundance 曲线 (9)八、微生物种属鉴定及相关分析 (10)九、OTU群落聚类及相关分析 (14)十、Rank Abundance 曲线 (15)十一、韦恩图(Venn) (16)一、OTU分类和统计OTU(operationaltaxonomicunits)是在系统发生学研究或群体遗传学研究中,为了便于进行分析,人为给某一个分类单元(品系,种,属,分组等)设置的同一标志。
通常按照97%的相似性阈值将序列划分为不同的OTU,每一个OTU通常被视为一个微生物物种。
相似性小于97%就可以认为属于不同的种,相似性小于93%-95%,可以认为属于不同的属。
样品中的微生物多样性和不同微生物的丰度都是基于对OTU的分析。
Coverage是指各样品文库的覆盖率,其数值越高,则样本中序列没有被测出的概率越低。
该指数实际反映了本次测序结果是否代表样本的真实情况。
计算公式为:C=1-n1/N其中n1=只含有一条序列的OTU的数目;N=抽样中出现的总的序列数目。
分类水平统计表主要是对每个样本在分类学水平上的数量进行统计,并且在表格中列出了在每个分类学水平上的物种数目(只显示前10个样本,如果样本超过10个,请查看结果中taxon_all.txt文件)其中SampleName表示样本名称;Phylum表示分类到门的OTU数量;Class表示分类到纲的OTU数量;Order表示分类到目的OTU数量;Family表示分类到科的OTU数量;Genus表示分类到属的OTU数量;Species表示分类到种的OTU数量。
高通量测序,名词解释
高通量测序基础知识汇总一代测序技术:即传统的Sanger测序法,Sanger法是根据核苷酸在待定序列模板上的引物点开始,随机在某一个特定的碱基处终止,并且在每个碱基后面进行荧光标记,产生以A、T、C、G结束的四组不同长度的一系列核苷酸,每一次序列测定由一套四个单独的反应构成,每个反应含有所有四种脱氧核苷酸三磷酸(dNTP),并混入限量的一种不同的双脱氧核苷三磷酸(ddNTP)。
由于ddNTP缺乏延伸所需要的3-OH基团,使延长的寡聚核苷酸选择性地在G、A、T或C处终止,使反应得到一组长几百至几千碱基的链终止产物。
它们具有共同的起始点,但终止在不同的的核苷酸上,可通过高分辨率变性凝胶电泳分离大小不同的片段,通过检测得到DNA碱基序列。
二代测序技术:next generation sequencing(NGS)又称为高通量测序技术,与传统测序相比,二代测序技术可以一次对几十万到几百万条核酸分子同时进行序列测定,从而使得对一个物种的转录组和基因组进行细致全貌的分析成为可能,所以又被称为深度测序(Deep sequencing)。
NGS主要的平台有Roche(454 & 454+),Illumina(HiSeq 2000/2500、GA IIx、MiSeq),ABI SOLiD等。
基因:Gene,是遗传的物质基础,是DNA或RNA分子上具有遗传信息的特定核苷酸序列。
基因通过复制把遗传信息传递给下一代,使后代出现与亲代相似的性状。
DNA:Deoxyribonucleic acid,脱氧核糖核酸,一个脱氧核苷酸分子由三部分组成:含氮碱基、脱氧核糖、磷酸。
脱氧核糖核酸通过3',5'-磷酸二酯键按一定的顺序彼此相连构成长链,即DNA链,DNA链上特定的核苷酸序列包含有生物的遗传信息,是绝大部分生物遗传信息的载体。
RNA:Ribonucleic Acid,,核糖核酸,一个核糖核苷酸分子由碱基,核糖和磷酸构成。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高通量测序领域常用名词解释大全什么是高通量测序?高通量测序技术(High-throughput sequencing,HTS)是对传统Sanger测序(称为一代测序技术)革命性的改变, 一次对几十万到几百万条核酸分子进行序列测定, 因此在有些文献中称其为下一代测序技术(next generation sequencing,NGS )足见其划时代的改变, 同时高通量测序使得对一个物种的转录组和基因组进行细致全貌的分析成为可能, 所以又被称为深度测序(Deep sequencing)。
什么是Sanger法测序(一代测序)Sanger法测序利用一种DNA聚合酶来延伸结合在待定序列模板上的引物。
直到掺入一种链终止核苷酸为止。
每一次序列测定由一套四个单独的反应构成,每个反应含有所有四种脱氧核苷酸三磷酸(dNTP),并混入限量的一种不同的双脱氧核苷三磷酸(ddNTP)。
由于ddNTP缺乏延伸所需要的3-OH基团,使延长的寡聚核苷酸选择性地在G、A、T或C处终止。
终止点由反应中相应的双脱氧而定。
每一种dNTPs和ddNTPs的相对浓度可以调整,使反应得到一组长几百至几千碱基的链终止产物。
它们具有共同的起始点,但终止在不同的的核苷酸上,可通过高分辨率变性凝胶电泳分离大小不同的片段,凝胶处理后可用X-光胶片放射自显影或非同位素标记进行检测。
什么是基因组重测序(Genome Re-sequencing)全基因组重测序是对基因组序列已知的个体进行基因组测序,并在个体或群体水平上进行差异性分析的方法。
随着基因组测序成本的不断降低,人类疾病的致病突变研究由外显子区域扩大到全基因组范围。
通过构建不同长度的插入片段文库和短序列、双末端测序相结合的策略进行高通量测序,实现在全基因组水平上检测疾病关联的常见、低频、甚至是罕见的突变位点,以及结构变异等,具有重大的科研和产业价值。
什么是de novo测序de novo测序也称为从头测序:其不需要任何现有的序列资料就可以对某个物种进行测序,利用生物信息学分析手段对序列进行拼接,组装,从而获得该物种的基因组图谱。
获得一个物种的全基因组序列是加快对此物种了解的重要捷径。
随着新一代测序技术的飞速发展,基因组测序所需的成本和时间较传统技术都大大降低,大规模基因组测序渐入佳境,基因组学研究也迎来新的发展契机和革命性突破。
利用新一代高通量、高效率测序技术以及强大的生物信息分析能力,可以高效、低成本地测定并分析所有生物的基因组序列。
测序名词关系图什么是fragmentsfragments 就是打成的片段,而测序测的就是这些fragments,测出来的结果就是reads,又可以分为单端侧和双端侧,单端测序的话,只是从fragments的一端测序,测多长read就多长,双端测序就是从一个fragments的两端测,就会得出两个reads什么是Reads高通量测序平台产生的序列就称为reads。
(测序读到的碱基序列片段,测序的最小单位;)什么是Contig拼接软件基于reads之间的overlap区,拼接获得的序列称为Contig(重叠群)。
(由reads通过对overlap区域拼接组装成的没有gap的序列段;)什么是Contig N50Reads拼接后会获得一些不同长度的Contigs。
将所有的Contig长度相加,能获得一个Contig总长度。
然后将所有的Contigs按照从长到短进行排序,如获得Contig 1,Contig 2,Contig 3...………Contig 25。
将Contig按照这个顺序依次相加,当相加的长度达到Contig总长度的一半时,最后一个加上的Contig 长度即为Contig N50。
举例:Contig 1+Contig 2+ Contig 3 +Contig 4=Contig总长度*1/2时,Contig 4的长度即为Contig N50。
Contig N50可以作为基因组拼接的结果好坏的一个判断标准。
什么是Scaffold基因组de novo测序(没有参考基因组的测序,需要研究人员从头拼接得到的序列),通过reads拼接获得Contigs后,往往还需要构建454 Paired-end库或Illumina Mate-pair库,以获得一定大小片段(如3Kb、6Kb、10Kb、20Kb)两端的序列。
基于这些序列,可以确定一些Contig之间的顺序关系,这些先后顺序已知的Contigs组成Scaffold。
(通过pair ends信息确定出的contig排列,中间有gap)什么是Scaffold N50Scaffold N50与Contig N50的定义类似。
Contigs拼接组装获得一些不同长度的Scaffolds。
将所有的Scaffold长度相加,能获得一个Scaffold总长度。
然后将所有的Scaffolds按照从长到短进行排序,如获得Scaffold 1,Scaffold 2,Scaffold 3...………Scaffold 25。
将Scaffold按照这个顺序依次相加,当相加的长度达到Scaffold总长度的一半时,最后一个加上的Scaffold长度即为Scaffold N50。
举例:Scaffold 1+Scaffold 2+ Scaffold 3 +Scaffold 4 +Scaffold 5=Scaffold总长度*1/2时,Scaffold 5的长度即为Scaffold N50。
Scaffold N50可以作为基因组拼接的结果好坏的一个判断标准。
什么是测序深度和覆盖度测序深度:是指测序得到的总碱基数与待测基因组大小的比值。
假设一个基因大小为2M,测序深度为10X,那么获得的总数据量为20M。
覆盖度:是指测序获得的序列占整个基因组的比例。
Gap:由于基因组中的高GC、重复序列等复杂结构的存在,测序最终拼接组装获得的序列往往无法覆盖有所的区域,这部分没有获得的区域就称为。
例如一个细菌基因组测序,覆盖度是98%,那么还有2%的序列区域是没有通过测序获得的。
什么是RPKM、FPKMRPKM,Reads Per Kilobase of exon model per Million mapped reads, is defined in thisway [Mortazavi etal., 2008]:每1百万个map上的reads中map到外显子的每1K个碱基上的reads个数。
假如有1百万个reads映射到了人的基因组上,那么具体到每个外显子呢,有多少映射上了呢,而外显子的长度不一,那么每1K个碱基上又有多少reads映射上了呢,这大概就是这个RPKM的直观解释。
如果对应特定基因的话,那么就是每1000000 mapped到该基因上的reads中每kb有多少是mapped到该基因上的exon的readTotal exon reads:This is the number in the column with header Total exonreads in the row for the gene. This is the number of reads that have beenmapped to a region in which an exon is annotated for the gene or across theboundaries of two exons or an intron and an exon for an annotated transcript ofthe gene. For eukaryotes, exons and their internal relationships are defined byannotations of type mRNA.映射到外显子上总的reads个数。
这个是映射到某个区域上的reads个数,这个区域或者是已知注释的基因或者跨两个外显子的边界或者是某个基因已经注释的转录本的内含子、外显子。
对于真核生物来说,外显子和它们自己内部的关系由某类型的mRNA来注释。
Exonlength: This is the number in the column with the header Exon length inthe row for the gene, divided by 1000. This is calculated as the sum of thelengths of all exons annotated for the gene. Each exon is included only once inthis sum, even if it is present in more annotated transcripts for the gene.Partly overlapping exons will count with their full length, even though theyshare the same region.外显子的长度。
计算时,计算所有某个基因已注释的所有外显子长度的总和。
即使某个基因以多种注释的转录本呈现,这个外显子在求和时只被包含一次。
即使部分重叠的外显子共享相同的区域,重叠的外显子以其总长来计算。
Mapped reads: The sum of all the numbers in the column with headerTotalgene reads. The Total gene reads for a gene is the total number ofreads that after mapping have been mapped to the region of the gene. Thus thisincludes all the reads uniquely mapped to the region of the gene as well asthose of the reads which match in more places (below the limit set in thedialog in figure 18.110) that have been allocated tothis gene's region. A gene's region is that comprised of the flanking regions(if it was specified in figure 18.110), the exons, the introns andacross exon-exon boundaries of all transcripts annotated for the gene. Thus,the sum of the total gene reads numbers is the number of mapped reads for thesample (you can find the number in the RNA-Seq report).map的reads 总和。
