常见的酸和碱第二课时常见的酸
常见的酸和碱(第2课时)(课件)九年级化学下册(沪教版)

交流讨论:
为什么不同的酸有一些相似的化学性质?
HCl = H+ + Cl-
H2SO4 = 2H+ + SO42-
酸在水溶液中都能解离出H+和酸根离子, 即在不同的酸溶液中都含有相同的H+, 所以酸有一些相似的性质。
二、酸的用途
酸与指示剂的作用
一、酸的化学性质
1. 酸与指示剂作用
点滴板
优点: 显色明显、 便于对比、 节约药品 。
稀盐酸 稀硫酸
紫色石蕊试液
变红 变红
无色酚酞试液
不变色 不变色
一、酸的化学性质
2. 酸与活泼金属反应
共同现象是:金属___逐__渐__溶__解____,并产生___气__泡____。
注意:铁与酸反应还会看到溶液由 无 色逐渐变为
一、酸的化学性质
(2)酸与氧化铜反应
现象: ① 黑 色的氧化铜逐渐 消失 ;
溶液中含有Cu2+呈蓝色
②溶液由 无 色逐渐变为 蓝 色。
反应方程式:
CuO + 2 HCl = CuCl2 + H2O CuO + H2SO4 = CuSO4 + H2O
一、酸的化学性质
4. 酸与金属氧化物反应
酸 + 金属氧化物 → 盐 + 水
第7章 应用广泛的酸、碱、盐
第2节 常见的酸和碱
(第2课时)
【学习目标】 1. 认识盐酸、稀硫酸的主要化学性质。 2. 认识金属活动性顺序,并能对常见金属能否与 稀盐酸(或稀硫酸)发生置换反应进行判断。
常见的酸和碱PPT课件53 人教版优质课件

把浓硫酸滴到一小 块布上
会穿洞,并变成黑色
浓硫酸有腐蚀性-----脱水性
浓
在稀释浓硫酸
硫 酸
时,一定要把浓
稀
硫酸沿器壁慢
释 的 正
慢注入水里,并 不断搅拌.切不
确
可将水倒进浓
操 作
硫酸里.
浓 硫 酸
水的密度较小, 浮在浓硫酸上 面,溶解时放出
稀
的热会使水立
释
刻沸腾,使硫酸
的 错 误 操
液滴向四周飞 溅,这是非常危 险的.
盐+酸=新盐+新酸
16 、生命的奖赏远在旅途终点,而非起点附近。我不知道要走多少步才能达到目标,踏上第一千步的时候,仍然可能遭到失败。但我不会因此放弃,我会坚持不懈,直至成功! 1 、成功就是凭着勇气和努力,不断地超越自己,做最好的自己。 3 、行动是通向成功的唯一途径。 18 、天使之所以会飞,是因为她们把自己看得很轻… 15 、甘其食,美其服,安其居,乐其俗。邻国相望,鸡犬之声相闻,民至老死,不相往来。 6 、我相信,无论今后的道路多么坎坷,只要抓住今天,迟早会在奋斗中尝到人生的甘甜。抓住人生中的一分一秒,胜过虚度中的一月一年! 9 、祸兮福之所倚,福兮祸之所伏。孰知其极?其无正也。正复为奇,善复为妖。人之迷,其日固久。 4 、成功离你很近,只要再多一点点坚持,你就会尝到胜利的果实。 7 、准备种子,就收获果实;准备努力,就收获成功;准备今天,就收获明天。 16 、生命的奖赏远在旅途终点,而非起点附近。我不知道要走多少步才能达到目标,踏上第一千步的时候,仍然可能遭到失败。但我不会因此放弃,我会坚持不懈,直至成功! 17 、人生伟业的建立,不在能知,乃在能行。 19 、做任何事都要经受得挫折,要有恒心和毅力,满怀信心坚持到底。 3 、有大目标,须有大动作;有大追求,须有大改变。 17 、只有满怀勇气,不畏艰辛,才能获得更大的成功。 6 、大成若缺,其用不弊。大盈若冲,其用不穷。大直若屈,大巧若拙,大辩若讷。 14 、自动自发地做事,同时为自己的所作所为承担责任,那么你终究会获得回报,取得最后的成功。 9 、眼泪不是我们的答案,拼搏才是我们的选择。 20 、想停下来深情地沉湎一番,怎奈行驶的船却没有铁锚;想回过头去重温旧梦,怎奈身后早已没有了归途。因为时间的钟摆一刻也不曾停顿过,所以生命便赋予我们将在汹涌的大潮之中不停地 颠簸。
第七章 第二节 常见的酸和碱ppt课件

干燥原理:干燥剂只吸收水分, 但不与被干燥的气体发生反应。
注意:长管进,短 管出(长进短出)
H2、H2O
H2
哪些气体能用浓硫酸来干 燥?哪些不能用?
通入液面下
不能干燥 :
能干燥
碱性气体:NH3 中性气体:H2、O2
酸性气体精品:pptCO2 、SO2、 HCl
洗气瓶
6
精品ppt
7
浓硫酸的腐蚀性
脱水性
注意:单质的铁和酸反应只能生成+2价的亚铁
化合物的铁和酸反应,反应前后铁元素的化合价不变
精品ppt
21
如果把上述实验中的稀盐酸换成稀硫酸,
你认为是否会产生类似的实验现象?
请试着写出这些反应的化学方程式。
Mg + H2SO4 = MgSO4 + H2↑
Fe + H2SO4 = FeSO4 + H2 ↑
氧化性:能与金属铜等反应。
精品ppt
16
二、浓硫酸的腐蚀性
纸张的笔画 木棒上蘸有浓硫 滴到酸的布 部分变黑 酸的部分变黑 由黄变黑
浓硫酸有很强的腐蚀性,能使纸张、 木条、布甚至皮肤脱水而腐蚀
使用浓硫酸要特别小心
精品ppt
17
探究二:稀硫酸和稀盐酸的化学性质
用稀硫酸和稀盐酸做几个简单的实验,把观察到 的现象填入下表,并与同学们讨论以下问题:
HCl 无色
液体 具有刺激性气味 比水的密度小 有白雾产生
挥发性
稀释浓硫酸的方法:
将浓硫酸沿着器壁慢慢注入水中 ,并不断搅拌。切不可将水倒入浓
硫酸中。
精品ppt
10
使用浓硫酸注意的问题: 1、浓硫酸的稀释方法:
稀释浓硫酸时,一定要把浓硫酸沿着器壁慢慢注入水里, 并用玻璃棒不断搅拌。 切不可将水倒进浓硫酸里!
2023化学《常见的酸和碱》教案

2023化学《常见的酸和碱》教案2023化学《常见的酸和碱》教案1【教学目标】1.知识与技能(1)了解常见酸碱指示剂及其变色情况。
(2)了解几种常见的酸及酸的通性。
(3)认识浓硫酸的腐蚀性。
2.过程与方法(1)进一步认识和体验科学探究的过程。
(2)运用实验的方法获取信息,运用比较概括的方法对获取的信息进行加工。
3.情感态度与价值观增强对化学现象的探究欲,培养善于合作、勤于思考的科学精神。
【教学重点】1.运用酸碱指示剂检验溶液的酸碱性。
2.浓硫酸的腐蚀性。
3.酸的化学性质。
【教学难点】1.酸碱指示剂的变色情况。
2.酸的化学性质。
【教具准备】白醋、苹果汁、石灰水、盐酸、氢氧化钠溶液、酚酞溶液、石蕊溶液、试管(若干)、牵牛花、万寿菊、蝴蝶兰花、玫瑰、月季、紫甘蓝、硫酸、玻璃棒等。
【导入新课】在日常生活中,你听说过、接触过酸和碱吗?【交流回答】接触过的酸有:碳酸、醋酸、盐酸、硫酸;碱有:氨水、石灰水、烧碱。
【提出问题】用什么较简单的方法区分酸和碱呢?【展示交流】请同学们做教材P50实验10-1,交流实验结果。
【阅读记忆】请同学们阅读并理解教材P51内容,归纳什么叫指示剂?指示剂遇酸和碱溶液变色有什么规律?【阅读回答】石蕊试液遇酸溶液变红,遇碱溶液变蓝;酚酞溶液遇酸溶液不变色,遇碱溶液变红。
【提出问题】请同学讨论白醋、石灰水、盐酸、氢氧化钠溶液这4种物质中,哪些可能是酸溶液,哪些可能是碱溶液。
【交流回答】白醋,盐酸是酸溶液;石灰水,氢氧化钠是碱溶液。
【归纳总结】检验溶液酸碱性的方法:取少量溶液,滴入几滴石蕊试液,若溶液呈红色,则说明该溶液为酸性溶液,若溶液呈蓝色,则说明该溶液为碱性溶液。
【过渡】酸碱指示剂的种类很多,不只是石蕊试液和酚酞试液。
在日常生活中指示剂随处可见,同学们可通过后面的活动体验一下。
【活动与探究1】请同学们按教材P51“探究”进行实验,并做好实验记录。
【展示交流】实验完成后请各组同学展示你们的实验成果。
初中中考化学知识点常见的酸和碱
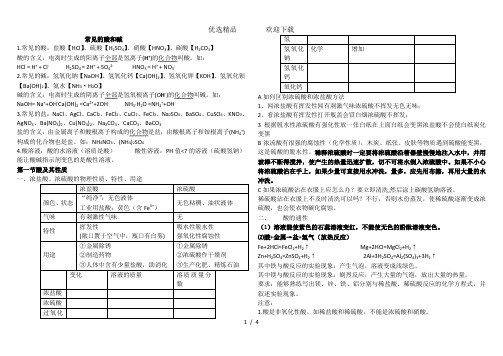
常见的酸和碱1.常见的酸:盐酸【HCl】、硫酸【H2SO4】、硝酸【HNO3】、碳酸【H2CO3】酸的含义:电离时生成的阳离子全部是氢离子(H+)的化合物叫酸。
如:HCl = H+ + Cl- H2SO4 = 2H+ + SO42- HNO3 = H+ + NO3-2.常见的碱:氢氧化钠【NaOH】、氢氧化钙【Ca(OH)2】、氢氧化钾【KOH】、氢氧化钡【Ba(OH)2】、氨水【NH3·H2O】碱的含义:电离时生成的阴离子全部是氢氧根离子(O H-)的化合物叫碱。
如:NaOH= Na++OH-Ca(OH)2 =Ca2++2OH-NH3·H2O =NH4++OH-3.常见的盐:NaCl、AgCl、CaCl2、FeCl2、CuCl2、FeCl3、Na2SO4、BaSO4、CuSO4、KNO3、AgNO3、Ba(NO3)2、Cu(NO3)2、Na2CO3、CaCO3、BaCO3盐的含义:由金属离子和酸根离子构成的化合物是盐;由酸根离子和铵根离子(NH4+)构成的化合物也是盐。
如:NH4NO3、(NH4)2SO44.酸溶液:酸的水溶液(溶质是酸)酸性溶液:PH值<7的溶液(硫酸氢钠)能让酸碱指示剂变色的是酸性溶液。
第一节酸及其性质一、浓盐酸、浓硫酸的物理性质、特性、用途1.4.8.A如何区别浓硫酸和浓盐酸方法1、闻浓盐酸有挥发性闻有刺激气味浓硫酸不挥发无色无味;2、看浓盐酸有挥发性打开瓶盖会冒白烟浓硫酸不挥发;3 根据脱水性浓硫酸有强化性放一张白纸在上面白纸会变黑浓盐酸不会使白纸炭化变黑B浓流酸有很强的腐蚀性(化学性质),木炭、纸张、皮肤等物质遇到硫酸能变黑,这是硫酸的脱水性。
稀释浓硫酸时一定要将浓硫酸沿着器壁慢慢地注入水中,并用玻棒不断得搅拌,使产生的热量迅速扩散,切不可将水倒入浓硫酸中。
如果不小心将浓硫酸沾在手上,如果少量可直接用水冲洗,量多,应先用布擦,再用大量的水冲洗。
《常见的酸和碱》PPT精品课件(第2课时)

硫酸 H2SO4
重要化工原料。用于生产化肥、农药、火药、染料以及冶炼金属、精炼 石油和金属除锈等。
浓硫酸有吸水性,在实验室中常用它做干燥剂。(不能干燥氨气)
实验
用玻璃棒蘸浓硫酸在纸上 写字
放置一会儿后的现象 纸上显出黑色字迹
用小木棍蘸 少量浓硫酸
蘸有硫酸的部位变黑
将浓硫酸滴到 一小块布上
滴有硫酸的部位变黑甚至烧成洞
慢慢倒
不断搅拌
浓硫酸
酸入水
水 沿内壁
简记: 酸入水中, 不断搅拌!
手的感觉 分析
发热或烫 浓硫酸溶于水放热
思考:如果不慎将浓硫酸沾到皮肤或衣服上,应如何处理?
立即用大量水冲洗,再涂上3%-5%的碳酸氢钠溶液。
思考:如果不慎将稀硫酸沾到皮肤或衣服上,是否也要进行这样的处理?为什 么? • 当稀硫酸沾到皮肤或衣服上,也必须及时这样处理,因为稀硫酸长期露置在空
愿知识与您相伴 让我们共同成长 感谢您的阅读与支持
1.浓盐酸、浓硫酸的物理性质 2.浓硫酸的特性:吸水性、脱水性、腐蚀性。 3.酸有一些相似的化学性质 (1)能使酸碱指示剂显示不同的颜色。 (2)能与多种活泼金属反响,生成氢气 Zn+H2SO4=ZnSO4+H2↑ (3)能与某些金属氧化物反响,生成水。 CuO+H2SO4=CuSO4+H2O
A 1、以下有关酸的说法中,正确的选项是〔 〕
锌
Zn+2HCl=ZnCl2 +H2 ↑
铁
Fe+2HCl=FeCl2 +H2↑
与稀硫酸反应
Mg+H2SO4=MgSO4+H2 ↑ Zn+H2SO4=ZnSO4+H2 ↑ Fe+H2SO4=FeSO4+H2↑
人教版九年级化学下册复习优秀教学案例:10.1常见的酸和碱(第二课时)

1.生活实例导入:通过展示酸雨对环境的影响,引发学生对酸碱知识的兴趣,使他们能够主动参与到课堂学习中。这种教学方式体现了“从生活到化学”的理念,有助于提高学生的学习积极性。
2.问题导向:本节课以问题为导向,引导学生深入思考和探讨酸碱中和反应的实际应用。通过解答问题,学生能够更好地理解和掌握酸碱知识,提高他们的问题解决能力。
3.小组合作:将学生分成小组,让他们在合作中探究酸碱中和反应的原理和应用。这种教学方式培养了学生的团队合作意识和沟通能力,有助于提高他们的实践能力。
4.实验操作:本节课注重实验教学,让学生亲身体验酸碱的变化。通过实验操作,学生能够更好地理解和掌握酸碱知识,提高他们的实验技能。
5.总结归纳:在课堂结束后,引导学生对自己的学习进行反思和总结,使学生能够自主构建酸碱知识体系。这种教学方式有助于提高学生的归纳总结能力,培养他们的自主学习能力。
为了达到以上教学目标,我准备了一系列教学资源,如实验器材、多媒体课件和习题。在教学过程中,我将注重启发式教学,引导学生主动探究,培养他们的创新精神和团队合作意识。同时,我会关注每一个学生的学习情况,及时给予反馈和指导,确保他们能够达到本节课的学习要求。
二、教学目标
(一)知识与技能
1.掌握酸碱中和反应的概念,了解中和反应的特点及应用。
2.学生通过对比、归纳、总结,自主构建酸碱知识体系。
3.强调酸碱知识在生活中的重要性,激发学生的学习兴趣。
(五)作业小结
1.布置作业:让学生设计一个关于酸碱中和反应的实验,并进行实验操作。
2.要求学生在作业中总结实验原理、操作步骤、实验现象及结论。
3.教师批改作业,及时了解学生的学习情况,给予反馈和指导。
三、教学策略
(一)情景创设
初中化学九年级下册-课题1 常见的酸和碱(第2课时 常见的酸)教案

课题1 常见的酸和碱第2课时常见的酸一、教学目标1.熟悉常见的酸——盐酸和硫酸的物理性质和用途;2.了解浓硫酸的特性,掌握浓硫酸的稀释方法;3.通过活动与探究,掌握酸的化学性质。
二、教学重难点重点:酸的化学性质。
难点:浓硫酸的稀释方法。
三、教学过程【知识回顾】请同学们写出所学过的有酸参与的化学反应的化学方程式。
【总结与交流】①CaCO3+2HCl=CaCl2+H2O+CO2↑②Na2CO3+2HCl=2NaCl+H2O+CO2↑③Zn+H2SO4=ZnSO4+H2↑④Fe+H2SO4=FeSO4+H2↑⑤Mg+2HCl=MgCl2+H2↑……【过渡】反应①是实验室制取二氧化碳的反应原理,反应③是实验室制取氢气的反应原理,所以盐酸和硫酸是我们在实验室中经常用到的酸,另外硝酸和醋酸也是实验室中常见的酸,那么这些酸具有哪些物理性质和化学性质呢?本节课我们一起探究吧!【实验探究】(1)观察盐酸、硫酸的颜色和状态;(2)分别打开盛有盐酸,硫酸的试剂瓶的瓶盖,观察现象并闻气味。
(注意闻气味的正确操作)【实验记录】【交流讨论】打开浓盐酸的瓶盖出现白雾的原因是什么?【总结与交流】浓盐酸具有挥发性,浓盐酸中挥发出的氯化氢气体遇到空气中的水蒸气生成的盐酸小液滴。
【交流讨论】现在有两瓶装着盐酸和硫酸的未贴标签的试剂瓶,根据它们的物理性质,你知道该如何区分它们吗?【总结与交流】轻轻摇晃观察液体是否黏稠、打开瓶盖看其是否出现白雾、闻其是否有刺激性气味等。
【学生活动】根据课本52页表格内容,总结硫酸和盐酸各有什么用途?【总结】生产、生活中很多地方都要用到盐酸和硫酸。
盐酸常用于金属除锈、制造含氯的药物,如生活中的洁厕灵等。
人的胃液中含有盐酸用以帮助消化。
硫酸也可用于金属除锈,还广泛用于生产化肥、农药、火药、冶炼金属、精炼石油等。
浓硫酸具有吸水性,还可以用作实验室里的干燥剂。
【交流讨论】两试剂瓶分别敞口放置的浓盐酸和浓硫酸,过一段时间后,该溶液的溶质质量分数会有什么变化,为什么?【总结与交流】浓盐酸易挥发,溶解的氯化氢气体易扩散到空气中,造成溶液的溶质质量分数变小;浓硫酸具有吸水性,易吸收空气中的水蒸气,造成溶质质量分数也变小。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
加紫色 加无色 石蕊溶液 酚酞溶液
稀盐酸 变红色 无变化
稀硫酸 变红色 无变化
结论: 石蕊试液遇酸变成红色,酚酞试液遇酸不变色。
课题1 常见的酸和碱
(2)酸溶液能与某些金属反应:(请回忆并填表)
与稀盐酸反应 镁 Mg+2HCl=MgCl2 +H2 ↑ 锌 Zn+2HCl=ZnCl2 +H2 ↑ 铁 Fe+2HCl=FeCl2 +H2↑
这两个实验在装置上 和操作顺序上有哪些 不同?我们如何选择 正确稀释呢?
硫酸液 滴向四 周飞溅
课题1 常见的酸和碱
问:浓硫酸有很强的腐蚀性,万一不慎将浓硫酸沾到皮肤 或衣服上,应如何处理? 应立即用大量水冲洗,然后涂上3%-5%的碳酸氢钠溶液。 3、酸的化学性质
活动与探究 (1) 酸溶液能与指示剂反应:
剂。
认识生活中的酸
食醋中含有醋酸,水 果中含有柠檬酸,蓄 电池中含有硫酸。
课题1 常见的酸和碱
2、浓硫酸的腐蚀性
[实验10-3]将纸、小木棍、布放在玻璃片上做实验。
实 验 放置一会儿后的现象
原理
用玻璃棒蘸浓硫 纸上显出黑色字迹 酸在纸上写字
用小木棍蘸 蘸有硫酸的部位变黑 少量浓硫酸 将浓硫酸滴到 滴有硫酸的部位变 一小块布上 黑甚至烧成洞
课题1 常见的酸和碱
课题1 常见的酸和碱
第二课时 常见的酸
课题1 常见的酸和碱
一、常见的酸
1、几种常见的酸
[实验10-2]
(1)观察盐酸、硫酸的颜色和状态
(2)分别打开盛有盐酸、硫酸的试剂瓶的瓶盖,观察现
象并闻气味。
浓盐酸
浓硫酸
颜色、状 态
无色液体 无色粘稠油状液体
打开瓶盖 有强挥发性,在空 不易挥发 后的现象 气中会形成白雾 有吸水性
浓硫酸能夺取
含碳、氢、氧等 元素组成的化合 物里的水分 ( 氢、 氧元素 ), 生成黑 色的炭和水。
课题1 常见的酸和碱
如何稀释浓硫酸
[实验10-4]将浓硫酸沿烧杯壁缓慢地注入盛有水的烧杯里, 用玻璃棒不断搅动,并用手接触烧杯外壁。
手的感觉
发热或烫
分 析 浓硫酸溶于水放热
[实验10-5]将水注入到浓硫酸中
与稀硫酸反应 Mg+H2SO4=MgSO4+H2 ↑ Zn+H2SO4=ZnSO4+H2 ↑ Fe+H2SO4=FeSO4+H2↑
讨论:上面反应的生成物有什么共同之处? 上述反应都会生成氢气,另一生成物是金属离子与酸根离 子构成的化合物(盐)
结论: 酸 + 活泼金属 → 盐 + 氢气
课题1 常见的酸和碱
(3)酸溶液能与金属氧化物反应:
现象
化学方程式
铁锈+盐酸
铁锈消失, 铁钉变得光
Fe2O3 + 6HCl = 2FeCl3+ 3H2O
铁锈+硫酸
亮,无色溶 液变黄
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
讨论:①上面反应的生成物有什么共同之处?
上述反应的生成物之一都是水,另一生成物是金属离子与 酸根离子构成的化合物(盐) 金属氧化物 + 酸→盐 + 水
小结:1、盐酸、硫酸的物理性质和用途,
2、试着找出酸的化学性质。
练习:向放有铁锈的钉子的试管中加入过量盐酸,充分反 应后,铁锈消失, 并有气泡产生,写出有关反应化学方程 式:_F_e_2_O_3_+__6_H_C_l_=__2_F_e_C_l_3 _+_3_H_2_O__、 _____F_e_+__2_H_C_l_=__H_2_↑_+__F_e_C_l_2_____ . 预习常见的碱
气味 有刺激性气味
无味
课题1 常见的酸和碱
盐酸、硫酸的用途很广。例如
用
途
盐酸
重要化工产品。用于金属表面除锈、制造药
物(如盐酸麻黄素、氯化锌)等;人体胃液中有
HCl 盐酸,可帮助消化。
重要化工原料。用于生产化肥、农药、火药、 硫 酸 染料以及冶炼金属、精炼石油和金属除锈等。
H2SO4
浓硫酸有吸水性,在实验室中常用它做干燥
②利用上面的反应可以清除金属制品表面的锈,除锈时能 否将金属制品长时间浸在酸中?为什么?
不能长时间浸在酸中,因为酸会与金属继续反应,造成金)根据上面的实验和讨论,试归纳出盐酸、硫酸等酸 有哪些相似的化学性质。
A、酸能使酸碱指示剂显示不同的颜色; B、酸能与多种活泼金属反应,生成氢气; C、酸能与某些金属氧化物反应,生成水。
