注射用培美曲塞二纳使用说明书
注射用培美曲塞二钠注意事项

注射用培美曲塞二钠注意事项关于《注射用培美曲塞二钠注意事项》,是我们特意为大家整理的,希望对大家有所帮助。
注射用培美曲塞二钠是归属于注射类药物,是乳白色粉状。
适用没法动手术的恶变皮瘤。
注射用培美曲塞二钠适用成年人病人,不强烈推荐少年儿童应用,肾脏功能不太好的病人不建议应用该药物。
注射用培美曲塞二钠也是有一定的副作用,服药时要搞好对药物的掌握,安全用药。
下边就要我介绍一下注射用培美曲塞二钠!(一)使用方法使用量培美曲塞应当在有抗肿瘤放疗运用工作经验的达标医生的具体指导下应用。
培美曲塞只有用以静脉滴注,其溶液的配制务必依照“静脉滴注水溶液配置”的表明开展。
[u]恶变胸膜间皮瘤:[/u]培美曲塞协同顺铂用以医治恶变胸膜间皮瘤的强烈推荐使用量为每21天500mg/m[sup]2[/sup],滴注10分钟,顺铂的强烈推荐使用量为75mg/m[sup]2[/sup]滴注超出2钟头,应在培美曲塞给药完毕30分钟后再给与顺铂滴注。
接纳顺铂医治要有凝固计划方案。
实际可参照顺铂说明书。
[u]预服药品:[/u]皮质类固醇——未预服皮质类固醇药品的病人,运用培美曲塞皮疹发病率较高。
预服地塞米松(或类似药品)能够减少皮肤反映的发病率以及比较严重水平。
给药方式:地塞米松4mg,内服,每天2次,培美曲塞给药前1天、给药当日和给药后1天连服3天。
维他命补充——以便降低毒副作用反映,培美曲塞医治务必另外服食小剂量叶酸片或别的带有叶酸片的多种维生素中药制剂。
服食時间:第一次给与培美曲塞医治刚开始前7天最少服食5隔日使用量的叶酸片,一直服食全部医治周期时间,在最终1次培美曲塞给药后21天可停止服用。
病人还需在第一次培美曲塞给药前7天内肌肉注射维生素b2一次,之后每3个周期时间肌肉注射一次,之后的维生素b2给药可与培美曲塞服药在同一天开展。
叶酸片给药使用量:350~1000μg,常见使用量400μg;维生素b2使用量1000μg。
(参照生产常见问题疫苗项下的“警示”一部分)。
培美曲塞二钠 质量标准

培美曲塞二钠质量标准培美曲塞二钠(Perampanel Sodium)是一种新型的抗癫痫药物,属于非竞争性α-amino-3-hydroxy-5-methyl-4-isoxazolepropionic acid受体拮抗剂。
它通过抑制神经元的兴奋性和减少谷氨酸释放,对癫痫的发作起到治疗作用。
培美曲塞二钠是钠盐形式,与其自由酸形式具有相同的药效。
培美曲塞二钠的化学结构是C23H20N4NaO,其分子量为414.42。
其化学名称是7-(3-氰基苯基)-5-苯基[1,2,4]三嗪-6-蓝烯-3-甲酸钠盐。
它是一种白色或类白色晶体粉末,溶于水、甲醇和乙醇,化学性质稳定。
培美曲塞二钠在临床上主要用于治疗癫痫。
目前,培美曲塞二钠已被批准用于治疗部分性癫痫随机化,双盲安慰剂对照研究显示,对癫痫的治疗有效率显著高于安慰剂组。
它可用作单药治疗或辅助治疗,并可用于儿童和成人患者。
剂量的选择应根据患者的具体情况来确定,一般从起始剂量开始,然后逐渐增加,直到达到有效的维持剂量。
通常,起始剂量为2毫克/天,剂量可逐步增加至最大剂量为12毫克/天。
培美曲塞二钠对于癫痫的治疗可以通过多种机制发挥作用。
首先,培美曲塞二钠作为一种非竞争性α-amino-3-hydroxy-5-methyl-4-isoxazolepropionic acid(AMPA)受体拮抗剂,它能够直接抑制AMPA 受体的活性,降低神经元的兴奋性。
其次,培美曲塞二钠能够抑制谷氨酸的释放,从而减少神经元间的兴奋性传递。
最后,培美曲塞二钠可以通过调节钙离子通道和钾离子通道的活性,影响神经元内外钙离子和钾离子的浓度,从而影响神经元的兴奋性。
培美曲塞二钠的治疗效果已在大量的临床试验中得到证实。
一项对于片剂配伍剂量的研究显示,培美曲塞二钠治疗癫痫的有效率达到了50%以上。
而另一项多中心、随机、双盲、安慰剂对照研究对治疗癫痫的患者进行了为期12周的评估,结果显示,培美曲塞二钠组的癫痫发作次数显著减少,有效率达到了70%以上。
培美曲塞二钠使用说明

培美曲塞二钠【用法用量】1.应该在有抗肿瘤化疗应用经验的合格医师的指导下使用。
2.本品只能用于静脉滴注,其溶液的配制必须按照“静脉滴注准备”的说明进行。
3.恶性胸膜间皮瘤:本品联合顺铂用于治疗恶性胸膜间皮瘤的推荐剂量为每21天500mg/m2滴注本品超过10分钟,顺铂的推荐剂量为75mg/m2滴注超过2小时,应在本品给药结束30分钟后再给予顺铂滴注。
接受顺铂治疗要有水化方案。
具体可参见顺铂说明书。
4.预服药物:皮质类固醇—未预服皮质类固醇药物的患者,应用本品皮疹发生率较高。
预服地塞米松(或相似药物)可以降低皮肤反应的发生率及其严重程度。
给药方法:地塞米松4mg口服每日2次,本品给药前1天、给药当天和给药后1天连服3天。
5.维生素补充:为了减少毒性反应,本品治疗必须同时服用低剂量叶酸或其他含有叶酸的复合维生素制剂。
6.服用时间:第一次给予本品治疗开始前7天至少服用5次日剂量的叶酸,一直服用整个治疗周期,在最后1次本品给药后21天可停服。
患者还需在第一次本品给药前7天内肌肉注射维生素B12一次,以后每3个周期肌注一次,以后的维生素B12给药可与本品用药在同一天进行。
7.叶酸给药剂量:350-1000ug,常用剂量是400ug;维生素B12剂量1000ug。
【注意事项】1.本品应在有抗肿瘤药物应用经验的合格医师指导下使用。
2.应在有足够诊断与治疗技术的医疗机构进行本品治疗,这也可以保证并发症的及时处理。
3.临床研究中看到的治疗相关不良反应均是可以恢复的。
4.给药前未给予类皮质激素预处理的患者易出现皮疹。
5.地塞米松(或相似药物)预处理可以降低皮肤反应的发生率及严重程度。
6.本品是否导致体液储留例如胸水或腹水还不清楚。
对于临床有明显症状的体液储留患者,可以考虑本品用药前进行体腔积液引流。
7.主要通过尿路以原药形式排除体外。
如果患者肌酐清除率345mL/min,本品ò无需剂量调整。
对于肌酐清除率8.临床研究中,曾有一位严重肾功能不全(肌酐清除率19ml/min)的患者,未接受叶酸和维生素B12补充治疗,接受单药本品治疗后,死于药物相关毒性。
培美曲塞二钠课件

30%
多靶点抗肿瘤
放疗科
同步化放疗
3
Ⅳ期
50%
多靶点抗肿瘤
高效 低毒
肿瘤科 呼吸科
放疗科 肿瘤科
一线 维持 二线
4
脑转移
高效,低毒 17-57% 多靶点抗肿瘤 可透过血脑屏 障
爱立汀
注射用培美曲塞二钠
爱立汀治疗非小细胞肺癌
一线的研究:培美曲塞/卡铂VS多西他赛/卡铂一线治疗晚期非鳞癌型NSCLC V.Ganju et.al. 2011WCLC. 032.07 ☆ 培美曲塞联合卡铂组一线治疗晚期非鳞癌型NSCLC,较多 西他赛组获得更长的SWT时间 ☆ 培美曲塞联合卡铂方案较多西他赛方案可能更适合一线治 疗晚期非鳞癌型NSCLC
注射用培美曲塞二钠
培美曲塞的作用机制
培美曲塞独特的多靶点作用机制 同时高效抑制三个叶酸依赖性酶
Shin C, et al. Cancer Res. 1997; 57: 1116-1123.
爱立汀
注射用培美曲塞二钠
培美曲塞的作用机制
爱立汀
注射用培美曲塞二钠
培美曲塞的三靶点协同作用
X
X
X
爱立汀
注射用培美曲塞二钠
3周内就诊姑息治疗 小组;以后至少每 月一次;其他拜访 由患者、肿瘤医师 和姑息治疗医生共 同决定
•
首要终点:12周时生活质量的改变
姑息治疗小组:一位姑息治疗医师和一位高级护士
爱立汀
Temel JS, et al. N Engl J Med 2010; 363:733-742 注射用培美曲塞二钠
早期姑息治疗改善晚期肺癌患者生存
爱立汀
注射用培美曲塞二钠
培美曲塞 2013 NCCN 指南
注射用培美曲塞最全说明书
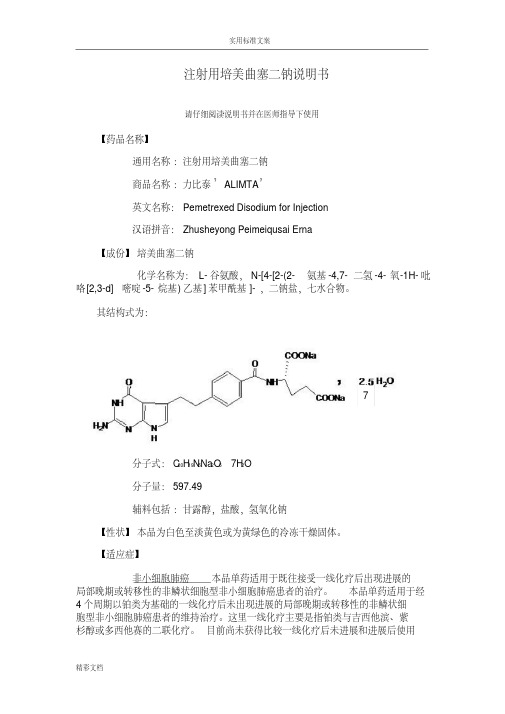
铂) 原剂量的 50%(培美曲塞和顺
绝对中性粒细胞最低值如何
铂)
aNCI 的 CTC标准(反应标准。
如果患者发生≥ 3 级的非血液学毒性 (不包括神经毒性) ,应暂停本 品治疗,直至恢复到治疗前水平或稍低于治疗前水平。应按照表 2 指南的要求恢 复治疗。
a:NCI 的 CTC标准; b:不包括神经毒性。
出现神经毒性,本品和顺铂的剂量调整见表 3,如果出现 3 级或 4 级神经毒性,应停止治疗。
本品单独用药 :非鳞状细胞型非小细胞肺癌 对于既往接受过化疗的非小细 胞肺癌患者,本品的推荐剂量为 500mg/m2 BSA,静脉输注 10 分钟以上。每 21 天
为一周期,在每周期的第 1 天给药。
预服药物 补充维生素 为了减轻毒性反应, 培美曲塞治疗必须同时服用低剂 量叶酸或其它含有叶酸的复合维生素制剂。服用时间:第 1 次给予培美曲塞治疗 开始前 7 天至少服用 5 次日剂量的叶酸,一直服用整个治疗周期,在最后 1 次培 美曲塞给药后 21 天可停服。患者还需在第 1 次培美曲塞给药前 7 天内肌内注射 维生素 B12 一次,以后每 3 个周期肌注一次,以后的维生素 B12 给药可与培美曲塞 用药在同一天进行。 临床试验中, 叶酸给药剂量范围为 350? 1000μg,最常使用 的口服剂量是 400μ g;维生素 B12剂量为 1000μ g。(见【注意事项】)
监测 所有准备接受培美曲塞的患者均应进行全血细胞计数检查,包括血小 板计数。应对患者的最低值和恢复情况进行监测, 在临床试验中, 在每次给药前及
每周期的第 8 天和 15 天进行检查。每次给药前还应进行定期的生化检查,以评估 肾功能和肝功能。只有当绝对嗜中性粒细胞计数( ANC)≥ 1500cell/mm 3、血小板 计数≥ 100,000cell/mm 3,肌酐清除率≥ 45ml/min ,总胆红素≤ 1.5 倍正常值上限,
化疗药物注射用培美曲塞二钠和注射用盐酸吉西他滨药品说明书信息

注射用培美曲塞二钠1、通用名称注射用培美曲塞二钠(医保乙类)2、产品简介培美曲塞(pemetrexed)是基于传统的抗代谢类药物甲氨蝶呤和氟尿嘧啶基础上研制的新一代抗代谢药,2004年由礼来公司研发上市。
2006年齐鲁赛珍上市后,齐鲁公司在国内首家开展晚期一线非鳞状NSCLC的大型临床试验并首家获得了非鳞状NSCLC的一线适应症。
3、注射用培美曲塞二钠作用机制注射用培美曲塞二钠是一种新的、多靶点抗叶酸制剂,主要作用于胸苷酸合成酶(TS),二氢叶酸还原酶(DHFR),甘氨酰核苷酸甲酰基转移酶(GARFT)。
通过破坏细胞内叶酸依赖性的正常代谢过程,抑制细胞复制,从而抑制肿瘤生长。
培美曲塞对酶的抑制活性高于其他抗叶酸代谢药物,多靶点抑制使其不易产生耐药性。
培美曲塞通过细胞膜上叶酸载体蛋白系统进入细胞后,在叶酰谷氨酸合成酶(FPGS)作用下转化为多谷氨酸化形式,多谷氨酸化后培美曲塞抗肿瘤活性大大增加。
多谷氨酸化的过程主要发生在肿瘤细胞内,正常细胞内的多聚谷氨酸化要比肿瘤细胞低得多,因此培美曲塞抗叶酸代谢的活性具有一定肿瘤特异性且较其他抗肿瘤药物不良反应更轻。
4、说书适应症及其他临床推广适应症说明书推荐:非鳞状非小细胞肺癌一线、二线、维持治疗;恶性胸膜间皮瘤。
还可用于NSCLC脑转移;神经淋巴瘤;头颈部肿瘤;妇瘤;骨肉瘤;乳腺癌;胃癌;十二指肠癌。
5、产品优势:(1)用于非小细胞肺癌的二线治疗,尤其是非鳞癌,优于多西他塞;用于非小细胞肺癌的一线治疗,尤其是非鳞癌,疗效优于吉西他滨;维持治疗(同药、异药)非鳞状非小细胞肺癌优于最佳支持治疗,有效延长生存期;被NCCN《非小细胞肺癌临床实践指南》推荐。
(2)恶性胸膜间皮瘤唯一有效方案,临床最好选择。
(3)培美曲塞是目前化疗药物中不良反应最低的一种,临床使用安全。
6、应用产品规格:100mg/200mg/500mg。
7、用法用量注:用药前须进行血液和生化检查;肌酐清除率<45mL/min的患者不建议使用注射用培美曲塞二钠;注射用培美曲塞二钠应以100ml0.9%氯化钠配制,培美曲塞二钠与钙、Ringer液不得混合使用。
注射用培美曲塞二钠说明书

核准日期: 2006年11月14日 修改日期: 2008年09月12日2008年12月09日 2010年01月27日 2010年06月24日 2010年07月05日 2010年08月31日 2011年05月05日 2013年09月22日 2014年05月04日 2014年10月18日 2014年11月26日 2014年12月03日 2015年08月13日 2016年04月12日 2017年05月27日 2020年03月05日 Xxxx 年xx 月xx 日注射用培美曲塞二钠说明书 请仔细阅读说明书并在医师指导下使用【药品名称】通用名称:注射用培美曲塞二钠 商品名称:力比泰® ALIMTA ®英文名称:Pemetrexed Disodium for Injection 汉语拼音:Zhusheyong Peimeiqusai Erna 【成份】 培美曲塞二钠化学名称: L-谷氨酸, N-[4-[2-(2-氨基-4,7-二氢-4-氧-1H -吡咯并[2,3-d]嘧啶-5-烷基)乙基]苯甲酰基]-,二钠盐,七水合物化学结构式:分子式:C 20H 19N 5Na 2O 6•7H 2O 分子量:597.49N HHN NO H 2NON HCO 2-CO 2-Na+Na+·7H 2O辅料包括:甘露醇、盐酸、氢氧化钠【性状】本品为白色至淡黄色或微黄绿色的冷冻干燥固体。
【适应症】非小细胞肺癌本品联合帕博利珠单抗和铂类用于表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的转移性非鳞状非小细胞肺癌(NSCLC)的一线治疗。
本品与顺铂联合,适用于局部晚期或者转移性非鳞状非小细胞肺癌患者的一线化疗。
本品单药适用于经4个周期以铂类为基础的一线化疗后未出现进展的局部晚期或转移性的非鳞状非小细胞肺癌患者的维持治疗。
本品单药适用于既往接受一线化疗后出现进展的局部晚期或转移性非鳞状非小细胞肺癌患者的治疗。
培美曲赛说明书

培美曲赛说明书一、药品名称通用名称:培美曲塞商品名称:_____英文名称:Pemetrexed二、成份本品主要成份为培美曲塞。
化学名称:L谷氨酸,N4-2-(2-氨基-4,7-二氢-4-氧-1H吡咯2,3-d 嘧啶-5-基)乙基苯甲酰基,二钠盐,七水合物。
化学结构式:_____分子式:C 20 H 19 N 5 Na 2 O 6 •7H 2 O分子量:59749辅料:甘露醇、盐酸、氢氧化钠。
三、性状本品为白色至类白色疏松块状物或粉末。
四、适应症本品联合顺铂用于治疗无法手术的恶性胸膜间皮瘤。
五、规格_____六、用法用量1、恶性胸膜间皮瘤本品联合顺铂治疗:培美曲塞 500mg/m²体表面积,静脉输注 10分钟以上,第 1 天;顺铂 75mg/m²体表面积,静脉输注超过 2 小时,第 1 天。
每 21 天为一周期。
在给予培美曲塞治疗前 7 天内肌肉注射维生素 B12 1mg,以后每 3 个周期重复肌肉注射一次。
在第一次给予培美曲塞治疗前 7 天内至少口服 5 次日剂量的叶酸 350-1000μg,整个治疗过程中以及培美曲塞末次给药后 21 天应继续口服叶酸。
在培美曲塞给药前 1 天、给药当天和给药后 1 天,口服地塞米松 4mg,每日 2 次。
2、剂量调整根据既往治疗周期中出现的血液学毒性和非血液学毒性对后续治疗周期的剂量进行调整。
如果患者经历了 3 级或 4 级的非血液学毒性(不包括 3 级的转氨酶升高),应暂停本品治疗,直至毒性恢复至 0-1 级。
重新开始治疗时,本品的剂量应减少 25%。
如果患者经历了 3 级或 4 级的中性粒细胞减少症伴发热或感染,3级或 4 级的血小板减少症导致出血,4 级的中性粒细胞减少症持续时间超过 7 天,4 级的血小板减少症持续时间超过 4 天,应暂停本品治疗,直至毒性恢复至 0-1 级。
重新开始治疗时,本品的剂量应减少 25%。
如果患者经历了 2 级的转氨酶升高,应暂停本品治疗,直至转氨酶恢复至 0-1 级。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
注射用培美曲塞二钠说明书成份本品主要成分是培美曲塞二钠,其化学名称为:N-[4-[2-(2-氨基-4,7-二氢-4-氧代-1H-吡咯[2,3-d]嘧啶-5-基)乙基]苯甲酰]-L-谷氨酸二钠二倍半水合物。
化学构造式为:分子式:C20H19N5Na2O6·2.5H2O分子量:516.41辅料名称:甘露醇。
性状本品为类白色或淡黄色疏松块状物或粉末。
适应症适用于与顺铂联合治疗无法手术的恶性胸膜间皮瘤。
规格0.2g〔按C20H19N5Na2O6计〕。
用法用量培美曲塞应该在有抗肿瘤化疗应用经历的合格医师的指导下使用。
培美曲塞只能用于静脉滴注,其溶液的配制必须按照“静脉滴注溶液配制〞的说明进展。
[u]恶性胸膜间皮瘤:[/u]培美曲塞联合顺铂用于治疗恶性胸膜间皮瘤的推荐剂量为每21天500mg/m[sup]2[/sup],滴注10分钟,顺铂的推荐剂量为75mg/m[sup]2[/sup]滴注超过2小时,应在培美曲塞给药完毕30分钟后再给予顺铂滴注。
承受顺铂治疗要有水化方案。
具体可参见顺铂说明书。
[u]预服药物:[/u]皮质类固醇——未预服皮质类固醇药物的患者,应用培美曲塞皮疹发生率较高。
预服地塞米松〔或相似药物〕可以降低皮肤反响的发生率及其严重程度。
给药方法:地塞米松4mg,口服,每日2次,培美曲塞给药前1天、给药当天和给药后1天连服3天。
维生素补充——为了减少毒性反响,培美曲塞治疗必须同时服用低剂量叶酸或其他含有叶酸的复合维生素制剂。
服用时间:第一次给予培美曲塞治疗开场前7天至少服用5次日剂量的叶酸,一直服用整个治疗周期,在最后1次培美曲塞给药后21天可停服。
患者还需在第一次培美曲塞给药前7天内肌肉注射维生素B12一次,以后每3个周期肌注一次,以后的维生素B12给药可与培美曲塞用药在同一天进展。
叶酸给药剂量:350~1000μg,常用剂量400μg;维生素B12剂量1000μg。
〔参见【考前须知】项下的“警告〞局部〕。
[u]实验室检查监测和推荐的剂量调整方法:[/u]监测——所有准备承受培美曲塞治疗的患者,用药前需完成包括血小板计数在内的血细胞检查,给药后需监测血细胞最低点及恢复情况,临床研究时每周期的开场、第8天和第15天需检查上述工程。
患者必须在中性粒细胞≥1500/mm[sup]3[/sup],血小板≥100,000cells/mm[sup]3[/sup]、肌酐去除率≥45ml/min时,才能开场培美曲塞治疗。
每周期治疗需进展肝功能和肾功能的生化检查。
推荐剂量调整方法——根据既往周期血细胞最低计数和最严重的非血液学毒性进展剂量调整。
患者如果21天周期仍未从不良反响中恢复,治疗应延迟进展。
等待患者恢复后,按照表1、表2、表3的要求进展治疗。
表1:出现血液学毒性时培美曲塞(单药或联合用药)和顺铂的剂量调整中性粒细胞最低值[500/mm[sup]3[/sup]和血小板最低值]50,000/mm[sup]3[/sup] 原剂量的75%(两药)血小板最低值[50,000/mm[sup]3[/sup]无论中性粒细胞最低值如何原剂量的50%(两药) 如果患者发生≥3度的非血液学毒性〔不包括神经毒性〕时〔不包括3度转氨酶上升〕,应停顿培美曲塞治疗,直至恢复到疗前水平或稍低于疗前水平。
再次开场治疗,按照表2的要求进展治疗。
表2:出现血液学毒性时培美曲塞(单药或联合用药)和顺铂的剂量调整[sup]a,b[/sup] 培美曲塞剂量(mg/m[sup]2[/sup]) 顺铂剂量(mg/m[sup]2[/sup])除粘膜炎之外的任何3度[sup]c[/sup]或4度非血液学毒性原剂量的75% 原剂量的75% 需要住院的腹泻(不分级别)或3度、4度腹泻原剂量的75% 原剂量的75%3度或4度粘膜炎原剂量的50% 原剂量的100%[sup]a[/sup]NCI的CTC标准[sup]b[/sup]不包括神经毒性[sup]c[/sup]不包括3度转氨酶升高出现神经毒性,培美曲塞和顺铂的剂量调整见表3。
如果出现3度或4度神经毒性,应停顿治疗。
表3:神经毒性所致培美曲塞(单药或联合用药)和顺铂的剂量调整CTC分级培美曲塞剂量(mg/m[sup]2[/sup]) 顺铂剂量(mg/m[sup]2[/sup])0-1 原剂量的100% 原剂量的100%2 原剂量的100% 原剂量的50%如果患者经历2次剂量调整后,再次出现3/4度血液学或非血液学毒性〔不包括3度转氨酶升高〕,应停顿培美曲塞治疗,如果出现3度或4度神经毒性,应立即停顿治疗。
老年患者—年龄≥65岁的患者除上述的剂量调整方案外无需特殊调整。
儿童——不推荐儿童应用培美曲塞,儿童用药的平安性和有效性尚未确定。
肾功能不全患者——只要患者肌酐去除率≥45ml/min,按照所有患者的剂量调整方法进展,无特殊剂量调整方法。
肌酐去除率低于45ml/min的剂量调整方法尚未确定。
因此,当按照Cockcroft-Gault公式计算或用Tc99m-DPTA血清去除方法计算肾小球滤过率后算得的肌酐去除率<45ml/min时,不应给予培美曲塞治疗。
男性:(140-年龄)*实际体重(kg) / 72*血清肌酐(mg/dl) = ml/min女性:男性肌酐去除率×0.85肌酐去除率<80ml/min的患者,如果培美曲塞同时合并非甾体类抗炎药应用应提高警觉,密切监测。
〔参见【药物相互作用】〕。
肝功能不全患者——培美曲塞不经肝脏代谢。
肝功能不全的剂量调整参见表2。
〔参见【考前须知】项下“肝功能不全的患者〞局部〕。
[u]配药及给药考前须知:[/u]培美曲塞是一种抗肿瘤药物,与其它有潜在毒性的抗肿瘤药一样,处置与配置培美曲塞时需特别小心,建议使用手套。
如果培美曲塞注射液接触到皮肤,立即用肥皂和水彻底清洗。
如果培美曲塞注射液接触到粘膜,用水彻底清洗。
处置抗癌药目前没有统一的推荐标准。
培美曲塞不是发泡糜烂剂,无特效解毒剂。
到目前为止,有几例培美曲塞注射液外渗的报告,但研究者均认为并不严重。
培美曲塞外渗处理可按照对非糜烂剂处理的常规方法进展。
[u]静脉滴注溶液的配制:[/u]1.配置过程应无菌操作。
2.计算培美曲塞用药剂量及用药支数。
每支药含有200mg培美曲塞。
每支瓶中实际所含培美曲塞大于200mg以保证静脉滴注时能到达标示量。
3.每支200mg药品用8ml 0.9%的氯化钠注射液〔无防腐剂〕溶解成浓度为25mg/ml的培美曲塞溶液,慢慢旋转直至粉末完全溶解。
完全溶解后的溶液澄清,颜色为无色至黄色或黄绿色都是正常的。
培美曲塞溶液的pH值为6.6~7.8。
且溶液需要进一步稀释。
4.静脉滴注前观察药液有无沉淀及颜色变化;如果有异样,不能滴注。
5.培美曲塞溶液配好后应用0.9%氯化钠注射液稀释至100ml,静脉滴注超过10分钟。
6.培美曲塞不能溶于含有钙的稀释剂,包括美国药典林格氏乳酸盐注射液和美国药典林格氏注射液。
其他稀释液和其他药物与培美曲塞能否混合尚未确定,因此不推荐使用。
不良反响本品不良反响资料均来自于国外临床研究中所获得的数据。
下表列出了在临床研究中随机承受培美曲塞和顺铂联合治疗的168名恶性胸膜间皮瘤患者及承受顺铂单药治疗的163名恶性胸膜间皮瘤患者中大于5%的不良反响的发生频率和严重程度的统计结果,在这两个试验组中之前未经化疗的患者均补充了充足的叶酸和维生素B12。
*不良反响分级参见NCI CTC 2.0版。
“非常常见〞指≥10%;“常见〞指>5%和<10%。
〔本表中列出的所有不良反响发生率均被减少5%以排除研究者主观认为可能与培美曲塞和顺铂相关〕。
随机承受培美曲塞和顺铂治疗的患者,发生率在1%和5%之间〔包括5%〕的临床相关的毒性反响包括:AST,ALT和GGT升高,感染,发热,中性粒细胞减少性发热,肾衰竭,胸痛和荨麻疹;发生率≤1%的临床相关的毒性反响包括心率失常和运动神经元病。
下表列出了在临床研究中随机承受培美曲塞单药治疗并且补充叶酸和维生素B12的265名患者及承受多烯紫杉醇单药治疗的276名患者中大于5%的不良反响的发生频率和严重程度的统计结果,在这两个试验组中患者均被诊断为局部晚期或转移性非小细胞肺癌,并已经过前期化疗。
*不良反响分级参见NCI CTC2.0版。
“非常常见〞指≥10%;“常见〞指]5%和[10%。
〔本表中列出的所有不良反响发生率均被减少5%以排除研究者主观认为可能与培美曲塞相关〕随机承受培美曲塞治疗的患者,发生率在1%和5%之间〔包括5%〕的临床相关的毒性反响包括:神经障碍,运动神经元病,腹痛,肌酐升高,中性粒细胞减少性发热,无中性粒细胞减少性感染,变态反响/过敏和多型红斑;发生率≤1%的临床相关的毒性反响包括室上性心律失常。
三个经整合的培美曲塞单独给药的Ⅱ期临床研究〔n=164〕中3度和4度实验室毒性反响的发生率与上面所列出的培美曲塞单独给药的Ⅲ期临床研究根本相似,除了中性粒细胞减少的发生率〔分别为12.8%和5.3%〕和丙氨酸转氨酶升高的发生率〔分别为15.2%和1.9%〕不同,主要是由受试人群不同造成的,因为在Ⅱ期研究中包含那些有肝脏转移和/或异常肝功能基线异常的乳腺癌患者,这些患者中有些之前未经过化疗而有些已经过屡次化疗。
禁忌禁用于对培美曲塞或药品其它成分有严重过敏史的患者。
考前须知警告肾功能下降的患者培美曲塞主要通过尿路以原药形式排出体外。
如果患者肌酐去除率≥ 45ml/min,培美曲塞无需剂量调整。
对于肌酐去除率[45ml/min的患者,无足够患者的研究资料来给予推荐剂量。
因此,对于肌酐去除率[45ml/min的患者,不应给予培美曲塞治疗。
〔参见【用法用量】中的“推荐剂量调整方法〞〕。
国外临床研究中,曾有一位严重肾功能不全〔肌酐去除率19ml/min〕的患者,未承受叶酸和维生素B12补充治疗,承受单药培美曲塞治疗后,死于药物相关毒性。
骨髓抑制培美曲塞可以引起骨髓抑制,包括中性粒细胞、血小板减少和贫血〔参见【不良反响】〕。
骨髓抑制是常见的剂量限制性毒性,应根据既往治疗周期中出现的最低中性粒细胞、血小板值和最严重非血液学毒性来进展剂量调整。
〔参见【用法用量】中的“推荐剂量调整方法〞〕。
叶酸及维生素B12的补充治疗承受培美曲塞治疗同时应承受叶酸和维生素B12的补充治疗,可以预防或减少治疗相关的血液学或胃肠道不良反响。
〔参见【用法用量】局部〕。
临床研究显示,给予叶酸和维生素B12补充治疗的患者,承受培美曲塞治疗时总的不良反响发生率降低,包括3/4度的血液学毒性及非血液学毒性,例如中性粒细胞减少、粒细胞减少性发热和3/4度粒细胞减少性感染。
一般考前须知培美曲塞应在有抗肿瘤药物应用经历的合格医师指导下使用。
