卤族元素化学方程式大全
卤族元素

卤族元素一、卤族元素包括:氟(F)、氯(Cl)、溴(Br)、碘(I)、砹(At)。
1、原子结构特征:最外层电子数相同,均为7个电子,从外界获得电子的能力依次减弱,单质的氧化性减弱。
2、卤素元素单质的物理性质:从F2 Cl2、Br2、到I2,颜色由浅到深(浅绿色、黄绿色、红棕色、紫色),状态由气到液到固,熔沸点和密度都逐渐增大,水溶性逐渐减小。
3、卤素单质化学性质比较相似性:均能与H2发生反应生成相应卤化氢,卤化氢均能溶于水,形成无氧酸。
H2+F2===2HF (黑暗中反应)H2+Cl22HCl (点燃或加热)H2+Br22HBr(加热)H2+I2(持续加热)均能与水反应生成相应的氢卤酸和次卤酸(氟除外)2F2+2H2O==4HF+O2X2+H2O======HX+HXO (X表示Cl Br I)4、萃取和分液的概念①在溴水中加入四氯碳振荡静置有何现象?(分层,下层橙红色上层无色)②在碘水中加入煤油振荡静置有何现象?(分层,上层紫红色,下层色)5、卤离子的鉴别:加入HNO3酸化的硝酸银溶液,Cl-:得白色沉淀Ag++ Cl-====AgCl↓Br-:得淡黄色沉淀Ag++ Br-====AgBr↓I-:得黄色沉淀Ag++ I-====Ag I↓6、卤素特性①F元素无正价,只有-1价,AgF可以溶于水,CaF2不溶于水。
②I2可以升华(常用于分离),且能使淀粉变蓝(常用于检验碘或淀粉)7、单质氧化性从F2到I2在减弱Cl2+2KBr=2KCl+Br2Br2+2KI=2KBr+I2Cl2+2KI=2KCl+I2二、拟卤素和卤素互化物拟卤素:⒈概念:拟卤素是指由二个或二个以上非金属元素原子组成的原子团,这些原子团在自由状态时,与卤素单质的性质相似。
有剧毒。
重要的拟卤素有氰(qíng)(CN)2、硫氰(SCN)2等。
⒉拟卤素的化学性质①与水发生歧化反应Cl2+ H2O = HCl + HClO(SCN)2+ H2O = HSCN + HSCNO①与碱反应Cl2+ 2NaOH = NaCl + NaClO + H2O(CN)2+2OH-=CN-+CNO-;Cl2+2OH-=Cl-+ClO-卤素互化物⒈概念:不同卤素原子之间可通过共用电子对形成物质叫卤素互化物。
高中化学方程式大全(完整版)

44、 2H (2 气) O(2 气) 2H 2O(液) 571.6kJ
45、 C(固) H 2 O(气)
CO (气) H (2 气) 131.3kJ
第三章 硫 硫酸
第一节 硫
46、 2Cu S
Cu 2S
47、 Fe S
FeS
48、 S H 2
H 2S
49、 S C 高温 CS2
50、 S O 2 点燃 SO2
CO 2 2SO2 2H 2O
81、 S 2H 2SO(4 浓)
3SO2 2 H 2O
82、 P H 2SO(4 浓)
H 3PO4 SO2 2 H 2O
83、 H 2S H 2SO(4 浓)
S SO 2 2H 2O
84、 Cu 2H 2SO(4 浓)
CuSO 4 SO 2 2H 2O
85、 BaCl 2 H 2SO4 BaSO 4 2HCl
第一节 摩尔
化学
38、 C O 2 CO 2
39、 Mg 2HCl MgCl 2 H 2 第二节 气体摩尔体积
40、 Zn 2HCl ZnCl 2 H 2
第三节 物质的量浓度
41、 2NaOH H 2SO 4 Na 2SO4 2H 2 O
第四节 反应热 42、 C(固) O(2 气) 点燃 CO(2 气) 393.5kJ 43、 2H (2 气) O(2 气) 2H 2O(气) 483.6kJ
10、 2NaOH Cl 2 NaClO NaCl H 2O
11、 4HCl MnO 2
MnCl 2 2 H 2 O Cl 2
12、 2KMnO 4 16HCl (浓) 2MnCl 2 2KCl 5Cl 2 13、 2HClO 见光 2HCl H 2SO(4 浓) NaHSO 4 HCl
卤素化学方程式及性质

卤素化学方程式及性质1、与非金属反应(HX:卤化氢/氢卤酸)F 2 + H 2 ====2HF Cl 2+H 2====2HCl Br 2+H 2 ====2HBr I 2+H 2垐垎?噲垐?加热2HI 反应条件越来越苛刻,且HX 稳定性降低,HI 在加热下易分解4HF+SiO 2===SiF 4↑+2H 2O(HF 保存在塑料瓶的原因,此反应广泛应用于测定矿样或钢样中SiO 2的含量)HF 为弱酸,酸性比较:HF<HCl<HBr<HI (写出6大强酸)3Cl 2+2P===2PCl 3 PCl 3+Cl 2===PCl 52、与金属反应3Cl 2+2Fe===2FeCl 3 (棕色烟) 3Br 2+2Fe===2FeBr 3 I 2+Fe===FeI 2Cl 2+Cu===CuCl 2(棕黄色烟,浓溶液为绿色,稀溶液为蓝色)Br 2+Cu===CuBr 2 I 2+2Cu===2CuI总结:1、F 2、Cl 2可与任何金属化合,Br 2、I 2与大多数金属化合(除Au 、Pt 外)。
2、对于变价金属,如Fe 、Cu,Cl 2、Br 2将金属氧化到最高价,I 2将金属氧化到较低价。
Zn+I 2==ZnI 2(H 2O 为催化剂) 滴水生紫烟,放热反应3、与水反应(X 2+H 2O 垐?噲?HX+HXO 除F 2外)Cl 2+H 2O 垐?噲?HCl+HClO Br 2+H 2O 垐?噲?HBr+HBrO I 2+H 2O 垐?噲?HI+HIO反应程度减弱2F 2 +2H 2O===4HF+O 2(氧化性:F 2>O 2,置换反应)4、与碱反应(以NaOH 为例)X 2+2NaOH===NaX+NaXO+H 2OCl 2+2NaOH===NaCl+NaClO+H 2O 3Cl 2+6NaOH===5NaCl+NaClO 3+3H 2OBr 2+2NaOH===NaBr+NaBrO+H 2O 3Br 2+6NaOH===5NaBr+NaBrO 3+3H 2OI 2+2NaOH===NaI+NaIO+H 2O 3I 2+6NaOH===5NaI+NaIO 3+3H 2O3Na 2CO 3+3Br 2==5NaBr +NaBrO 3+3CO 2↑以上均为歧化反应。
高三化学高考必记的化学方程式

高三化学高考必记的化学方程式一、非金属元素的反应1. 卤族元素(1)氯气H 2+Cl 2=====点燃2HCl2Fe +3Cl 2=====点燃2FeCl 3Cl 2+H 2O===HCl +HClO2NaOH +Cl 2===NaClO +NaCl +H 2O2Ca(OH)2+2Cl 2===Ca(ClO)2+CaCl 2+2H 2O6FeBr 2+3Cl 2===4FeBr 3+2FeCl 3(氯气少量)2FeBr 2+3Cl 2===2FeCl 3+2Br 2(氯气过量)[活学巧用] 氯水成分复杂,性质多样:强酸性——H +的性质;杀菌、漂白性——HClO 的性质;强氧化性——Cl 2的性质。
氯气溶于水,但不溶于饱和食盐水,因此可用饱和食盐水除去Cl 2中的HCl 。
Cl 2与NaOH 溶液的反应被用于实验室除去多余的Cl 2,常出现在框图推断中。
[易错警示] 氯气与FeBr 2溶液反应时,一定要注意二者量的关系,Cl 2首先氧化的是Fe 2+,然后氧化Br -;但Cl 2与FeI 2溶液反应时,首先氧化的是I -,然后氧化Fe 2+。
根据得失电子守恒可得出相应反应的离子方程式,如等物质的量的Cl 2与FeBr 2在溶液中反应时,其离子方程式为2Fe 2++2Cl 2+2Br -===2Fe 3++4Cl -+Br 2。
(2)含氯化合物2HClO=====光照2HCl +O 2↑Ca(ClO)2+CO 2+H 2O===CaCO 3↓+2HClONaClO +2HCl===NaCl +Cl 2↑+H 2OMnO 2+4HCl(浓)=====△MnCl 2+Cl 2↑+2H 2O[活学巧用] HClO 可作漂白剂和杀菌剂是由于HClO 具有强氧化性,长时间放置的氯水易变质是由于HClO 在光照条件下极易分解,所以新制的氯水需避光保存。
(3)卤素单质间的置换反应Cl 2+2NaBr===Br 2+2NaClCl 2+2NaI===I 2+2NaClBr 2+2KI===2KBr +I 2[活学巧用] 以上反应可用于比较Cl 2、Br 2、I 2氧化性(非金属性)的强弱或与CCl 4、淀粉溶液相结合用于溶液中Br -、I -的检验。
卤素化学方程式

卤素化学方程式2Na+Cl2点燃2NaCl2Fe+3Cl2点燃2FeCl3Cu+Cl2点燃CuCl2H2+Cl2点燃2HCl2P+3Cl2点燃2PCl3PCl3+Cl2=PCl52P+5Cl2点燃2PCl5Cl2+SO2+2H2O=2HCl+H2SO4Cl2+H2SO3+H2O=2HCl+H2SO4Cl2+H2S=S↓+2HClCl2+Na2S=2NaCl+S↓Cl2+2Fe2+=2Fe3++2Cl-Cl2+2I-=2Cl-+I2Cl2+2Br-=2Cl-+Br22NH3+3Cl2=N2+6HCl3Cl2+8NH3=N2+6NH4ClCl2+H2O HCl+HClO2HClO====2HCl+O2↑Cl2+2NaOH=NaCl+NaClO+H2O工业制漂白粉:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO Ca(ClO)2+2HCl=CaCl2+2HClO实验室制氯气:MnO2+4HCl(浓)△MnCl2+Cl2↑+2H2O2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2OKClO3+6HCl(浓)=KCl+3Cl2↑+3H2O氯碱工业:2NaCl+2H2O电解2NaOH+H2↑+Cl2↑2Fe+3Br2△2FeBr3Fe+I2△2H2+Br2△2HBrH2+I2△2HIX2+SO2+2H2O=2HX+H2SO4(X=Cl\Br\I)X2+H2S=2HX+S↓(X=Cl\Br\I)X2+2Fe2+=2Fe3++2X-(X=Cl\Br)Br2+2I-=2Br-+I22F2+2H2O=4HF+O2X2+H2O HX+HXO(X=Cl\Br\I)X2+2NaOH=NaX+NaXO+H2O(X=Cl\Br\I)4HF+SiO2=SiF4+2H2O2AgX======2Ag+X2(X=Cl\Br\I)碱金属化学方程式2Na+Cl2点燃2NaCl4Na+O2=2Na2O2Na+O2点燃Na2O22Na+S△Na2S2Na+2H2O=2NaOH+H2↑Na与NH4Cl溶液2Na+2NH4Cl=2NaCl+2NH3↑+H2↑Na与CuSO4溶液2Na+2H2O+CuSO4=Na2SO4+Cu(OH)2↓+H2↑Na2O+H2O=2NaOHNa2O+CO2=Na2CO3Na2O+2HCl=2NaCl+H2O2Na2O2+2H2O=4NaOH+O2↑2Na2O2+2CO2=2Na2CO3+O22Na2O2+4HCl=4NaCl+2H2O+O2↑Na2CO3+Ca(OH)2=CaCO3↓+2NaOHNa2CO3与Al2(SO4)3反应离子方程式:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑NaHCO3与Al2(SO4)3反应离子方程式Al3++3HCO3-=Al(OH)3↓+3CO2↑Na2O2+SO2=Na2SO4Na2O2+H2S=2NaOH+S↓Na2CO3+H2O+CO2=2NaHCO32NaHCO3△Na2CO3+H2O+CO2↑NaHCO3+NaOH=Na2CO3+H2ONa2CO3中加入过量HClNa2CO3+2HCl=2NaCl+H2O+CO2↑向Na2CO3中逐滴加入HC l①Na2CO3+HCl=NaHCO3+NaCl②NaHCO3+HCl=NaCl+H2O+CO2↑工业制取钠方法2NaCl(熔融)电解2Na+Cl2↑过量Ca(OH)2与NaHCO3离子方程式Ca2++OH-+HCO3-=CaCO3↓+H2O光照或加热光照过量NaHCO3与Ca(OH)2离子方程式Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32-侯氏制碱法NaCl+NH3+CO2+H2O=NH4Cl+NaHCO32NaHCO3△2CO3+H2O+CO2↑镁及其化合物2Mg+O2点燃2MgO Mg+Cl2点燃MgCl2 3Mg+N2点燃Mg3N2Mg+2H2O △Mg(OH)2+H2↑Mg+2HCl=MgCl2+H2↑Mg+2NH4Cl=MgCl2+2NH3↑+H2↑2Mg+CO2点燃2MgO+CMgO+2H+=Mg2++H2OMg(OH)2+2H+=Mg2++2H2OMg(OH)2△MgO+H2OMgCO3△+CO2↑从海水中提取镁涉及的方程式①CaCO3高温CaO+CO2↑②CaO+H2O=Ca(OH)2③Mg2++2OH-=Mg(OH)2↓④Mg(OH)2+2HCl=MgCl2+2H2O⑤MgCl2.6H2O △MgCl2+6H2O⑥MgCl2电解Mg+Cl2↑铝及其化合物4Al+3O2点燃2Al2O3 2Al+3Cl2点燃2AlCl32Al+3S △2S32Al+6H+=2Al3++3H2↑2Al+2NaOH+2H2O=2NaAlO2+3H2↑2Al+3Cu2+=2Al3++3Cu2Al+Fe2O3高温Al2O3+2Fe8Al+3Fe3O4高温4Al2O3+9Fe 4Al+3MnO2高温2Al2O3+3Mn工业冶铝2Al2O3电解4Al+3O2↑Al2O3+6H+=2Al3++3H2↑Al2O3+2OH-=2AlO2-+H2O2Al(OH)3△Al2O3+3H2OAl(OH)3+3H+=Al3++3H2OAl(OH)3+OH-=AlO2-+2H2OAl3++3OH-===Al(OH)3↓H++AlO2-+H2O=Al(OH)3↓AlO2-+4H+=Al3++2H2OAl3++4OH-=AlO2-+2H2OAl3++3NH3·H2O=Al(OH)3↓+3NH4+AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-2AlO2-+CO2+3H2O=CO32-+2Al(OH)3↓AlO2-+HCO3-+H2O=CO32-+Al(OH)3↓Al3++3AlO2-+6H2O=4Al(OH)3↓Al3++3HCO3-=3CO2↑+Al(OH)3↓NH4++AlO2-+H2O=NH3↑+Al(OH)3↓KAl(SO4)2与Ba(OH)2反应当沉淀物质的量最大时:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓当SO42-恰好完全沉淀时:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O铁及其化合物3Fe+2O2点燃Fe3O42Fe+3Cl2点燃2FeCl3Fe+I2△FeI2Fe+S△FeS3Fe+4H2O(g)高温Fe3O4+4H2↑Fe+2H+=Fe2++H2↑Fe与HNO3反应当HNO3过量时:Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O当Fe过量时:3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O Fe+Cu2+=Fe2++CuFe+2Fe3+=3Fe2+HCl2Fe2++Cl2=2Fe3++2Cl-2Fe2++H2O2+2H+=2Fe3++2H2O 2Fe3++Cu=2Fe2++Cu2+4Fe(OH)2+O2+2H2O=4Fe(OH)3 Fe(OH)2+2H+=Fe2++2H2OFe2++2OH-=Fe(OH)2↓Fe(OH)3+3H+=Fe3++3H2O2Fe(OH)3△Fe2O3+3H2OFe3++3OH-=Fe(OH)3↓Fe3++3SCN-=Fe(SCN)3冶铁中涉及的方程式①C+O2点燃CO2②C+CO2高温2CO③Fe2O3+3CO高温2Fe+3CO2产生炉渣的反应④CaCO3高温CaO+CO2↑⑤CaO+SiO2高温CaSiO3铜及其化合物2Cu+O2△2CuOCu+Cl2点燃CuCl22Cu+S △2SCu+2Ag+=Cu2++2Ag Cu+2Fe3+=Cu2++2Fe2+Cu+2H2SO4(浓)△CuSO4+SO2↑+2H2OCu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O CuO+2H+=Cu2++2H2O3CuO+2NH3△3Cu+N2+3H2O 含硅矿物与信息材料工业制玻璃:①Na2CO3+SiO2高温Na2SiO3+CO2↑②CaCO3+SiO2高温CaSiO3+CO2↑Si+2F2=SiF4Si+4HF=SiF4↑+2H2↑Si+2NaOH+H2O=Na2SiO3+2H2↑Si+O2△SiO2工业制取Si的反应①SiO2+2C高温Si+2CO↑(制粗硅)②Si+2Cl2高温SiCl4③SiCl4+2H2高温Si+4HCl(②③提纯)SiO2+2NaOH=Na2SiO3+H2OSiO2+CaO高温CaSiO3SiO2+4HF=SiF4↑+2H2OSiO32-+2H+=H2SiO3↓Na2SiO3+CO2+H2O=Na2CO3+H2SiO3↓含硫化合物的性质和应用S+O2点燃SO2S+H2△H2SFe+S△FeSSO2+H2O H2SO3SO2+CaO=CaSO3SO2+2NaOH=Na2SO3+H2OSO2+Na2CO3=Na2SO3+CO22SO2+O2催化剂加热2SO3SO2+X2+2H2O=H2SO4+2HXSO2+2H2S=3S↓+2H2O形成酸雨涉及的方程式主要:①SO2+H2O H2SO3②2H2SO3+O2=2H2SO4次要:①2SO2+O2催化剂加热2SO3②SO3+H2O=H2SO4工业制硫酸方程式①4FeS2+11O2高温2Fe2O3+8SO2或:S+O2点燃SO2②2SO2+O2催化剂加热2SO3③SO3+H2O=H2SO4体现稀H2SO4酸的通性的反应:与碱、与碱性氧化物、与活泼金属、与某些盐的反应略,自己举例完成。
化学方程式大全

高中化学(必修一)化学方程式大全一、卤族元素Cl2+Cu Cu Cl23Cl2+2Fe2FeCl3Cl2+2 Na 2Na Cl Cl2 + H22HClCl2+H2O HCl+HClO Cl2+H2O H++Cl-+HClOCl2+2NaOH=NaCl+NaClO+H2O Cl2+2OH—=Cl—+ClO—+H2O2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O Cl2+2OH—=Cl-+ClO-+H2OCl2+2FeCl2=2FeCl3Cl2+2Fe2+=2Fe3++2Cl—Ca(ClO)2+H2O+ CO2=Ca CO3↓+2 HClOCa(ClO)2+2 HCl =CaCl2+2 HClO(强酸制弱酸)ClO—+2 H+=HClO2HClO2HCl+O2↑Cl2+2NaBr=2NaCl+Br2Cl2+2Br-=2Cl-+Br2Cl2 +2 K I =2 KCl+I2 Cl2 +2 I-=2 Cl-+I2Br2 +2 K I =2 K Br+I2 Br2 +2 I-=2 Br-+I24HCl(浓)+MnO2MnCl2+Cl2↑+2H2O 4H++2Cl-+MnO2Mn2++Cl2↑+2H2O HCl + AgNO3=AgCl↓(白色)+HNO3 Cl- + Ag+=AgCl↓(白色)NaBr+AgNO3=AgBr↓(浅黄色)+NaNO3 Br-+Ag+=AgBr↓(浅黄色)NaI + AgNO3=AgI↓(黄色)+ Na NO3 I- + Ag+=AgI↓(黄色)二、碱金属元素4Na+O2=2Na2O 2Na2O+ O22Na2O24Na+2O22Na2O22Na+S=Na2S(爆炸)2Na+2H2O=2NaOH+H2↑2Na+2H2O=2Na++2OH—+H2↑Na2O+H2O=2NaOH Na2O+H2O=2Na++2OH—2Na2O2+2H2O=4NaOH+O2↑2Na2O2+2H2O=4Na++4OH—+O2↑Na2O+CO2=Na2CO32Na2O2+2CO2=2Na2CO3+O2Na2CO3+2HCl=2NaCl+ H2O+ CO2↑ CO32-+2H+=H2O+ CO2↑NaHCO3+HCl=NaCl+H2O+CO2↑HCO3-+H+=H2O+CO2↑2NaHCO3Na2CO3+ H2O+ CO2↑ 2K+2H2O=2KOH+H2↑NaHCO3 + NaOH=Na2CO3 + H2O HCO3—+ OH—=CO32—+ H2ONa2CO3+ H2O+ CO2=2NaHCO3 CO32—+ H2O+ CO2 =2HCO3—2NaOH+ CO2 (少量)=Na2CO3 + H2O 2OH—+ CO2 (少量)=CO32—+ H2O NaOH+ CO2(多量)=NaHCO3OH—+ CO2(多量)=HCO3-Na2CO3+ Ca(OH)2=Ca CO3↓+2 NaOH CO32—+ Ca2+=Ca CO3↓NaOH+HCl=NaCl+H2O OH—+H+=H2OCO2+Ca(OH)2(过量)=CaCO3↓+H2O CO2+Ca2++2OH—(过量)=CaCO3↓+H2O 2CO2(过量)+Ca(OH)2===Ca(HCO3)2 OH—+ CO2(多量) =HCO3—Na2O+2HCl=2NaCl+H2O Na2O+2H+=2Na++H2O2NaCl+2H2O H2↑+Cl2↑+2NaOH2Cl—+2H2O H2↑+Cl2↑+2OH—2NaCl2Na+Cl2↑三、镁2Mg+ O22MgO Mg+Cl2 MgCl23Mg+N2Mg3N22Mg+CO22MgO+CMg+2H2O M g(O H)2+H2↑Mg+2HCl=MgCl2+H2↑Mg+2H+=Mg2++H2↑MgCl2+2NaOH=M g(O H)2↓+2NaCl Mg2++2OH—=M g(O H)2↓四、铝4Al + 3O22Al2O32Al+6HCl=2AlCl3+3H2↑2Al+6H+=2Al3++3H2↑2Al+3H2SO4=Al2(SO4)3+3H2↑ 2Al+6H+=2Al3++3H2↑2Al + 2NaOH +2H2O=2NaAlO2 + 3H2↑2Al + 2OH- +2H2O=2AlO2—+ 3H2↑Al2O3 + 6HCl=2AlCl3+ 3H2O Al2O3 + 6H+=2Al3++ 3H2OAl2O3 + 2NaOH=2NaAlO2 + H2O Al2O3 + 2OH—=2AlO2—+ H2OAl(OH)3 + 3HCl=AlCl3 + 3H2O Al(OH)3 + 3H+=Al3++ 3H2OAl(OH)3 + NaOH=NaAlO2 + 2H2O Al(OH)3 + OH—=AlO2—+ 2H2O2Al(OH)3Al2O3 + 3H2O (Fe(OH)3、Cu(OH)2类似)AlCl3 + 3NH3·H2O=Al(OH)3↓+3NH4Cl Al3++ 3NH3·H2O=Al(OH)3↓+3NH4+ NaAlO2+HCl+H2O=NaCl+Al(OH)3↓AlO2-+H++H2O=Al(OH)3↓CO2+NaAlO2+2H2O=Al(OH)3↓+Na HCO3 CO2+AlO2—+2H2O=Al(OH)3↓+HCO3—3NaAlO2+AlCl3+6H2O=4Al(OH)3↓+ 3 NaCl3AlO2—+Al3++6H2O=4Al(OH)3↓2Al +Cr2O3Al2O3+2Cr 2Al + Fe 2O3Al2O3+2 Fe4Al +3MnO22Al2O3+3Mn 2Al2O34Al+ 3O2↑五、铁Fe + S FeS 3Fe + 2O2Fe3O43Fe + 4H2O Fe3O4 + 4H2↑Fe+2HCl=FeCl2+H2↑ Fe+2H+=Fe2-+H2↑Fe+CuCl2=FeCl2+Cu Fe+Cu2+=Fe2++Cu2FeCl3+Fe=3FeCl22Fe3++Fe=3Fe2+2FeCl3+Cu=2FeCl2+CuCl2 (用于雕刻铜线路版) 2Fe3++Cu=2Fe2++Cu2+2Fe(OH)3Fe 2O3 + 3H2O2FeCl2+Cl2=2FeCl3 2Fe2++Cl2=2Fe3++2Cl—4Fe(OH)2+ 2H2O+ O2=4Fe(OH)3Fe2O3 + 6HCl =2FeCl3 + 3H2O Fe2O3 + 6H+ =2Fe3+ + 3H2OFe2O3 + 3H2SO4 =Fe2(SO4)3 + 3H2O Fe2O3 + 6H+ =2Fe3+ + 3H2O3NaOH + FeCl3 ==Fe(OH)3↓ + 3NaCl3OH—+ Fe3+=Fe(OH)3↓FeCl3+3H2O Fe(OH)3+3HCl Fe3++3H2O Fe(OH)3+3H+FeCl3+3KSCN=Fe(SCN)3+3KCl Fe3++3SCN-=Fe(SCN)3六、氧族元素H2 + S H2S 2Na + S Na2SFe + S FeS S + O2SO23O22O32H2O2 2H2O+ O2↑SO2 + H2O H2SO3SO2 + 2NaOH=Na2SO3 + H2O SO2 + 2OH—=SO32—+ H2OSO2 + Ca(OH)2=CaSO3↓+ H2O 2SO2 + O2 2 SO3Cl2 + SO2 + 2H2O=H2SO4+2HCl (Br2、I2 类似) Cl2 +SO2 +2H2O=4H++SO42-+2Cl—SO3 + H2O=H2SO4 2H2SO4(浓)+Cu CuSO4+2H2O +SO2↑2H2SO4(浓) + C CO2↑+ 2H2O + 2SO2↑2Na2SO3 + O2=2Na2SO44FeS2 + 11O22Fe2O3 + 8SO2Na2SO3+H2SO4=Na2SO4+SO2↑+H2O SO32—+2H+=SO2↑+H2ONa2SO3+ H2O +Cl2=Na2SO4 +2HCl SO32—+ H2O +Cl2=SO42- +2H++2Cl—七、碳族元素C + O2点燃CO22C + O2点燃2CO2CO + O2点燃2CO2CO+ CuO 加热Cu + CO23CO+ Fe2O3高温2Fe + 3CO22NaOH + CO2=Na2CO3 + H2O2NaOH + SO2=Na2SO3 + H2O 2NaOH + SO3=Na2SO4 + H2OCa(OH)2 + CO2=CaCO3↓+ H2O Ca(OH)2 + SO2=CaSO3↓+ H2OCO2 + H2O =H2CO3C+ H2O CO + H2 (生成水煤气) C+CO2加热2CO2C+ SiO22CO↑ + Si Si +O2SiO22F2+ Si=SiF4 Si + 4HF=SiF4↑+2H2↑Si+2NaOH+ H2O=Na2SiO3+2H2↑SiO2+2NaOH =Na2SiO3+H2OSiO2+ 4HF=SiF4+2H2O CaO+ SiO2CaSiO3SiO2 + Na2CO3Na2SiO3+ CO2SiO2 + CaCO3CaSiO3+ CO2↑八、氮族元素NH3 + H2O NH3·H2O NH4++OH-4NH3 + 5O24NO + 6H2ON2 +3Mg Mg3N2N2 + O22NO2NO + O2=2NO23NO2 + H2O =2HNO3 + NO4NO + 3O2 + 2H2O==4HNO34NO2 + O2 + 2H2O=4HNO34HNO34NO2↑+ O2↑+ 2H2O Cu+4HNO3(浓)=Cu(NO3)2 +2NO2↑+2H2O 3Cu+8HNO3(稀)=3Cu(NO3)2 +2NO↑+4H2O C+4HNO3(浓) =CO2↑+4NO2↑+2H2ONH3 + HCl=NH4Cl (白烟)。
硫氮氯铁铝有机化学化学方程式归纳

卤族元素化学方程式归纳氯气及其化合物(Cl 2、HCl 、HClO 、F 2、NaCl )FeCl 2 FeCl 3 Ca(ClO)2 F 2 HFAgCl HCl Cl 2 HClO O 2 SiF 4Cl 2:1.Cl 2 + H 2 → 2HCl (光照时爆炸;点燃时安静燃烧:苍白色火焰、瓶口有白雾) 2.Cl 2 + P → PCl 3 PCl 3 + Cl 2 → PCl 5 (两个反应同时发生,有白色烟雾) 3.Cl 2 + H 2OHCl + HClO(氯水的成分:Cl 2、H 2O 、HCl 、HClO ;微粒:三分子四离子Cl 2、H 2O 、HClO 、H +、Cl -、ClO -、OH -)4.Cl 2 + 2Na −−→−点燃2NaCl (黄色火焰,有白烟) 5、3Cl 2 + 2Fe −−→−点燃2FeCl 3(剧烈,有褐色的烟) Cl 2 + Cu −−→−点燃CuCl 2(剧烈,有棕色的烟) 6.2Cl 2 + 2Ca(OH)2 → CaCl 2 + Ca(ClO)2 + 2H 2O (工业用石灰乳和Cl 2制漂粉精) 7.Cl 2 + 2NaOH → NaCl + NaClO + H 2O (实验室用NaOH 溶液吸收多余Cl 2,防止污染空气)8.Cl 2 + H 2S → S ↓ + 2HCl (以此可证明氧化性Cl 2比S 强,不能用自来水配制氢硫酸)NaCl NaClOI 2 Br 2 SAgIAgBrPCl 3 / PCl 5134 2 68511129 107131415 15201821 19 23 21 212425 I -Br -2627 1617229.Cl 2 + 2KI → I 2 + 2KCl (用湿润的KI 淀粉试纸变蓝色检验Cl 2) 10.Cl 2 + 2KBr → Br 2 + 2KClHClO :强氧化性(漂白性)、不稳定性、弱酸性11.2HClO −−→−光照2HCl + O 2↑ 12.HClO + HCl → Cl 2↑ + H 2O 13.HClO + NaOH → NaClO + H 2O14.Ca(ClO)2 + 2CO 2 + 2H 2O → Ca(HCO 3)2 + 2HClO (漂粉精的漂白原理)F 2:最活泼的非金属单质 15.2F 2 + 2H 2O → 4HF + O 2↑16.F 2 + H 2 → 2HF (黑暗条件下爆炸,放出大量的热)17.4HF + SiO 2 → SiF 4↑+ 2H 2O (HF 酸用塑料瓶保存,HF 酸可用来刻画玻璃) HCl :18.Fe + 2HCl → FeCl 2 + H 2↑(注意与3Cl 2 + 2Fe −−→−点燃2FeCl 3区别) 19.HCl + NaOH → NaCl + H 2O20.4HCl (浓)+ MnO 2 −→−∆MnCl 2 + Cl 2↑+ 2H 2O (实验室制氯气,盐酸一半作酸、一半作还原剂) 21.Cl - + Ag + → AgCl ↓ NaCl :22.NaCl + H 2SO 4(浓)−−→−微热NaHSO 4 + HCl ↑(实验室制HCl ) 23.2NaCl + 2H 2O −−→−电解2NaOH + H 2↑+ Cl 2↑(氯碱工业)24.2AgI −−→−光照2Ag + I 2(AgI 作人工降雨剂)25.2AgBr2Ag + Br 2(变色镜的原理)26.Ag + + Br - → AgBr ↓(浅黄色,遇硝酸不溶解) 27.Ag + + I - → AgI ↓(黄色,遇硝酸不溶解)光照 CuO硫和氮化学方程式归纳硫及其化合物(S 、H 2S 、SO 2、H 2SO 4) CuSH 2S SSO 2SO 3H 2SO 4S :1.S + 2Cu −→−∆Cu 2S(黑色) 2.S + 2Na −→−∆ Na 2S 3.S + Fe −→−∆ FeS(黑色) 4.S + Hg → HgS (用硫粉处理散落的汞滴)5.S + H 2 −→−∆ H 2S 6.S + O 2 −−→−点燃SO 2(淡蓝色火焰)或S + 2H 2SO 4(浓)−→−∆3SO 2↑ + 2H 2O (黑火药:S + 2KNO 3 + 3C −−→−点燃K 2S + N 2↑+ 3CO 2↑) H 2S :7.H 2S −→−∆S + H 2 (不稳定性) 2H 2S + O 2 → 2H 2O + 2S ↓(氢硫酸敞开放置变质) H 2S+H 2SO 4(浓) → 2H 2O + SO 2↑ + S ↓2H 2S+O 2 −−→−点燃 2H 2O + 2S (不完全燃烧); 2H 2S+3O 2 −−→−点燃2H 2O + 2SO 2(完全燃烧) 8.H 2S + 2NaOH → Na 2S + 2H 2O (氢硫酸的酸性) 9.H 2S + Pb(AC)2 → 2HAC+PbS ↓(硫化氢气体的检验) 10.H 2S + CuSO 4 → H 2SO 4+CuS ↓(硫化氢气体的吸收)Na 2SCu 2SFeS HgS H 2SO 3 HClFeSO 4 Na 2SO 4 BaSO 422Cu 、23C 、24S 14O 24 3 2 15 678 9 10⑨11⑨12⑨1819 20 21PbS11.FeS + H 2SO 4(稀) → FeSO 4 + H 2S ↑(硫化氢气体的实验室制法) SO 2:12.SO 2 + 2H 2S → 3S + 2H 2O (现象:瓶壁上有黄色粉末和小水珠生成)13.SO 2 + H 2O H 2SO 3(酸雨的形成,pH<5.6)14.2H 2SO 3 + O 2 → 2H 2SO 4(酸雨放置一段时间酸性增强,pH 减小)15.2SO 2+O 22SO 316.SO 2 + Cl 2 + H 2O → H 2SO 4 + 2HCl (SO 2与Cl 2等体积混合不具有漂白性) 17.SO 2 + Br 2 + H 2O → H 2SO 4 + 2HBr (SO 2使溴水褪色) H 2SO 4:18.H 2SO 4 + Fe → FeSO 4 + H 2↑ 19.H 2SO 4 + 2NaOH → Na 2SO 4 + 2H 2O 20.H 2SO 4 + BaCl 2 → BaSO 4↓+ 2HCl(SO 42-的检验:取样,先加盐酸无现象,再加BaCl 2有白色沉淀,Ba 2++SO 42-→BaSO 4↓)21.H 2SO 4(浓)+ NaCl −−→−微热NaHSO 4 + HCl ↑(浓硫酸的难挥发性,制易挥发性的酸)22.2H 2SO 4(浓)+ Cu −→−∆CuSO 4 + SO 2↑ + 2H 2O (一半作酸,一半作氧化剂) 23.2H 2SO 4(浓)+ C −→−∆ CO 2↑ + 2SO 2↑ + 2H 2O (2mol 全部作酸用) 24.S + 2H 2SO 4(浓) −→−∆2H 2O + 3SO 2↑(SO 2既是氧化产物、又是还原产物,1:2)氮及其化合物(N 2、NH 3、NH 4+、NO )N 2:1.N 2 + 3Mg −−→−点燃 Mg 3N 22.N 2 + 3H 22NH 33.N 2 + O 2 −−→−放电 2NO NH 3:4.NH 3 + H 2ONH 3•H 2ONH 4++ OH -(显弱碱性,使酚酞变红色)5.4NH 3 + 5O 2 −−→−32O Cr 4NO + 6H 2O (氨的催化氧化,现象是:催化剂继续保持红热,有红棕色气体生成,有水生成)6.NH 3 + HCl → NH 4Cl (白烟)7.4NH 3 + 3O 2 → 2N 2 + 6H 2O(在纯氧中燃烧) 2NH 3(适量) + 3Cl 2 → N 2 + 6HCl8NH 3(过量) + 3Cl 2 → N 2 + 6NH 4Cl (用浓氨水检验Cl 2管道是否有泄露) NH 4+:8.2NH 4Cl + Ca(OH)2−→−∆2NH 3↑ + CaCl 2 + 2H 2O (NH 3的实验室制法) NH 4Cl −→−∆NH 3↑ + HCl ↑(铵盐不稳定,受热易分解) NH 4+的检验:取样,加入NaOH 溶液,加热试管,用湿润的红色石蕊试纸放在试管口,若变蓝色,则含NH 4+。
无机化学反应式-卤素元素
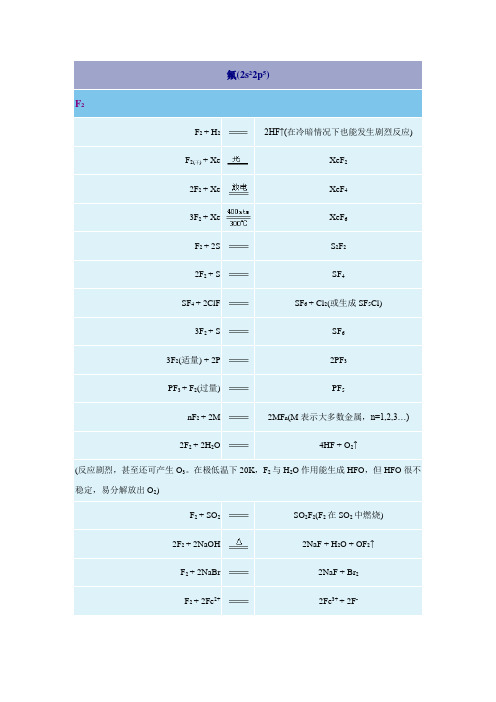
HBr3 2Br2 + 2H2O ZnBr2 + H2↑ Br2 + 2H2O MnBr2 + Br2↑+ 2H2O SO2↑+ Br2↑+ 2H2O KH2PO4 + HBr 2KNO3 + 2NO2 + Br2 + 2H2O 3Br2 + 2Cr3+ + 7H2O Pb(CH3COO)2 + 2CH3COONa + Br2 + 2H2O AgBr↓+ ClHBr3 2PBr5 + 5H2O 2Br2 + 2H2O O2↑+ H2O + Br2
HF
4 2HF(液体) + H2SO4(浓) 6HF + CaSiO3(固) HF(液) + C6H12O6 SiF4↑ + 2H2O NaF + H2O H3O+ + HSO3F + FCaF2 + SiF4↑ + 3H2O [C6H12O6·H]+ + F-
Cl2O6
Cl2O6 Cl2O6 + H2O Cl2O6 + 2NaOH 2ClO3 HClO4 + HClO3 NaClO4 + NaClO3 + H2O
ClO4
2ClO4 + Mg Mg(ClO4)2(Zn 和 Cu 亦可发生类似反应)
溴(4s24p5) Br2
Br2 + H2 Br2 + Cl2 Br2 + Cl2 + 2H2O Br2 + 5Cl2 + 6H2O Br2 + 2S(固) 3Br2 + 2P 3Br2 + 2P + 6H2O Br2 + 2Na Br2 + Mg Br2 + H2O 3Br2 + 3H2O Br2 + H2O2 2Br2(蒸气) + HgO 3Br2 + 6KOH Br2 + HCl Br2 + H2S 2HBr 2BrCl 2HBrO + 2HCl 2HBrO3 + 10HCl S2Br2(还可生成 SBr2) 2PBr3 2H3PO3 + 6HBr 2NaBr MgBr2 HBrO + HBr HBrO3 + 5HBr 2HBr + O2↑ HgBr2 + Br2O(深棕色) KBrO3 + 5KBr + 3H2O HClBr2 2HBr + S↓
