高中化学各类有机物之间的相互转化关系
高三有机化学中有机物间相互转化关系图

高三有机化学中有机物间相互转化关系图高三有机化学中有机物间相互转化关系图Document number:WTWYT-WYWY-BTGTT-YTTYU-2018GT一、有机物间相互转化关系二、能与溴水发生化学反应而使溴水褪色或变色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等)⑶ 石油产品(裂化气、裂解气、裂化汽油等)⑷ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等)⑸ 天然橡胶(聚异戊二烯) 2、无机物:⑴ -2价的S (硫化氢及硫化物)⑵ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐)⑶ + 2价的Fe6FeSO 4 + 3Br 2 = 2Fe 2(SO 4)3 + 2FeBr 3 6FeCl 2 + 3Br 2 = 4FeCl 3 + 2FeBr 32FeI 2 + 3Br 2 = 2FeBr 3 + 2I 2 ⑷ Zn 、Mg 等单质如⑸ -1价的I (氢碘酸及碘化物)变色⑹ NaOH 等强碱、Na 2CO 3和AgNO 3等盐 Br 2 + H 2O = HBr + HBrO2HBr + Na 2CO 3 = 2NaBr + CO 2↑+ H 2O HBrO + Na 2CO3 = NaBrO + NaHCO 3三、能萃取溴而使溴水褪色的物质上层变无色的(ρ>1):卤代烃(CCl 4、氯仿、溴苯等)、CS 2等;变色Mg + Br 2 === MgBr 2 (其中亦有Mg 与H +、Mg 与HBrO 的反应)△下层变无色的(ρ<1):直馏汽油、煤焦油、苯及苯的同系物、低级酯、液态环烷烃、液态饱和烃(如己烷等)等四、能使酸性高锰酸钾溶液褪色的物质1、有机物:⑴不饱和烃(烯烃、炔烃、二烯烃等)⑵不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等)⑶石油产品(裂化气、裂解气、裂化汽油等)⑷醇类物质(乙醇等)⑸含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等)⑹天然橡胶(聚异戊二烯)⑺苯的同系物2、无机物:⑴氢卤酸及卤化物(氢溴酸、氢碘酸、浓盐酸、溴化物、碘化物)⑵ + 2价的Fe(亚铁盐及氢氧化亚铁)⑶-2价的S(硫化氢及硫化物)⑷ + 4价的S(二氧化硫、亚硫酸及亚硫酸盐)⑸双氧水(H2O2)五、常见的各类有机物的官能团,结构特点及主要化学性质(1) 烷烃A)官能团:无;通式:C n H2n+2;代表物:CH4B) 结构特点:键角为109°28′,空间正四面体分子。
高三有机化学中有机物间相互转化关系图全解
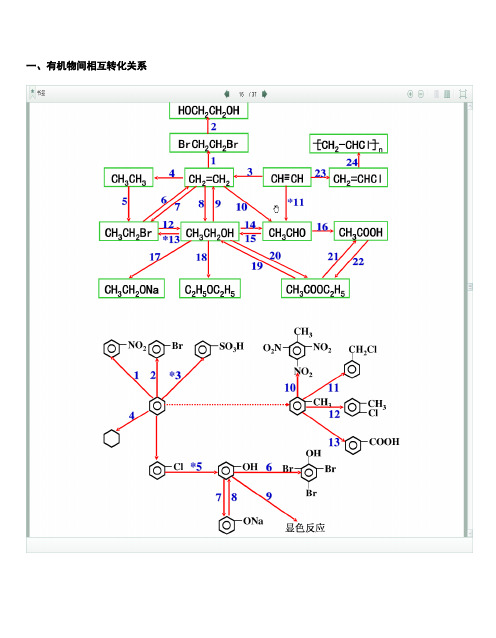
一、有机物间相互转化关系二、能与溴水发生化学反应而使溴水褪色或变色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等)⑷ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑸ 天然橡胶(聚异戊二烯)2、无机物:⑴ -2价的S (硫化氢及硫化物)⑵ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐) ⑶ + 2价的Fe6FeSO 4 + 3Br 2 = 2Fe 2(SO 4)3 + 2FeBr 36FeCl 2 + 3Br 2 = 4FeCl 3 + 2FeBr 32FeI 2 + 3Br 2 = 2FeBr 3 + 2I 2⑷ Zn 、Mg 等单质 如 ⑸ -1价的I (氢碘酸及碘化物)变色 ⑹ NaOH 等强碱、Na 2CO 3和AgNO 3等盐 Br 2 + H 2O = HBr + HBrO2HBr + Na 2CO 3 = 2NaBr + CO 2↑+ H 2O HBrO + Na 2CO 3 = NaBrO + NaHCO 3三、能萃取溴而使溴水褪色的物质上层变无色的(ρ>1):卤代烃(CCl 4、氯仿、溴苯等)、CS 2等;下层变无色的(ρ<1):直馏汽油、煤焦油、苯及苯的同系物、低级酯、液态环烷烃、液态饱和烃(如己烷等)等 四、能使酸性高锰酸钾溶液褪色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等) ⑷ 醇类物质(乙醇等)⑸ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑹ 天然橡胶(聚异戊二烯) ⑺ 苯的同系物变色 Mg + Br 2 === MgBr 2 (其中亦有Mg 与H +、Mg 与HBrO 的反应)△2、无机物:⑴ 氢卤酸及卤化物(氢溴酸、氢碘酸、浓盐酸、溴化物、碘化物) ⑵ + 2价的Fe (亚铁盐及氢氧化亚铁) ⑶ -2价的S (硫化氢及硫化物)⑷ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐) ⑸ 双氧水(H 2O 2)五、常见的各类有机物的官能团,结构特点及主要化学性质(1) 烷烃A) 官能团:无 ;通式:C n H 2n +2;代表物:CH 4B) 结构特点:键角为109°28′,空间正四面体分子。
高三有机化学中有机物间相互转化关系图

一、有机物间相互转化关系二、能与溴水发生化学反应而使溴水褪色或变色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等)⑷ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑸ 天然橡胶(聚异戊二烯)2、无机物:⑴ -2价的S (硫化氢及硫化物)⑵ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐) ⑶ + 2价的Fe6FeSO 4 + 3Br 2 = 2Fe 2(SO 4)3 + 2FeBr 36FeCl 2 + 3Br 2 = 4FeCl 3 + 2FeBr 32FeI 2 + 3Br 2 = 2FeBr 3 + 2I 2⑷ Zn 、Mg 等单质 如 ⑸ -1价的I (氢碘酸及碘化物)变色 ⑹ NaOH 等强碱、Na 2CO 3和AgNO 3等盐 Br 2 + H 2O = HBr + HBrO2HBr + Na 2CO 3 = 2NaBr + CO 2↑+ H 2O HBrO + Na 2CO 3 = NaBrO + NaHCO 3三、能萃取溴而使溴水褪色的物质上层变无色的(ρ>1):卤代烃(CCl 4、氯仿、溴苯等)、CS 2等;下层变无色的(ρ<1):直馏汽油、煤焦油、苯及苯的同系物、低级酯、液态环烷烃、液态饱和烃(如己烷等)等 四、能使酸性高锰酸钾溶液褪色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等) ⑷ 醇类物质(乙醇等)⑸ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑹ 天然橡胶(聚异戊二烯) ⑺ 苯的同系物变色 Mg + Br 2 === MgBr 2 (其中亦有Mg 与H +、Mg 与HBrO 的反应)△2、无机物:⑴ 氢卤酸及卤化物(氢溴酸、氢碘酸、浓盐酸、溴化物、碘化物) ⑵ + 2价的Fe (亚铁盐及氢氧化亚铁) ⑶ -2价的S (硫化氢及硫化物)⑷ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐) ⑸ 双氧水(H 2O 2)五、常见的各类有机物的官能团,结构特点及主要化学性质(1) 烷烃A) 官能团:无 ;通式:C n H 2n +2;代表物:CH 4B) 结构特点:键角为109°28′,空间正四面体分子。
高三有机化学中有机物间相互转化关系图

一、有机物间相互转化关系二、能与溴水发生化学反应而使溴水褪色或变色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等)⑷ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑸ 天然橡胶(聚异戊二烯)2、无机物:⑴ -2价的S (硫化氢及硫化物)⑵ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐) ⑶ + 2价的Fe6FeSO 4 + 3Br 2 = 2Fe 2(SO 4)3 + 2FeBr 36FeCl 2 + 3Br 2 = 4FeCl 3 + 2FeBr 32FeI 2 + 3Br 2 = 2FeBr 3 + 2I 2⑷ Zn 、Mg 等单质 如 ⑸ -1价的I (氢碘酸及碘化物)变色 ⑹ NaOH 等强碱、Na 2CO 3和AgNO 3等盐 Br 2 + H 2O = HBr + HBrO2HBr + Na 2CO 3 = 2NaBr + CO 2↑+ H 2O HBrO + Na 2CO 3 = NaBrO + NaHCO 3三、能萃取溴而使溴水褪色的物质上层变无色的(ρ>1):卤代烃(CCl 4、氯仿、溴苯等)、CS 2等;下层变无色的(ρ<1):直馏汽油、煤焦油、苯及苯的同系物、低级酯、液态环烷烃、液态饱和烃(如己烷等)等 四、能使酸性高锰酸钾溶液褪色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等) ⑷ 醇类物质(乙醇等)⑸ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑹ 天然橡胶(聚异戊二烯) ⑺ 苯的同系物变色 Mg + Br 2 === MgBr 2 (其中亦有Mg 与H +、Mg 与HBrO 的反应)△2、无机物:⑴ 氢卤酸及卤化物(氢溴酸、氢碘酸、浓盐酸、溴化物、碘化物) ⑵ + 2价的Fe (亚铁盐及氢氧化亚铁) ⑶ -2价的S (硫化氢及硫化物)⑷ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐) ⑸ 双氧水(H 2O 2)五、常见的各类有机物的官能团,结构特点及主要化学性质(1) 烷烃A) 官能团:无 ;通式:C n H 2n +2;代表物:CH 4B) 结构特点:键角为109°28′,空间正四面体分子。
有机物间的转化关系
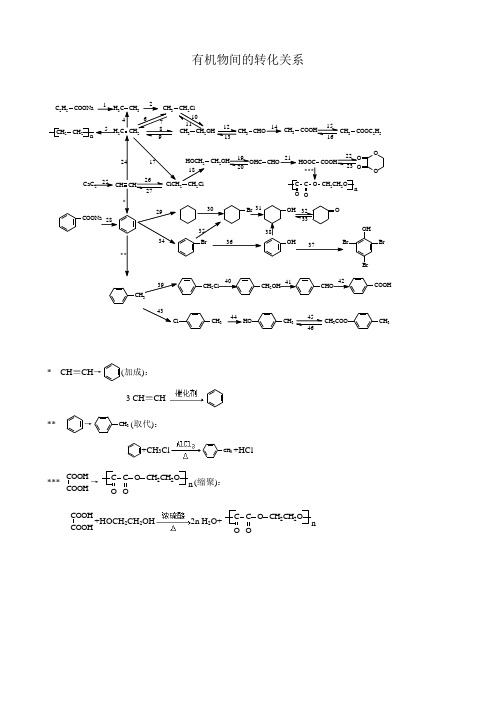
有机物间的转化关系CH 3ClCH 3HOCH 3CH 3COO 44* CH ≡CH →(加成): 3 CH ≡CH**→CH 3(取代):+CH 3ClCH 3+HCl***COOHCOOH→C C O O OCH 2CH 2O n (缩聚):COOHCOOH+HOCH 2CH 2OH 2n H 2O+C C O O OCH 2CH 2O n1.C 2H 5COONa →CH 3CH 3(脱羧):C 2H 5COONa+NaOH CH 3CH 3↑+Na 2CO 32.CH 3CH 3→CH 3CH 2Cl(取代): CH 3CH 3+Cl 2CH 3CH 2Cl+HCl 4.CH 2=CH 2→CH 3CH 3(加成):CH 2=CH 2+H 2CH 3CH 35.CH 2=CH 2→CH 2CH 2n(加聚):n CH 2=CH 2 CH 2CH 2n6.CH 2=CH 2→CH 3CH 2Cl(加成):CH 2=CH 2+HCl CH 3CH 2Cl7. CH 3CH 2Cl →CH 2=CH 2(消去):CH 3CH 2Cl CH 2=CH 2+HCl8. CH 2=CH 2→CH 3CH 2OH(加成):CH 2=CH 2+H 2O CH 3CH 2OH9. CH 3CH 2OH →CH 2=CH 2(消去):CH 3CH 2OH CH 2=CH 2↑+H 2O10. CH 3CH 2Cl →CH 3CH 2OH(取代):CH 3CH 2Cl+NaOH CH 3CH 2OH +NaCl 11. CH 3CH 2OH →CH 3CH 2Cl(取代): CH 3CH 2OH+HCl CH 3CH 2Cl+H 2O12. CH 3CH 2OH →CH 3CHO(氧化):2CH 3CH 2OH+O 22CH 3CHO+2H 2OCH 3CH 2OH+CuOCu+CH 3CHO+H 2O13. CH 3CHO →CH 3CH 2OH(加成、还原):CH 3CHO+H 2CH 3CH 2OH14. CH 3CHO →CH 3COOH(氧化): 2CH 3CHO+O 22CH 3COOHCH 3CHO+2[Ag(NH 3)]++2OH - CH 3COO -+NH 4++3NH 3+H 2OCH 3CHO+2Cu(OH)2CH 3COOH+Cu 2O+2H 2OCH 3CHO+Br 2+H 2O →CH 3COOH+2HBr15.CH 3COOH →CH 3COOC 2H 5(酯化):CH 3COOH+HOC 2H 5H 2O+CH 3COOC 2H 516. CH 3COOC 2H 5→CH 3COOH(水解):H 2O+CH 3COOC 2H 5 CH 3COOH+HOC 2H 5NaOH+CH 3COOC 2H 5CH 3COONa+HOC 2H 517.CH 2=CH 2→ClCH 2CH 2Cl(加成):CH 2=CH 2+Cl 2→ClCH 2CH 2Cl 18. ClCH 2CH 2Cl →HOCH 2CH 2OH(水解):ClCH 2CH 2Cl+2NaOH 2NaCl+HOCH 2CH 2OH19. HOCH 2CH 2OH →OHCCHO(氧化):HOCH 2CH 2OH+O 22H 2O+OHCCHO 20. OHCCHO →HOCH 2CH 2OH(还原):OHCCHO+2H 2HOCH 2CH 2OH21. OHCCHO →HOOCCOOH(氧化):OHCCHO+4Cu(OH)2HOOCCOOH+2Cu 2O+4H 2O22. COOH COOH →OO O O(酯化):COOH COOH +HO CH 22HO 2H 2O+OOOO23.OO O O→COOH (水解):OOOO+2H 2OCOOH +HO CH 2CH 2HO 24.CH ≡CH →CH 2=CH 2(加成):CH ≡CH+H 2CH 2=CH 225.CaC 2→CH ≡CH(水解): CaC 2+2H 2O →Ca(OH)2+CH ≡CH ↑ 26. CH ≡CH →ClCH 2CH 2Cl(加成): CH ≡CH+2HCl ClCH 2CH 2Cl 27. ClCH 2CH 2Cl →CH ≡CH(水解):ClCH 2CH 2ClCH ≡CH+2HCl28.COONa→(脱羧):COONa+NaOH Na 2CO 3+29.→(加成):+3H 230. →Br(取代):+Br 2Br+HBr31.Br→OH(水解):Br+NaOH →OH+NaBr32.OH→O(氧化):2OH+O 22O+2H 2O33.O→OH(还原):O+H 2OH34.→Br(取代):+Br 2Br+HBr35.Br→Br(加成):Br+3H 2Br36.Br→OH(水解):Br+H 2OOH+HBr37.OH→BrOHBr(取代):OH+3Br 2→BrOHBr↓+3HBr38.OH→OH(加成):OH+3H 2OH39.CH 3→CH 2Cl (取代):CH 3+Cl 2CH 2Cl +HCl40.CH 2Cl→CH 2OH(水解):CH 2Cl+NaOH →CH 2OH+NaCl41.CH 2OH→CHO(氧化): 2CH 2OH+O 22CHO+2H 2O42.CHO→COOH(氧化):CHO+2Cu(OH)2COOH+Cu 2O+2H 2O43.CH 3→CH 3Cl (取代):CH 3+Cl 2CH 3Cl+HCl44. CH 3Cl→CH 3HO (水解):CH 3Cl+H 2OCH 3HO+HCl45. CH 3HO→CH 3CH 3COO (酯化):CH 3COOH+CH 3HO H 2O+CH 3CH 3COO46. CH 3CH 3COO →CH 3HO (水解):CH 3CH 3COO +H 2O CH 3COOH+CH 3HO。
重要有机物间相互转化

A~J均为有机化合物,它们之间的转化如上图所示:实验表明: ①D既能发生银镜反应,又能与金属钠反应放出氢气:②核磁共振氢谱 表明F分子中有三种氢,且其峰面积之比为1:1:1;③G能使溴的四氯 化碳溶液褪色;④1mol J与足量金属钠反应可放出22.4L氢气(标准状 况)。请根据以上信息回答下列问题: (1)A的结构简式为__(不考虑立体结构),由A生成B的反应类型是 _________反应; (2)D的结构简式为__________; (3)由E生成F的化学方程式为_______,E中官能团有____(填名称), 与E具有相同官能团的E的同分异构体还有____________(写出结构简式, 不考虑立体结构) (4)G的结构简式为 _______ (5)由I生成J的化学 方程式_____。
中间体
目标化合物
逆向合成分析法
目标化合物
中间体
中间体
基础原料
有机推断题型之一:根据衍变关系的推断
例1、由乙烯和其它无机原料合成环状化合 物E,请在下列方框内填入合适的化合物的 结构简式。
A
B
C
D
乙烯 Br2
水解
氧化
氧化
失水
O O
O O
E
练习:用2-丁烯、乙烯为原料设计合 成路线
O O
O O
例2.某芳香烃A有如下转化关系:
与Na反应
—OH —COOH
与NaOH溶 —X、 —COO—、
液反应
—COOH、酚羟基
与Na2CO3溶 液反应
—COOH 酚羟基
与NaHCO3 溶液反应
—COOH
转化方法之——官能团的转化
包括官能团种类变化、数目变化、位置变化等。
a.官能团种类变化:
高三有机化学中有机物间相互转化关系图解析
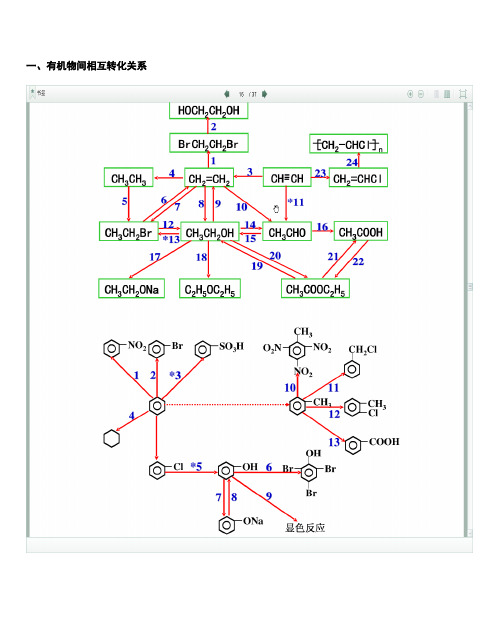
一、有机物间相互转化关系二、能与溴水发生化学反应而使溴水褪色或变色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等)⑷ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑸ 天然橡胶(聚异戊二烯)2、无机物:⑴ -2价的S (硫化氢及硫化物)⑵ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐) ⑶ + 2价的Fe6FeSO 4 + 3Br 2 = 2Fe 2(SO 4)3 + 2FeBr 36FeCl 2 + 3Br 2 = 4FeCl 3 + 2FeBr 32FeI 2 + 3Br 2 = 2FeBr 3 + 2I 2⑷ Zn 、Mg 等单质 如 ⑸ -1价的I (氢碘酸及碘化物)变色 ⑹ NaOH 等强碱、Na 2CO 3和AgNO 3等盐 Br 2 + H 2O = HBr + HBrO2HBr + Na 2CO 3 = 2NaBr + CO 2↑+ H 2O HBrO + Na 2CO 3 = NaBrO + NaHCO 3三、能萃取溴而使溴水褪色的物质上层变无色的(ρ>1):卤代烃(CCl 4、氯仿、溴苯等)、CS 2等;下层变无色的(ρ<1):直馏汽油、煤焦油、苯及苯的同系物、低级酯、液态环烷烃、液态饱和烃(如己烷等)等 四、能使酸性高锰酸钾溶液褪色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等) ⑷ 醇类物质(乙醇等)⑸ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑹ 天然橡胶(聚异戊二烯) ⑺ 苯的同系物变色 Mg + Br 2 === MgBr 2 (其中亦有Mg 与H +、Mg 与HBrO 的反应)△2、无机物:⑴ 氢卤酸及卤化物(氢溴酸、氢碘酸、浓盐酸、溴化物、碘化物) ⑵ + 2价的Fe (亚铁盐及氢氧化亚铁) ⑶ -2价的S (硫化氢及硫化物)⑷ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐) ⑸ 双氧水(H 2O 2)五、常见的各类有机物的官能团,结构特点及主要化学性质(1) 烷烃A) 官能团:无 ;通式:C n H 2n +2;代表物:CH 4B) 结构特点:键角为109°28′,空间正四面体分子。
高三有机化学中有机物间相互转化关系图

一、有机物间相互转化关系二、能与溴水发生化学反应而使溴水褪色或变色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等)⑷ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑸ 天然橡胶(聚异戊二烯)2、无机物:⑴ -2价的S (硫化氢及硫化物)⑵ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐) ⑶ + 2价的Fe6FeSO 4 + 3Br 2 = 2Fe 2(SO 4)3 + 2FeBr 36FeCl 2 + 3Br 2 = 4FeCl 3 + 2FeBr 32FeI 2 + 3Br 2 = 2FeBr 3 + 2I 2⑷ Zn 、Mg 等单质 如 ⑸ -1价的I (氢碘酸及碘化物)变色 ⑹ NaOH 等强碱、Na 2CO 3和AgNO 3等盐 Br 2 + H 2O = HBr + HBrO2HBr + Na 2CO 3 = 2NaBr + CO 2↑+ H 2O HBrO + Na 2CO 3 = NaBrO + NaHCO 3三、能萃取溴而使溴水褪色的物质上层变无色的(ρ>1):卤代烃(CCl 4、氯仿、溴苯等)、CS 2等;下层变无色的(ρ<1):直馏汽油、煤焦油、苯及苯的同系物、低级酯、液态环烷烃、液态饱和烃(如己烷等)等 四、能使酸性高锰酸钾溶液褪色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等) ⑷ 醇类物质(乙醇等)⑸ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑹ 天然橡胶(聚异戊二烯) ⑺ 苯的同系物变色 Mg + Br 2 === MgBr 2 (其中亦有Mg 与H +、Mg 与HBrO 的反应)△2、无机物:⑴ 氢卤酸及卤化物(氢溴酸、氢碘酸、浓盐酸、溴化物、碘化物) ⑵ + 2价的Fe (亚铁盐及氢氧化亚铁) ⑶ -2价的S (硫化氢及硫化物)⑷ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐) ⑸ 双氧水(H 2O 2)五、常见的各类有机物的官能团,结构特点及主要化学性质(1) 烷烃A) 官能团:无 ;通式:C n H 2n +2;代表物:CH 4B) 结构特点:键角为109°28′,空间正四面体分子。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
+3HO—NO2——a-
CH3
I NO2
Il+3H2O
CH2=CH2+Br2”CH2BrCH2Br
CH2=CH2+HBr尸CH3CH2Br
CH2=CH2+H2O浓H2S°4- CH3CH2OH
催化剂.
n CH2=CH2-^CH2—CH2十
催化剂
CH三CH+H2催化-CH2=CH2
CH三CH+HCl催化剂■CH2=CHCl
(30)
(28)
(29)
CH
(14)
C°°H
°H
(16)
(17)
N°2
(18)
N°2
Br
°H
Br
n°2
°Na
(31)
CH3C°°CH2CH3^CHsC°°Na
高中化学各类有机物之间的相互转化关系
光昭
CH3CH3+Br2光昭.CH3CH2Br+HBr
CH2=CH2+H2
催化剂
△
-CH3CH3
(14)
CH3
n CH2=CH
Cl
(15)
CH3
I酸性KMnO4
COOH
I I或酸性K2Cr2o7 I I
(16)
OH+NaOH
OH+Na2CO3
ONa+HCI
催化剂-一CH2—CH
_n
Cl
ONa+CO2+H2O
CaC2+2H2O» CH三CHf+Ca(OH)2
+Br2
催化剂*
A
HBr
(18)
+HO—NO2
I I+3H2
浓H2SO4
(21)C2H5—OH+HO—C2H51400CC2H5—O—C2H5+H2O
(1)
(2)
(3)
(4)
(5)
(6)
(7)
(8)
(9)
(10)
(11)
(⑵
(13)
高中化学各类有机物之间的相互转化关系
(22)CH3CH2OH+HBr△-CH3CH2Br+H2O
(23)2CH3CH2OH+O2催化剂-2CH3CHO+2H2O
+3NH3+H2O
(26)
CH3CHO+2Cu(OH)2厶CH3COOH+CU2OJ+2H2O
(27)
CH3CHO+H2催化剂1CH3CH2OH
(28)
浓H2SO4
CH3(29)
CH3COOC2H5+H2OFHf04-CH3COOH+C2H5OH
/
T
(9)
(20)CH2—CH—
CH3—CH3 w⑵
(8)
2
Cl
Ag
CH
—n Cl
Cu2°
(ii)
(12)
(13)
(26)
_(23).Z(24)
CH3CH2—Br < »CH3—CH2—°H « " CH3CHOCH3C°°H
(27)I
(22)
(21)(19)
CH3CH2°CH2CH3CH3CH2°Na
I
CHO
+2H2
CH2OH
I
CH2OH
COOH CH20H浓H2SO4
COOH+CH2OH△*
COOHCH2OH浓H2SO4
门COOH+ nCH2OH△“
O
22
HH
cc
cc
o
+2出0
o- h+(2n-1)H2O
高中化学各类有机物之间的相互转化关系
各类有机物之间的相互转化关系
高聚酯
(40)人
CH3
ch2—ch
(6)
(3)
CH2CH2(34).CH2°^(36\CH°(37).C°°H
CH2°H(38)CH° C°°H
Br Br
CaC2
(35)
(10)
⑺
(39)
六元环状酯
CH2CH2
CH「CH
z^\
(1)
/汀
浓h2so4
Br
+
+
H2O
催化剂》
△
ONa+H2f
2-OH+2Na ”2
”一ONa+H2。
—ONa+NaHCO3
OH+NaCl
”一OH+NaHCO3
J+3HBr
Br
(19)2CH3CH2OH+2Na-2CH3CH2ONa+H2f
浓H2SO4人
(20)CH3CH2OH仃00Ca CH2=CH2f+H2O
CH3CH2OH+CUO△-CH3CHO+CU+H20
水
(32)CH3CH2Br+NaOH水一CH3CH2OH+NaBr
(33)CH3CH2Br+NaOH
CH2f+NaBr+H2O
(24)
2CH3CHO+O2
催化剂
△
-2CH3COOH
(25
)CH3CHO+2Ag(NH3)2OH
△
〜CH3COONH4+2Ag
CH2Br
(34)CH2Br+ 2Na0H
水
△ch2oh
+2NaBr
(35)
(36)
CH2BrCH2Br+2NaOH
CH2OH+O2催化剂
CH2OH2△
乙醇
肿CH三CHf+2NaBr+2H2O
CHO
CHO+2H2°
(37)CHO+O2催化剂■COOH丿CHO2△COOH
(39)
(40)
(38)
CHO
(30)2CH3COOH+2Na■ 2CH3COONa+H2f
2CH3COOH+Na2O" 2CHsCOONa+H2O
CHsCOOH+NaOHCHsCOONa+HzO
2CH3COOH+Na2CO3-2CHsCOONa+H2O+CO2f
CHsCOOH+NaHCO3”CH3COONa+H2O+CO2f
(31)CH3COOC2H5+NaOH△”CH3COONa+C2H5OH
