2006江苏省高中学生化学竞赛初赛苏州赛区市级奖简报.
2006江苏省高中学生化学竞赛初赛苏州赛区市级奖简报.

女
郑朝霞
苏州市第三中学
李梦婷
女
戴志芬
苏州市第十中学
潘德龙
男
倪江红
苏州新区一中
努拉提
男
吴光明仇剑芳
苏州市吴县中学
张雷
男
陆春明
苏州中学
陆庠
男
严建波
苏州中学
沈凯杰
男
冯澜
苏州实验中学
陈菲
女
王希俭
苏州中学园区校
孙綝意
女
顾利吉
苏州市第一中学校
袁梦羽
男
唐敏
苏州市第三中学
韦凌枫
男
戴志芬
苏州市第三中学
何晟
男
戴志芬
苏州市工业园区第二中学
王晨曦
男
徐进安
苏州中学
王珂清
女
严建波
苏州实验中学
江铖
男
程敏
苏州实验中学
蒯乐
男
沈志华
苏州实验中学
陈侃
男
沈志华
苏州实验中学
姜方昕
男
陈飞
苏州中学园区校
王新刚
男
顾利吉
苏州市第一中学校
朱强强
男
马以瑾
苏州市第三中学
樊忆薇
女
戴志芬
苏州大学附属中学
戴骊融
女
季厚鹏
苏州新区一中耿万里Fra bibliotek男吴光明仇剑芳
季厚鹏
苏州大学附属中学
姚叶明
男
季厚鹏
苏州新区一中
朱磊
男
吴光明仇剑芳
苏州中学
丁景辰
男
冯澜
苏州实验中学
阙喜峰
男
2006年全国高中数学联赛江苏赛区初赛试卷(含参考答案)

2006年全国高中数学联赛江苏赛区初赛试卷一.选择题(本题满分36分,每小题6分) 1.已知数列{}n a 的通项公式2245n a n n =-+,则{}n a 的最大项是 ( )()A 1a()B 2a()C 3a()D 4a2.函数3log 3xy =的图象是( )()A()B()C()D3.已知抛物线22y px =,O 是坐标原点,F 是焦点,P 是抛物线上的点,使得△POF 是直角三角形,则这样的点P 共有( )()A 0个()B 2个()C 4个()D 6个4.设()f x 是定义在R 上单调递减的奇函数.若120x x +>,230x x +>,310x x +>,则( ) ()A ()()()1230f x f x f x ++> ()B ()()()1230f x f x f x ++<()C ()()()1230f x f x f x ++=()D ()()()123f x f x f x +>5.过空间一定点P 的直线中,与长方体1111ABCD A B C D -的12条棱所在直线成等角的直线共有( )()A 0条()B 1条()C 4条()D 无数多条6.在△ABC 中,1tan 2A =,cos 10B =.若△ABC 的最长边为1,则最短边的长为( )()A 5()B 5()C 5()D 5二.填空题(本题满分54分,每小题9分)7.集合{}3,,010A x x n n N n ==∈<<,{}5,,06B y y m m N m ==∈≤≤,则集合A B 的所有元素之和为 .8.设cos 2ϑ=,则44cos sin ϑϑ+的值是 . 9.()323x x-的展开式中,5x 的系数为 .10.已知030330y x y x y ≥⎧⎪-≥⎨⎪+-≤⎩,则22x y +的最大值是 .11.等比数列{}n a 的首项为12020a =,公比12q =-.设()f n 表示这个数列的前n 项的积,则当n = 时,()f n 有最大值.12.长方体1111ABCD A B C D -中,已知14AB =,13AD =,则对角线1AC 的取值范围是 .三.解答题(本题满分60分,第13题、第14题各12分,第15题16分,第16题20分)13.设集合()12log 32A x x ⎧⎫⎪⎪=-≥-⎨⎬⎪⎪⎩⎭,21a B x x a ⎧⎫=>⎨⎬-⎩⎭.若A B ≠∅,求实数a 的取值范围.14.椭圆22194x y +=的右焦点为F ,1224,,,P P P 为24个依逆时针顺序排列在椭圆上的点,其中1P 是椭圆的右顶点,并且122334241PFP P FP P FP P FP ∠=∠=∠==∠.若这24个点到右准线的距离的倒数和为S ,求2S 的值.15.△ABC 中,AB AC <,AD 、AE 分别是BC 边上的高和中线,且BAD EAC ∠=∠. 证明BAC ∠是直角.16.设p 是质数,且271p +的不同正因数的个数不超过10个.求p .B2006年全国高中数学联赛江苏赛区初赛试卷【参考答案】1.B2.A3.B4.B5.C6.D 7.2258.11189.27 10.9 11.1212.()4,513.解:{}13A x x =-≤<,()(){}30B x x a x a =--<. 当0a >时,{}03B x a x a =<<<,由A B ≠∅得03a <<; 当0a <时,{}30B x a x a =<<<,由A B ≠∅得1a >-;当0a =时,{}20B x x =<=∅,与A B ≠∅不符.综上所说,()()1,00,3a ∈-.14.解:椭圆中,3a =,2b =,故c =)F,e =设i FP 与x 轴正向的夹角为i ϑ,i d 为点i P 到右准线的距离.则()2cos 1i i a d e c c ϑ+=-.即()21cos 1i i ce d b ϑ=+.同理()()1222121cos 1cos 1i i i c ce d b b ϑϑ++=+=-+. 所以2121122i i c d d b ++==. 从而2411i id ==∑ 2180S =. 15.如图,取AB 中点I ,连ID 、IE .则IE 为中位线,所以//IE AC ,且I E A E ∠=∠.而B A D E∠=∠,所以 IEA BAD ∠=∠.…………①在直角△ADB 中,I 为斜边中点,所以ID IA =,从而BAD IDA ∠=∠.…………② 联合①、②得A 、I 、D 、E 四点共圆.所以BAD IEB C ∠=∠=∠,∴ 90B C ∠+∠=︒,即90BAC ∠=︒.16.解:当2p =时,22717535p +==⨯,有()()11216++=个正因数;BC当3p =时,24718025p +==⨯,有()()411110++=个正因数.所以2p =、3p =满足条件.当3p >时,()()2711172p p p +=-++.其中p 为奇质数,所以()1p -与()1p +是相邻的两个偶数,从而必然有一个2的倍数和4个倍数,还必然有一个3的倍数,从而()()11p p -+是24的倍数. 设23712423p m m +=⨯=⨯⨯,其中4m ≥.若m 中有不同于2、3的质因数,则271p +的正因数个数()()()31111110≥+++>;若m 中含有质因数3,则则271p +的正因数个数()()312110≥++>;若m 中仅有质因数2,则271p +的正因数个数()()511110≥++>.所以3p >不满足条件.综上所说,所求得的质数p 是2或3.。
2006年全国高中学生化学竞赛决赛理论试题

2006年全国高中学生化学竞赛决赛理论试题参考答案与评分标准(2006年1月7日上海)第1题(9分)(评判分36分)1—1(共11分)A:Na2WO4;B:H2WO4或WO3·H2O;C:WO3(每个1分,合计3分)(1)4FeWO4(s)+8NaOH(l)+O2(g)== 4Na2WO4(l)+2Fe2O3(s)+4H2O(g)2MnWO4(s)+4NaOH(l)+O2(g)== 2Na2WO4(l)+2MnO2(s)+2H2O(g)(产物写成三氧化二锰或四氧化三锰也可)(2)Na2WO4(aq)+2HCl(aq)==H2WO4(s)+2NaCl(aq)(3)H2WO4(s)==WO3(s)+H2O(g)(每个方程式2分,未配平扣1分,不写物态不扣分,合计8分)1—2(共9分)[1] 2 WO3(s)+3C(石墨)==2W(s)+3CO2(g)(2分,未配平不得分)[2]反应在298.15K时的标准焓变,标准熵变和标准自由能变化分别为:△Hφ= ∑ν△f H mφ= [2×0+3×(-393.51)-2×(-842.87)-3×0]=505.21kJ/mol (1.5分)△Sφ= ∑νS mφ= [2×32.64+3×213.64-2×75.90-3×5.74]=537.18J/(mol·K)(1.5分)△Gφ=△Hφ-T△Sφ=[505.21-298.15×537.18/1000]=345.05kJ/mol(2分)298.15K下反应的标准自由能变化是正值,说明此反应不能在该温度下自发进行。
当温度T>[505.21×1000/537.18]=940.49K时,反应才在可能发生。
(2分)(方程式产物为CO,计算正确不扣分)1—3(共4分)因为钨的熔点很高,不容易转变为液态。
如果用碳做还原剂,混杂在金属中的碳不易除去,而且碳会在高温下和金属钨反应形成碳化钨(WC,W2C),不容易获得纯的金属钨。
2006年第十六届“天原杯”全国初中学生化学素质和实验能力竞赛(江苏赛区)初赛试卷

2006年第十六届“天原杯”全国初中学生化学素质和实验能力竞赛(江苏赛区)初赛试卷2006年第十六届“天原杯”全国初中学生化学素质和实验能力竞赛(江苏赛区)初赛试卷一、选择题(本题l0小题,每小题1分,共10分.每小题有1个选项符合题意)2.(1分)为使2008年北京奥运会办成“绿色奥运会”,某校同学提出下列建议:①开发新清洁能源,减少化石燃料的燃烧;②开发生产无汞电池;③分类回收垃圾;④提倡使用一次性发泡塑料餐具和塑料袋;⑤提倡使用手帕,减3.(1分)煤矿坑道内的“瓦斯”爆炸往往造成重大矿难事故,“瓦斯”的主要成分是甲烷气体.以下措施不能防止煤).5.(1分)下图是某兴趣小组设计的一套实验装置,装置足以维持实验过程中小白鼠的生命活动,瓶口密封.装置气密性良好.经数小时后,这样会导致试剂瓶中的气体越来越少,压强不断减小,则会出现下列哪种情况?(忽略水蒸气和温度变化对实验结果的影响)()6.(1分)1911年著名物理学家卢瑟福等人为探索原子的内部结构进行了下面的实验.他们用一束带正电的、质量比电子大得多的高速运动的α粒子轰击金箔,发现:①大多数α粒子能穿透金箔而不改变原来的运动方向;②一小部分α粒子改变了原来的运动方向;③有极少数α粒子被弹了回来.由此推出关于原子内部结构的一些假设不合理的是()7.(1分)(2005•佛山)锂电池是新型的高能电池,以质量轻、电容量大,颇受手机、手提电脑等用户的青睐.某种锂电池的总反应可表示为Li+MnO2═LiMnO2.以下说法正确的是()①该反应中Mn的化合价发生了变化:+4→+3②该反应属于化合反应③LiMnO2为新型的氧化物8.(1分)在一个密闭的钢筒内有A、B、C、D四种物质,通过电火花引燃后,充分发生反应.经测定,钢筒内反10.(1分)目前,科学家提出了一种最经济最理想的获得氢能源的循环体系(如图).下列说法错误的是()O二、选择题(本题8小题,每小题3分,共24分.每小题有1-2个选项符合题意.若有两个答案的错选1个不得分,漏选1个扣2分)11.(3分)“达菲”是治疗人类感染禽流感的一种药物,而合成“达菲”的主要原料莽草酸(分子式C7H10O5)存在于12.(3分)根据图判断,下列说法错误的是().C D.14.(3分)(2004•南通)向AgNO3、Cu(NO3)2的混合溶液中加入一些铁粉,完全反应后过滤.不可能存在的情15.(3分)(2009•潍坊)在甲溶液中滴加几滴石蕊试液,溶液呈蓝色;然后再滴加乙溶液,当滴至甲、乙两物质正好完全反应时,溶液呈紫色;再继续滴加乙溶液时,溶液呈红色.在上述过程中,表示溶液的pH(纵坐标)与滴.C D.16.(3分)铜和铝是日常生活和生产中重要的金属.钛(Ti)有许多神奇的性能,越来越引起人们的关注,是2117.(3分)利用化学实验可以鉴别生活中的一些物质.下表中各组物质的鉴别方法能将本组待鉴别的物质都区分出18.(3分)对于一定温度时某饱和溶液,可提供以下数据:①溶液的质量、②溶剂的质量、③溶液的体积、④溶质三、填空题(本题包括7小题,共33分)19.(3分)美国“勇气”号火星探测器成功登陆火星,使人类对火星的研究进入了新阶段.现在已测知,火星大气层上方无臭氧层,大气中95%为C02,O2和H20的含量极少.火星目前还不适宜人类生存的理由是(写3点)①_________;②_________;③_________.20.(4分)(2005•荆州)氨气(NH3)是一种无色有刺激性气味的气体,极易溶于水,其水溶液称为氨水,显碱性.其化学方程式为:2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H20.氨气在化工生产中应用广泛,如“侯氏制碱法”中就用到氨气.试回答下列问题:(1)实验室制氨气的发生装置与_________相同(选择“A”或“B”填空).A.实验室用KMnO4制O2B.实验室用大理石与稀盐酸制CO2(2)收集氨气_________用排水法收集(填“能”或“不能”).(3)“侯氏制碱法”中关键一步的反应原理可表示为:NH3+CO2+H2O+NaCl=NaHCO3+XX是一种氮肥,其化学式为_________.21.(4分)常温下,将50mL水和50mL酒精(密度:0.789克/cm3)依次缓缓注入下图100mL带有刻度“细颈”容器(容量瓶)中,注满后立刻塞紧塞子振荡,静置片刻,容量瓶细颈上部有空柱形成.实验发现,若水和酒精的注入先后顺序不同(其他条件相同),形成空柱的长短也不同.何种加液顺序形成的空柱长,为什么?_________.22.(4分)钛(Ti)和钛的合金被认为是2l世纪重要的金属材料.目前大规模生产钛的方法是:第一步,在高温时,将金红石(Ti02)、碳粉混合并通入氯气制得TiCl4和一种可燃性气体,写出该反应的化学方程式_________;第二步,在氩气的环境中,用过量的镁在加热条件下与TiCl4.反应制得金属钛(氩气不参加反应).写出该反应的化学方程式_________.23.(7分)航天飞行器座舱内空气更新过程如下图所示:(1)装置I的作用是_________.(2)装置Ⅱ是CO2和H2的反应装置,该反应的化学方程式为_________(可不写出反应条件).反应类型是_________.(3)装置Ⅲ发生反应的化学方程式为_________.反应类型是_________.(4)从装置I、Ⅱ、Ⅲ可看出,O2的来源是C02和H20,若产生896g 02,消耗1012g C02,则同时消耗H20_________ g.24.(6分)复分解反应是我们学过的化学基本反应类型之一.学习时,应注意将知识进行归纳、总结,深刻理解复分解反应发生的条件,形成完整的知识体系.(已知BaS04难溶于水)(1)写出下列反应的化学方程式:①氯化钡溶液与硫酸钠混合:_________:②碳酸钾溶液与稀盐酸混合:_________;③氢氧化钡溶液与稀硝酸混合:_________.(2)你想过上述复分解反应为什么能够发生吗?这是因为在这些反应物中含有一些“特殊”的阴、阳离子,它们能相互结合.如上述反应①中,实际参加反应的离子是Ba2+和S042一,而Cl一、Na+则是“旁观者”,并没有参加反应.请你分析上述反应②中实际参加反应的离子是_________;上述反应③中实际参加反应的离子是_________.(3)请根据你的想象,在下图右边的容器中画出体现NaOH溶液和稀盐酸反应产物的示意图.25.(5分)从HCl、NaCl、FeCl3、NaOH、Na2CO3、CuSO4几种溶液中取出其中的两种混合后充分振荡,静置后得到一无色无沉淀的混合溶液,继续进行实验,所观察到的现象记录如下:(1)取少量混合溶液,用pH试纸测定得混合溶液的pH>7.(2)再取少量混合溶液,向其中滴入足量浓CaCl2溶液,有白色沉淀出现.试根据实验现象推断所取的两种溶液的可能组合(写出溶质的化学式,有几组写几组,不一定填满).①_________,②_________,③_________,④_________,⑤_________.四、实验题(本题共3小题,共23分)26.(8分)乙醇是以高粱、玉米、薯类等为原料,经发酵、蒸馏而制得,属于可再生能源.在汽油中加入适量乙醇作为汽油燃料,可节省石油资源,减少汽车尾气的污染.2001年4月2日国家技术监督局发布《车用乙醇汽油》国家标准,并于同年4月15日开始实施.乙醇(C2H5OH)完全燃烧时生成CO2和H20.如果氧气不充足,乙醇燃烧可能还生成CO.现用以上装置进行实验,确证乙醇燃烧产物中有CO、CO2和H20.请回答下列问题:(1)能确证产物中有H20的现象是无水CuS04变蓝;能确证产物中有CO的现象是_________(2)实验时,可观察到装置B中石灰水变浑浊,D中石灰水无变化.B装置的作用是_________;C装置的作用是_________;D装置的作用是_________.(3)若乙醇燃烧产物中CO和CO2的总质量为25.2g,其中碳元素与氧元素的质量比为2:5,则参加化学反应的乙醇的质量为_________,反应产物中H2O的质量为_________.27.(8分)某工厂排出的废液中主要含有Zn(N03)2和AgNO3,为了回收金属银和硝酸锌,某学生设计了以下实验步骤:试推断:X为_________,Y为_________,A为_________(以上均填化学式),加入适量的Ba(N03)2溶液,发生的化学方程式为_________.28.(7分)某化学兴趣小组的学生研究过量的炭粉与Fe2O3在高温条件下反应的气体产物成分.探究过程如下:(1)提出假设:气体产物全部是C02.(2)查阅资料:a.氮气不能与炭粉及Fe2O3反应b.高温下可以发生下列反应:2Fe203+3C4Fe+3CO2↑C+C022CO(3)设计方案:将一定量氧化铁在隔绝空气的环境下与过量炭粉充分反应.用实验中实际测得产生气体的质量,与理论计算得到的CO2的质量进行比较.(4)实验装置:如图所示.(5)实验操作:①称量:反应前Fe2O3的质量3.20g;炭粉的质量2.00g;玻璃管C的质量48.48g.反应后玻璃管与残留固体共52.24g.②加热前先通一段时间氮气,再夹紧弹簧夹T,点燃酒精喷灯加热.(6)问题分析:①用酒精喷灯而不用酒精灯的目的是_________.②加热前先通一段时间氮气的目的是_________.③理论计算:若氧化铁与炭粉反应的气体产物全部是C02,求3.20g氧化铁完全反应时生成CO2的质量.④根据实验数据计算实验中实际获得气体的质量.(7)结论:(要求简述获得结论的理由)五、计算题(本题共2小题,共10分)29.(4分)“骨质疏松症”是人体缺钙引起的,可服用补钙剂来治疗.乳酸钙(CaC6H10O6•5H20)是一种常见的补钙剂,市售乳酸钙片剂每片含乳酸钙200mg,一个成年缺钙病人每天服用20片乳酸钙片剂可达到补钙目的.试计算:若该成年缺钙病人改用喝牛奶(每100 mL牛奶中含钙约0.104 g)来补钙,每天喝多少毫升牛奶相当于服用20片乳酸钙片剂?(CaC6H10O6•5H20的相对分子质量为308)30.(6分)二氧化硫是大气污染物之一.我国的环境空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空含碘(I.)1.27mg的碘水,再加入2~3滴淀粉溶液(淀粉遇I2变蓝色),通过抽气装置抽气,使空气由导气管进入试管与碘水充分接触,当溶液由蓝色变为无色时,恰好完全反应.反应的化学方程式是:S02+I2+2H20=H2SO4+2HI.实验过程中进入试管内的空气的总体积为1 000L.请通过计算说明该法测定的此空气中二氧化硫的浓度级别.2006年第十六届“天原杯”全国初中学生化学素质和实验能力竞赛(江苏赛区)初赛试卷参考答案与试题解析一、选择题(本题l0小题,每小题1分,共10分.每小题有1个选项符合题意)2.(1分)为使2008年北京奥运会办成“绿色奥运会”,某校同学提出下列建议:①开发新清洁能源,减少化石燃料的燃烧;②开发生产无汞电池;③分类回收垃圾;④提倡使用一次性发泡塑料餐具和塑料袋;⑤提倡使用手帕,减3.(1分)煤矿坑道内的“瓦斯”爆炸往往造成重大矿难事故,“瓦斯”的主要成分是甲烷气体.以下措施不能防止煤).5.(1分)下图是某兴趣小组设计的一套实验装置,装置足以维持实验过程中小白鼠的生命活动,瓶口密封.装置气密性良好.经数小时后,这样会导致试剂瓶中的气体越来越少,压强不断减小,则会出现下列哪种情况?(忽略水蒸气和温度变化对实验结果的影响)()6.(1分)1911年著名物理学家卢瑟福等人为探索原子的内部结构进行了下面的实验.他们用一束带正电的、质量比电子大得多的高速运动的α粒子轰击金箔,发现:①大多数α粒子能穿透金箔而不改变原来的运动方向;②一小部分α粒子改变了原来的运动方向;③有极少数α粒子被弹了回来.由此推出关于原子内部结构的一些假设不合理的是()7.(1分)(2005•佛山)锂电池是新型的高能电池,以质量轻、电容量大,颇受手机、手提电脑等用户的青睐.某种锂电池的总反应可表示为Li+MnO2═LiMnO2.以下说法正确的是()①该反应中Mn的化合价发生了变化:+4→+3②该反应属于化合反应③LiMnO2为新型的氧化物8.(1分)在一个密闭的钢筒内有A、B、C、D四种物质,通过电火花引燃后,充分发生反应.经测定,钢筒内反:=110.(1分)目前,科学家提出了一种最经济最理想的获得氢能源的循环体系(如图).下列说法错误的是()O二、选择题(本题8小题,每小题3分,共24分.每小题有1-2个选项符合题意.若有两个答案的错选1个不得分,漏选1个扣2分)11.(3分)“达菲”是治疗人类感染禽流感的一种药物,而合成“达菲”的主要原料莽草酸(分子式C7H10O5)存在于=12.(3分)根据图判断,下列说法错误的是().C D.14.(3分)(2004•南通)向AgNO3、Cu(NO3)2的混合溶液中加入一些铁粉,完全反应后过滤.不可能存在的情15.(3分)(2009•潍坊)在甲溶液中滴加几滴石蕊试液,溶液呈蓝色;然后再滴加乙溶液,当滴至甲、乙两物质正好完全反应时,溶液呈紫色;再继续滴加乙溶液时,溶液呈红色.在上述过程中,表示溶液的pH(纵坐标)与滴.C D.16.(3分)铜和铝是日常生活和生产中重要的金属.钛(Ti)有许多神奇的性能,越来越引起人们的关注,是2117.(3分)利用化学实验可以鉴别生活中的一些物质.下表中各组物质的鉴别方法能将本组待鉴别的物质都区分出18.(3分)对于一定温度时某饱和溶液,可提供以下数据:①溶液的质量、②溶剂的质量、③溶液的体积、④溶质100%三、填空题(本题包括7小题,共33分)19.(3分)美国“勇气”号火星探测器成功登陆火星,使人类对火星的研究进入了新阶段.现在已测知,火星大气层上方无臭氧层,大气中95%为C02,O2和H20的含量极少.火星目前还不适宜人类生存的理由是(写3点)①缺少氧气;②缺少水;③易受太阳紫外线灼伤.20.(4分)(2005•荆州)氨气(NH3)是一种无色有刺激性气味的气体,极易溶于水,其水溶液称为氨水,显碱性.其化学方程式为:2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H20.氨气在化工生产中应用广泛,如“侯氏制碱法”中就用到氨气.试回答下列问题:(1)实验室制氨气的发生装置与A相同(选择“A”或“B”填空).A.实验室用KMnO4制O2B.实验室用大理石与稀盐酸制CO2(2)收集氨气不能用排水法收集(填“能”或“不能”).(3)“侯氏制碱法”中关键一步的反应原理可表示为:NH3+CO2+H2O+NaCl=NaHCO3+XX是一种氮肥,其化学式为NH4Cl.21.(4分)常温下,将50mL水和50mL酒精(密度:0.789克/cm3)依次缓缓注入下图100mL带有刻度“细颈”容器(容量瓶)中,注满后立刻塞紧塞子振荡,静置片刻,容量瓶细颈上部有空柱形成.实验发现,若水和酒精的注入先后顺序不同(其他条件相同),形成空柱的长短也不同.何种加液顺序形成的空柱长,为什么?先注入酒精后加水产生的空气柱较长.因为当水向酒精中缓缓注入时,由于水的密度大于酒精,能比较快地渗入酒精分子间的间隙之中,所以振荡后静置形成的空柱比较长..22.(4分)钛(Ti)和钛的合金被认为是2l世纪重要的金属材料.目前大规模生产钛的方法是:第一步,在高温时,将金红石(Ti02)、碳粉混合并通入氯气制得TiCl4和一种可燃性气体,写出该反应的化学方程式Ti02+2C+2C12TiCl4+2CO;第二步,在氩气的环境中,用过量的镁在加热条件下与TiCl4.反应制得金属钛(氩气不参加反应).写出该反应的化学方程式TiCl4+2Mg Ti+2MgCl2.Ti+2MgCl23.(7分)航天飞行器座舱内空气更新过程如下图所示:(1)装置I的作用是分离空气、水和二氧化碳.(2)装置Ⅱ是CO2和H2的反应装置,该反应的化学方程式为2H2+C02═2H2O+C(可不写出反应条件).反应类型是置换反应.(3)装置Ⅲ发生反应的化学方程式为2H2O2H2↑+O2↑.反应类型是分解反应.(4)从装置I、Ⅱ、Ⅲ可看出,O2的来源是C02和H20,若产生896g 02,消耗1012g C02,则同时消耗H20180 g.O×÷=180gO24.(6分)复分解反应是我们学过的化学基本反应类型之一.学习时,应注意将知识进行归纳、总结,深刻理解复分解反应发生的条件,形成完整的知识体系.(已知BaS04难溶于水)(1)写出下列反应的化学方程式:①氯化钡溶液与硫酸钠混合:BaCl2+Na2SO4=BaSO4↓+2NaCl:②碳酸钾溶液与稀盐酸混合:K2CO3+2HCl=2KCl+CO2↑+H2O;③氢氧化钡溶液与稀硝酸混合:Ba(OH)2+2HNO3=Ba(NO3)2+2H2O.(2)你想过上述复分解反应为什么能够发生吗?这是因为在这些反应物中含有一些“特殊”的阴、阳离子,它们能相互结合.如上述反应①中,实际参加反应的离子是Ba2+和S042一,而Cl一、Na+则是“旁观者”,并没有参加反应.请你分析上述反应②中实际参加反应的离子是CO32﹣、H+;上述反应③中实际参加反应的离子是H+、OH﹣.(3)请根据你的想象,在下图右边的容器中画出体现NaOH溶液和稀盐酸反应产物的示意图.25.(5分)从HCl、NaCl、FeCl3、NaOH、Na2CO3、CuSO4几种溶液中取出其中的两种混合后充分振荡,静置后得到一无色无沉淀的混合溶液,继续进行实验,所观察到的现象记录如下:(1)取少量混合溶液,用pH试纸测定得混合溶液的pH>7.(2)再取少量混合溶液,向其中滴入足量浓CaCl2溶液,有白色沉淀出现.试根据实验现象推断所取的两种溶液的可能组合(写出溶质的化学式,有几组写几组,不一定填满).①NaCl、Na2CO3,②NaOH、Na2CO3,③NaCl、NaOH,④Na2CO3与HCl,⑤NaOH与HCl.四、实验题(本题共3小题,共23分)26.(8分)乙醇是以高粱、玉米、薯类等为原料,经发酵、蒸馏而制得,属于可再生能源.在汽油中加入适量乙醇作为汽油燃料,可节省石油资源,减少汽车尾气的污染.2001年4月2日国家技术监督局发布《车用乙醇汽油》国家标准,并于同年4月15日开始实施.乙醇(C2H5OH)完全燃烧时生成CO2和H20.如果氧气不充足,乙醇燃烧可能还生成CO.现用以上装置进行实验,确证乙醇燃烧产物中有CO、CO2和H20.请回答下列问题:(1)能确证产物中有H20的现象是无水CuS04变蓝;能确证产物中有CO的现象是装置E中黑色粉末变成亮红色;装置F中石灰水变浑浊(2)实验时,可观察到装置B中石灰水变浑浊,D中石灰水无变化.B装置的作用是检验C02的存在;C装置的作用是吸收CO2;D装置的作用是证明C02已被除尽.(3)若乙醇燃烧产物中CO和CO2的总质量为25.2g,其中碳元素与氧元素的质量比为2:5,则参加化学反应的乙醇的质量为13.8g,反应产物中H2O的质量为16.2g.×÷÷=13.8g=27.(8分)某工厂排出的废液中主要含有Zn(N03)2和AgNO3,为了回收金属银和硝酸锌,某学生设计了以下实验步骤:试推断:X为Zn,Y为H2SO4,A为Ag、Zn(以上均填化学式),加入适量的Ba(N03)2溶液,发生的化学方程式为ZnSO4+Ba(N03)2=Zn(N03)2+BaS04↓.28.(7分)某化学兴趣小组的学生研究过量的炭粉与Fe2O3在高温条件下反应的气体产物成分.探究过程如下:(1)提出假设:气体产物全部是C02.(2)查阅资料:a.氮气不能与炭粉及Fe2O3反应b.高温下可以发生下列反应:2Fe203+3C4Fe+3CO2↑C+C022CO(3)设计方案:将一定量氧化铁在隔绝空气的环境下与过量炭粉充分反应.用实验中实际测得产生气体的质量,与理论计算得到的CO2的质量进行比较.(4)实验装置:如图所示.(5)实验操作:①称量:反应前Fe2O3的质量3.20g;炭粉的质量2.00g;玻璃管C的质量48.48g.反应后玻璃管与残留固体共52.24g.②加热前先通一段时间氮气,再夹紧弹簧夹T,点燃酒精喷灯加热.(6)问题分析:①用酒精喷灯而不用酒精灯的目的是获取反应所需的高温条件.②加热前先通一段时间氮气的目的是清除试管中空气(氧气),防止炭粉与空气中氧气发生反应.③理论计算:若氧化铁与炭粉反应的气体产物全部是C02,求3.20g氧化铁完全反应时生成CO2的质量.④根据实验数据计算实验中实际获得气体的质量.(7)结论:(要求简述获得结论的理由)+3C4Fe+3CO2+3C五、计算题(本题共2小题,共10分)29.(4分)“骨质疏松症”是人体缺钙引起的,可服用补钙剂来治疗.乳酸钙(CaC6H10O6•5H20)是一种常见的补钙剂,市售乳酸钙片剂每片含乳酸钙200mg,一个成年缺钙病人每天服用20片乳酸钙片剂可达到补钙目的.试计算:若该成年缺钙病人改用喝牛奶(每100 mL牛奶中含钙约0.104 g)来补钙,每天喝多少毫升牛奶相当于服用20片乳酸钙片剂?(CaC6H10O6•5H20的相对分子质量为308)×30.(6分)二氧化硫是大气污染物之一.我国的环境空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空含碘(I.)1.27mg的碘水,再加入2~3滴淀粉溶液(淀粉遇I2变蓝色),通过抽气装置抽气,使空气由导气管进入试管与碘水充分接触,当溶液由蓝色变为无色时,恰好完全反应.反应的化学方程式是:S02+I2+2H20=H2SO4+2HI.实验过程中进入试管内的空气的总体积为1 000L.请通过计算说明该法测定的此空气中二氧化硫的浓度级别.参与本试卷答题和审题的老师有:blq728;727056;zlfzlf;lzhx;xinxiuhua;sdpylytx;xzoldman;lsj1660;巴淑侠;723383;高宪奎;mlp;王老师;737560;海影;fqk(排名不分先后)菁优网2013年4月27日。
第28届中国化学奥赛(江苏赛区)喜报

喜报
第28届中国化学奥林匹克竞赛(江苏赛区)暨江苏省高中学生化学奥林匹克竞赛成绩已经揭晓,我校取得喜人的成绩:高三(5)班李扬、徐斌两位同学荣获江苏省一等奖、高三(5)班陈文元等44位同学荣获江苏省二等奖、高三(5)班高星等16位同学荣获江苏省三等奖。
特向全校师生报喜!
江苏省一等奖:
高三(5)班李扬徐斌辅导老师:厉业余江苏省二等奖:
高三(5)班:
方定君、汤尧禹、李梦蝶、杨菲菲、张思雨、谢天宇、倪行楷、陈文元、
刘远程、林童、陆起、龚冠睿、康雯、王天昊、黄宜冬、董宇阳、董志鹏、
丁文龙、刘玉洁、田宇、潘若凡、郑杰、王涵、吴婧谌、吴瑞、薛启东、
杨荷馨、张越、赵远、郑鸿飞、郑礼平、林浚哲、许学仁高三(6)班:
彭城、吴德文、徐武辅导老师:康玉琴高三(7)班:
马乐、李婉苏辅导老师:项维松高二(1)班:
刘苇辅导老师:李继龙高二(2)班:
柏夏星、蒋希程、钱鹏昊、赵康、王小马辅导老师:孟翔江苏省三等奖:
高三(5)班:
高星、纪云鹏、李鼎、缪言、王家凌、杨欣妍、杨俣
高三(6)班:
李伟、马成宇、钱玉东、余华山、周天伦、邹少飞
高二(2)班:
陈嘉琳、沈达文、王汇雯。
2006年全国高中生化学竞赛(省级赛区)试题例析与思考

中的部分试题展开了分析,并且对今后同一级别化学竞赛的辅导提出了几点思考。
关键词:化学竞赛特点思考跟往年的试题相比,2006年的试题在试卷长度、题目类型上基本稳定,在内容覆盖上主要涉及到原子结构、分子结构、晶体结构、配合物知识等理论和常见的元素化合物知识,在知识点上仍然注重基础知识考查,当然涉及的知识水平是高于高中化学,大致与大学底年级课本相当,在能力上强调学生获取信息、加工信息、从化学视角去分析解决实际问题等能力的考查。
但是,今年试题也稳中有变,第一次出现开放性的有机物合成题、突出了化学平衡常数的计算、要求学生具备一定的英语基础,在题意表达上多处出现用英语或代号等。
今年的试题对今后高中生化学竞赛(省级赛区)的辅导有很强的指导意义。
1 例析06年试题的特点1.1 继承了传统题型跟往年的全国高中生化学竞赛(省级赛区)试题一样,今年的试题仍有许多常规题型,体现“思维容量大,应答书写少”的命题意图。
1.1.1 科学谜语题这类题与我们平时的“猜谜”有相似之处,但又有不同。
平时“猜谜”得出的谜底是猜谜人已有的知识,一旦被猜出,感觉就很自信;而科学谜语题的谜底,却是大多数学生未知的知识,所以,即便得出了结果,也会觉得是难以把握。
当然,也不排除有学生已经有了该知识,但绝不是一般的高中学生能够具备的知识,只有学习主动、肯钻研的学生才有可能具备。
由于得出的结论是新的知识,所以对学生创造性思维的要求特别高。
例1(第6 题)潜在储氢材料——化合物A 是第二周期两种氢化物形成的路易斯酸碱对,是乙烷的等电子体,相对分子质量30.87,常温下为白色晶体,稳定而无毒。
刚刚融化的A 缓慢释放氢气,转变为化合物B(乙烯的等电子体)。
B 不稳定,易聚合成聚合物C(聚乙烯的等电子体)。
C 在155℃释放氢气转变为聚乙炔的等电子体,其中聚合度为3的化合物D 是苯的等电子体。
高于500℃时D 释放氢气,转变为化合物E,E 有多种晶型。
(1)写出A、B、C、D、E 的化学式。
2006年中国高中化学竞赛奥林匹克(初赛)试题及答案、评分标准与细则
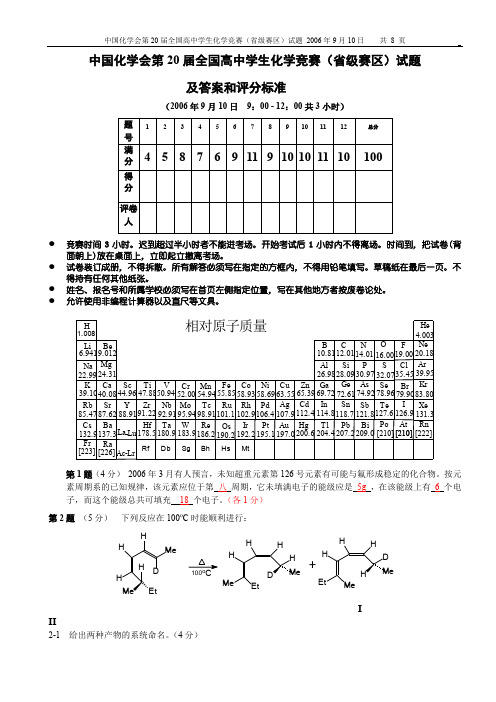
● 竞赛时间3小时。
迟到超过半小时者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
● 试卷装订成册,不得拆散。
所有解答必须写在指定的方框内,不得用铅笔填写。
草稿纸在最后一页。
不得持有任何其他纸张。
● 姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。
● 允许使用非编程计算器以及直尺等文具。
1.008Zr Nb Mo Tc Ru Rh Pd Ag Cd InSn Sb Te I Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Ac-Lr HLi BeB C N O F Na MgAl Si P Cl S K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Rb Cs Fr Sr BaRaY La Lu -6.9419.01222.9924.3139.1040.0885.4787.62132.9137.3[223][226]44.9647.8850.9452.0054.9455.8558.9363.5558.6965.3910.8126.9869.7212.0128.0972.61114.8204.4118.7207.2112.4200.6107.9197.0106.4195.1102.9192.2101.1190.298.91186.295.94183.992.91180.991.22178.588.9114.0116.0019.0030.9774.92121.8209.032.0778.96127.6[210][210]126.979.9035.454.00320.1839.9583.80131.3[222]HeNe Ar KrXe Rn相对原子质量Rf Db Sg Bh Hs Mt第1题(4分) 2006年3月有人预言,未知超重元素第126号元素有可能与氟形成稳定的化合物。
2006年苏州市初中毕业暨升学考试试卷(化学)

2006年苏州市初中毕业暨升学考试试卷化学本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,第Ⅰ卷l至2页,第Ⅱ卷3至8页;共5大题、30小题,满分100分;考试用时100分钟。
第Ⅰ卷(选择题,共30分)注意事项:1.答第Ⅰ卷前,考生务必将自己的姓名、考点名称用钢笔或圆珠笔写在答题卡的相应位置上;将考场号、座位号、准考证号、考试科目用铅笔涂在答题卡上。
2.每小题选出答案后,用铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。
不能答在试卷上。
3.考试结束,请将本试卷和答题卡一并交回。
可能用到的相对原子质量:H—l C—12 O一16 S一32 Ca一40一、选择题(本题包括15小题,每小题2分,共30分。
每小题只有一个....选项符合题意。
) 1.《苏州市国民经济和社会发展第十一个五年规划纲要》提出了关于资源环境发展的目标,其中有利于控制我市空气污染的是A.二氧化硫年排放总量在2005年的基础上减少5%以上B.城市生活污水集中。
处理率达85%以上C.氨氮等主要水污染物年排放总量在2005年的基础上减少8%以上D.通过资源空间配置,提高土地集约利用效率2.考古发现,早在一万多年前我国已开始制造和使用陶器。
现代人们已能生产新型陶瓷材料,如用氧化铝等为原料生产的陶瓷已制造发动机零件。
下列有关氧化铝陶瓷的说法错误..的是A.该陶瓷属于无机非金属材料B.该陶瓷中的原料氧化铝属于非金属氧化物C.该陶瓷耐高温、强度高D.该陶瓷耐酸、碱等化学物质的腐蚀3.下列化学符号与名称相符合的是A.氧元素O2 B.氯离子C1-C.碳酸钠NaCO3D.金AU4.下列物质属于纯净物的是A.食用醋B.天然气C.含碘盐D.蒸馏水5.氧气是空气的主要成分之一,有关氧气说法错误..的是A.用带火星的木条可以检验氧气B.用加热高锰酸钾的方法可以制取氧气C.鱼类能在水中生活,证明氧气易溶于水D.铁丝能在氧气中燃烧,火星四溅,产生黑色固体6.有道是:水火无情。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
男
季厚鹏
苏州新区一中
王伟
男
吴光明仇剑芳:
苏州新区一中
杨君
男
吴光明仇剑芳
苏州中学
夏威仪
男
冯澜
苏州实验中学
俞霆霆
男
陈飞—
苏州市第一中学校
濮雯
女
唐敏
苏州市第三中学
范坚
男
戴志分
苏州市第十中学
俞钢
男
艾水高「
苏州大学附属中学
戴允浪
男
季厚鹏
苏州大学附属中学
吴桂华
男
季厚鹏
苏州大学附属中学
姚叶明
男
季厚鹏1
苏州新区一中
:苗静
女:
吴光明仇剑芳:
苏州外国语学校
季晓婷
女—
刘富兵
苏州市工业园区第二中学
张勤勇
男
叶梅
苏州中学
:李成溪
女
王小莉
苏州中学
王逸骏
男
顾菲菲
苏州中学
钱晨熹
男
顾菲菲
苏州实验中学
:陆丽芳
女
陈飞:
苏州实验中学
庄严
男
陈飞
苏州实验中学
沈龙
男
陈飞
苏州市第一中学校
r芮沁恰
女
郑朝霞
苏州市第一中学校
张鞠琳
男—
马以瑾
苏州市第一中学校
顾峰
男
王永银
苏州市吴中区苏苑中学
李侠
女
杨美秀
苏州市江苏省外国语学校
朱迪
男
王永银
苏州市江苏省外国语学校
干澄姣
女
王永银
办州市吴中区甪直中学
严建文
男
汤彩虹
苏州市江苏省外国语学校
朱晓玲
女
王永银
江苏省木渎咼级中学
朱伟伟
男
陈瑾
苏州市吴中区苏苑中学
褚纯隽
女
杨美秀
苏州市江苏省外国语学校
陈洁
女
王永银
江苏省木渎咼级中学
苏州中学:
张伟
男
李雷雷:
苏州实验中学
陆斐
男
沈志华
苏州大学附属中学
杨扬
男
季厚鹏
苏州外国语学校「
窦峥
男
刘富兵
苏州中学
刘洋
女
严建波
苏州中学
纪路
男
严建波
苏州中学:
俞舟
女
李雷雷「
苏州实验中学
钱璐
女
王希俭
苏州市第一中学校
孙莹
女
唐敏
苏州市第一中学校:
奚陵
男
唐敏
苏州市第一中学校
沙菲菲
女
郑朝霞
苏州市第三中学
李梦婷
女
戴志分
男
沈志华
苏州实验中学
贺鸣一
男
沈志华
苏州实验中学
石凤燕
女:
陈飞:
苏州市第一中学校
陶心韵
女
唐敏
苏州市第一中学校
王小青
女
唐敏
苏州市第一中学校
蔡睿
男
唐敏
苏州市第一中学校
P顾莹
女
马以瑾
苏州市第三中学
刘禹
男
戴志分
苏州市第三中学
:徐竹筠
女
纪露希
苏州市第三中学
r成晓奕
女
纪露希
苏州市第十中学
徐一峰
男
艾水高
苏州新区一中
女
王永银
相城区一等奖
学校
学生
性别
辅导教师
黄埭中学
周岩1
男
陈新
黄埭中学
周文超
男
潘红星
黄埭中学
顾洁
男
陆小鹏
黄埭中学
钱怡]
女
陈新
黄埭中学
郁金珠
女
陈新
黄埭中学
唐敏
苏州市第一中学校
张柱军
男
唐敏
苏州市第三中学
董君毅
男
周斌
苏州市第十中学
王莉娜
女
张莉
苏州大学附属中学
金亚兰
女
季厚鹏-
苏州中学
「张聪
男:
严建波
苏州中学
陈玄玄
女
李雷雷
苏州中学
刘旭旻
男
李雷雷
苏州中学
:查宇振
男「
李雷雷:
苏州实验中学
朱晶
男
程敏
苏州实验中学
梁超
男
王希俭
苏州实验中学
沈斌
男:
沈志华
苏州实验中学
范一鸣
林晨
男
沈志华
苏州实验中学
毛云鹏
男
陈飞
苏州实验中学
伍佳玉
男
陈飞
苏州市第一中学校
董晓蝶
女
唐敏
苏州市第一中学校:
丁志或
男
唐敏「
苏州市第一中学校
钱子辛
男
唐敏
苏州市第十中学
陈熙旳
女
艾水高
苏州市第十中学
归靖慷
男
艾水高:
苏州市第十中学
施远
女
杨宇红
苏州大学附属中学
孙流洋
男
季厚鹏
苏州大学附属中学
张昊
男
季厚鹏
苏州大学附属中学
苏州市第十中学
潘德龙
男
倪江红:
苏州新区中
努拉提
男
吴光明仇剑芳1
苏州市吴县中学
张雷
男
陆春明
苏州中学
陆庠
男
严建波
苏州中学
沈凯杰
男
冯澜
苏州实验中学
陈菲
女
王希俭
苏州中学园区校
孙綝意
女
顾利吉
苏州市第一中学校
袁梦羽
男
唐敏
苏州市第三中学
韦凌枫
男
戴志分
苏州市第三中学
何晟
男
戴志分
苏州市第十中学
沈怡
女
艾水高
苏州市第十中学
王珂清
女
严建波
苏州实验中学
江铖
男
程敏:
苏州实验中学
蒯乐
男
沈志华
苏州实验中学
陈侃
男
沈志华
苏州实验中学
姜方昕
男
陈飞
苏州中学园区校
王新刚
男
顾利吉
苏州市第一中学校
朱强强
男
马以瑾
苏州市第三中学
樊忆薇
女
戴志分
苏州大学附属中学
戴骊融
女
季厚鹏
苏州新区一中
耿万里
男
吴光明仇剑芳
苏州外国语学校
杜月潭
男
刘富兵
学校
学生
性别
辅导教师
陶嗣廉
男
马以瑾
苏州市第三中学
:邵俊
男
戴志分
苏州外国语学校
蒋臻真
女
刘富兵
苏州外国语学校
张遥宏
男
刘富兵
苏州市吴县中学
顾晓锋
男
陆春明
苏州中学
:刘宇晟
男—
严建波
苏州中学
翁炳辰
男
严建波
苏州中学
蒋媛君
女
冯澜
苏州中学
崔湛远
男—
李雷雷
苏州实验中学
:王白車 李碧雯
女
程敏
苏州实验中学
陆平
男
沈志华
苏州实验中学:
周骏
男
沈志华
赵赤宇
男
潘刚
苏州新区一中
沈成强
男
吴光明仇剑芳
苏州外国语学校
陈洁
女
刘富兵
苏州外国语学校
石润玉
男
刘富兵
苏州工业园区第三中学
高枫
男
吴中区
学校
学生
性别
辅导教师
江苏省木渎咼级中学
周石石
男
r陆文明
江苏省木渎咼级中学
胡文磊
男
陈绮雯
苏州市江苏省外国语学校
钱晶
男
王永银
苏州市吴中区苏苑中学
张琪
男
杨美秀
苏州市江苏省外国语学校
王乾
男
陆文明
苏州市吴中区苏苑中学
莫涛
男
杨美秀
苏州市江苏省外国语学校
邱玉立
女
王永银
苏州市江苏省外国语学校
张英琦
女
王永银
苏州市江苏省外国语学校
邹家栋
男
王永银
江苏省木渎咼级中学
杨昊哲
男
卢怀跃
苏州市江苏省外国语学校
蔡良
男
王永银
苏州市吴中区苏苑中学
顾斌
男
杨美秀
江苏省外国语学校
周惠仙
女
王永银
江苏省外国语学校
陈玮
朱磊
男
吴光明仇剑芳1
苏州中学
丁景辰
男
冯澜
苏州实验中学
阙喜峰
男
程敏
苏州实验中学
孙睿
男
沈志华
苏州实验中学
张文彬
男
沈志华
苏州实验中学
黄一平
男
沈志华
苏州实验中学
骆一炜
男
陈飞
苏州大学附属中学
邵壮
男
季厚鹏1
苏州新区一中
陆裔飞
男
吴光明仇剑芳
苏州新区一中
李静
女
吴光明仇剑芳1
