铁和铜及其化合物知识梳理
铁 铜及其化合物讲义

高三化学——金属元素及其化合物第三讲铁铜及其化合物考点一、铁铜的性质1.铁元素位于元素周期表中第_____周期第_______族,其价电子排布式______ ,铜元素位于元素周期表中第_____周期第_______族,其价电子排布式______ . 2.铁与弱氧化性物质反应(如:____________)失去________个电子显 +2价,与强氧化性物质(如:____________)失去________个电子显 +3价。
注意:(1)铁元素在高铁酸盐如K2FeO4中呈__________价。
(2) 铁与氧气、水反应的产物为________ __。
(3) 铁的吸氢腐蚀和吸氧腐蚀的正极反应为________________,______________。
(4) 铁与足量的稀硝酸溶液反应的离子方程式铁与少量的稀硝酸溶液反应的离子方程式【例题】下列物质反应后一定有+3价铁生成的是①过量的Fe与Cl2加热时发生反应②Fe与过量稀H2SO4反应后,再向其中加KNO3③Fe与过量的S加热时发生反应④Fe(NO3)2溶液中加少量盐酸⑤Fe和Fe2O3的混合物溶于盐酸中A.只有①②⑤B.只有②④ C.只有①②④D.只有②③④【针对训练】1.出土的锡青铜(铜锡合金)文物常有Cu2(OH)3Cl覆盖在其表面。
下列说法正确的是A. 锡青铜的熔点比纯铜高B.在自然环境中,锡青铜中的锡对铜起保护作用C.锡青铜文物在潮湿环境中的腐蚀比干燥环境中快D.生成Cu2(OH)3Cl覆盖物是电化学腐蚀过程,但不是化学反应过程2.在铁与铜的混合物中,加入一定量的稀硝酸,充分反应后剩余金属m1g,再向其中加入一定量的稀硫酸,充分振荡后,剩余金属m2g,则m1与m2之间的关系是:A.m1一定大于m2B.m1可能等于m2C.m1一定等于m2D.m1可能大于m23. 向含有0.8 mol的稀硝酸溶液中慢慢加入22.4 g的铁粉。
假设反应分为两个阶段。
铁铜及其化合物

④
⑤ Cl2、Br2、HNO3、
H2O2、KMnO4(H+)
⑥还原剂:Zn等
Fe + Cu2+ = Fe2+ + Cu
Fe+2Fe3+=3Fe2+
2Fe2++Cl2=2Fe3++2Cl-
六、Fe3+和Fe2+旳检验:
1.Fe3+在溶液中为 _棕__黄___色 ①加入NaOH溶液,产生__红__褐___色沉淀。 ②加入KSCN溶液,溶液变成__血__红____色。
电化学腐蚀:
不纯旳金属跟电解质溶液接触时, 会发生氧化还原反应,比较活泼旳 金属失去电子被氧化。
特点:是有电流产生
电化学腐蚀
1、吸氧腐蚀
发生条件: 钢铁表面吸附旳水膜中溶有O2 并呈极
弱酸性或中性或碱性,反应中O2 得电 子被还原为OH铁: 2Fe-4e-=2Fe2+ 杂质: O2+2H2O+4e- =4OH总式: 2Fe+O2+2H2O=2Fe(OH)2
(4)铁与盐溶液反应 Fe + Cu2+ = Fe2+ + Cu
Fe+ቤተ መጻሕፍቲ ባይዱFe3+=3Fe2+
五、Fe、Fe2+、Fe3+相互转化
⑥ ⑤
Fe3+
Fe
① H+、Cu2+、S、I2、Fe3+
③
① ②
② 还原剂:Zn等 ③ Fe、Cu、SO2、I- ④Cl2、Br2、HNO3、
Fe2+ H2O2、KMnO4(H+)
(6) 炼铁和环境保护节 高炉煤气处理 能:
高中化学【铁、铜及其化合物】基础知识

高中化学【铁、铜及其化合物】基础知识一、铁及其化合物1. 知识网络构建2. 重要反应必练写出下列反应的方程式,是离子反应的写出离子方程式。
①Fe高温下和水蒸气的反应:________________________②Fe2O3和Al在高温下反应:_________________________③Fe2O3和CO的反应:_________________________________④Fe和过量稀HNO3的反应:_____________________________⑤过量铁粉和稀HNO3的反应:____________________________⑥FeCl3溶液和Cu的反应:____________________________⑦FeCl3溶液和KSCN溶液的反应:______________________⑧FeO和稀HNO3的反应:___________________________⑨Fe3O4和稀HCl的反应:_________________________⑩Fe3O4和稀HNO3的反应:___________________________⑪Fe(OH)2和稀HNO3的反应:____________________________⑫Fe(OH)2长时间置于空气中:__________________________⑬FeCl2溶液中通入Cl2:__________________________⑭FeCl2溶液中加入NaClO:__________________________⑮FeCl2溶液中加入等物质的量的Na2O2:______________⑯FeCl2溶液中加入HNO3:_________________⑰FeCl2溶液中加入酸性KMnO4溶液:______________________⑱Fe(OH)3与HI的反应:____________________________⑲Fe2(SO4)3溶液中通入SO2气体:_____________________⑳FeCl3溶液中通入H2S气体:_____________________○21FeI2和少量Cl2反应:_______________________○22FeI2和过量Cl2反应:______________________3. 实验现象强化记忆①铁丝在氧气中燃烧的现象___________________。
铁、铜及其化合物知识点
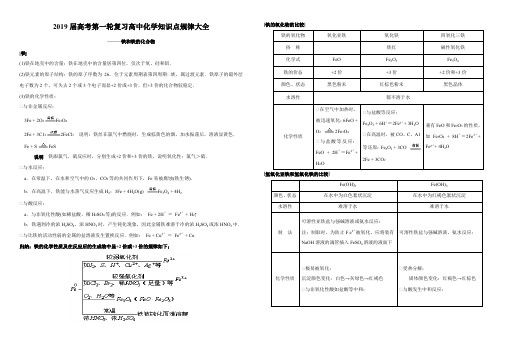
2019届高考第一轮复习高中化学知识点规律大全——铁和铁的化合物[铁](1)铁在地壳中的含量:铁在地壳中的含量居第四位,仅次于氧、硅和铝.(2)铁元素的原子结构:铁的原子序数为26,位于元素周期表第四周期Ⅶ族,属过渡元素.铁原子的最外层电子数为2个,可失去2个或3个电子而显+2价或+3价,但+3价的化合物较稳定.(3)铁的化学性质:Ⅶ与非金属反应:3Fe + 2O2Fe3O42Fe + 3C122FeCl3 说明:铁丝在氯气中燃烧时,生成棕黄色的烟,加水振荡后,溶液显黄色.Fe + S FeS说明铁跟氯气、硫反应时,分别生成+2价和+3价的铁,说明氧化性:氯气>硫.Ⅶ与水反应:a.在常温下,在水和空气中的O2、CO2等的共同作用下,Fe易被腐蚀(铁生锈).b.在高温下,铁能与水蒸气反应生成H2:3Fe + 4H2O(g) Fe3O4 + 4H2Ⅶ与酸反应:a.与非氧化性酸(如稀盐酸、稀H2SO4等)的反应.例如:Fe + 2H+=Fe2++ H2↑b.铁遇到冷的浓H2SO4、浓HNO3时,产生钝化现象,因此金属铁难溶于冷的浓H2SO4或浓HNO3中.Ⅶ与比铁的活动性弱的金属的盐溶液发生置换反应.例如:Fe + Cu2+=Fe2++ Cu归纳:铁的化学性质及在反应后的生成物中显+2价或+3价的规律如下;[铁的氧化物的比较]Ⅶ在空气中加热时,被迅速氧化;6FeO +O22Fe3O4Ⅶ与盐酸等反应:FeO + 2H+=Fe2++H2OⅦ与盐酸等反应:Fe2O3 + 6H+=2Fe3++ 3H2OⅦ在高温时,被CO、C、A1等还原:Fe2O3 + 3CO2Fe + 3CO2[氢氧化亚铁和氢氧化铁的比较][Fe3+和Fe2+的相互转化]例如:2Fe3++ Fe =3Fe2+应用:Ⅶ除去亚铁盐(含Fe2+)溶液中混有的Fe3+;Ⅶ亚铁盐很容易被空气中的O2氧化成铁盐,为防止氧化,可向亚铁盐溶液中加入一定量的铁屑.例如:2Fe2++ Cl2=2Fe3++ 2Cl-应用:氯化铁溶液中混有氯化亚铁时,可向溶液中通入足量氯气或滴加新制的氯水,除去Fe2+离子.Fe2+Fe3+[Fe2+、Fe3+的检验](1)Fe2+的检验方法:Ⅶ含有Fe2+的溶液呈浅绿色;Ⅶ向待检液中滴加NaOH溶液或氨水,产生白色絮状沉淀,露置在空气中一段时间后,沉淀变为灰绿色,最后变为红褐色,说明含Fe2+.Ⅶ向待检液中先滴加KSCN溶液,无变化,再滴加新制的氯水,溶液显红色,说明含Fe2+.有关的离子方程式为:2Fe2++ Cl2 =2Fe3++ 2Cl-Fe3++ 3SCN-=Fe(SCN)3Ⅶ加入K3[Fe(CN)6],若产生特征蓝色沉淀,说明含Fe2+(2)Fe3+的检验方法:Ⅶ含有Fe3+的溶液呈黄色;Ⅶ向待检液中滴加NaOH溶液或氨水,产生红褐色沉淀,说明含Fe3+.Ⅶ向待检液中滴加KSCN溶液,溶液呈血红色,说明含Fe3+.进行铁及其化合物的计算时应注意的事项:(1)铁元素有变价特点,要正确判断产物;(2)铁及其化合物可能参加多个反应,要正确选择反应物及反应的化学方程式;(3)反应中生成的铁化合物又可能与过量的铁反应,因此要仔细分析铁及其化合物在反应中是过量、适量,还是不足量;(4)当根据化学方程式或离子方程式计算时,找出已知量与未知量的关系,列出方程式或方程式组;(5)经常用到差量法、守恒法.2019届高考第一轮复习高中化学知识点规律大全——铜1、单质铜(1)物理性质:铜是硬度较小的紫红色金属,具有良好的延展性、导电性和导热性,广泛应用于电器和电子工业中。
第12讲 铁铜及其化合物(讲义)(解析版)

第12讲 铁铜及其化合物一 铁的位置和物理性质1.铁及其化合物间的主线Fe―→⎩⎪⎨⎪⎧FeO Fe 2O 3Fe 3O 4―→⎩⎨⎧Fe OH2Fe OH 3―→⎩⎨⎧FeSO 4·7H 2OFeCl 32.铁及其化合物间的转化关系3.铁元素的变价 (1)单质铁①生成+2价:铁与S 、H +、Cu 2+、I 2等反应生成+2价。
如:Fe +SFeS 、Fe +Cu 2+===Fe 2++Cu 。
①生成+3价:铁与Cl 2、Br 2等反应生成+3价。
如2Fe +3Cl 2=====点燃2FeCl 3。
①生成+2、+3价:铁与H 2O 、O 2反应生成Fe 3O 4。
3Fe +4H 2O(g)=====高温Fe 3O 4+4H 2。
①铁与HNO 3反应:当Fe 过量生成+2价,3Fe +8H ++2NO -3===3Fe 2++2NO +4H 2O ; 当Fe 不足时生成+3价,Fe +4H ++NO -3===Fe 3++NO +2H 2O 。
(2)铁的化合物:FeO 、Fe 3O 4、Fe 2O 3、Fe(OH)2、Fe(OH)3、Fe 2+、Fe 3+等。
+2价铁具有还原性,与强氧化性物如HNO 3、Cl 2等发生氧化还原反应: 如:3FeO +10HNO 3===3Fe(NO 3)3+NO +5H 2O 。
+3价铁具有氧化性,与强还原性物质, 如:HI 、Fe 、Cu 、I -、S 2-等发生氧化还原反应,如:Fe 2O 3+6HI===2FeI 2+I 2+3H 2O,2Fe 3++Cu===2Fe 2++Cu 2+。
特别强调:①Fe 与一般酸反应生成Fe 2+,与酸的量无关,但Fe 与稀HNO 3反应时最终铁的价态与铁的量有关。
①铁与硫蒸气反应生成的是FeS 而不是Fe 2S 3;铁与碘蒸气反应生成的是FeI 2而不是FeI 3。
4.铁的氧化物特别强调:①FeO 、Fe 3O 4、Fe 2O 3与硝酸反应时均生成Fe 3+。
铁和铜及其化合物

Fe 铜、铁及其化合物一、铁及其化合物1.物理性质:银白色,具有金属光泽;质地较软,有良好的导电性、延展性。
密度7.86 g/cm 3,熔沸点较高。
位置:第四周期,第Ⅷ 族 2.化学性质:(1)与非金属反应 Fe+S (I 2)FeS (FeI 2) 4Fe+3O 22Fe 3O 4 2Fe+3Cl 2(Br 2)2FeCl 3弱氧化剂 Fe 3+、H +、I 2、S 、铁后的金属阳离子(置换)… 强氧化剂 Cl 2、Br 2、HNO 3、浓H 2SO 4、MnO 4-(H +) … (2)与水反应 3Fe + 4H 2O(g)Fe 3O 4 + 4 H 2 ↑(置换)注意:铁在常温下不会和水发生反应,但在水和空气中O 2和CO 2的共同作用下,铁却很容易被腐蚀(生锈/电化学腐蚀) (3) 与酸反应a.与非氧化性酸反应 Fe +2H +== Fe 2++ H 2 b.与氧化性酸反应c.常温下,铁在冷浓硫酸,浓硝酸中发生钝化d.与浓硫酸反应:2Fe +6 H 2SO 4(浓)Fe 2(SO 4)3 +3SO 2 +6 H2Oe.与稀硝酸反应:①当Fe 少量时,离子方程式为:Fe + 4H ++ NO 3-== Fe 3++NO↑+2H 2O②当Fe 过量时,,离子方程式为:3Fe+8H ++2NO 3-== 3Fe 2++2NO↑+4H 2O ③当1:4<n( Fe) :n (HNO 3)<3:8 时,此情况下,Fe 3+和Fe 2+共存。
(4)与盐溶液反应:2Fe 3++ Cu = 2Fe 2++ Cu 2+ Fe + 2Fe 3+ = 3 Fe 2+ Fe + Cu 2+ = Fe 2++ Cu3.铁的氧化物FeO Fe 2O 3 Fe 3O 4 铁的化合价 +2 +3 +2、+3 颜色、状态黑色粉末红棕色粉末 黑色晶体 俗名 铁红 磁性氧化铁 水溶性 不溶于水 不溶于水 不溶于水氧化物类别碱性氧化物碱性氧化物Fe 2+Fe 3+与非氧化性酸反应FeO+2H + =Fe2+ +H2O Fe2O3+6H + =2Fe3+ +3H2O Fe3O4+8H + =2Fe3+ + Fe2++4H2O与还原剂反应(H2、CO、Al等) FeO+CO Fe+CO2Fe2O3+3CO2Fe+3CO23Fe3O4+8Al9Fe+4Al2O3用途用作红色油漆和涂料;赤铁矿是炼铁原料注:3FeO+10HNO3(稀)=3Fe(NO3)3+NO↑+5H2O4、铁的氢氧化物(1)Fe(OH)2的制备Fe(OH)2易被氧化,在制备时应注意:①FeSO4晶体中不能有 Fe3+;②配制后的FeSO4溶液中要加入少量铁粉;③配制溶液的蒸馏水以及所用NaOH溶液均须煮沸以除去其中溶解的氧气;实验:FeSO4溶液中加NaOH.①现象:生成白色沉淀,后又迅速转变为灰绿色,最后生成红褐色②Fe2+容易被氧化,所以FeSO4溶液要新配制.③为了防止滴加NaOH时带入空气,可将吸收NaOH的长滴管伸入FeSO4溶液液面下,再挤出NaOH溶液.④为了防止Fe2+被氧化,还可以向盛有FeSO4溶液的试管中加入少量煤油或其它密度比水小但不溶于水的有机物以隔绝空气.化学方程式: FeSO4 + 2NaOH = Fe(OH)2↓+Na2SO4 Fe2++ 2OH -= Fe(OH)2↓(白色)4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3(红褐色)(白色→灰绿色→红褐色)(2)Fe(OH)3的制备实验:FeCl3溶液中加NaOH溶液.①现象:生成红褐色沉淀②化学方程式:FeCl3+3NaOH= Fe(OH)3↓+3NaCl Fe 3++ 3OH -= Fe(OH)3↓(红褐色)③热稳性:Fe(OH)3对热不稳定,受热能失去水生成红棕色的Fe2O3粉末.化学方程式: 2Fe(OH)3Fe2O3 +3H2O[小结]难溶性或微溶性的碱受热不稳定,容易分解。
铁铜及其化合物重要方程式汇总
铁铜及其化合物重要方程式汇总金属及其化合物重要方程式汇总(三)铁、铜及其化合物1、铁与非金属单质反应:(1)Fe在纯O2中燃烧:化学方程式:;(2)Fe与S的反应:化学方程式:(3)Fe与Cl2点燃:化学方程式:;(4)Fe与I2的反应:化学方程式:;2、铁与水反应:(1)与水蒸汽反应:化学方程式:;(2)常温下,铁与水不起反应,但潮湿的空气里形成原电池,铁易被腐蚀,最终形成铁锈。
原电池反应:负极:正极:总反应:后续反应:3、铁与酸反应:(1)与非氧化性酸①铁和稀盐酸:化学方程式:;②铁和稀硫酸:化学方程式:;离子方程式:;(2)与氧化性酸(与浓硫酸、稀硝酸、浓硝酸)①常温下,浓硫酸和浓硝酸会使、钝化,加热反应。
②铁与浓硫酸:化学方程式:;③铁与足量浓硝酸:化学方程式:;离子方程式:;④少量铁与稀硝酸:化学方程式:;离子方程式:;⑤过量Fe与稀硝酸:化学方程式:;离子方程式:;4.铁与盐溶液反应:(1)铁和氯化铜溶液:化学方程式:离子方程式:;(2)除去FeCl2溶液中的FeCl3:化学方程式:;离子方程式:;第1页,共2页5.Fe3O4粉末和稀盐酸:化学方程式:;离子方程式:;6.CO还原磁性氧化铁(工业炼铁):化学方程式:;7.CO还原氧化铁(工业炼铁):化学方程式:;8.氧化铁和Al做铝热剂的铝热反应:化学方程式:9.向FeCl2溶液中通Cl2:化学方程式:;离子方程式:;10.向Fe(NO3)2溶液中滴加稀硝酸:化学方程式:;离子方程式:;11.向硫酸亚铁溶液滴加过量氨水,生成白色沉淀,迅速变灰绿色,最终变成红褐色:生成白色沉淀化学方程式:;离子方程式:;白色沉淀迅速变灰绿色最终变成红褐色,化学方程式_______________________________12.用氯化铁溶液制作铜制印刷电路板:化学方程式:;离子方程式:;13.Fe3+和I-不能大量共存,离子方程式_____________________________________________14.Fe3+和S2-不能大量共存,离子方程式____________________________________________15.Fe3+的检验:(1)常用硫氰化钾溶液:离子方程式:;(2)高浓度时加氢氧化钠溶液:离子方程式:;16.Fe2+的检验:(1)常用:先滴加硫氰化钾溶液,观察后,再加氯水:现象:;化学方程式:①;②;离子方程式:①;②;(2)高浓度时可以加氢氧化钠溶液:现象:;化学方程式:①;②;(3)当Fe2+和Fe3+共存时,用酸性高锰酸钾,现象是_______________________配平离子方程式:Fe2++MnO4-+H+=Fe3++Mn2++H2O第2页,共2页。
专题4 第三单元 铁、铜及其化合物
10.铁与水蒸气反应,通常有以下两种装置,请回答下列问题:
装置一
装置二
(1)装置二中湿棉花的作用为_提__供__水__蒸__气___。
(2) 实 验 完 毕 后 , 取 出 装 置 一 的 少 量 固 体 , 溶 于 足 量 稀 盐 酸 , 再 滴 加 KSCN溶液,溶液颜色无明显变化,试解释原因:F__e3_O__4+__8_H__+_=_=_=_F_e_2_+_ _+__2_F_e_3_+_+__4_H_2_O_、__2_F_e_3_+_+__F_e_=_=_=_3_F__e2_+_(用离子方程式表示)。
该方法是先在装置Ⅰ中产生FeSO4溶液,并利用产生的H2排尽整个装置 中 的 空 气 , 待 检 验 H2 的 纯 度 后 , 再 关 闭 止 水 夹 K , 利 用 产 生 的 H2 把 FeSO4溶液压入装置Ⅱ中与NaOH溶液进行反应。
专题精练
1.用下列方法可制得白色的Fe(OH)2沉淀:用不含Fe3+的FeSO4溶液与用 不含O2的蒸馏水配制的NaOH溶液反应制备。 (1)用硫酸亚铁晶体配制上述FeSO4溶液时还需加入_稀__硫__酸__、__铁__屑___。 (2)除去蒸馏水中溶解的O2常采用_加__热__煮__沸___的方法。 (3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液, 插 入 FeSO4 溶 液 液 面 下 , 再 挤 出 NaOH 溶 液 。 这 样 操 作 的 理 由 是 _避__免__生__成__的__F_e_(_O_H__)_2与__氧__气__接__触__而__被__氧__化__。
在少量Cl2中燃烧生成FeCl2 (4)Fe分别与氯气、盐酸反应得到相同
的氯化物 (5)Fe3O4中Fe的化合价有+2价和+3价,
铁铜及其化合物的性质
铜的发现简史
• 铜是古代就已经知道的金属之一。一般认为人类知道的 第一种金属是金,其次就是铜。铜在自然界储量非常丰 富,并且加工方便。铜是人类用于生产的第一种金属, 最初人们使用的只是存在于自然界中的天然单质铜,用 石斧把它砍下来,便可以锤打成多种器物。随着生产的 发展,只是使用天然铜制造的生产工具就不敷应用了, 生产的发展促使人们找到了从铜矿中取得铜的方法。含 铜的矿物比较多见,大多具有鲜艳而引人注目的颜色, 例如:金黄色的黄铜矿CuFeS2,鲜绿色的孔雀石 CuCO3· Cu(OH)2或者Cu2(OH)2CO3,深蓝色的石青 2CuCO3· Cu(OH)2等,把这些矿石在空气中焙烧后形成 氧化铜CuO,再用碳还原,就得到金属铜。纯铜制成的 器物太软,易弯曲。人们发现把锡掺到铜里去,可以制 成铜锡合金──青铜。铜,COPPER,源自Cuprum, 是以产铜闻名的塞浦路斯岛的古名,早为人类所熟知。 它和金是仅有的两种带有除灰白黑以外颜色的金属。铜 与金的合金,可制成各种饰物和器具。加入锌则为黄铜; 加进锡即成青铜。
从浅绿色 变为血红 色。 从浅绿色 变为血红 色。 无血红 色出现
离子方程式
2Fe2++Cl2=2 Fe3+ + 2Cl-
Fe3+
在试管中依次加入: FeCl2溶液、KSCN 溶液、溴水
在试管中依次加入: FeCl2溶液、KSCN 溶液、碘水
2Fe2++Br2=2Fe3氧化剂
Fe3+
探究三
提供以下药品: 铁粉 KI 淀粉试纸 FeCl3溶液 KSCN溶液 请根据以上药品,设计实验,探究Fe3+ 到 Fe2+的转化
Fe3+ 到 Fe2+的转化实验
三节铁铜及其化合物
现 变
象, 血
K
溶液变血红色
SC
N
溶 液
原 因
2Fe2++Cl2=2Fe3++2ClFe3++3SCN-=Fe(SCN)3
Fe3++3SCN-=Fe(SCN)3
15
措施
Fe2+
Fe3+
滴加
现 象
生成白色絮状沉淀,迅 速转化为灰绿色,最终 变为红褐色
产生红褐色沉 淀
NaOH
溶液
原 Fe2++2OH-=Fe(OH)2↓ 因 4Fe(OH)2+O2+2H2O=
3
③铁与非氧化性酸(如盐酸)反应: Fe+2HCl=FeCl2+H2↑ , 常 温 下 遇 浓 H2SO4 、 浓HNO3会发生钝化作用,加热时会剧烈反 应,但不会有H2产生。
④铁与某些盐溶液反应: Fe+CuSO4=FeSO4+Cu;Fe+2FeCl3=3FeCl2 。
*⑤铁与水蒸气旳反应:
高温
第三节 铁、铜及其化合物
1
基础知识回忆
一、铁
1.铁在地壳中旳含量仅次于铝,主要以化 合态形式存在(除陨铁)。我国在商代开始使用铁, 在春秋早期我国已掌握冶铁技术。铁位于元素 周期表中第四面期,第Ⅷ族。铁原子在化学反 应中轻易失去2个或3个电子,所以,铁旳常见 化合价是+2价和+3价。其化合物及其水溶液往 往带有颜色。
氢氧化铁
Fe(OH)3 红棕色固体, 不溶于水
Fe(OH)3+△3H+=Fe3++3H2O
2Fe(OH)3=Fe2O3+3H2O
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
铁和铜及其化合物
金属Fe
一、重要反应
1、高炉炼铁
2、铁在空气中燃烧
现象
3、高温下铁与水蒸气反应
4、铁与氯气反应现象
6、铁与稀盐酸反应(离子方程式)
7、铁与过量稀硝酸反应
8、过量铁与稀硝酸反应
9、氢氧化亚铁的制取
如何操作
10、氯化铁与铜反应(刻制印刷电路板)(离子方程式)
11、曾青得铁则化为铜(离子方程式)
12、氯化铁溶液通入SO2(离子方程式)
13、氢氧化亚铁放置在空气中
现象
14、制取氢氧化铁胶体反应方程式
操作
15、四氧化三铁与硫酸反应(离子方程式)
16、四氧化三铁与硝酸反应(离子方程式)
17、氧化亚铁与硝酸反应(离子方程式)
18、铁与氯化铁溶液反应离子方程式
19、铁与硫反应
20、铁与碘单质反应
21、铁与少量氯气
22、检验铁离子的离子方程式
23、检验亚铁离子只用一种试剂为现象
反应离子方程式
24、氯化亚铁与酸性高锰酸钾溶液反应离子方程式
25、溴化亚铁溶液中通入少量氯气离子方程式
26、溴化亚铁溶液中通入过量氯气离子方程式
27、碘化亚铁溶液中通入少量氯气离子方程式
28、碘化亚铁溶液中通入过量氯气离子方程式
二、其他重要知识
1、由氯化铁溶液制备无水氯化铁晶体时加入
原因
2、配制氯化亚铁溶液加入和,原因(用必要文字解释)
3、颜色:铁离子,亚铁离子;四氧化三铁
氧化亚铁氧化铁(俗名)硫化亚铁
七水硫酸亚铁
4、红棕色的固体有红棕色液体有红棕色气体有
5、最早使用的合金是目前用量最大、用途最广的合金是,根据
其化学成分,可分为和两大类。
黑色金属材料包括
以及它们合金。
青铜是铜和组成的合金。
稀土元素包括系的15种元素以及钇和钪,共17种元素。
稀土元素被称为冶金工业的。
6、高铁酸钾中Fe元素化合价,可用于自来水的剂和剂,
原因
7、写出化学式:高铁酸钾铁氰化钾
亚铁氰化钾
9、Fe3+检验:
Fe2+检验:
Fe2+(Fe3+)检验:
10、如何检验四氧化三铁中二价铁和三价铁,操作方法为
金属Cu
一、重要反应:
1、铜与氧气
2、铜与硫
3、铜与氯气
4、铜与FeCl3(写离子方程式)
5、铜在空气中生锈
6、铜绿受热分解
7、铜与浓硫酸反应
8、铜和稀硝酸反应
9、铜和浓硝酸反应
10、湿法炼铜
11、火法炼铜
二、其他重要知识
1、除杂:N2(O2)CO2(CO)
2、颜色:铜氧化铜氧化亚铜硫化铜硫化亚铜
胆矾碱式碳酸铜无水硫酸铜胆矾
3、向硫酸铜溶液中逐滴加氨水,首先形成
离子方程式
继续加氨水,溶解,得到色溶液,离子方程式
若加入极性较小的溶剂(如乙醇),将析出
4、画出四水合铜离子的结构。
